Etilene
| Etilene | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| etene | |
| Nomi alternativi | |
| etilene gas di olefina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H4 |
| Massa molecolare (u) | 28,054 |
| Aspetto | gas incolore |
| Numero CAS | |
| Numero EINECS | 200-815-3 |
| PubChem | 6325 |
| SMILES | C=C |
| Proprietà chimico-fisiche | |
| Densità (kg·m−3, in c.s.) | 1,2612 |
| Solubilità in acqua | insolubile |
| Temperatura di fusione | −169 °C (104 K) |
| ΔfusH0 (kJ·mol−1) | 3,35 |
| ΔfusS0 (J·K−1mol−1) | 32,2 |
| Temperatura di ebollizione | −103,7 °C (169,4 K) |
| ΔebH0 (kJ·mol−1) | 13,544 |
| ΔebS0 (J·K−1mol−1) | 79,95 |
| Punto triplo | 104,0 K 120 Pa |
| Punto critico | 282,5 K 5,06 × 106 Pa |
| Tensione di vapore (Pa) a 273 K | 4,1 × 106 |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | 52,4 |
| ΔfG0 (kJ·mol−1) | 68,4 |
| S0m(J·K−1mol−1) | 219,3 |
| C0p,m(J·K−1mol−1) | 42,9 |
| Indicazioni di sicurezza | |
| Punto di fiamma | −136 °C (137 K) |
| Limiti di esplosione | 2,7 – 36% |
| Temperatura di autoignizione | 450 °C (723 K) |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 220 - 280 - 336 |
| Consigli P | 210 - 260 - 304+340 - 315 - 377 - 381 - 405 - 403 [1] |
L'etilene (nome IUPAC: etene) è il più semplice degli alcheni, avente formula chimica C2H4. A temperatura e pressione ambiente si presenta come un gas incolore, estremamente infiammabile,dal lieve odore dolce, muschiato e un po' pungente.[2] Oltre ad essere un importante prodotto nell'industria chimica (è ad esempio il composto chimico da cui si ottiene il polietilene), è anche un ormone (per la maturazione) di molte specie vegetali.[3] È un anestetico e come tale fu usato fino a circa il 1940.[4]
Il gruppo funzionale corrispondente a una molecola di etilene privata di un atomo di idrogeno, il più semplice degli alchenili, si chiama comunemente vinile e i composti contenenti tale gruppo sono detti composti vinilici.
Storia[modifica | modifica wikitesto]
Il gas sarebbe stato osservato consapevolmente per la prima volta nel 1669 dal chimico tedesco Johann Becher (Physica subterranea), che l'avrebbe ottenuto facendo reagire etanolo e acido solforico. Con certezza, l'etilene fu noto a partire dal 1795 col nome di "gas di olefina", che gli venne dato dopo aver osservato che per reazione con il cloro forma l'1,2-dicloroetano, liquido oleoso, sintetizzato per la prima volta nel 1785 da quattro chimici olandesi.
John Dalton ne propose la formula di struttura nel 1806. Nella seconda metà del XIX secolo la formula proposta per l'etilene venne usata come base per quella degli acidi carbossilici vegetali (ad esempio l'acido succinico).
Il nome "etilene" entrò in uso nella metà del XIX secolo, dove il suffisso -ene, utilizzato nel senso di "deriva da", fu aggiunto al nome del radicale etile (C2H5-) e rimase in uso fino al 1852.
Nel 1866 August Wilhelm von Hofmann, proponendo una nuova nomenclatura, ne cambiò il nome in etene. La nomenclatura di Hofmann divenne poi la base su cui si sviluppò la nomenclatura IUPAC.
Geometria molecolare[modifica | modifica wikitesto]
I due atomi di carbonio sono uniti da un doppio legame covalente, la rotazione attorno al quale richiede di gran lunga molta più energia rispetto alla rotazione attorno ad un legame singolo. Di fatto, in condizioni normali, la rotazione è impedita.
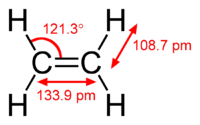
Per via dell'ibridazione sp² degli orbitali degli atomi di carbonio, la molecola è planare, ovvero tutti e sei gli atomi giacciono su un unico piano. L'angolo formato dai due legami carbonio-idrogeno di ciascun atomo di carbonio è di 117,4º, di poco diverso dall'angolo di 120º previsto teoricamente per una geometria trigonale. Tale piccola diminuzione rispetto al valore ideale per l'ibridazione sp² è legata al fatto che un legame doppio richiede un maggior spazio angolare rispetto a un legame semplice, in accordo con la teoria VSEPR [5]. Similmente accade nel fosgene, nella formaldeide e nell'acetone.
Il doppio legame tra i due atomi di carbonio, con la sua elevata densità elettronica, rende la molecola dell'etilene chimicamente molto più reattiva di quella di molecole simili ma prive del doppio legame (come l'etano).
Proprietà e precauzioni[modifica | modifica wikitesto]
La reattività dell'etilene e di tutti gli alcheni si esplica principalmente attraverso la reazione di addizione al doppio legame e la sua conversione in due legami semplici; tale reazione è esotermica ed è accompagnata quindi da uno sviluppo di calore.
L'etilene è poco solubile in acqua (250 mg/L a 0 °C) e molto più solubile nei solventi organici apolari. Ha un odore dolciastro e sgradevole; come tutti gli alcheni è percepibile dall'olfatto umano, la soglia di sensibilità è di 260 ml/m³.
L'etilene brucia rapidamente all'aria con una fiamma luminosa e fuligginosa. Per via della sua elevata infiammabilità, i contenitori di etilene vanno conservati in un luogo ben ventilato. Va tenuto ben lontano da scintille o altre fonti di ignizione, occorre avere inoltre cura di evitare scariche dovute all'accumulo di elettricità statica. In percentuali comprese tra il 3% ed il 36%, forma con l'aria una miscela esplosiva.
Per inalazione, l'etilene dà nausea, capogiro e può portare allo stato di incoscienza.
Produzione e disponibilità[modifica | modifica wikitesto]
La produzione annuale di etilene su scala industriale nel 2000 è stata di circa 100 milioni di tonnellate (delle quali 26,6 milioni di tonnellate sono state prodotte negli Stati Uniti).[6] Nel 1989 la Germania, con 2,9 milioni di tonnellate è stata il più grande produttore europeo di etilene, seguita dalla Francia (2,5 milioni di tonnellate) e dal Regno Unito (1,9 milioni di tonnellate).
La produzione europea di etilene (EU-15 + Norvegia) nel 2011 è stata di circa 19,6 milioni di tonnellate[7].
Inizialmente l'etilene fu sintetizzato per disidratazione dell'etanolo e per isolamento dal gas di cokeria; benché questi processi siano stati sostituiti da altri, sono oggi ancora in uso in alcune nazioni in via di sviluppo in America del Sud, Asia ed Africa. Nei paesi industrializzati, la principale fonte di etilene è costituita dal cracking termico del gas naturale, dell'etano e di altri idrocarburi superiori (nafta, gasolio)[6] e dal suo isolamento dai gas ottenuti nei processi di cracking e reforming nelle raffinerie di petrolio.
In laboratorio, l'etilene può essere ottenuto per reazione di eliminazione, facendo reagire l'1,2-dicloroetano con zinco metallico:
L'etilene è anche il principale componente del gas di legna, ossia del gas che si ottiene per distillazione della legna in assenza di aria.
Le piante lo producono a partire dall'amminoacido metionina. Per gli organismi vegetali è un ormone che stimola la maturazione.
È presente nei giacimenti di gas naturale; alcuni di essi (principalmente in America) ne contengono fino al 20%.
La rete di distribuzione[modifica | modifica wikitesto]
In Germania ed in alcune parti dei Paesi Bassi esiste una rete di distribuzione dell'etilene (e di altri prodotti di base per l'industria chimica) per trasportarlo da Rotterdam e Anversa verso i siti chimici delle zone di Colonia e di Emscher-Lippe. I governi locali della Bassa Sassonia e dello Schleswig-Holstein mantengono una rete di distribuzione che va dalla regione della Ruhr fino alla costa tedesca. Inoltre, 54 chilometri di linea collegano gli insediamenti industriali di Brunsbüttel e Stade, a nord e a sud del fiume Elba.
Lo Schleswig-Holstein e la Bassa Sassonia, all'interno di un piano di collegamento tra gli impianti promosso dalla federazione delle industrie chimiche tedesche (Verbands der Chemischen Industrie - VCI), sono intenzionati ad espandere e migliorare la rete. Dall'area di Stade la rete è collegata al gasdotto diretto a Böhlen, in Sassonia ed è allo studio un ulteriore collegamento con i grandi siti chimici di Wilhelmshaven e Gelsenkirchen.
Utilizzi e applicazioni[modifica | modifica wikitesto]
Processi chimici industriali[modifica | modifica wikitesto]

L'etilene è la materia prima delle sintesi di innumerevoli composti organici, tra cui l'antracene, il 2-cloroetanolo, il cloroetano, il propanale, l'acetaldeide, l'isoprene, l'acetato di vinile, l'acido propanoico, il butene, lo stirene, l'etandiolo.
Minori quantità ne vengono impiegate anche per la sintesi dell'ossido di etilene e dell'etanolo.
Nel processo Wacker l'etilene viene convertito su scala industriale ad acetaldeide per reazione con ossigeno molecolare catalizzata da sali di rame e di palladio. Enormi quantità di aldeidi vengono prodotte con questo processo.
Oggi l'etilene rappresenta nell'industria chimica la materia prima da cui si produce il 30% di tutti i composti petrolchimici; grazie al suo minore costo di produzione e alla sua maggiore disponibilità rispetto al petrolio, ha rimpiazzato l'acetilene in questo ruolo di composto-chiave sin dalla fine della seconda guerra mondiale.
È inoltre il composto di partenza per la produzione di numerose materie plastiche, quali il polietilene (che ne consuma la maggiore quantità in questo campo), l'etere polivinilico, il cloruro di polivinile (PVC), i poliesteri, il copolimero tra etilene e acetato di vinile (E/VA), l'acetato di polivinile, il polistirene (tramite l'etilbenzene).
Nello schema seguente sono riportati alcuni tra i più importanti processi chimici industriali che utilizzano l'etilene come materia prima:
| Etilene | |||||||||||||||||||||||||||||||||||||||||
| (alchilazione) | (ossidazione parziale diretta) | (polimerizzazione) | (ossidazione parziale) | (clorurazione diretta o ossiclorurazione) | |||||||||||||||||||||||||||||||||||||
| Etilbenzene | Ossido di etilene | Polietilene | Acetaldeide | 1,2-dicloroetano | |||||||||||||||||||||||||||||||||||||
| (deidrogenazione) | (catalisi acida o via termica) | (ossidazione) | (termolisi) | ||||||||||||||||||||||||||||||||||||||
| Stirene | Glicol etilenico | Glicoleteri, etanolammine e polietossilati | Acido acetico | Cloruro di vinile | |||||||||||||||||||||||||||||||||||||
| (polimerizzazione) | (polimerizzazione) | (polimerizzazione) | |||||||||||||||||||||||||||||||||||||||
| Polistirene | Polietilenglicole | Polivinilcloruro | |||||||||||||||||||||||||||||||||||||||
Altri impieghi[modifica | modifica wikitesto]
Insieme al gas esilarante, l'etilene ha trovato impiego anche come anestetico per qualche anno. Ha un effetto narcotico e rilassante sui muscoli. Con questo impiego, fu utilizzato pubblicamente per la prima volta a Chicago nel 1923; il suo potere narcotico è lievemente superiore a quello del gas esilarante ed ha un meccanismo di azione simile ad esso. Oggi non è più usato come anestetico per via del suo sgradevole odore e della sua infiammabilità. Inoltre, il suo potere narcotico è meno efficace di quello di altre sostanze; per poter aver un buon effetto, la miscela narcotica deve infatti contenere almeno l'80% di etilene.
L'etilene trova uso anche per completare la maturazione dei frutti acerbi di alcune piante (ananas, banana, pomodoro).[8]
L'etilene è utilizzato anche come combustibile per lanciafiamme.
Trova infine impiego nella produzione di armi chimiche (quali l'iprite, chiamata anche 2,2'-dicloroetilsolfuro). Nella Germania dell'immediato dopoguerra, in mancanza di carburante, in forma di gas di legna (ottenuto per distillazione della legna in assenza di ossigeno), è stato usato anche come carburante per i camion.
Fitoregolatore[modifica | modifica wikitesto]

È stato visto che le cellule animali producono e rispondono all'etilene, sebbene il suo ruolo non sia chiaro[9].
L'etilene è però più famoso come fitoormone, ovvero un ormone delle piante. Viene sintetizzato dalle piante a partire dall'amminoacido metionina, parzialmente stimolato dal fitoormone auxina. Come ormone, influisce sulla germinazione e sull'invecchiamento della pianta. Provoca la maturazione dei frutti, lo sviluppo dei germogli, la caduta delle foglie in autunno e la morte di parti della pianta. In quanto gas, si trova in tutti gli spazi intracellulari.
Già nel 1901 Dimitri Neljubow dimostrò che l'etilene provoca nelle piante la cosiddetta tripla risposta, che si manifesta sulle piante gassate con esso. Ben visibile è l'effetto riscontrato sulle piante nelle vicinanze di condotti che perdono, che subiscono una crescita notevole.
Si tratta di un'inibizione della crescita verticale in associazione ad un ispessimento dello stelo e una disattivazione del gravitropismo e quindi della crescita in direzione della gravità terrestre. Questo effetto avviene tramite un riorientamento dei microtubuli che agiscono come una sorta di struttura scheletrica fornendo la direzione di crescita (di accumulo delle fibre di cellulosa) del germoglio. Lo scopo biologico si suppone essere il superamento di ostacoli, l'etilene si forma durante l'intera crescita e si accumula a monte degli ostacoli stimolando l'ispessimento e aumentando quindi la forza espressa dalla punta della radice.
La seconda funzione dell'etilene riguarda i diversi processi legati all'invecchiamento della pianta, tra cui la maturazione dei frutti, lo sviluppo dei germogli, la caduta delle foglie (abscissione) e la morte di parti della pianta (senescenza). Per queste funzioni è essenziale l'effetto di crescita esponenziale dell'etilene disponibile, da cui si deduce che la sintesi dell'etilene è un processo auto-catalitico che consente, per esempio, a tutti i frutti della pianta di maturare contemporaneamente. Questo effetto è sfruttato in agricoltura per riattivare in un secondo tempo i processi metabolici e quindi far completare la maturazione di frutti raccolti acerbi.
Spesso i pomodori vengono raccolti non ancora maturi, trasportati e solo a destinazione fatti maturare con l'aiuto dell'etilene o anche mettendoli a contatto con frutti già maturi che, liberando etilene, ne completano la maturazione.
Sin dalla metà degli anni novanta sono stati coltivati pomodori geneticamente modificati (Flavour-Saver) particolarmente durevoli perché il loro gene per la produzione dell'etilene è stato appositamente bloccato. Pomodori di questo genere possono essere fatti maturare su richiesta, tramite gassatura con etilene.
L'etilene è essenziale anche nel ruolo di "segnale d'allarme" chimico-fisico in caso di infestazioni della pianta da parte di parassiti nonché di rotture o storture. Insieme ad altre sostanze quali l'acido salicilico, l'etilene marchia la zona danneggiata e stimola la produzione di fitotossine. Essendo un gas, e quindi diffondendosi, l'etilene "mette in allarme" stimolando reazioni a cascata anche le parti della pianta prossime e le piante vicine.
Il meccanismo d'azione dell'etilene, come peraltro quello degli altri fitoormoni, è ancora poco indagato. Si presume che l'etilene agisca su specifici recettori (i recettori ETR) sulla membrana del reticolo endoplasmatico innescando così una cascata di eventi all'interno della cellula. Di fatto, si tratta dell'attivazione dell'enzima serotonina-treonina-chinasi CTR1 che a sua volta attiva una specifica proteina del nucleo cellulare (la proteina EIN3/EIL) che funge da fattore di trascrizione nella sintesi proteica e avvia l'espressione di alcuni geni specifici. Il primo gene individuato come bersaglio di questa proteina è stato chiamato ethen-response-factor 1, ERF1. Questo fattore regola l'attività di numerosi geni, cosicché l'azione dell'etilene su di esso innesca un'ampia serie di effetti genetici. Per esempio, durante la maturazione porta alla produzione di enzimi che ammorbidiscono le pareti cellulari; durante la senescenza, stimola la produzione di enzimi che degradano la chitina e la cellulosa (la chitinasi e la cellulasi). Particolarmente ampia è la gamma di risposte modulate dall'etilene allo stress dovuto a parassiti o rotture della pianta; in questi casi vengono prodotti oltre alla chitinasi (che agisce come veleno sugli insetti), la glucanasi, gli inibitori della proteinasi (che, bloccando l'attività degli enzimi che degradano le proteine, ostacolano l'attecchire dei funghi) e molte altre sostanze difensive.
La sintesi dell'etilene nelle piante costituisce un ciclo metabolico che prende il nome di ciclo di Yang. Il ciclo parte dall'amminoacido metionina, che in un primo stadio forma la S-adenosil metionina per accoppiamento con una unità di adenosina. Questa decade in acido 1-amminociclopropancarbossilico (ACC) che per azione dell'ACC-ossidasi libera etilene. La produzione di ACC-ossidasi è a sua volta stimolata dall'etilene, si crea quindi una reazione a catena che stimola la produzione di etilene anche nelle cellule vicine.
Reazioni[modifica | modifica wikitesto]
In condizioni di ossigenazione ottimale, l'etilene brucia completamente trasformandosi in anidride carbonica e acqua:
Per riscaldamento in assenza di aria, si decompone in metano e carbonio
Per via dell'insaturazione dovuta al doppio legame carbonio-carbonio, l'etilene subisce molto facilmente reazioni di addizione elettrofila. Può sommare, ad esempio, acqua, idrogeno o alogeni.
L'etilene somma una molecola di acqua a dare etanolo, tuttavia in assenza di un opportuno catalizzatore la velocità di reazione è molto piccola.
L'etilene somma facilmente una molecola di cloro a dare l'1,2-dicloroetano
L'etilene reagisce con l'idrogeno ad alta pressione a dare etano in presenza di un catalizzatore metallico quale platino o nichel.
L'etilene, in presenza di radicali liberi, ad alte pressioni e a temperature di circa 200 °C, oppure in presenza di catalizzatori (come ad es. quelli di tipo Ziegler Natta), polimerizza, dando il polietilene (o politene)
Con reazione endotermica, può inoltre essere decomposto in idrogeno ed acetilene (o etino)
Infine, per reazione con aria o ossigeno ad alta pressione, in presenza di argento quale catalizzatore, a temperature comprese tra 220 °C e 280 °C, l'etilene subisce una epossidazione e si trasforma in ossido di etilene (o ossirano)
Immagini 3D della molecola[modifica | modifica wikitesto]


Note[modifica | modifica wikitesto]
- ^ scheda dell'etilene su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ (EN) Heinz Zimmermann e Roland Walzl, Ethylene, Wiley-VCH Verlag GmbH & Co. KGaA, 15 aprile 2009, pp. a10_045.pub3, DOI:10.1002/14356007.a10_045.pub3, ISBN 978-3-527-30673-2. URL consultato il 31 dicembre 2021.
- ^ (EN) Kevin L.-C. Wang, Hai Li e Joseph R. Ecker, Ethylene Biosynthesis and Signaling Networks, in The Plant Cell, vol. 14, suppl 1, 2002-05, pp. S131–S151, DOI:10.1105/tpc.001768. URL consultato il 31 dicembre 2021.
- ^ (EN) Francis X. Whalen, Douglas R. Bacon e Hugh M. Smith, Inhaled anesthetics: an historical overview, in Best Practice & Research Clinical Anaesthesiology, vol. 19, n. 3, 2005-09, pp. 323–330, DOI:10.1016/j.bpa.2005.02.001. URL consultato il 31 dicembre 2021.
- ^ J.E. Huheey, E.A. Keiter e R.L. Keiter, 6 - La struttura e la reattività delle molecole, in Chimica Inorganica, Seconda edizione italiana, sulla quarta edizione inglese, Piccin Nuova Libraria, Padova, 1999, pp. 209-223, ISBN 88-299-1470-3.
- ^ a b Weissermel-Arpe, p. 63.
- ^ Appe - Quarterly Production Statistics 2004-2011 Archiviato l'8 novembre 2012 in Internet Archive. (cons. 27.08.2012)
- ^ Si veda la sezione "ruolo biologico"
- ^ Abeles FB, Morgan PW, Saltveit ME, Ethylene in Plant Biology, New York: Academic Press, 1992.
Bibliografia[modifica | modifica wikitesto]
- (EN) Klaus Weissermel, Hans-Jürgen Arpe, Charlet R. Lindley, Industrial organic chemistry, 4ª ed., Wiley-VCH, 2003, ISBN 3-527-30578-5.
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «etilene»
Wikizionario contiene il lemma di dizionario «etilene» Wikimedia Commons contiene immagini o altri file su etilene
Wikimedia Commons contiene immagini o altri file su etilene
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) Francis A. Carey, ethylene, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- L'etilene su CompChemWiki, su compchemwiki.org (archiviato dall'url originale il 27 settembre 2007).
| Controllo di autorità | Thesaurus BNCF 24418 · LCCN (EN) sh85045433 · GND (DE) 4140264-9 · BNE (ES) XX534539 (data) · BNF (FR) cb12062004j (data) · J9U (EN, HE) 987007557798205171 · NDL (EN, JA) 00562060 |
|---|






![{\displaystyle {\ce {n CH2=CH2 -> [-CH2-CH2-]n}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/56efc52c42042ad5a5ac5b4c1d243f213c993900)

