Cicloalcani
I cicloalcani (o nafteni[1]) sono composti organici monociclici saturi (cioè che non contengono legami doppi o tripli tra atomi di carbonio) costituiti solamente da atomi di carbonio e di idrogeno (e per questo appartenenti alla più ampia classe degli idrocarburi).[2] Appartengono inoltre alla classe dei composti aliciclici (che comprende inoltre i cicloalcheni e i cicloalchini).
I cicloalcani presentano formula bruta CnH2n.
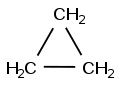
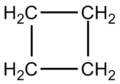
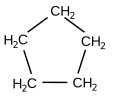
Esempi di cicloalcani sono il ciclobutano e il cicloesano.
Simili agli alcani, si differenziano da questi ultimi in quanto nella loro struttura gli atomi di carbonio sono uniti a formare un anello chiuso.
Benché tale anello venga rappresentato per comodità con un poligono regolare, i cicloalcani non hanno una struttura planare (ad eccezione del ciclopropano). L'angolo di legame di 109,5°, tipico degli atomi di carbonio con ibridazione sp3 fa sì che l'anello risulti piegato.
Quando il numero di atomi di carbonio nell'anello è 3 (ciclopropano) o 4 (ciclobutano), gli atomi di carbonio sono forzati a formare legami con angoli molto piccoli, 60° e 88° rispettivamente, ben inferiori al valore di 109,5° tipico della struttura tetraedrica. Questa forzatura produce una tensione (detta tensione d'anello) che rende la molecola meno stabile. Un esempio estremo di molecola in tensione è quello del cubano.
Nomenclatura IUPAC[modifica | modifica wikitesto]
- Come radice si utilizza il nome del cicloalcano progenitore, quindi i cicloalcani saranno nominati come cicloalcani sostituiti e non come sostituenti cicloalcani. Questo accade tranne in alcuni casi dove si ha una catena carboniosa che contiene più atomi di carbonio dell'anello stesso (es 1-ciclopropilbutano)
- si comincia a numerare da un carbonio sostituito facendo in modo che la somma dei numeri di tutti i sostituenti sia la più bassa possibile. Se sono presenti più gruppi diversi si ordina secondo l'ordine alfabetico e i sostituenti non alchilici (es alogeni) vengono trattati alla stregua di gruppi alchilici.
Le formule utilizzate in questo esempio sono formule di struttura semplificate. Ogni vertice rappresenta un atomo di carbonio e gli atomi di idrogeno direttamente legati ad essi non sono evidenziati - con l'eccezione degli atomi dei gruppi legati ai cicli, voluta in questo caso dall'autore per evidenziare i criteri di assegnazione dei nomi.
cicloesano metilciclopentano 1,2-dietilcicloesano
Isomeria nei cicloalcani[modifica | modifica wikitesto]
Nei cicloalcani, data la loro particolare struttura tridimensionale non lineare, manca la possibilità di avere rotazione libera di legami come ad esempio negli n-alcani. Nonostante questa maggior rigidità, i cicloalcani possono manifestare fenomeni di isomeria e questa è data dalla posizione dei loro sostituenti rispetto al piano orizzontale. I sostituenti possono infatti presentarsi sulla stessa faccia e saranno quindi in cis (a) oppure presentarsi su facce opposte ed essere quindi in trans (b). A differenza degli isomeri di struttura i sostituenti sono legati nello stesso ordine ma hanno disposizione tridimensionale differente. Composti con queste proprietà sono definiti stereoisomeri.
Fonti industriali[modifica | modifica wikitesto]
Le reazioni condotte su scala maggiore sono l'addizione di idrogeno al benzene e ad altri composti aromatici sostituiti per convertirli nei corrispondenti cicloesani. Data la stabilità degli anelli aromatici, la reazione richiede un catalizzatore e condizioni di lavoro piuttosto drastiche. Generalmente il catalizzatore è nichel, l'idrogeno viene mantenuto a pressioni non inferiori alle 15 atmosfere e la temperatura di reazione a non meno di 150 °C.
Preparazioni per sintesi[modifica | modifica wikitesto]
I ciclopropani si preparano per
- addizione di carbene agli alcheni
R-CH=CH-R' + CH2N2 → R-CH---CH-R'
\ /
CH2
- il carbene è una particella poco stabile che può esistere in due forme, una di queste è il biradicale .CH2. che, con i suoi due elettroni spaiati è in grado di inserirsi nel doppio legame di un alchene convertendolo in un ciclopropano.
- Il carbene viene solitamente generato in situ dalla decomposizione del diazometano, CH2N2, attivata dalla luce.
- Similmente, il trattamento di un alchene con cloroformio e sodio idrato porta alla conversione dell'alchene nel corrispondente 1,1-diclorociclopropano a seguito dell'inserimento sul doppio legame del diclorocarbene .CCl2. generato dall'azione del sodio idrato sul cloroformio.
- ciclizzazione di 1,3-dialogenuri alchilici per reazione con metalli, generalmente zinco
CH2---CH2
Cl-CH2-CH2-CH2-Cl + Zn → \ /
CH2
I cicloalcani superiori ed i sistemi policiclici possono venire preparati ricorrendo alle reazioni elettrocicliche; tra esse la più comune è la reazione di Diels-Alder tra un diene ed un alchene sostituito con gruppi elettron-attrattori (detto dienofilo). La reazione produce un cicloalchene che viene successivamente idrogenato (vedi alcheni) a cicloalcano.
Reazioni tipiche[modifica | modifica wikitesto]
I cicloalcani hanno una reattività pressoché identica a quella degli alcani. Come questi sono infiammabili e subiscono facilmente reazioni di sostituzione radicalica catalizzate dalla luce o dal calore.
Per via della tensione d'anello, il ciclopropano reagisce con idrogeno attraverso apertura dell'anello, trasformandosi in propano:
CH2---CH2 \ / + H2 → CH3-CH2-CH3 CH2
o con acidi alogenidrici attraverso apertura dell'anello, trasformandosi nei corrispondenti propani alogenati:
CH2---CH2 \ / + HX → CH3-CH2-CH2-X CH2
Note[modifica | modifica wikitesto]
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su cicloalcani
Wikimedia Commons contiene immagini o altri file su cicloalcani
Collegamenti esterni[modifica | modifica wikitesto]
- cicloalcano / naftène, su sapere.it, De Agostini.
- (EN) cycloalkane, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 37223 · LCCN (EN) sh85035091 · GND (DE) 4148484-8 · BNF (FR) cb121074472 (data) · J9U (EN, HE) 987007538313705171 |
|---|