Eteri corona
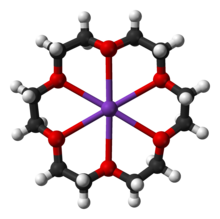
Gli eteri corona sono una famiglia di polieteri ciclici derivati dal glicole etilenico, in cui l'unità strutturale fondamentale, la cui ripetizione caratterizza questi composti, è formata dal gruppo -OCH2CH2-. Derivano il nome dal fatto che le loro configurazioni più stabili assumono la forma di una corona.
Un'importante caratteristica strutturale degli eteri corona è che il diametro della cavità creata dagli atomi di ossigeno che si ripetono nel ciclo è paragonabile al diametro degli ioni di metalli alcalini. La cavità di un etere corona è una regione polare e le coppie di elettroni non condivisi degli ossigeni che formano la cavità solvatano efficacemente gli ioni dei metalli alcalini. Da ciò deriva il loro uso in chimica organica che permette di ottenere soluzioni non acquose di composti che altrimenti sarebbero insolubili in solventi organici apolari o poco polari. In particolare, la dimensione degli ioni metallici chelabili è funzione della dimensione dell'etere ciclico: così, ad esempio, 18-corona-6 è in grado di chelare K+, 15-corona-5 chela Na+ mentre il più piccolo 12-corona-4 riesce a chelare solamente il piccolo ione Li+.
La superficie esterna dell'etere corona è apolare e con caratteristiche di idrocarburo. In conseguenza di ciò, gli eteri corona e i loro complessi con gli ioni dei metalli alcalini si sciolgono facilmente in solventi organici non polari.
Un grosso contributo alla conoscenza della chimica degli eteri corona è stato dato dal chimico organico Charles J. Pedersen che nel 1967 notò che un sottoprodotto dalla reazione di condensazione di molecole di catecolo era in grado di solubilizzare i sali di potassio. I suoi studi approfonditi in questo campo gli permisero di vincere il premio Nobel per la chimica nel 1987.
Nomenclatura[modifica | modifica wikitesto]
La nomenclatura IUPAC ufficiale prevede l'indicazione nel primo numero nel nome dell'etere del numero di atomi dell'anello (in genere indicato in parentesi quadre). Nel secondo numero il numero di atomi di ossigeno (o di altri donatori). Eventuali sostituenti vengono indicati con un prefisso; es. benzo-, dicicloesano-, ecc. Tra i due numeri è interposto il termine corona. Ad esempio il dibenzo[18]corona-6 indica un etere corona sostituito da due gruppi benzo e avente un anello macrociclico di 18 membri, di cui 6 sono atomi di ossigeno donatori.
Un sistema di nomenclatura più generalizzato per questi leganti organici neutri è stato sviluppato da Vögtle e Weber nel 1979, ma modificato successivamente da Cram nel 1986; in questo sistema qualunque macrociclico, è chiamato corando. Le molecole lineari aperte sono indicate come podandi; sistemi biciclici o oligociclici sono chiamati criptandi; sistemi rigidi basati su frammenti di ''p''-metilanisolo, sono chiamati sferandi. Tuttavia in generale, per gli eteri corona con donatori all'ossigeno viene mantenuta la vecchia nomenclatura.

|

|

|
| 12-corona-4 (1,4,7,10-tetraossaaciclododecano) | 15-corona-5 (1,4,7,10,13-pentaossaaciclopentadecano) | 18-corona-6 (1,4,7,10,13,16-esaossaciclottadecano) |
Affinità per i cationi[modifica | modifica wikitesto]
Gli eteri corona presentano in genere alta affinità per cationi metallici come lo ione potassio. Studi su questo tipo di strutture sono fatti in chimica ospite/ospitante. Molecole quali il 18-corona-6 può anche accettare ammine protonate e formare complessi molto stabili in soluzione e in fase gassosa. Ad esempio l'ammino acido lisina, contenente una ammina primaria nella catena laterale, quando protonata è capace di legare la cavità del 18-corona-6 tramite legami a idrogeno tra i tre atomi di idrogeno dell'ammina protonata e i tre atomi di ossigeno dell'ospitante.
Aza-corone[modifica | modifica wikitesto]
Alcuni o tutti gli atomi di ossigeno di un etere corona possono essere rimpiazzati da atomi di azoto dando luogo a aza-corone; nel caso di una parziale sostituzione si possono formare criptandi. Un noto per la tetrazacorna è il ciclene nel quale tutti gli atomi di ossigeno sono sostituiti.[1]
Note[modifica | modifica wikitesto]
- ^ Vincent J. Gatto, Steven R. Miller, and George W. Gokel (1988), "4,13-Diaza-18-Crown-6 Archiviato il 1º settembre 2012 in Internet Archive.", Org. Synth., Coll. Vol. 8: 152
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Eteri corona
Wikimedia Commons contiene immagini o altri file su Eteri corona
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) IUPAC Gold Book, "crown", su goldbook.iupac.org.
| Controllo di autorità | LCCN (EN) sh89006653 · GND (DE) 4165804-8 · J9U (EN, HE) 987007539200705171 |
|---|