Acido fumarico
| Acido fumarico | |
|---|---|
 | |
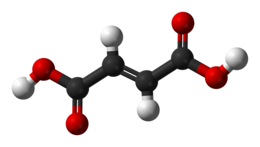 | |
| Nome IUPAC | |
| acido E-butendioico | |
| Nomi alternativi | |
| acido trans-butendioico
acido trans-1,4-butendioico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C4H4O4 |
| Massa molecolare (u) | 116,07 |
| Aspetto | solido cristallino bianco |
| Numero CAS | |
| Numero EINECS | 203-743-0 |
| PubChem | 444972 |
| DrugBank | DB01677 |
| SMILES | C(=CC(=O)O)C(=O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,635 g/cm3 (20 °C) |
| Costante di dissociazione acida (pKa) a 291 K | pKa1 = 3.03, pKa2 = 4.44 |
| Solubilità in acqua | 6,3g/l a 20 °C |
| Temperatura di fusione | 287 °C (560 K) |
| Temperatura di ebollizione | 290 °C (563 K) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 273 °C (vaso aperto: 546 K) |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 319 |
| Consigli P | 305+351+338 [1] |
L'acido fumarico (anche acido trans-butendioico) è un acido presente in natura nella frutta e verdura, ed è stato isolato nelle radici della pianta erbacea selvatica Fumaria officinalis (Fumariaceae) da cui deriva il nome.
L'acido fumarico è isomero dell'acido maleico (acido cis-butendioico). Le due sostanze sono isomeri stabili e distinti, dato che la rotazione attorno ad un legame doppio carbonio-carbonio è impedita, poiché la transizione tra gli isomeri cis (Z) e trans (E) possiede una notevole energia di attivazione.
Le caratteristiche dei due acidi sono molto diverse, ad esempio l'acido maleico è tossico, mentre il fumarico è una biomolecola fondamentale ed è usato come medicinale e in prodotti alimentari.
È prodotto industrialmente sia per via fermentativa che sintetica.
Sintesi[modifica | modifica wikitesto]
L'acido fumarico è stato preparato per la prima volta dall'acido succinico.[2] Una tradizionale via di sintesi prevede l'ossidazione del furfurale (ottenibile dalla trasformazione del mais) utilizzando un clorato in presenza di un catalizzatore a base di vanadio.[3] Attualmente, la sintesi industriale dell'acido fumarico è principalmente basata sull'isomerizzazione catalitica dell'acido maleico in soluzioni acquose a pH basso. Quest'ultimo è accessibile in grandi volumi come prodotto di idrolisi dell'anidride maleica, prodotta mediante ossidazione catalitica del benzene o del butano.[4]
Biologia[modifica | modifica wikitesto]
L'acido fumarico si trova nelle piante del genere fumaria (es.Fumaria officinalis), nei funghi porcini (in particolare nel Boletus fomentarius var. Pseudo-igniarius), nei licheni e nella Cetraria islandica.
Il fumarato, quindi la sua forma anionica, è un intermedio nel ciclo dell'acido citrico utilizzato dalle cellule per produrre energia sotto forma di adenosin trifosfato (ATP) da alimenti. Esso è formato dall'ossidazione da parte della succinato deidrogenasi del succinato. Poi il fumarato viene convertito dalla fumarasi a malato. La pelle umana produce naturalmente acido fumarico quando esposta alla luce solare.[5]
Utilizzi[modifica | modifica wikitesto]
Medicina[modifica | modifica wikitesto]
È utilizzato per il trattamento della psoriasi. Viene somministrato in dosi di 60–105 mg al giorno e può incrementare fino a 1290 mg. Inoltre è stato approvato per il trattamento della sclerosi multipla. Tra gli effetti collaterali vi possono essere disordini gastrointestinali e ai reni o arrossamento della pelle.
Industria alimentare[modifica | modifica wikitesto]
È utilizzato come stabilizzante di diversi prodotti e come regolatore di acidità in prodotti alimentari dal 1946, generalmente in sostituzione dell'acido tartarico e a volte, dell'acido citrico. È denotato con la sigla E297.[6]
Altri usi[modifica | modifica wikitesto]
L'acido fumarico è utilizzato nella fabbricazione di resine poliesteree e polialcoli e come mordente per i coloranti. Fin dai primi anni del XXI secolo è stato utilizzato per sintetizzare una delle prime strutture metallo-organiche che presentano applicazioni commerciali grazie alle sue notevoli proprietà meccaniche e di adsorbimento, in combinazione con una bassa tossicità rispetto ad altri MOFs ben studiati.[7]
Note[modifica | modifica wikitesto]
- ^ scheda dell'acido fumarico su IFA-GESTIS (archiviato dall'url originale il 16 ottobre 2019).
- ^ (EN) J. Volhard, Darstellung von Maleïnsäureanhydrid, in Justus Liebigs Annalen der Chemie, vol. 268, n. 1-2, 1º gennaio 1892, pp. 255–256, DOI:10.1002/jlac.18922680108/abstract. URL consultato il 30 giugno 2016.
- ^ Milas, N. A. "Fumaric Acid" Organic Synthesis 1943, Collective Volume 2, page 302. Online version (PDF).
- ^ British Patent No. 775,912, publicated on the May 29, 1957, by Monsanto Chemical Company.
- ^ Active Ingredients Used in Cosmetics: Safety Survey, Council of Europe. Committee of Experts on Cosmetic Products
- ^ Current EU approved additives and their E Numbers, su food.gov.uk.
- ^ (EN) Pascal G. Yot, Louis Vanduyfhuys e Elsa Alvarez, Mechanical energy storage performance of an aluminum fumarate metal–organic framework, in Chem. Sci., vol. 7, n. 1, 17 dicembre 2015, pp. 446–450, DOI:10.1039/c5sc02794b. URL consultato il 30 giugno 2016.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su acido fumarico
Wikimedia Commons contiene immagini o altri file su acido fumarico
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) fumaric acid / fumarate, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | GND (DE) 4155633-1 |
|---|