Acido α-parinarico
| Acido α-parinarico | |
|---|---|
 | |
| Nome IUPAC | |
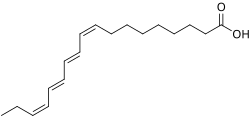
| Acido 9Z,11E,13E,15Z-octadecatrienoico | |
| Abbreviazioni | |
| 18:4Δ9c,11t,13t,15c | |
| Nomi alternativi | |
| Acido cis parinarico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C18H28O2 |
| Massa molecolare (u) | 276,413 |
| Numero CAS | |
| PubChem | 5460995 |
| SMILES | O=C(O)CCCCCCC/C=C\C=C\C=C\C=C/CC |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 85-86 °C |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | --- |
L'acido α-parinarico è un acido grasso coniugato omega 3 con 18 atomi di carbonio e 4 doppi legami in configurazione cis, trans, trans, cis, descritto in notazione delta come 18:4Δ9c,11t,13t,15c. Si può trovare tra i lipidi di origine vegetale in particolare nell'olio di semi di Impatiens balsamina (Balsaminaceae), che ne può contenere oltre il 30%, Sebastiana brasiliensis (Euphorbiaceae) (~20%), Parinarium laurinum o altre Chrysobalanaceae ( ~50%)[1][2][3]. Deve il suo nome alla sua scoperta nel 1933 da parte di Tsujimoto e Koyanagi nell'olio di Parinarium laurinu[4] L'alternanza di doppi legami coniugati conferisce all'acido α-parinarico una specifica fluorescenza che lo rende sfruttabile come sonda molecolare e negli studi sulle interazioni lipide-lipide[5][6][7] e proteina-lipide[8][9][10][11][12].
Biosintesi
[modifica | modifica wikitesto]Negli oli che contengono acido α-parinarico tipicamente si possono trovare anche alte concentrazioni di acido α- linolenico e/o suoi isomeri come l'acido α-eleostearico (18:3Δ9c,11t,13t)[13][14][15]. L'enzima responsabile per la creazione di 2 doppi legami coniugati al posto di un singolo doppio legame è chiamato coniugasi. Questo enzima è considerato una variante degli enzimi desaturasi[16].
Effetti sulla salute
[modifica | modifica wikitesto]Come per altri acidi grassi coniugati, all'acido α-parinarico viene attribuita un'attività antitumorale che si esprime con una specifica citotossicità verso le cellule tumorali della leucemia, del glioma[17][18][19].
Note
[modifica | modifica wikitesto]- ^ Gunstone, F.D e al., The Lipid Handbook, CRC Press, 2007, p. 11.
- ^ Cyberlipid: POLYENOIC FATTY ACIDS, su cyberlipid.org. URL consultato il 31 gennaio 2017 (archiviato dall'url originale il 30 settembre 2018).
- ^ Takagi T.,Itabashi Y., Lipids, vol. 16, p. 546.
- ^ Tsujimoto M, Koyanagi H. (1933). New unsaturated acid in the kernel oil of "akarittom", "Parinarium laurinum". I. Kogyo Kagaku Zasshi 36 (Suppl): 110–113.
- ^ Sklar LA, Hudson BS, Simoni RD, Conjugated polyene fatty acids as membrane probes: preliminary characterization, in Proc. Natl. Acad. Sci. U.S.A., vol. 72, n. 5, maggio 1975, pp. 1649-53, DOI:10.1073/pnas.72.5.1649, PMC 432600, PMID 1057769.
- ^ Rintoul DA, Simoni RD, Incorporation of a naturally occurring fluorescent fatty acid into lipids of cultured mammalian cells [collegamento interrotto], in J. Biol. Chem., vol. 252, n. 22, novembre 1977, pp. 7916-8, PMID 914848.
- ^ Harris WE, Stahl WL, Incorporation of cis-parinaric acid, a fluorescent fatty acid, into synaptosomal phospholipids by an acyl-CoA acyltransferase, in Biochim. Biophys. Acta, vol. 736, n. 1, dicembre 1983, pp. 79-91, DOI:10.1016/0005-2736(83)90172-4, PMID 6580918.
- ^ Sklar LA, Hudson BS, Simoni RD, Conjugated polyene fatty acids as fluorescent probes: binding to bovine serum albumin, in Biochemistry, vol. 16, n. 23, novembre 1977, pp. 5100-8, DOI:10.1021/bi00642a024, PMID 911814.
- ^ Berde CB, Hudson BS, Simoni RD, Sklar LA, Human serum albumin. Spectroscopic studies of binding and proximity relationships for fatty acids and bilirubin [collegamento interrotto], in J. Biol. Chem., vol. 254, n. 2, gennaio 1979, pp. 391-400, PMID 216673.
- ^ Keuper HJK, Klein RA, Spener F. (1985). Spectroscopic investigations on the binding site of bovine hepatic fatty-acid binding protein: evidence for the existence of a single binding site for two fatty-acid molecules. Chemistry and Physics of Lipids 38(1–2): 159–174.
- ^ Ben-Yashar V, Barenholz Y, Characterization of the core and surface of human plasma lipoproteins. A study based on the use of five fluorophores, in Chem. Phys. Lipids, vol. 60, n. 1, novembre 1991, pp. 1-14, DOI:10.1016/0009-3084(91)90009-Z, PMID 1813177.
- ^ Kasurinen J, van Paridon PA, Wirtz KW, Somerharju P, Affinity of phosphatidylcholine molecular species for the bovine phosphatidylcholine and phosphatidylinositol transfer proteins. Properties of the sn-1 and sn-2 acyl binding sites, in Biochemistry, vol. 29, n. 37, settembre 1990, pp. 8548-54, DOI:10.1021/bi00489a007, PMID 2271538.
- ^ Spitzer, V.Tomberg, W. Zucolotto, M., Identification of alpha-parinaric acid in the seed oil of Sebastiana brasiliensis Sprengel (Euphorbiaceae), in Journal J. Amer. Oil Chem. Soc., 1996, pp. 569-573.
- ^ Badami, R. C., Patil, K. B., Journal Prog. Lipid Res., vol. 19, pp. 119-153.
- ^ Tulloch, A. P., Journal Lipids, vol. 17, p. 544.
- ^ Cahoon EB, Carlson TJ, Ripp KG, Schweiger BJ, Cook GA, Hall SE, Kinney AJ, Biosynthetic origin of conjugated double bonds: production of fatty acid components of high-value drying oils in transgenic soybean embryos, in Proc. Natl. Acad. Sci. U.S.A., vol. 96, n. 22, ottobre 1999, pp. 12935-40, DOI:10.1073/pnas.96.22.12935, PMC 23170, PMID 10536026.
- ^ Cornelius AS, Yerram NR, Kratz DA, Spector AA, Cytotoxic effect of cis-parinaric acid in cultured malignant cells, in Cancer Res., vol. 51, n. 22, novembre 1991, pp. 6025-30, PMID 1933865.
- ^ Traynelis VC, Ryken TC, Cornelius AS, Cytotoxicity of cis-parinaric acid in cultured malignant gliomas [collegamento interrotto], in Neurosurgery, vol. 37, n. 3, settembre 1995, pp. 484-9, DOI:10.1097/00006123-199509000-00017, PMID 7501114.
- ^ Zaheer A, Sahu SK, Ryken TC, Traynelis VC, Cis-parinaric acid effects, cytotoxicity, c-Jun N-terminal protein kinase, forkhead transcription factor and Mn-SOD differentially in malignant and normal astrocytes, in Neurochem. Res., vol. 32, n. 1, gennaio 2007, pp. 115-24, DOI:10.1007/s11064-006-9236-2, PMID 17160503.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su acido α-parinarico
Wikimedia Commons contiene immagini o altri file su acido α-parinarico