Acido isopentadecanoico
| Acido isopentadecanoico | |
|---|---|
 | |
| Nome IUPAC | |
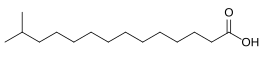
| acido 13-metiltetradecanoico | |
| Abbreviazioni | |
| i-15:0 ; 13-MTD ; 13-Me-14:0 | |
| Nomi alternativi | |
| acido 13-metiltetradecanoico; acido 13-metilmiristico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C15H30O2 |
| Numero CAS | |
| Numero EINECS | 636-731-2 |
| PubChem | 151014 |
| SMILES | CC(C)CCCCCCCCCCCC(=O)O |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| Frasi H | 315 - 319 - 335 - 413 |
| Consigli P | 261 - 264 - 271 - 273 - 280 - 302+352 - 304+340 - 305+351+338 - 312 - 321 - 332+313 - 337+313 - 362 - 403+233 |
L’acido isopentadecanoico o 13-metilmiristico o acido 13-metiltetradecanoico, è un acido grasso saturo metil-ramificato con un totale di 15 atomi di carbonio. È strutturalmente affine all'acido pentadecanoico. Presenta la struttura di un acido miristico con un gruppo metilico in posizione 13:
CH3-CH-(CH2)11-COOH
|
CH3
È presente nei gliceridi del latte dei ruminanti e dei suoi derivati lattiero-caseari, come il burro.[1][2] È biosintetizzato con successive condensazioni di Claisen con il malonil-CoA come cessore di C2, su un substrato di isovalerico-CoA da batteri presenti in particolare nei rumine di ruminanti, in una reazione complessiva che può essere scritta come:[3]:
Isovalerico-CoA + 5 malonil-CoA +10 NADPH + H+ → acido isopalmitico + 5 CO 2+ 10 NADP+ + 4H2O+ 6CoA.
Il percorso della sintesi degli acidi grassi a catena medio lunga ramificata de novo differisce solo nelle fasi iniziali da quello dell'acido grasso a catena lineare, l'acido palmitico, presente nella maggior parte degli organismi, per la presenza come substrato di un acido ramificato a catena corta come l'acido isovalerico.[4][5] Può essere rilevato nella soia fermentata, Natto in giapponese, prodotta con il metodo sviluppato dal prof. Jun Hanzawa.[6]
Alcune analisi lo avrebbero individuato nell'olio di semi di Balanites aegyptiacus (≈10%)[7] e di Grevillea robusta[8] e in alcuni pesci.[9]
È usato per studiare l'induzione dell'apoptosi mitocondriale mediata attraverso i percorsi AKT e Mitogen-activated protein kinases.[10][11] L'acido isopentadecanoico può essere un possibile integratore chemioterapico. Da varie ricerche viene riconosciuta la sua capacità di inibire le cellule cancerose attraverso l'apoptosi con livelli di tossicità e di effetti collaterali minimi.[10][11][12][13][14]
Note
[modifica | modifica wikitesto]- ^ (EN) R. P. Hansen, F. B. Shorland e N. June Cooke, The branched-chain fatty acids of butterfat. 4. The isolation of (+)-12-methyltetradecanoic acid and of 13-methyltetradecanoic acid, in Biochemical Journal, vol. 57, n. 2, 1º giugno 1954, pp. 297–301, DOI:10.1042/bj0570297. URL consultato il 3 febbraio 2020.
- ^ Bösze, Zsuzsanna., Bioactive components of milk, Springer, 2008, ISBN 978-0-387-74087-4, OCLC 233971409. URL consultato il 3 febbraio 2020.
- ^ T Kaneda, Iso- and anteiso-fatty acids in bacteria: biosynthesis, function, and taxonomic significance., in Microbiological Reviews, vol. 55, n. 2, 1991-06, pp. 288–302. URL consultato il 3 febbraio 2020.
- ^ Toshi Kaneda, BIOSYNTHESIS OF BRANCHED-CHAIN FATTY ACIDS: IV. FACTORS AFFECTING RELATIVE ABUNDANCE OF FATTY ACIDS PRODUCED BY BACILLUS SUBTILIS, in Canadian Journal of Microbiology, vol. 12, n. 3, 1º giugno 1966, pp. 501–514, DOI:10.1139/m66-073. URL consultato il 3 febbraio 2020.
- ^ (EN) Joseph P. Dewulf, Isabelle Gerin e Mark H. Rider, The synthesis of branched-chain fatty acids is limited by enzymatic decarboxylation of ethyl- and methylmalonyl-CoA, in Biochemical Journal, vol. 476, n. 16, 30 agosto 2019, pp. 2427–2447, DOI:10.1042/BCJ20190500. URL consultato il 3 febbraio 2020.
- ^ Hokkaidō daigaku daigakuin nōgaku kenkyūin. e 北海道大学大学院農学研究院., Agricultural Sciences for Human Sustainability : Meeting the Challenges of Food Safety and Stable Food Production, Kaiseisha, 2012, ISBN 978-4-86099-283-5, OCLC 798613711. URL consultato il 3 febbraio 2020.
- ^ S.S. El-Saadany, E.A. Abdel-Rahim e M.M. Wasif, Chemical and Physical Studies on Balanites aegyptiaca Oil Abdel-Rahim. Grasas y Aceites 37 81, in Grasas y Aceites, vol. 37, 1986-01, p. 81, DOI:10.1016/0308-8146(86)90054-3. URL consultato il 3 febbraio 2020.
- ^ J.R. Vickery, The fatty acid composition of the seed oils of proteaceae: A chemotaxonomic study, in Phytochemistry, vol. 10, n. 1, 1971-01, pp. 123–130, DOI:10.1016/s0031-9422(00)90259-0. URL consultato il 3 febbraio 2020.
- ^ Dong Hao Wang, James R. Jackson e Cornelia Twining, Saturated Branched Chain, Normal Odd-Carbon-Numbered, and n-3 (Omega-3) Polyunsaturated Fatty Acids in Freshwater Fish in the Northeastern United States, in Journal of Agricultural and Food Chemistry, vol. 64, n. 40, 4 ottobre 2016, pp. 7512–7519, DOI:10.1021/acs.jafc.6b03491. URL consultato il 3 febbraio 2020.
- ^ a b Qingqing Cai, Huiqiang Huang e Dong Qian, 13-Methyltetradecanoic Acid Exhibits Anti-Tumor Activity on T-Cell Lymphomas In Vitro and In Vivo by Down-Regulating p-AKT and Activating Caspase-3, in PLoS ONE, vol. 8, n. 6, 7 giugno 2013, DOI:10.1371/journal.pone.0065308. URL consultato il 3 febbraio 2020.
- ^ a b Albert H. Kim, Gus Khursigara e Xuan Sun, Akt Phosphorylates and Negatively Regulates Apoptosis Signal-Regulating Kinase 1, in Molecular and Cellular Biology, vol. 21, n. 3, 2001-2, pp. 893–901, DOI:10.1128/MCB.21.3.893-901.2001. URL consultato il 3 febbraio 2020.
- ^ (EN) Tianxin Lin, XinBao Yin e Qingqing Cai, 13-Methyltetradecanoic acid induces mitochondrial-mediated apoptosis in human bladder cancer cells, in Urologic Oncology: Seminars and Original Investigations, vol. 30, n. 3, 2012-05, pp. 339–345, DOI:10.1016/j.urolonc.2010.04.011. URL consultato il 3 febbraio 2020.
- ^ R. P. Hansen, F. B. Shorland e N. J. Cooke, The branched-chain fatty acids of mutton fat. 2. The isolation of (+)-12-methyltetradecanoic acid and of 13-methyltetradecanoic acid, in Biochemical Journal, vol. 53, n. 3, 1º febbraio 1953, pp. 374–379, DOI:10.1042/bj0530374. URL consultato il 3 febbraio 2020.
- ^ Roger A. Klein, David Halliday e Philippe G. Pittet, The use of 13-methyltetradecanoic acid as an indicator of adipose tissue turnover, in Lipids, vol. 15, n. 8, 1980-08, pp. 572–579, DOI:10.1007/bf02534181. URL consultato il 3 febbraio 2020.