Beclometasone
| Beclometasone | |
|---|---|
 | |
 | |
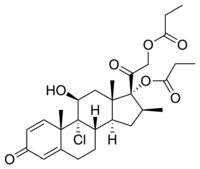
| Nome IUPAC | |
| (8S,9R,10S,11S,13S,14S,16S,17R)-9-cloro-11-idrossi-10,13,16-trimetil-3-osso-17-[2-(propionilossi)acetil]-6,7,8,9,10,11,12,13,14,15,16,17-dodecaidro-3H-ciclopenta[a]fenantren-17-ile propionato | |
| Nomi alternativi | |
| Clenil e altri | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C28H37ClO7 |
| Massa molecolare (u) | 521.042 g/mol |
| Numero CAS | |
| Numero EINECS | 226-886-0 |
| Codice ATC | A07 |
| PubChem | 21700 |
| DrugBank | DB00394 |
| SMILES | CCC(=O)OCC(=O)C1(C(CC2C1(CC(C3(C2CCC4=CC(=O)C=CC43C)Cl)O)C)C)OC(=O)CC |
| Dati farmacologici | |
| Categoria farmacoterapeutica | corticosteroidi, antinfiammatori |
| Modalità di somministrazione | nasale, topica, orale |
| Dati farmacocinetici | |
| Emivita | 2,8 ore |
| Escrezione | rettale |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | --- [1] |
Il beclometasone è un principio attivo utilizzato come antinfiammatorio steroideo, un derivato del cortisone appartenente alla classe dei glucocorticoidi. Trova impiego nella profilassi e nel trattamento dell'asma bronchiale, delle riniti allergiche e della rettocolite e proctosigmoidite ulcerosa. In clinica viene spesso utilizzato sotto forma di profarmaco, il beclometasone dipropionato. Si preferisce l'esterificazione con l'acido propionico in quanto la molecola vede un incremento della propria lipofilia, che ne facilita l'assorbimento da parte della mucosa nasale e, in generale, delle membrane fosfolipidiche. La molecola esterificata viene successivamente biotrasformata nell'organismo nella sua forma attiva, appunto il beclometasone.
Chimica[modifica | modifica wikitesto]
Si presenta come una polvere bianca inodore, poco solubile in acqua ma facilmente solubile in etanolo e acetone.
Farmacodinamica[modifica | modifica wikitesto]
Il beclometasone dipropionato è un corticosteroide di sintesi, caratterizzato da una scarsa attività mineralcorticoide, ma dotato di potente attività antinfiammatoria. La molecola, una volta oltrepassata la membrana cellulare, si lega a specifici recettori nel citoplasma. Il complesso recettore-farmaco muove verso il nucleo ove stimola la trascrizione di RNA e aumenta la sintesi di specifiche proteine. L'inalazione della molecola comporta una riduzione degli eosinofili e dei linfociti, venendo così a deprimere le reazioni ritardate agli allergeni. Il beclometasone agisce anche sulla sintesi delle immunoglobuline di tipo IgE (coinvolte nelle reazioni di ipersensibilità), determinandone una ridotta produzione. Inibisce inoltre il metabolismo dell'acido arachidonico, con conseguente riduzione di prostaglandine, prostacicline e leucotrieni, noti mediatori dell'infiammazione.[2]
Farmacocinetica[modifica | modifica wikitesto]
A seguito di inalazione di una dose solo una minima percentuale (20-25% circa) viene assorbita, mentre circa il 51–60% di una dose viene a depositarsi nel tratto respiratorio.[3] Il picco di concentrazione plasmatica viene raggiunto dopo circa 30 minuti - 1 ora dall'inalazione. Il miglioramento della sintomatologia si registra nell'arco di 24 ore. Per raggiungere il massimo del beneficio è necessario un periodo di trattamento variabile da 1 a 4 settimane. Nell'organismo il beclometasone è metabolizzato per via epatica tramite l'isoenzima CYP3A4. Il farmaco e i suoi metaboliti sono eliminati principalmente con le feci e in misura minore con le urine (meno del 10% della dose). Il legame con le proteine plasmatiche è pari all'87% circa. L'emivita della molecola è pari a 2,8 ore.
Usi clinici[modifica | modifica wikitesto]
Il beclometasone viene utilizzato per la profilassi dell'asma bronchiale, sia negli adulti sia nei bambini,[4] della rinite allergica e vasomotoria, del raffreddore da fieno e della sinusite. Trova impiego anche in altre condizioni di broncostenosi e perciò nella stessa broncopneumopatia cronica ostruttiva.[5][6] Impieghi off-label lo vedono utilizzato nel trattamento della stomatite aftosa e di alcune malattie della pelle come l'eczema, non rispondenti a steroidi meno potenti. È stato anche impiegato nella cura della psoriasi. In letteratura medica è segnalato il suo impiego per il trattamento della malattia di Crohn, della rettocolite ulcerosa e delle proctosigmoiditi, in fase di attività da lieve a moderata.[7][8][9]
Effetti collaterali e indesiderati[modifica | modifica wikitesto]
La somministrazione della molecola per aerosol può comportare la comparsa di candidosi del cavo orale o della faringe in circa il 5-14% dei pazienti. Questo effetto avverso sembra essere in relazione con la dose assunta. Il disturbo può essere minimizzato risciacquando regolarmente la bocca dopo ogni singola inalazione per eliminare la quantità di farmaco che si deposita in sede, inoltre risponde generalmente bene a un'adeguata terapia antimicotica topica. Raramente è necessario procedere all'interruzione del trattamento. Sono stati segnalati rari casi di candidosi esofagea.
L'assunzione del farmaco può comportare raucedine. Se la raucedine non si associa al mughetto orale è possibile che sia dovuta ad anomalie delle corde vocali dovute allo steroide. In alcuni casi la disfonia e le anomalie delle corde vocali persistono per mesi dopo l'interruzione del farmaco.
Alcuni soggetti possono accusare tosse e dispnea. Questi pazienti in genere beneficiano di un pretrattamento con un beta-agonista per via inalatoria prima della somministrazione di beclometasone.[10][11]
Altri disturbi psichiatrici quali cefalea, ansia, eccitazione, aggressività, agitazione psicomotoria, insonnia e altri disturbi del sonno, depressione, si riscontrano con minore frequenza. In alcuni casi è stata segnalata l'insorgenza di variazioni dell'umore, sintomi di psicosi e mania.[12][13][14] Per questo motivo è opportuno evitare di somministrare il farmaco nei pazienti con preesistente instabilità emotiva, disturbi di personalità e tendenze psicotiche.
In particolare nei soggetti anziani si è evidenziato il rischio d'insorgenza di porpora dopo uso di beclometasone, e tale evento incrementa all'aumentare dell'età del paziente, della dose e della durata del trattamento.[15][16][17]
Raramente il trattamento con beclometasone può comportare la soppressione dell'asse ipotalamo-ipofisi-surrene, in particolare nella popolazione pediatrica.[18][19][20][21] Il rischio di soppressione surrenale è inferiore a quello associato con l'uso di altri corticosteroidi sistemici e decisamente raro con dosi giornaliere di 2 mg o inferiori. L'uso di un distanziatore di grande volume sembra possa comportare una minimizzazione del rischio di soppressione surrenale quando la molecola viene inalata. In ogni caso durante il trattamento può essere opportuno valutare periodicamente la funzionalità dell'asse ipotalamo-ipofisario, ad esempio tramite l'esecuzione del test del cortisolo urinario libero e del test della stimolazione con ACTH. Il rischio di soppressione surrenalica è maggiore in caso di terapie a dosaggio elevato e/o prolungate nel tempo.[22]
La somministrazione di corticosteroidi, anche per via inalatoria, può influenzare la crescita lineare (in altezza) nel bambino. È noto che la somministrazione di corticosteroidi per via sistemica può provocare una riduzione definitiva della statura, con un rischio più importante nel caso di trattamenti a dosaggio elevato e per tempi prolungati.[23] La somministrazione di corticosteroidi per via inalatoria, in particolare di beclometasone dipropionato, comporta un ritardo nella crescita in altezza del bambino, che per altro non sembra pregiudicare il raggiungimento della statura finale anche con terapie a dosaggio elevato o durate superiori ai 3 anni.[24][25]
I corticosteroidi, incluso il beclometasone dipropionato, possono mascherare i segni di infezioni che possono insorgere durante il trattamento. Ciò è dovuto all'attività immunosoppressiva propria di queste molecole. Le infezioni che sembra possano svilupparsi con maggiore frequenza sono soprattutto le infezioni funginee (ad esempio da candida) e di tipo virale. Fra queste ultime le più comuni sono quelle sostenute da Herpes simplex o zoster (virus della varicella). Gli steroidi sono anche sospettati di poter causare una riattivazione di una pregressa infezione tubercolare.[26] Allo stato non è disponibile alcuna prova conclusiva che sostenga l'evidenza di un aumento di tubercolosi o infezioni virali in soggetti trattati con beclometasone per via inalatoria. Si segnala che uno studio indiano su 548 pazienti asmatici trattati con beclometasone ha dimostrato lo sviluppo di tubercolosi in otto soggetti. Due di questi che hanno accettato di riprendere l'uso dello steroide hanno sperimentato una riattivazione della tubercolosi entro due settimane dalla ripresa del trattamento.[27]
La somministrazione di beclometasone per via nasale o inalatoria può comportare la comparsa di corioretinopatia sierosa centrale.[28] Inoltre, in caso di infezioni oculari virali o fungine, si associa un aumentato rischio di perforazione della cornea.
La somministrazione di corticosteroidi, soprattutto se a dosaggi elevati e/o per terapie prolungate è stata associata a riduzione di massa ossea con aumentato rischio di fratture. Gli effetti sul metabolismo osseo dipendono dal tipo di corticosteroide somministrato. In letteratura esistono lavori discordanti che tendono a escludere effetti negativi sulla densità minerale ossea,[29][30] mentre altri suggeriscono che l'effetto sull'osso degli steroidi per via inalatoria non sia piccolo, specialmente nei soggetti che assumono dosaggi moderati o elevati per lunghi periodi di tempo.[31][32][33][34] In caso di osteoporosi da glucocorticoidi, i farmaci di prima linea sono rappresentati dai bifosfonati, mentre la somministrazione di vitamina D3 e di vitamina K2 rappresenta un intervento terapeutico di seconda linea.[35]
L'inalazione di beclometasone dipropionato teoricamente può provocare il diabete o un suo peggioramento per i suoi effetti iperglicemizzanti. Questo rischio di nuova insorgenza di diabete e di progressione di un disturbo preesistente appare piuttosto modesto, eventualmente associato solo a dosaggi di cortisonico estremamente elevati.[36][37][38] Molti lavori scientifici tendono invece a escludere una simile evenienza.[39][40] In ogni caso nei soggetti in trattamento con ipoglicemizzanti orali, si rende opportuno monitorare la glicemia, in particolare all'inizio e alla sospensione della terapia con beclometasone.[41] Gli stessi β2 agonisti selettivi, spesso associati alla terapia corticosteroidea nel trattamento dell'asma bronchiale (ad esempio beclometasone più salbutamolo o formoterolo), hanno un effetto iperglicemizzante in quanto stimolano la sintesi di glucosio nel fegato (gluconeogenesi epatica) e la conversione del glicogeno in glucosio (glicogenolisi epatica).
Alcuni studi sembrano indicare un'associazione tra l'uso prolungato di corticosteroidi per via inalatoria e il riscontro di una pressione intraoculare elevata in soggetti con una storia familiare positiva per glaucoma.[42][43][44][45][46]
Come avviene per altre sostanze medicamentose somministrate per via inalatoria, può manifestarsi broncospasmo paradosso, con aumento del respiro affannoso a distanza di pochi minuti dall'inalazione del farmaco. Nell'eventualità che si presenti questo effetto, è necessario interrompere immediatamente la terapia e assumere un broncodilatatore a rapida insorgenza d'azione.[47][48]
Controindicazioni[modifica | modifica wikitesto]
Il beclometasone è controindicato nei soggetti con ipersensibilità nota al principio attivo, oppure a uno qualsiasi degli eccipienti presenti nella formulazione farmaceutica.
Dosi terapeutiche[modifica | modifica wikitesto]
Per inalazione
- Adulti: 200 µg, 2 volte al giorno. In alternativa si utilizzano 100 µg 3-4 volte al giorno.
- Bambini: 50-100 µg 2 volte al giorno
Interazioni[modifica | modifica wikitesto]
- Farmaci β2 agonisti (salbutamolo, bitolterolo, procaterolo e altri): come è noto i farmaci β2 agonisti possono provocare ipokaliemia, pertanto l'associazione con beclometasone dipropionato deve essere somministrata con cautela nei soggetti a rischio di sviluppare ipokaliemia o nei pazienti con ipokaliemia non trattata. Basse concentrazioni plasmatiche di potassio sono favorite anche dall'ipossia, dalla somministrazione di diuretici o di derivati xantinici (ad esempio teofillina) oltre che da derivati steroidei.
- Fenitoina: la co-somministrazione può aumentare il metabolismo dello steroide.
- Carbamazepina: la co-somministrazione può determinare una diminuzione dei livelli plasmatici dello steroide.
- Rifampicina: la contemporanea assunzione con questo potente induttore di alcuni enzimi del citocromo P-450 può rendere necessario un aggiustamento del dosaggio dello steroide.
- Amfotericina B: la somministrazione con beclometasone può comportare l'insorgenza di ipokaliemia.
- Barbiturici (fenobarbital, secobarbital, primidone e altri): la co-somministrazione comporta una diminuzione di efficacia dello steroide per un aumento del suo catabolismo.
- Neostigmina, piridostigmina: in soggetti affetti da miastenia grave e in trattamento steroideo l'assunzione di queste molecole può determinare grave debolezza muscolare.
- Farmaci antinfiammatori non steroidei (FANS) e salicilati: la terapia di associazione aumenta il rischio di sanguinamenti a livello gastrointestinale,[49] e determina una riduzione delle concentrazioni ematiche di acido acetilsalicilico e derivati.
- Terapia anticoagulante (warfarin, acenocumarolo): i soggetti che ricevono terapia anticoagulante possono richiedere una modifica della dose di anticoagulante sia all'inizio sia alla sospensione del trattamento con corticosteroidi. Le interazioni con warfarin possono determinare sia diminuzione sia innalzamento dei valori di PT/INR, mentre acenocumarolo viene generalmente potenziato nel suo effetto anticoagulante. Per questo motivo in caso di impiego in combinazione con questi farmaci, devono essere eseguiti con maggiore frequenza i test di coagulazione.
- Vaccini vivi: è opportuno non somministrare beclometasone dipropionato a soggetti sottoposti a vaccinazione con vaccini vivi per il rischio di una insufficiente risposta anticorpale. Inoltre è possibile che la molecola comporti un'aumentata replicazione di alcuni organismi contenuti nei vaccini vivi attenuati.
Gravidanza e allattamento[modifica | modifica wikitesto]
Il beclometasone dipropionato non deve essere somministrato nel primo trimestre di gravidanza. Nei successivi trimestri può essere somministrato solo dopo un'attenta valutazione del rapporto rischio/beneficio. In vivo lo steroide è stato associato a tossicità embriofetale e a teratogenicità. La Food and Drug Administration (FDA) ha inserito il beclometasone dipropionato in classe C per l'uso in gravidanza. In questa classe sono inseriti i farmaci privi di studi controllati sulle donne ma i cui studi sugli animali hanno rilevato effetti dannosi sul feto (teratogenico, letale o altro), oppure i farmaci per i quali non sono disponibili studi né sull'uomo né sull'animale.[50][51]
È possibile che il beclometasone dipropionato sia escreto nel latte materno, similmente a quanto osservato per altre molecole corticosteroidi. È quindi necessario che il medico valuti con attenzione il rapporto rischio/beneficio prima di far assumere il composto a una donna che allatta al seno.
Avvertenze[modifica | modifica wikitesto]
Coronaropatie, ipertiroidismo, ipertensione arteriosa, glaucoma, feocromocitoma, ipertrofia prostatica: l'associazione beclometasone più salbutamolo (beta2-agonista a breve durata d'azione) deve essere somministrata solo in caso di necessità. I pazienti che presentano grave patologia cardiaca (cardiopatia ischemica, aritmia, insufficienza cardiaca) potrebbero manifestare tachicardia dopo somministrazione di salbutamolo con un peggioramento della patologia cardiaca sottostante. Il salbutamolo è stato associato, inoltre, in rari casi, a ischemia miocardica (segnalazione post-marketing). La comparsa di sintomi quali dolore al torace di tipo anginoso o dispnea deve essere prontamente segnalata.[52]
Doping: la somministrazione non terapeutica di beclometasone per via enterica (orale, rettale) o parenterale (intramuscolare, endovenosa) durante le gare sportive costituisce doping e può determinare positività ai test antidoping. L'uso di beclometasone per via inalatoria richiede una dichiarazione specifica da parte dell'atleta, mentre la somministrazione per via cutanea o nasale non è proibita e non richiede nessuna dichiarazione d'uso.[53]
Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. del 09.01.2013
- ^ RN. Brogden, RC. Heel; TM. Speight; GS. Avery, Beclomethasone dipropionate. A reappraisal of its pharmacodynamic properties and therapeutic efficacy after a decade of use in asthma and rhinitis., in Drugs, vol. 28, n. 2, Ago 1984, pp. 99-126, PMID 6381025.
- ^ P. Fireman, BM. Prenner; W. Vincken; M. Demedts; SJ. Mol; RM. Cohen, Long-term safety and efficacy of a chlorofluorocarbon-free beclomethasone dipropionate extrafine aerosol., in Ann Allergy Asthma Immunol, vol. 86, n. 5, Mag 2001, pp. 557-65, DOI:10.1016/S1081-1206(10)62905-5, PMID 11379808.
- ^ A. Nayak, R. Lanier; S. Weinstein; P. Stampone; M. Welch, Efficacy and safety of beclomethasone dipropionate extrafine aerosol in childhood asthma: a 12-week, randomized, double-blind, placebo-controlled study., in Chest, vol. 122, n. 6, Dic 2002, pp. 1956-65, PMID 12475833.
- ^ AS. Robertson, RI. Gove; GA. Wieland; PS. Burge, A double-blind comparison of oral prednisolone 40 mg/day with inhaled beclomethasone dipropionate 1500 ug/day in patients with adult onset chronic obstructive airways disease., in Eur J Respir Dis Suppl, vol. 146, 1986, pp. 565-9, PMID 3465581.
- ^ CS. Shim, MH. Williams, Aerosol beclomethasone in patients with steroid-responsive chronic obstructive pulmonary disease., in Am J Med, vol. 78, n. 4, aprile 1985, pp. 655-8, PMID 3985039.
- ^ R. Arcidiacono, G. Zanasi; Z. Pirone; M. Borzio; F. Borzio; G. Milano; L. Cestari; P. Ravelli; C. Terraroli; R. de Franchis; M. Vecchi, [The topical therapy of ulcerative colitis. A multicenter study with beclomethasone dipropionate foam]., in Minerva Chir, vol. 54, n. 9, Set 1999, pp. 635-44, PMID 10549210.
- ^ M. Borzio, F. Borzio; G. Milano; M. Biraghi; L. Cestari; P. Ravelli; R. de Franchis; M. Vecchi; G. Minoli; A. Prada; M. Curzio, [Topical beclomethasone dipropionate (BDP) in intestinal inflammatory diseases: the results of a multicentre trial]., in Minerva Gastroenterol Dietol, vol. 45, n. 1, marzo 1999, pp. 59-73, PMID 16498317.
- ^ F. Fascì Spurio, A. Aratari; G. Margagnoni; MT. Doddato; F. Chiesara; C. Papi, Oral beclomethasone dipropionate: a critical review of its use in the management of ulcerative colitis and Crohn's disease., in Curr Clin Pharmacol, vol. 7, n. 2, Mag 2012, pp. 131-6, PMID 22432845.
- ^ C. Shim, MH. Williams, Cough and wheezing from beclomethasone aerosol., in Chest, vol. 91, n. 2, febbraio 1987, pp. 207-9, PMID 3802930.
- ^ CS. Shim, MH. Williams, Cough and wheezing from beclomethasone dipropionate aerosol are absent after triamcinolone acetonide., in Ann Intern Med, vol. 106, n. 5, Mag 1987, pp. 700-3, PMID 3565967.
- ^ MC. Phelan, Beclomethasone mania., in Br J Psychiatry, vol. 155, Dic 1989, pp. 871-2, PMID 2620226.
- ^ ET. Goldstein, SH. Preskorn, Mania triggered by a steroid nasal spray in a patient with stable bipolar disorder., in Am J Psychiatry, vol. 146, n. 8, Ago 1989, pp. 1076-7, PMID 2750983.
- ^ L. Ganzini, SB. Millar; JR. Walsh, Drug-induced mania in the elderly., in Drugs Aging, vol. 3, n. 5, Set-Ott 1993, pp. 428-35, PMID 8241607.
- ^ S. Capewell, S. Reynolds; D. Shuttleworth; C. Edwards; AY. Finlay, Purpura and dermal thinning associated with high dose inhaled corticosteroids., in BMJ, vol. 300, n. 6739, Giu 1990, pp. 1548-51, PMID 2372620.
- ^ K. Mase, [Corticosteroid purpura]., in Ryoikibetsu Shokogun Shirizu, 21 Pt 2, 1998, pp. 403-4, PMID 9833526.
- ^ DL. Maxwell, J. Webb, Adverse effects of inhaled corticosteroids., in BMJ, vol. 298, n. 6676, marzo 1989, pp. 827-8, PMID 2496872.
- ^ CM. Law, JL. Marchant; JW. Honour; MA. Preece; JO. Warner, Nocturnal adrenal suppression in asthmatic children taking inhaled beclomethasone dipropionate., in Lancet, vol. 1, n. 8487, aprile 1986, pp. 942-4, PMID 2871242.
- ^ S. Sorkin, D. Warren, Probable adrenal suppression from intranasal beclomethasone., in J Fam Pract, vol. 22, n. 5, Mag 1986, pp. 449-50, PMID 2422315.
- ^ HM. Brown, Nocturnal adrenal suppression in children inhaling beclomethasone dipropionate., in Lancet, vol. 1, n. 8492, Mag 1986, pp. 1269, PMID 2872406.
- ^ CM. Law, MA. Preece; JO. Warner, Nocturnal adrenal suppression in children inhaling beclomethasone dipropionate., in Lancet, vol. 1, n. 8545, Giu 1987, pp. 1321, PMID 2884442.
- ^ RS. Francis, Adrenocortical function during high-dose beclomethasone aerosol therapy., in Clin Allergy, vol. 14, n. 1, gennaio 1984, pp. 49-53, PMID 6697473.
- ^ SD. Shenoy, SD. Shenoy; PG. Swift; D. Cody, Growth impairment and adrenal suppression on low-dose inhaled beclomethasone., in J Paediatr Child Health, vol. 42, n. 3, marzo 2006, pp. 143-4, DOI:10.1111/j.1440-1754.2006.00814.x, PMID 16509916.
- ^ DB. Allen, M. Mullen; B. Mullen, A meta-analysis of the effect of oral and inhaled corticosteroids on growth., in J Allergy Clin Immunol, vol. 93, n. 6, Giu 1994, pp. 967-76, PMID 8006318.
- ^ D. Skoner, Update of growth effects of inhaled and intranasal corticosteroids., in Curr Opin Allergy Clin Immunol, vol. 2, n. 1, febbraio 2002, pp. 7-10, PMID 11964744.
- ^ AB. Dey, Corticosteroid inhalers and pulmonary tuberculosis., in Natl Med J India, vol. 6, n. 1, Gen-Feb 1993, pp. 23-4, PMID 8453357.
- ^ WA. Shaikh, Pulmonary tuberculosis in patients treated with inhaled beclomethasone., in Allergy, vol. 47, 4 Pt 1, Ago 1992, pp. 327-30, PMID 1443454.
- ^ R. Haimovici, ES. Gragoudas; JS. Duker; RN. Sjaarda; D. Eliott, Central serous chorioretinopathy associated with inhaled or intranasal corticosteroids., in Ophthalmology, vol. 104, n. 10, Ott 1997, pp. 1653-60, PMID 9331207.
- ^ H. Luo, Q. Tan; G. Zhang; S. Liu; N. Yan; H. Jiang; P. Zeng; J. Liang; P. Wang, [Effects of long term use of beclomethasone dipropionate nasal spray on bone density with perennial allergic rhinitis]., in Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, vol. 22, n. 2, gennaio 2008, pp. 52-4, PMID 18422164.
- ^ KS. Ben Hamida, N. Fajraoui Krichene; K. Ben Ghars Amara; R. Haouachi; H. Sahli; S. Sellami; MR. Charfi; B. Zouari, [Effect of inhaled corticosteroids on bone mineral density in asthmatic adults: a 20 cases study]., in Tunis Med, vol. 89, n. 5, Mag 2011, pp. 434-9, PMID 21557179.
- ^ KJ. Mortimer, TW. Harrison; AE. Tattersfield, Effects of inhaled corticosteroids on bone., in Ann Allergy Asthma Immunol, vol. 94, n. 1, gennaio 2005, pp. 15-21; quiz 22-3, 79, DOI:10.1016/S1081-1206(10)61280-X, PMID 15702810.
- ^ Y. Ieda, Y. Nagasaka, [Secondary osteoporosis: Inhaled corticosteroids induced osteoporosis in respiratory diseases]., in Clin Calcium, vol. 17, n. 6, Giu 2007, pp. 955-62, PMID 17548937.
- ^ S. Muraki, N. Yoshimura, [Steroids as a risk factor for osteoporotic fracture]., in Clin Calcium, vol. 16, n. 11, novembre 2006, pp. 1797-1803, PMID 17079845.
- ^ S. Wada, S. Kamiya; T. Fukawa, [Management of osteoporosis in patients with inhaled glucocorticoids]., in Clin Calcium, vol. 16, n. 11, novembre 2006, pp. 1871-77, PMID 17079855.
- ^ H. Nawata, S. Soen; R. Takayanagi; I. Tanaka; K. Takaoka; M. Fukunaga; T. Matsumoto; Y. Suzuki; H. Tanaka; S. Fujiwara; T. Miki, Guidelines on the management and treatment of glucocorticoid-induced osteoporosis of the Japanese Society for Bone and Mineral Research (2004)., in J Bone Miner Metab, vol. 23, n. 2, 2005, pp. 105-9, DOI:10.1007/s00774-004-0596-x, PMID 15750687.
- ^ S. Suissa, A. Kezouh; P. Ernst, Inhaled corticosteroids and the risks of diabetes onset and progression., in Am J Med, vol. 123, n. 11, novembre 2010, pp. 1001-6, DOI:10.1016/j.amjmed.2010.06.019, PMID 20870201.
- ^ P. Ernst, S. Suissa, Systemic effects of inhaled corticosteroids., in Curr Opin Pulm Med, vol. 18, n. 1, gennaio 2012, pp. 85-9, DOI:10.1097/MCP.0b013e32834dc51a, PMID 22112998.
- ^ CG. Slatore, CL. Bryson; DH. Au, The association of inhaled corticosteroid use with serum glucose concentration in a large cohort., in Am J Med, vol. 122, n. 5, Mag 2009, pp. 472-8, DOI:10.1016/j.amjmed.2008.09.048, PMID 19375557.
- ^ PM. O'Byrne, S. Rennard; H. Gerstein; F. Radner; S. Peterson; B. Lindberg; LG. Carlsson; DD. Sin, Risk of new onset diabetes mellitus in patients with asthma or COPD taking inhaled corticosteroids., in Respir Med, vol. 106, n. 11, novembre 2012, pp. 1487-93, DOI:10.1016/j.rmed.2012.07.011, PMID 22902134.
- ^ N. Dendukuri, L. Blais; J. LeLorier, Inhaled corticosteroids and the risk of diabetes among the elderly., in Br J Clin Pharmacol, vol. 54, n. 1, Lug 2002, pp. 59-64, PMID 12100226.
- ^ JL. Faul, SR. Wilson; JW. Chu; J. Canfield; WG. Kuschner, The effect of an inhaled corticosteroid on glucose control in type 2 diabetes., in Clin Med Res, vol. 7, n. 1-2, Giu 2009, pp. 14-20, DOI:10.3121/cmr.2009.824, PMID 19251584.
- ^ EB. Dreyer, Inhaled steroid use and glaucoma., in N Engl J Med, vol. 329, n. 24, dicembre 1993, pp. 1822, DOI:10.1056/NEJM199312093292421, PMID 8232507.
- ^ GA. Friday, Inhaled and nasal glucocorticoids and the risks of ocular hypertension or open-angle glaucoma., in Clin Pediatr (Phila), vol. 36, n. 9, Set 1997, pp. 551, PMID 9307092.
- ^ N. Macris, Glucocorticoid use and risks of ocular hypertension and glaucoma., in JAMA, vol. 277, n. 24, Giu 1997, pp. 1929; author reply 1930, PMID 9200624.
- ^ E. Garbe, J. LeLorier; JF. Boivin; S. Suissa, Inhaled and nasal glucocorticoids and the risks of ocular hypertension or open-angle glaucoma., in JAMA, vol. 277, n. 9, marzo 1997, pp. 722-7, PMID 9042844.
- ^ P. Mitchell, RG. Cumming; DA. Mackey, Inhaled corticosteroids, family history, and risk of glaucoma., in Ophthalmology, vol. 106, n. 12, Dic 1999, pp. 2301-6, DOI:10.1016/S0161-6420(99)90530-4, PMID 10599661.
- ^ G. Facchini, L. Antonicelli; B. Cinti; F. Bonifazi; V. Massei, Paradoxical bronchospasm and cutaneous rash after metered-dose inhaled bronchodilators., in Monaldi Arch Chest Dis, vol. 51, n. 3, Giu 1996, pp. 201-3, PMID 8766194.
- ^ RE. Ruffin, DA. Campbell; MM. Chia, Post-inhalation bronchoconstriction by beclomethasone dipropionate: a comparison of two different CFC propellant formulations in asthmatics., in Respirology, vol. 5, n. 2, Giu 2000, pp. 125-31, PMID 10894101.
- ^ M. Kusunoki, K. Miyake; C. Sakamoto, [Risk factors and comorbidities for NSAID associated ulcer]., in Nihon Rinsho, vol. 65, n. 10, OTt 2007, pp. 1781-7, PMID 17926524.
- ^ Onyeka Otugo, Olabode Ogundare, Christopher Vaughan, Emmanuel Fadiran, Leyla Sahin, Consistency of Pregnancy Labeling Across Different Therapeutic Classes (PDF), su fda.gov, Food and Drug Administration - Office of Women’s Health, 1979. URL consultato il 27 giugno 2013.
- ^ R. Sannerstedt, P. Lundborg; BR. Danielsson; I. Kihlström; G. Alván; B. Prame; E. Ridley, Drugs during pregnancy: an issue of risk classification and information to prescribers., in Drug Saf, vol. 14, n. 2, febbraio 1996, pp. 69-77, PMID 8852521.
- ^ AIFA, Nota informativa del 16/5/2007
- ^ WADA: Codice Mondiale Antidoping - Lista delle sostanze e dei metodi proibiti, 2009, disponibile on line www.iss.it
Bibliografia[modifica | modifica wikitesto]
- British national formulary, Guida all’uso dei farmaci 4ª edizione, Lavis, agenzia italiana del farmaco, 2007.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su beclometasone
Wikimedia Commons contiene immagini o altri file su beclometasone