Cloruro di acetile
| Cloruro di acetile | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| cloruro di etanoile | |
| Nomi alternativi | |
| acetocloruro
cloruro dell'acido acetico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H3ClO |
| Massa molecolare (u) | 78,5 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 200-865-6 |
| PubChem | 6367 |
| DrugBank | DB14623 |
| SMILES | CC(=O)Cl |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,1 |
| Solubilità in acqua | reazione energica |
| Temperatura di fusione | −112 °C (161 K) |
| Temperatura di ebollizione | 52 °C (325 K) |
| Tensione di vapore (Pa) a 293 K | 32000 |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −272,9 |
| ΔfG0 (kJ·mol−1) | −208 |
| S0m(J·K−1mol−1) | 200,8 |
| C0p,m(J·K−1mol−1) | 117 |
| Indicazioni di sicurezza | |
| Punto di fiamma | 4 °C (277 K) |
| Limiti di esplosione | 7,3 - 19% vol. |
| Temperatura di autoignizione | 390 °C (663 K) |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 225 - 314 - EUH014 |
| Consigli P | 210 - 280 - 301+330+331 - 305+351+338 - 309+310 [1] |
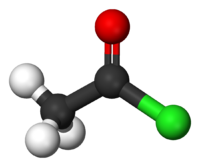
Il cloruro di acetile è un alogenuro acilico, di formula molecolare CH3COCl; può essere assimilato ad una anidride mista tra acido acetico e acido cloridrico.
A temperatura e pressione ambiente è un liquido incolore che reagisce in maniera violenta con l'acqua, idrolizzandosi nei due acidi sopra menzionati. Per questo è un composto irritante e corrosivo e va manipolato con attenzione, sotto cappa.
Viene prodotto per reazione tra l'acido acetico ed il cloruro di tionile
e trova impiego come reagente per condurre reazioni di acetilazione, ovvero di inserimento di un gruppo acetile, CH3CO-, su una molecola organica.
Esempi di acetilazione possono essere trovati nell'esterificazione e nella reazione di Friedel-Crafts acilica.
Note[modifica | modifica wikitesto]
- ^ scheda della sostanza su IFA-GESTIS
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Cloruro di acetile
Wikimedia Commons contiene immagini o altri file su Cloruro di acetile
| Controllo di autorità | GND (DE) 4326984-9 |
|---|
