Clorobenzene
| Clorobenzene | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | |
| benzene cloruro | |
| Abbreviazioni | |
| Ph-Cl | |
| Nomi alternativi | |
| clorobenzolo fenilcloruro | |
| Caratteristiche generali | |
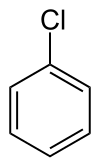
| Formula bruta o molecolare | C6H5Cl |
| Massa molecolare (u) | 112,6 g/mol |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 203-628-5 |
| PubChem | 7964 |
| SMILES | C1=CC=C(C=C1)Cl |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,11 (20 °C) |
| Solubilità in acqua | 0,05 g /100 ml (20 °C) |
| Temperatura di fusione | −45 °C (228 K) |
| Temperatura di ebollizione | 132 °C (405 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
  
| |
| attenzione | |
| Frasi H | 226 - 332 - 411 |
| Consigli P | 273 [1] |
Il clorobenzene (o benzene cloruro) è un composto chimico derivante dal benzene, dove un atomo di idrogeno è sostituito da un atomo di cloro. La sua formula chimica è C6H5Cl.
A temperatura ambiente si presenta come un liquido incolore dall'odore caratteristico; è infiammabile.
Produzione[modifica | modifica wikitesto]
Il clorobenzene viene prodotto principalmente dalle industrie chimiche dove, specie in passato, era utilizzato come intermedio nella sintesi di pesticidi clorurati, come il celebre DDT (dicloro-difenil-tricloroetano) ; tuttora è utilizzato come solvente per la produzione di erbicidi, adesivi, vernici e come reagente di sintesi per altre sostanze.
Altra fonte di origine del clorobenzene è, nell'ambito dell'incenerimento dei rifiuti, la combustione incompleta di sostanze clorurate (PVC, plastiche, ecc.).
Tossicità[modifica | modifica wikitesto]
Il clorobenzene è nocivo e molto pericoloso per l'ambiente, soprattutto per gli organismi acquatici; può essere assorbito dall'organismo per l'inalazione dei suoi vapori, attraverso la cute e per ingestione. Irrita in modo particolare gli occhi e la cute mentre, se inalato, può portare gravi danni ai polmoni (polmonite chimica), al sistema nervoso centrale, al fegato e ai reni.
È riconosciuto come cancerogeno per gli animali, mentre non c'è un dato preciso per l'uomo.

Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. del 12.12.2012
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su clorobenzene
Wikimedia Commons contiene immagini o altri file su clorobenzene
Collegamenti esterni[modifica | modifica wikitesto]
| Controllo di autorità | GND (DE) 4268618-0 · NDL (EN, JA) 01116563 |
|---|