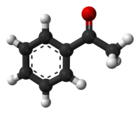
Acetofenone
| Acetofenone | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| 1-feniletanone | |
| Nomi alternativi | |
| fenil metil chetone | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C8H8O |
| Massa molecolare (u) | 120,15 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 202-708-7 |
| PubChem | 7410 |
| DrugBank | DB04619 |
| SMILES | CC(=O)C1=CC=CC=C1 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,03 g/mL |
| Solubilità in acqua | 6,9 g/L a 25 °C |
| Temperatura di fusione | 20 °C (293,15 K) |
| Temperatura di ebollizione | 202 °C (475 K) |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 815 mg/kg (ratto, orale) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 77 °C (350 K) |
| Temperatura di autoignizione | 535 °C |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 - 319 |
| Consigli P | 305+351+338 [1] |
L'acetofenone è il composto organico di formula C6H5C(O)CH3. È il più semplice chetone aromatico. È un liquido viscoso incolore (fonde a 20 °C), usato principalmente per la sintesi di resine e fragranze.[2]
Sintesi[modifica | modifica wikitesto]
L'acetofenone può essere ottenuto in vari modi.
Un metodo non industriale prevede una acilazione di Friedel-Crafts tra benzene e anidride acetica.
Industrialmente si recupera come sottoprodotto dell'ossidazione dell'etilbenzene, che forma principalmente l'idroperossido usato nella produzione di ossido di propilene[2]; dalla decomposizione selettiva dell'isopropilbenzene del processo di Hock (catalizzata da Cu(NO3)2) oppure come sottoprodotto dello stesso[3].
Usi[modifica | modifica wikitesto]
Precursore di resine[modifica | modifica wikitesto]
L'acetofenone è usato assieme a formaldeide e ad una base per produrre resine importanti dal punto di vista commerciale. I polimeri ottenuti sono convenzionalmente descritti con la formula [(C6H5C(O)CH]x(CH2)x}n, dato che derivano da una condensazione aldolica. Queste sostanze sono componenti utilizzati in film e inchiostri. Modificando per idrogenazione le resine chetoniche precedentemente menzionate si ottengono resine acetofenone-formaldeide modificate. I polioli risultanti possono essere ulteriormente reticolati con isocianati.[2] Queste resine modificate si trovano in film, inchiostri e adesivi.
Precursore dello stirene[modifica | modifica wikitesto]
Nei laboratori didattici, l'acetofenone viene convertito in stirene in un processo di due stadi che illustra la riduzione dei carbonili e la disidratazione degli alcoli:
Un processo analogo è usato industrialmente, ma lo stadio di idrogenazione a 1-feniletanolo è condotto su un catalizzatore di rame.[2]
Usi in campo farmaceutico e simili[modifica | modifica wikitesto]
L'acetofenone è usato come materia prima nella sintesi di alcuni prodotti farmaceutici[4][5] ed è anche un eccipiente approvato dalla Food and Drug Administration degli Stati Uniti.[6] In un rapporto del 1994 pubblicato da cinque compagnie statunitensi produttrici di sigarette, l'acetofenone è elencato come uno dei 599 additivi utilizzati nelle sigarette.[7]
Utilizzi minori[modifica | modifica wikitesto]
L'acetofenone viene utilizzato per creare fragranze che assomigliano a mandorla, ciliegia, caprifoglio, gelsomino e fragola. Viene utilizzato nella gomma da masticare.[8] Essendo prochirale, l'acetofenone è anche un substrato di prova comunemente usato negli esperimenti di trasferimento asimmetrico di idrogeno. L'acetofenone è anche usato come aromatizzante in molte bevande e dolci al sapore di ciliegia, dato che costa molto meno e dà risultati soddisfacenti per i consumatori.
Farmacologia[modifica | modifica wikitesto]
L'acetofenone è stato usato in medicina tra la fine del XIX secolo e l'inizio del XX secolo. Era commercializzato come ipnotico e anticonvulsivante con il nome di Hypnone. La dose tipica era 0,12–0,30 millilitri.[9] L'effetto sedativo era considerato superiore a quello della paraldeide e dell'idrato di cloralio.[10] Nell'uomo l'acetofenone è metabolizzato ad acido benzoico, acido carbonico e acetone.[11]
Presenza in natura[modifica | modifica wikitesto]
L'acetofenone si trova in natura in molti alimenti tra cui mele, formaggi, albicocche, banane, carne di manzo e cavolfiori.[12]
Sicurezza[modifica | modifica wikitesto]
L'acetofenone è nocivo per ingestione e molto irritante per gli occhi. Non ci sono dati che indichino proprietà cancerogene.[13]
Note[modifica | modifica wikitesto]
- ^ Scheda dell'acetofenone su IFA GESTIS, su gestis-en.itrust.de.
- ^ a b c d Siegel e Eggersdorfer 2002
- ^ (EN) Hardo Siegel e Manfred Eggersdorfer, Ullmann's Encyclopedia of Industrial Chemistry, American Cancer Society, DOI:10.1002/14356007.a15_077. URL consultato il 17 aprile 2018.
- ^ Sittig 1988, pp. 39, 177.
- ^ Gadamasetti e Braish 2007, pp. 142–145.
- ^ Inactive Ingredients in FDA Approved Drugs
- ^ T. Martin, What's in a cigarette?, su quitsmoking.about.com. URL consultato il 20-9-201 (archiviato dall'url originale il 23 maggio 2006).
- ^ Burdock 2004, p. 15.
- ^ Bartholow 1908
- ^ Norman 1887
- ^ Autore sconosciuto 1885
- ^ The Merck Index, 12ª Edizione
- ^ Alfa Aesar, Scheda di sicurezza dell'acetofenone (PDF), su alfa.com. URL consultato il 20 settembre 2011.
Bibliografia[modifica | modifica wikitesto]
- H. Siegel, M. Eggersdorfer, Ketones, in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, 2002, DOI:10.1002/14356007.a15_077.
- M. Sittig, Pharmaceutical Manufacturing Encyclopedia, Andrew, 1988, ISBN 978-0-8155-1144-1.
- K. Gadamasetti, T. Braish, Process Chemistry in the Pharmaceutical Industry, vol. 2, CRC Press, 2007, ISBN 978-0-8493-9051-7.
- G. A. Burdock, Fenaroli's Handbook of Flavor Ingredients, 5ª ed., CRC Press, 2004, ISBN 978-0-8493-3034-6.
- R. Bartholow, A Practical Treatise On Materia Medica And Therapeutics, 1908, Appleton & Co, 1891.
- C. Norman, Cases illustrating the sedative effects of aceto-phenone, in Journal of Mental Science, vol. 32, 1887, pp. 519–525, DOI:10.1192/bjp.32.140.519. URL consultato il 20 settembre 2011.
- Hypnone - The new hypnotic, in J Am Med Assoc., vol. 23, 1885, p. 632, DOI:10.1001/jama.1885.02391220016006. URL consultato il 20 settembre 2011.
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «acetofenone»
Wikizionario contiene il lemma di dizionario «acetofenone» Wikimedia Commons contiene immagini o altri file su acetofenone
Wikimedia Commons contiene immagini o altri file su acetofenone
| Controllo di autorità | Thesaurus BNCF 17618 · LCCN (EN) sh2005002607 · GND (DE) 4141249-7 · J9U (EN, HE) 987007547017505171 |
|---|

