Malattia di Crohn
| Malattia di Crohn | |
|---|---|
 | |
| Specialità | gastroenterologia |
| Classificazione e risorse esterne (EN) | |
| OMIM | 266600 |
| MeSH | D003424 |
| MedlinePlus | 000249 |
| eMedicine | 172940, 928288 e 367666 |
| Sinonimi | |
| Enterite regionale | |
| Eponimi | |
| Burrill Bernard Crohn | |
La malattia di Crohn o morbo di Crohn, nota anche come enterite regionale, è una malattia infiammatoria cronica dell'intestino (MICI) che può colpire qualsiasi parte del tratto gastrointestinale, dalla bocca all'ano, provocando una vasta gamma di sintomi. Essa causa principalmente dolori addominali, diarrea (che può anche essere ematica se l'infiammazione è importante), vomito o perdita di peso[1][2][3], ma può anche causare complicazioni in altri organi e apparati, come eruzioni cutanee, artriti, infiammazione degli occhi, stanchezza e mancanza di concentrazione[1].
La malattia di Crohn è considerata una malattia autoimmune, in cui il sistema immunitario aggredisce il tratto gastrointestinale provocando l'infiammazione, anche se viene classificata come un tipo particolare di patologia infiammatoria intestinale. Ci sono prove di una predisposizione genetica per la malattia e questo porta a considerare gli individui con fratelli ammalati tra gli individui ad alto rischio[4]. La malattia di Crohn tende a presentarsi inizialmente negli adolescenti e nei ventenni, con un altro picco di incidenza tra i cinquanta e i settant'anni, anche se la malattia può manifestarsi a qualsiasi età[1][5].
Non esiste ancora una terapia farmacologica risolutiva o una terapia chirurgica eradicante per la malattia di Crohn[6]. Le possibilità di trattamento sono limitate al controllo dei sintomi, al mantenimento della remissione e alla prevenzione delle ricadute.
La malattia prende il nome dal gastroenterologo statunitense Burrill Bernard Crohn, che nel 1932, insieme a due colleghi, ha descritto per primo una serie di pazienti con infiammazione dell'ileo terminale, solitamente la zona più colpita dalla malattia[7]. Per questo motivo, la malattia è stata anche chiamata ileite regionale[7] o enterite regionale.
Classificazione[modifica | modifica wikitesto]

La malattia di Crohn è un tipo di malattia infiammatoria cronica intestinale (MICI). Si manifesta solitamente nel tratto gastrointestinale e può essere classificata in base alla regione specifica colpita. Nel 50% dei casi viene classificata come ileocolica di Crohn e colpisce l'ileo (l'ultima parte dell'intestino tenue che si collega all'intestino crasso) e l'intestino crasso. Nel 30% di essi prende il nome di ileite di Crohn, manifestandosi solo nell'ileo, mentre nel restante 20% colpisce esclusivamente l'intestino crasso, chiamandosi colite di Crohn e può risultare particolarmente difficile da distinguersi dalla colite ulcerosa.
La malattia di Crohn gastroduodenale causa l'infiammazione allo stomaco e alla prima parte dell'intestino tenue, chiamata duodeno. La malattia può attaccare qualsiasi parte del tratto digerente, dalla bocca all'ano. Tuttavia, gli individui colpiti dalla malattia raramente escono al di fuori di queste tre classificazioni[1].
La malattia di Crohn può essere anche classificata in base al suo comportamento in fase di progressione. Questa classificazione prende il nome di "classificazione di Vienna"[8]. La malattia può presentarsi in tre categorie diverse: stenosante, penetrante e infiammatoria. La tipologia stenosante provoca un restringimento dei visceri che può portare ad una occlusione intestinale o alla modifica delle dimensioni delle feci. La malattia penetrante crea dei passaggi anomali (fistole) tra l'intestino e le altre strutture, come la pelle. La tipologia infiammatoria causa l'infiammazione senza causare stenosi o fistole[8][9].
Storia[modifica | modifica wikitesto]
Nel 1932 fu descritta per la prima volta l'ileite segmentaria, ritenuta una malattia dell'ileo, dal dottor Burrill Bernard Crohn, che tenne una conferenza a New Orleans, insieme ai suoi collaboratori Leon Ginzburg, e Gordon Oppenheimer al congresso dell'American Medical Association. Tale malattia era localizzata nella parte finale dell'ileo, tanto da essere chiamata anche ileite terminale.
In seguito alla descrizione di numerosi casi, divenne evidente che la localizzazione ileale è preponderante ma non esclusiva, pertanto la malattia fu ribattezzata in onore del più importante fra gli scopritori.
Epidemiologia[modifica | modifica wikitesto]
La malattia di Crohn è diffusa in tutto il mondo e raggiunge la massima prevalenza nelle nazioni occidentali. Il rapporto tra femmine e maschi colpiti è intorno a 1,35:1. I fumatori presentano due volte di più la probabilità di sviluppare la malattia di Crohn rispetto ai non fumatori[10]. La malattia di Crohn colpisce tra le 400.000 e 600.000 persone nel Nord America[11]. La prevalenza stimata per il Nord Europa va da 27 a 48 per 100.000 abitanti[12].
La sua incidenza annuale è di circa 3 casi ogni 100.000 abitanti negli Stati Uniti e tra i 4 e i 10 ogni 100.000 abitanti in Scandinavia e in Gran Bretagna. L'incidenza e la prevalenza di questa patologia è in aumento. Può manifestarsi a qualsiasi età, con un picco nella seconda e terza decade e uno secondario tra sesta e settima. Alcuni gruppi etnici (come gli ebrei ashkenaziti) hanno tassi di incidenza significativamente più alti della media.
In alcune famiglie è stata notata una maggiore presenza della malattia; ciò suggerisce l'ipotesi di una predisposizione genetica, collegata in special modo al gene HLA-B27; ciò non è però provato, e l'ipotesi risulta dunque ancora incerta.
La malattia si riscontra in percentuale maggiore nelle persone di sesso femminile oltre i 20 anni, ma va estendendosi anche a soggetti di più giovane età.
Eziologia[modifica | modifica wikitesto]
Anche se l'eziologia esatta della malattia di Crohn è ancora sconosciuta, una combinazione di fattori ambientali e predisposizione genetica sembra essere la causa più probabile.[13] I fattori di rischio genetici sono stati completamente chiariti, rendendo la malattia di Crohn la prima malattia genetica complessa in cui si sia fatta luce sul contesto genetico.[14] Il rischio relativo di contrarre la malattia quando si ha una mutazione in uno dei geni di rischio, tuttavia, è in realtà molto basso (circa 1:200). In termini generali, i dati genetici indicano disfunzioni del sistema immunitario innato nei pazienti con malattia di Crohn, e la valutazione diretta di immunità del paziente conferma questa caratteristica.[15] Ciò aveva portato la malattia a essere vista come un'innata deficienza immunitaria, in quanto l'infiammazione cronica è causata da immunità adattativa che cerca di compensare la ridotta funzionalità del sistema immunitario innato.[16]
Genetica[modifica | modifica wikitesto]

Alcune ricerche hanno indicato che la malattia di Crohn possa avere una causa genetica.[17] Le persone che hanno un fratello o sorella affetto dalla malattia hanno 30 volte più probabilità di svilupparla rispetto alla popolazione generale.
Le mutazioni nel gene CARD15 (noto anche come il gene NOD2), presente sul cromosoma 16, sono associate alla malattia di Crohn.[18]
Anche modificazioni a carico dei TLR (Toll-like Receptor, una famiglia di recettori di membrana cui è deputato il riconoscimento di determinate parti batteriche), presenti sulle cellule endoteliali intestinali e sulle cellule presentanti l'antigene, sembrerebbero essere implicate nella malattia di Crohn.
In studi precedenti, solo due geni erano stati legati alla malattia, ma gli scienziati ora credono che più di trenta geni giochino un ruolo in essa, sia direttamente attraverso causalità che indirettamente come una variabile mediatore. Anomalie del gene XBP1 sono state identificate come fattori causali delle malattie infiammatorie intestinali.[19][20]
Fattori ambientali[modifica | modifica wikitesto]
Per la sua prevalenza nelle zone ad alta industrializzazione, si crede che la dieta possa essere una delle cause della malattia. Una correlazione positiva è stata trovata tra l'incidenza della malattia e un apporto maggiore di proteine animali, proteine del latte e un rapporto maggiore di omega-6 e acidi grassi polinsaturi omega-3.[21] È stata invece trovata una correlazione negativa dell'incidenza della malattia nell'aumento del consumo di proteine vegetali e nessuna correlazione con le proteine di pesce.[21] Il fumo è stato dimostrato essere un fattore determinante nell'aumento del rischio del ritorno della malattia in fase attiva.[10] L'introduzione della contraccezione ormonale negli Stati Uniti nel 1960 è collegata a un drammatico aumento del tasso di incidenza della malattia di Crohn. Anche se un legame causale non è stato effettivamente dimostrato, permangono i timori che questi farmaci agiscano sul sistema digestivo in modo simile al fumo.[22] Numerosi studi scientifici hanno postulato l'isotretinoina come una possibile causa della malattia di Crohn in alcuni pazienti.[23][24][25]
Microbi[modifica | modifica wikitesto]
Si ritiene che alcuni microrganismi possano sfruttare a proprio vantaggio la debolezza della mucosa e l'incapacità di rimuovere i batteri dalla parete intestinale dell'ospite, condizioni entrambe presenti nella malattia di Crohn.[26] La presenza di diversi batteri nei tessuti e le risposte variabili agli antibiotici suggeriscono che la malattia di Crohn non sia singola, ma una serie di malattie correlate a differenti agenti patogeni.[27][28]
Diversi studi[29][30][31][32] hanno rilevato una forte associazione del Mycobacterium avium subspecies paratuberculosis (MAP), che causa una malattia simile nei bovini, la paratubercolosi[33]. Alcuni hanno permesso di osservare un miglioramento della prognosi con i farmaci specifici per micobatteri[34][35], mentre altri hanno escluso l'efficacia della terapia antibiotica[36]; tuttavia, trattandosi di terapie ex adiuvantibus, uno schema terapeutico standardizzato in termini di scelta degli antibiotici e di posologia non è ancora stato identificato. Il gene NOD2, coinvolto nella suscettibilità genetica alla malattia di Crohn, è associato ad una ridotta capacità dei macrofagi di uccidere il MAP, diminuite immunità innata e adattativa dell'ospite e una risposta immunitaria insufficiente, necessaria al controllo dei micobatteri intracellulari.[37][38] I macrofagi infettati col MAP sono associati a un'alta produzione di TNF-α.[39][40]
Altri studi hanno associato alla malattia specifici ceppi di Escherichia coli enteroaderente[41]: in particolare il ceppo aderente-invasivo (AIEC) è più comune nelle persone affette dalla malattia di Crohn[42][43][44], produce rispetto alle specie non enteroaderenti biofilm più potenti che si correlano a una sostanziale adesione e invasività[45][46] dei neutrofili e riesce a bloccare l'autofagia durante la fase autolisosomiale, garantendo la sopravvivenza dei batteri intracellulari e l'induzione dell'infiammazione.[47] L'infiammazione promuove la proliferazione dell'AIEC e la disbiosi nell'ileo, indipendentemente dal genotipo.[48] Le specie AIEC si replicano estensivamente all'interno dei macrofagi e inducono la secrezione di vaste quantità di TNF-α.[49]
L'ipotesi della "catena del freddo" è che batteri criofili come Yersinia e Listeria contribuiscano alla malattia. Una correlazione statistica è stata trovata tra l'avvento dell'utilizzo della refrigerazione negli Stati Uniti e varie parti d'Europa e l'aumento della malattia.[50][51]
Apparentemente c'è un collegamento tra la malattia di Crohn, Mycobacterium e altri batteri patogeni e marcatori genetici.[52][53] In molte persone, fattori genetici predispongono gli individui all'infezione da Mycobacterium avium subspecies paratuberculosis. Questo batterio produce mannani, che proteggono dalla fagocitosi esso e diversi altri batteri, causando una varietà di infezioni secondarie.[54]
La relazione tra determinati tipi di batteri e la malattia di Crohn resta tuttora poco chiara.[55][56]
Sistema immunitario[modifica | modifica wikitesto]
Anomalie nel sistema immunitario sono state spesso ritenute causa della malattia di Crohn. Molti ritengono la malattia una malattia autoimmune causata da una risposta abnorme alle citochine da parte dei linfociti.[57][58] Il gene, che studi hanno fortemente correlato alla malattia, è l'ATG16L1 il quale può indurre l'autofagia ed è in grado di ostacolare la capacità del corpo di attaccare i batteri invasivi.[59]
Contrariamente all'opinione prevalente che indica la malattia di Crohn come un disordine autoimmune delle cellule T, alcuni studi fanno pensare che essa sia il risultato di un'innata compromissione del sistema immunitario.[60] L'immunodeficienza, che è dimostrata essere dovuta (almeno in parte) alla ridotta secrezione di citochine da parte dei macrofagi, è ritenuta essere la causa dell'elevata risposta infiammatoria, in particolare nel colon, dove la carica batterica è particolarmente elevata.[15][61]
Segni e sintomi[modifica | modifica wikitesto]
Sintomi gastrointestinali[modifica | modifica wikitesto]

Molte persone affette dalla malattia di Crohn presentano i sintomi per anni prima che venga formulata una diagnosi.[62] Solitamente l'esordio è tra i 15 e i 30 anni di età, ma può verificarsi a qualsiasi età.[63] A causa della natura "irregolare" della malattia gastrointestinale e la profondità del coinvolgimento dei tessuti, i sintomi iniziali possono essere più labili di quelli tipici della colite ulcerosa. Le persone con malattia di Crohn accusano periodi cronici ricorrenti di acutizzazione dei sintomi e periodi di remissione.[64]
Il dolore addominale può essere il sintomo iniziale della malattia di Crohn. È spesso accompagnato da diarrea, specialmente in coloro che hanno subito un intervento chirurgico. La diarrea può essere più o meno sanguinosa. La natura della diarrea nella malattia di Crohn dipende dalla parte dell'intestino tenue o del colon coinvolti. Le ileiti portano tipicamente a grandi volumi di feci acquose. La colite può provocare un minor volume di feci ma con frequenza più alta. La consistenza fecale può variare da solida a acquosa. Nei casi più gravi, un individuo può avere più di 20 scariche intestinali al giorno e potrebbe essere necessario svegliarsi di notte per defecare.[1][5][65][66] Il sangue nelle feci è meno comune nella malattia di Crohn rispetto alla colite ulcerosa, ma può essere presente.[1] Le scariche intestinali di sangue sono tipicamente intermittenti e possono essere di colore rosso vivo o scuro. Nel caso di grave colite di Crohn, il sanguinamento può essere abbondante.[5] Flatulenza e gonfiore possono anche aggiungersi al disagio intestinale.[5]
| Malattia di Crohn | Colite ulcerosa | |
|---|---|---|
| Defecazione | Spesso, talvolta steatorrea[67] | Spesso, simile a muco e con presenza di sangue[67] |
| Tenesmo rettale | Poco comune[67] | Molto comune[67] |
| Febbre | Comune[67] | Indicazione di grave malattia[67] |
| Fistole | Comune[68] | Raramente |
| Perdita di peso | Spesso | Molto raramente |
I sintomi causati da stenosi intestinale sono comuni anche nella malattia di Crohn. Il dolore addominale è spesso più acuto nelle aree dell'intestino che la presentano. Nel quadro di grave stenosi, vomito e nausea possono indicare l'inizio di ostruzione dell'intestino tenue.[5] Anche se la correlazione è maggiore nel contesto della colite ulcerosa, la malattia di Crohn può anche essere correlata con la colangite sclerosante primitiva, un tipo di infiammazione dei dotti biliari.[69]
Disagi nella zona perianale, possono risultare importanti nella malattia di Crohn. Prurito o dolore intorno all'ano possono suggerire infiammazione, fistolizzazione o il formarsi di un ascesso locale.[1] Appendici cutanee perianali sono comuni.[70] L'incontinenza fecale può accompagnare la malattia perianale di Crohn. All'estremità opposta del tratto gastrointestinale, la bocca, può essere colpita da piaghe che non guariscono (ulcere aftose). Raramente l'esofago e lo stomaco possono essere coinvolti nella malattia. Se colpiti, questi possono causare sintomi quali difficoltà a deglutire (disfagia), dolore addominale superiore e vomito.[71]
Sintomi sistemici[modifica | modifica wikitesto]
La malattia di Crohn, come molte altre malattie croniche infiammatorie, può causare una varietà di sintomi sistemici.[1] Tra i bambini, la mancata crescita è frequente. A molti di essi viene diagnosticata la malattia proprio in conseguenza dell'incapacità di mantenere un corretto sviluppo.[72] Fino al 30% dei bambini con la malattia presentano un ritardo di crescita.[72] La febbre può essere presente, anche se superiore a 38,5 °C è rara se non si verificano complicazioni come un ascesso.[1] Tra gli individui più anziani, la malattia di Crohn può manifestarsi come perdita di peso, di solito legata alla diminuzione dell'assunzione di cibo. Infatti, pazienti con sintomi intestinali da malattia di Crohn, spesso si sentono meglio quando non mangiano.[73] Le persone colpite dalla malattia in ampie zone dell'intestino tenue possono anche avere malassorbimento di carboidrati o lipidi, ciò può ulteriormente aggravare la perdita di peso.[74]
Il deficit nutrizionale, dovuto al ridotto apporto dietetico per anoressia e autorestrizione, determina steatorrea, anemia microcitica o megaloblastica, ipoprotidemia, edema, demineralizzazione ossea, ipokaliemia e disidratazione.
Sintomi extraintestinali[modifica | modifica wikitesto]
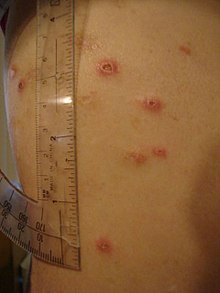
Oltre al coinvolgimento sistemico e gastrointestinale, la malattia può colpire anche molti altri organi.[75] L'infiammazione della parte interna dell'occhio, nota come uveite, può provocare un forte dolore, specialmente quando l'occhio è esposto alla luce (fotofobia). L'infiammazione può coinvolgere anche la parte bianca dell'occhio (sclera), una condizione chiamata episclerite. Sia l'episclerite che la uveite possono portare alla perdita della vista se non trattate.
Alla malattia di Crohn è associata un tipo di malattia reumatologica conosciuta come spondiloartropatia sieronegativa. Questa è caratterizzata da infiammazione di una o più articolazioni (artrite) o delle inserzioni muscolari (entesite). L'artrite può interessare articolazioni più grandi, come il ginocchio o la spalla, o può coinvolgere esclusivamente le piccole articolazioni delle mani e dei piedi. L'artrite può coinvolgere anche la colonna vertebrale, portando a spondilite anchilosante se l'intera struttura viene coinvolta o semplicemente sacroileite se solo la porzione inferiore di colonna vertebrale viene coinvolta. I sintomi di artrite sono dolore, sensazione di caldo, gonfiore, rigidità delle articolazioni e la perdita della mobilità articolare o di funzionalità.[76]

La malattia di Crohn può anche colpire la pelle, il sangue e il sistema endocrino. Un tipo di manifestazione cutanea, l'eritema nodoso, si presenta come noduli rossi che di solito appaiono sugli stinchi. L'eritema nodoso è dovuto ad infiammazione del tessuto sottocutaneo sottostante ed è caratterizzata da panniculite settale. Un'altra lesione cutanea, il pioderma gangrenoso, è tipicamente caratterizzato da un nodulo doloroso ulcerato. La malattia di Crohn aumenta anche il rischio di coaguli di sangue, gonfiore e dolore della parte inferiore delle gambe e può essere un segno di trombosi venosa profonda, mentre la difficoltà di respirazione può essere una conseguenza di una embolia polmonare. L'anemia emolitica autoimmune è una condizione in cui il sistema immunitario attacca i globuli rossi, che è comune nella malattia di Crohn e può causare stanchezza, pallore, e altri sintomi comuni nell'anemia. Il clubbing (dita ippocratiche), una deformità delle estremità delle dita, può anche essere un risultato della presenza della malattia. Infine, la malattia di Crohn può causare osteoporosi o l'assottigliamento delle ossa. I soggetti con osteoporosi presentano un aumentato del rischio di fratture ossee.[77]
La malattia di Crohn può anche causare complicanze neurologiche (come riportato nel 15% dei pazienti).[78] Le più comuni sono convulsioni, ictus, miopatia, neuropatia periferica, cefalea e depressione.[78]
Gli affetti dalla malattia possono, inoltre, soffrire di cheilite granulomatosa e altre forme di granulomatosi oro-facciale.[79]
Complicanze[modifica | modifica wikitesto]

La malattia di Crohn può portare a diverse complicanze all'interno dell'intestino, tra cui l'ostruzione, lo sviluppo di fistole e ascessi. L'ostruzione si verifica in genere per stenosi o aderenze che restringono il lume, bloccando il passaggio del contenuto intestinale. Le fistole possono svilupparsi tra due anse intestinali, tra l'intestino e la vescica, tra l'intestino e la vagina e tra l'intestino e la pelle. Gli ascessi possono verificarsi in addome o nella zona perianale.
La malattia di Crohn aumenta anche il rischio di cancro nella zona di infiammazione. Per esempio, gli individui con malattia di Crohn che coinvolge il piccolo intestino sono a maggior rischio per cancro intestinale. Allo stesso modo, le persone con colite di Crohn hanno un rischio relativo di 5.6 per sviluppare il cancro del colon.[80] Screening per il cancro del colon con colonscopia sono consigliati per chi ha avuto la colite di Crohn per almeno otto anni.[81]
| Malattia di Crohn | Colite ulcerosa | ||
|---|---|---|---|
| Malnutrizione | Alto rischio | ||
| Rischio di cancro al colon | Leggero | Significante | |
| Prevalenza di complicanze extraintestinali | |||
| Irite/uveite | Femmine | 2.2% | 3.2% |
| Maschi | 1.3% | 0.9% | |
| Colangite sclerosante primitiva |
Femmine | 0.3% | 1% |
| Maschi | 0.4% | 3% | |
| Spondilite anchilosante | Femmine | 0.7% | 0.8% |
| Maschi | 2.7% | 1.5% | |
| Pioderma gangrenoso | Femmine | 1.2% | 0.8% |
| Maschi | 1.3% | 0.7% | |
| Eritema nodoso | Femmine | 1.9% | 2% |
| Maschi | 0.6% | 0.7% | |
Gli individui con malattia di Crohn sono a rischio di malnutrizione per molte ragioni, tra cui la diminuzione dell'assunzione di cibo e il malassorbimento. Il rischio aumenta dopo la resezione del piccolo intestino. Tali individui possono aver bisogno di integratori orali per aumentare il loro apporto calorico, o nei casi più gravi, nutrizione parenterale totale (TPN). La maggior parte delle persone con malattia moderata o grave di Crohn si rivolgono ad un dietista per l'assistenza nella nutrizione.[82]
Malattia di Crohn può risultare problematica durante la gravidanza e alcuni farmaci possono causare eventi avversi per il feto o la madre. La consultazione con un ostetrico e un gastroenterologo circa la malattia di Crohn e tutti i farmaci assumibili, consente di adottare misure preventive. In alcuni casi, durante la gravidanza, si può verificare la remissione della malattia. Alcuni farmaci possono anche avere un impatto sugli spermatozoi o possono comunque influenzare negativamente la fertilità di un uomo.[83]
Un'altra complicanza della malattia può essere l'infezione all'iride e l'anoressia. Può essere inoltre associata a ipovitaminosi D.[84]
Diagnosi[modifica | modifica wikitesto]
La formulazione di una diagnosi di malattia di Crohn a volte può risultare impegnativa[62] e una serie di test sono spesso necessari per aiutare il medico.[5] Anche una serie completa di esami potrebbe non essere sufficiente per una diagnosi di Crohn fatta con assoluta certezza. Una colonscopia è efficace al 70% nel diagnosticare la malattia. Quando la malattia si presenta nell'intestino tenue è particolarmente difficile da diagnosticare, infatti la colonscopia tradizionale consente l'accesso solo alla porzione inferiore del tenue; l'introduzione della capsula endoscopica[85] ha però aiutato molto in questo tipo di diagnosi.
Endoscopia[modifica | modifica wikitesto]




La colonscopia è il miglior test per formulare una diagnosi di malattia di Crohn, in quanto permette la visualizzazione diretta del colon e dell'ileo terminale, individuandone il livello di progressione delle alterazioni. A volte, il colonscopio può arrivare oltre l'ileo terminale, ma questo varia da paziente a paziente. Durante la procedura, il gastroenterologo può anche eseguire una biopsia, prelevando piccoli campioni di tessuto per compiere analisi di laboratorio. Ciò può aiutare a confermare una diagnosi. Il 30% delle malattie di Crohn coinvolge solo l'ileo[1] e perciò il raggiungimento di questa porzione di intestino è necessaria per formulare la diagnosi. Trovare una distribuzione a chiazze di malattia, con coinvolgimento del colon o dell'ileo ma non del retto, suggerisce la presenza della malattia.[86] L'utilità della capsula endoscopica è ancora incerta.[87]
Esame radiologico[modifica | modifica wikitesto]
Un esame con mezzo di contrasto al bario dell'intestino tenue può essere utilizzato per la diagnosi della malattia di Crohn quando essa lo coinvolge esclusivamente. La colonscopia e la gastroscopia consentono la visualizzazione diretta del solo l'ileo terminale e dell'inizio del duodeno, non possono infatti essere utilizzati per valutare il resto dell'intestino tenue. Con l'indagine radiologica effettuata facendo assumere il solfato di bario per via orale al paziente si possono studiare eventuali infiammazioni o restringimenti.[86][88] Grazie al clisma opaco e alla fluoroscopia è possibile avere l'immagine del colon e quindi analizzarlo per la ricerca della malattia, ma questa procedura è andata in disuso con l'avvento della colonscopia. Questa rimane comunque utile per identificare anomalie anatomiche quando eventuali stenosi del colon rendono impossibile l'attraversamento di esse da parte del colonscopio o per la rilevazione di fistole del colon (in questo caso si usa un mezzo di contrasto iodato e non baritato a causa della sua tossicità).[89]
La tomografia computerizzata (TC) è utile per la valutazione dell'intestino tenue.[90] È anche utile per la ricerca di complicanze intra-addominali della malattia di Crohn, come ascessi, ostruzioni dell'intestino tenue o fistole.[91] La risonanza magnetica è un'altra opzione per l'imaging dell'intestino tenue e per la ricerca di complicanze, anche se è più costosa e meno facilmente disponibile.[92]
Medicina nucleare[modifica | modifica wikitesto]
Anche la medicina nucleare si è rivelata efficace per individuare la posizione della malattia. La procedura utilizza i globuli bianchi rimossi dal paziente e poi contrassegnati con un radioisotopo. Essi poi vengono iniettati di nuovo nel paziente per via endovenosa e successivamente vengono osservati per ricercare eventuali accumuli anomali nell'intestino. Gli studi hanno anche suggerito che tali esami siano utili per monitorare la malattia e valutare l'efficacia della terapia.[93]
Confronto con colite ulcerosa[modifica | modifica wikitesto]
La malattia più comune che imita i sintomi della malattia di Crohn è la colite ulcerosa. Entrambe sono malattie infiammatorie croniche intestinali che possono colpire il colon con sintomi simili. È importante distinguere queste due malattie poiché il loro decorso e i trattamenti disponibili possono essere molto diversi. In alcuni casi, tuttavia, potrebbe non essere possibile individuarne la differenza, in questi casi la malattia viene classificata come colite indeterminata.[1][5][65]
| Segno | Malattia di Crohn | Colite ulcerosa |
|---|---|---|
| Coinvolgimento dell'ileo terminale | Frequente | Raro |
| Coinvolgimento Colon | Frequente | Sempre |
| Coinvolgimento del retto | Raro | Frequente[94] |
| Coinvolgimento intorno all'ano | Frequente[68] | Raro |
| Coinvolgimento dotti biliari | Nessun aumento del tasso di colangite sclerosante primaria | Aumento del tasso[95] |
| Distribuzione della malattia | Chiazze di infiammazione | Aree continue di infiammazione[94] |
| Endoscopia | Ulcere profonde e serpinginose | Ulcere continue |
| Profondità dell'infiammazione | Potrebbe essere trasmurale, profonda nei tessuti[1][68] | Della mucosa |
| Stenosi | Comune | Rara |
| Granuloma in biopsia | Potrebbero esserci granulomi non necrotizzanti[68][96][97] | Non si trovano granulomi[94] |
Trattamento[modifica | modifica wikitesto]
| Malattia di Crohn | Colite ulcerosa | |
|---|---|---|
| Mesalazina | Poco utilizzata[98] | Molto utilizzata[98] |
| Antibiotici | Efficaci a lungo termine[99] | Generalmente non usati[100][101] |
| Chirurgia | Recidive dopo asportazione |
Di solito curata con asportazione del colon |
Al momento non esiste una cura per la malattia di Crohn, ma al massimo si possono verificare temporanee remissioni.[102] Nei casi in cui ciò si verifica, si possono prevenire recidive e controllare i sintomi grazie all'utilizzo di farmaci, alla modifica dello stile di vita e, in alcuni casi, con l'intervento chirurgico. Adeguatamente controllata, la malattia di Crohn non incide sensibilmente sulla vita quotidiana.[103] Il trattamento è perciò finalizzato a gestire sintomi prima della fase acuta e in un secondo momento al mantenimento dello stato di remissione.
Modifiche nello stile di vita[modifica | modifica wikitesto]
Modifiche di un certo stile di vita possono ridurre i sintomi della malattia. A esempio, adeguare la dieta[104], assumere una corretta idratazione e smettere di fumare[105] sono cambiamenti fortemente consigliati agli ammalati. Mangiare piccoli pasti frequenti, invece di grandi pasti, può aiutare chi lamenta una riduzione di appetito. Una regolare attività fisica è altresì raccomandata[106]. Alcuni pazienti devono seguire una dieta povera di fibre per controllare i sintomi. I pazienti devono evitare il latte o prodotti caseari: una ricerca del 2007 ha infatti dimostrato che essi possono contribuire alla malattia di Crohn o addirittura causarla[103].
L'utilizzo di integratori alimentari, specialmente in pazienti che hanno subito resezione di parti di intestino, è consigliato. Tra questi, una ricerca del 2017 ha dimostrato l'utilità della curcumina (estratta da Curcuma longa) "libera" (biologicamente attiva e benefica), grazie al suo potere antinfiammatorio, nella riduzione dei sintomi della malattia e dei marker infiammatori[107].
Terapia farmacologica[modifica | modifica wikitesto]
Il trattamento acuto per la malattia utilizza i farmaci per gestire eventuali infezioni (di solito antibiotici) e ridurre l'infiammazione (normalmente tramite farmaci anti-infiammatori e corticosteroidi). Quando i sintomi sono in remissione, il trattamento consiste nel mantenimento, con l'obiettivo di evitare il ripetersi dei sintomi. L'uso prolungato di corticosteroidi comporta però significativi effetti collaterali, di conseguenza, essi non sono utilizzati per trattamento a lungo termine[108]. L'alternativa include gli aminosalicilati, anche se solo una minoranza di pazienti è in grado di mantenere il trattamento e molti richiedono farmaci immunosoppressivi[68]. È stato anche suggerito che l'uso degli antibiotici possa cambiare il microbiota umano e il loro uso continuativo può comportare il rischio di proliferazione di agenti patogeni quali il C. difficile[109].
I farmaci utilizzati nel trattamento dei sintomi della malattia di Crohn includono: mesalazina (5-ASA), prednisone, modulatori del sistema immunitario come l'azatioprina[110], la mercaptopurina[111], il metotrexato[112]. Inoltre sono entrati in terapia gli anticorpi monoclonali quali l'infliximab[113], l'adalimumab[65], certolizumab pegol[114] e il Natalizumab[115][116].
L'idrocortisone e i cortisonici in genere vengono usati per controllare gli attacchi severi della malattia[117].
Alcuni studi indicano che i cannabinoidi (principalmente THC e CBD) possono influenzare positivamente l'andamento della patologia, come testimoniato dalla riduzione degli indici di attività, del fabbisogno di altri farmaci e del ricorso alla chirurgia[118]. Uno studio del 2013 con controllo su placebo ha evidenziato i suoi effetti positivi; anche se la remissione non è stata raggiunta in tutti i pazienti, un trattamento breve ha mostrato benefici clinici significanti per i pazienti con malattia attiva, senza effetti collaterali[119].
Trattamento chirurgico[modifica | modifica wikitesto]
La malattia di Crohn può essere anche trattata con la chirurgia, quando si verifica un blocco parziale o totale dell'intestino. La chirurgia può essere utilizzata anche per risolvere complicazioni come: ostruzioni, fistole e/o ascessi o se la malattia non risponde al trattamento farmacologico. Dopo il primo intervento di resezione, la malattia tende a ricomparire in altri luoghi. Dopo una resezione, il tessuto cicatriziale si accumula e può causare stenosi che si ha quando l'intestino diventa troppo stretto per permettere agli escrementi di passare con facilità, portando ad un blocco. Ciò può spesso rendere necessario un altro intervento analogo entro cinque anni[120]. Per i pazienti con ostruzione causata da stenosi, ci sono due opzioni di trattamento: la strictureplasty e la resezione di parte di intestino. In questi casi, i tassi di re-intervento sono stati del 31% e 27%, rispettivamente, ad indicare che la strictureplasty è un trattamento sicuro ed efficace per pazienti selezionati che presentano interessamento duodenale.[121]
La sindrome dell'intestino corto può essere causata dalla rimozione chirurgica del piccolo intestino. Di solito si sviluppa nei pazienti che hanno avuto la metà o più del loro intestino tenue rimosso[122]. La diarrea è il sintomo principale di tale condizione, tuttavia altri sintomi possono includere crampi, gonfiore e bruciore di stomaco. Questa sindrome viene trattata con cambiamenti nella dieta, supplementi di alimentazione per via endovenosa (vitamine e minerali) e tramite il trattamento farmacologico. Un'altra complicanza dopo un intervento chirurgico in cui l'ileo terminale viene rimosso è lo sviluppo di una eccessiva diarrea acquosa. Ciò è dovuto all'incapacità dell'ileo di riassorbire gli acidi biliari.
In alcuni casi di sindrome di intestino corto, può essere valutata la chirurgia di trapianto intestinale, anche se il numero dei centri che offrono questa procedura è piuttosto piccolo e essa comporta un elevato rischio a causa della possibilità di infezione e rigetto[123].
Medicina alternativa[modifica | modifica wikitesto]
Spesso i malati affetti da malattia di Crohn si sottopongono a terapie complementari o alternative[124]. Gli approcci seguiti comprendono le diete, l'uso di probiotici, l'olio di pesce (omega-3) e altri integratori a base di erbe (fitoterapia) e nutrizionali.
Il beneficio di questi trattamenti non è provato e importanti metanalisi hanno mostrato come manchino studi seri e ben svolti sull'utilità dei trattamenti alternativi[125].
Prognosi[modifica | modifica wikitesto]
La malattia di Crohn è una malattia cronica per la quale non esiste alcuna cura. Essa è caratterizzata da periodi di miglioramento seguiti da episodi di riacutizzazione dei sintomi. Con il trattamento, la maggior parte dei pazienti mantiene un corretto peso e una vita normale. Il tasso di mortalità per la malattia è relativamente più alto rispetto alla popolazione sana[126][127].
Inoltre, la malattia di Crohn sembra associata ad un aumentato rischio di carcinoma dell'intestino tenue e del colon-retto[128].
Note[modifica | modifica wikitesto]
- ^ a b c d e f g h i j k l Baumgart DC, Sandborn WJ, Inflammatory bowel disease: clinical aspects and established and evolving therapies., in The Lancet, vol. 369, n. 9573, 12 maggio 2007, pp. 1641–57, DOI:10.1016/S0140-6736(07)60751-X, PMID 17499606. URL consultato il 4 novembre 2009.
- ^ (EN) Crohn's disease - Symptoms and causes, su Mayo Clinic. URL consultato il 18 luglio 2021.
- ^ National Digestive Diseases Information Clearinghouse, su digestive.niddk.nih.gov. URL consultato il 19 luglio 2011 (archiviato dall'url originale il 9 giugno 2014).
- ^ JC et al. Barrett, S Hansoul, DL Nicolae, JH Cho, RH Duerr, JD Rioux, SR Brant, MS Silverberg e KD Taylor, Genome-wide association defines more than 30 distinct susceptibility loci for Crohn's disease, in Nature Genetics, vol. 40, n. 8, agosto 2008, pp. 955–962, DOI:10.1038/ng.175, PMC 2574810, PMID 18587394. URL consultato il 4 novembre 2009.
- ^ a b c d e f g George Y Wu, Marcy L Coash, Senthil Nachimuthu, Crohn Disease, su emedicine.medscape.com, eMedicine, 17 marzo 2010. URL consultato il 15 aprile 2010.
- ^ Tri H Le, Ulcerative colitis, su emedicine.medscape.com, eMedicine, 17 marzo 2010. URL consultato il 15 aprile 2010.
- ^ a b Crohn BB, Ginzburg L, Oppenheimer GD, Regional ileitis: a pathologic and clinical entity. 1932, in Mt. Sinai J. Med., vol. 67, n. 3, 2000, pp. 263–8, PMID 10828911.
- ^ a b Gasche C, Scholmerich J, Brynskov J, D'Haens G, Hanauer S, Irvine E, Jewell D, Rachmilewitz D, Sachar D, Sandborn W, Sutherland L, A simple classification of Crohn's disease: report of the Working Party for the World Congresses of Gastroenterology, Vienna 1998, in Inflamm Bowel Dis, vol. 6, n. 1, 2000, pp. 8–15, DOI:10.1002/ibd.3780060103, PMID 10701144.
- ^ Dubinsky MC, Fleshner PP., Treatment of Crohn's Disease of Inflammatory, Stenotic, and Fistulizing Phenotypes, in Curr Treat Options Gastroenterol, vol. 6, n. 3, 2003, pp. 183–200, DOI:10.1007/s11938-003-0001-1, PMID 12744819.
- ^ a b Cosnes J, Tobacco and IBD: relevance in the understanding of disease mechanisms and clinical practice, in Best Pract Res Clin Gastroenterol, vol. 18, n. 3, giugno 2004, pp. 481–96, DOI:10.1016/j.bpg.2003.12.003, PMID 15157822. URL consultato il 4 novembre 2009.
- ^ E.V. Loftus, P. Schoenfeld, W. J. Sandborn, The epidemiology and natural history of Crohn's disease in population-based patient cohorts from North America: a systematic review, in Alimentary Pharmacology & Therapeutics, vol. 16, n. 1, gennaio 2002, pp. 51–60, DOI:10.1046/j.1365-2036.2002.01140.x, PMID 11856078. URL consultato il 4 novembre 2009.
- ^ Charles N Bernstein, Andre Wajda e Lawrence W Svenson, The Epidemiology of Inflammatory Bowel Disease in Canada: A Population-Based Study, in The American Journal of Gastroenterology, vol. 101, n. 7, 2006-07, pp. 1559–1568, DOI:10.1111/j.1572-0241.2006.00603.x. URL consultato il 18 luglio 2021.
- ^ Braat H, Peppelenbosch MP, Hommes DW, Immunology of Crohn's disease, in Ann. N. Y. Acad. Sci., vol. 1072, agosto 2006, pp. 135–54, DOI:10.1196/annals.1326.039, PMID 17057196. URL consultato il 4 novembre 2009.
- ^ Henckaerts L, Figueroa C, Vermeire S, Sans M, The role of genetics in inflammatory bowel disease, in Curr Drug Targets, vol. 9, n. 5, maggio 2008, pp. 361–8, DOI:10.2174/138945008784221161, PMID 18473763. URL consultato il 4 novembre 2009.
- ^ a b Marks DJ, Harbord MW, MacAllister R, Rahman FZ, Young J, Al-Lazikani B, Lees W, Novelli M, Bloom S, Segal AW, Defective acute inflammation in Crohn's disease: a clinical investigation, in Lancet, vol. 367, n. 9511, 2006, pp. 668–78, DOI:10.1016/S0140-6736(06)68265-2, PMC 2092405, PMID 16503465.
- ^ Comalada M, Peppelenbosch MP, Impaired innate immunity in Crohn's disease, in Trends Mol Med, vol. 12, n. 9, settembre 2006, pp. 397–9, DOI:10.1016/j.molmed.2006.07.005, PMID 16890491. URL consultato il 4 novembre 2009.
- ^ Crohn's disease has strong genetic link: study, su ccfa.org, Crohn's and Colitis Foundation of America, 16 aprile 2007. URL consultato il 7 novembre 2009 (archiviato dall'url originale il 2 maggio 2007).
- ^ Ogura Y, Bonen DK, Inohara N, et al., A frameshift mutation in NOD2 associated with susceptibility to Crohn's disease, in Nature, vol. 411, n. 6837, 2001, pp. 603–6, DOI:10.1038/35079114, PMID 11385577.
- ^ Arthur Kaser, Ann-Hwee Lee e Andre Franke, XBP1 links ER stress to intestinal inflammation and confers genetic risk for human inflammatory bowel disease, in Cell, vol. 134, n. 5, 5 settembre 2008, pp. 743–756, DOI:10.1016/j.cell.2008.07.021. URL consultato il 18 luglio 2021.
- ^ Hans Clevers, Inflammatory Bowel Disease, Stress, and the Endoplasmic Reticulum, in New England Journal of Medicine, vol. 360, n. 7, 12 febbraio 2009, pp. 726–727, DOI:10.1056/NEJMcibr0809591. URL consultato il 18 luglio 2021.
- ^ a b R. Shoda, K. Matsueda e S. Yamato, Epidemiologic analysis of Crohn disease in Japan: increased dietary intake of n-6 polyunsaturated fatty acids and animal protein relates to the increased incidence of Crohn disease in Japan, in The American Journal of Clinical Nutrition, vol. 63, n. 5, 1996-05, pp. 741–745, DOI:10.1093/ajcn/63.5.741. URL consultato il 18 luglio 2021.
- ^ S. M. Lesko, D. W. Kaufman e L. Rosenberg, Evidence for an increased risk of Crohn's disease in oral contraceptive users, in Gastroenterology, vol. 89, n. 5, 1985-11, pp. 1046–1049, DOI:10.1016/0016-5085(85)90207-0. URL consultato il 18 luglio 2021.
- ^ Reddy D, Siegel CA, Sands BE, Kane S, Possible association between isotretinoin and inflammatory bowel disease, in The American journal of gastroenterology, vol. 101, n. 7, luglio 2006, pp. 1569–73, DOI:10.1111/j.1572-0241.2006.00632.x, PMID 16863562.
- ^ E. Borobio, A. Arín e A. Valcayo, [Isotretinoin and ulcerous colitis], in Anales Del Sistema Sanitario De Navarra, vol. 27, n. 2, 2004-05, pp. 241–243, DOI:10.4321/s1137-66272004000300009. URL consultato il 18 luglio 2021.
- ^ Reniers DE, Howard JM, Isotretinoin-induced inflammatory bowel disease in an adolescent, in Ann Pharmacother, vol. 35, n. 10, ottobre 2001, pp. 1214–6, DOI:10.1345/aph.10368, PMID 11675849. URL consultato il 7 settembre 2011 (archiviato dall'url originale il 29 giugno 2012).
- ^ Sartor, R. Balfour., Mechanisms of Disease: Pathogenesis of Crohn's disease and ulcerative colitis, in Nature Clinical Practice Gastroenterology & Hepatology, 2006, DOI:10.1038/ncpgasthep0528.
- ^ Dogan B1, Scherl E, Bosworth B, Yantiss R, Altier C, McDonough PL, Jiang ZD, Dupont HL, Garneau P, Harel J, Rishniw M, Simpson KW., Multidrug resistance is common in Escherichia coli associated with ileal Crohn's disease., in Inflammatory Bower Diseases, 2013, DOI:10.1002/ibd.22971, PMID 22508665.
- ^ Jordana Campbell, Thomas J. Borody, Sharyn Leis., The many faces of Crohn’s Disease: Latest concepts in etiology., in Open Journal of Internal Medicine, 2012, DOI:10.4236/ojim.2012.22020.
- ^ Ingrid Olsen, Knut E Lundin, and Ludvig M Sollid, Increased frequency of intestinal CD4+ T cells reactive with mycobacteria in patients with Crohn's disease, in Scandinavian J Gastroenterology, 2013.
- ^ Hermon-Taylor J., Mycobacterium avium subspecies paratuberculosis, Crohn's disease and the Doomsday scenario., in US National Library of Medicine, 2009.
- ^ Behr MA , Kapur V ., The evidence for Mycobacterium paratuberculosis in Crohn's disease., in Curr Opin Gastroenterol., 2008.
- ^ Sechi LA, Scanu AM, Molicotti P, Cannas S, Mura M, Dettori G, Fadda G, Zanetti S., Detection and Isolation of Mycobacterium avium subspecies paratuberculosis from intestinal mucosal biopsies of patients with and without Crohn's disease in Sardinia., in Am J Gastroenterol., 2005.
- ^ Naser, Saleh A; Collins, Michael T., Debate on the lack of evidence of Mycobacterium avium subsp. Paratuberculosis in Crohn's disease, in Inflammatory Bowel Diseases, 2005, DOI:10.1097/01.MIB.0000191609.20713.ea.
- ^ Hampson SJ1, Parker MC, Saverymuttu SH, Joseph AE, McFadden JJ, Hermon-Taylor J., Quadruple antimycobacterial chemotherapy in Crohn's disease: results at 9 months of a pilot study in 20 patients., in US National Library of Medicine, 1989.
- ^ Hermon-Taylor J., Treatment with drugs active against Mycobacterium avium subspecies paratuberculosis can heal Crohn's disease: more evidence for a neglected public health tragedy., in US National Library of Medicine, 2002.
- ^ Selby W, Pavli P, Crotty B, Florin T, Radford-Smith G, Gibson P, Mitchell B, Connell W, Read R, Merrett M, Ee H, Hetzel D, Two-year combination antibiotic therapy with clarithromycin, rifabutin, and clofazimine for Crohn's disease., in Gastroenterology, 2007, DOI:10.1053/j.gastro.2007.03.031, PMID 17570206.
- ^ Lalande JD, Behr M., NOD2 mediates host resistance to Mycobacterium Avium Paratubercolosis infection (PDF). URL consultato il 14 aprile 2014 (archiviato dall'url originale il 19 febbraio 2013).
- ^ Glubb, Dylan M; Gearry, Richard B; Barclay, Murray L; Roberts, Rebecca L; Pearson, John; Keenan, Jacqui I; McKenzie, Judy; Bentley, Robert W, NOD2 and ATG16L1 polymorphisms affect monocyte responses in Crohn's disease., in World Journal of Gastroenterology, 2011, DOI:10.3748/wjg.v17.i23.2829, PMID 21734790.
- ^ Clancy, R; Ren, Z; Turton, J; Pang, G; Wettstein, A, Molecular evidence for Mycobacterium avium subspecies paratuberculosis (MAP) in Crohn's disease correlates with enhanced TNF-alpha secretion, in Digestive and liver disease : official journal of the Italian Society of Gastroenterology and the Italian Association for the Study of the Liver, 2007, DOI:10.1016/j.dld.2006.12.006, PMID 17317344.
- ^ Nakase, H; Tamaki, H; Matsuura, M; Chiba, T; Okazaki, K, Involvement of mycobacterium avium subspecies paratuberculosis in TNF-α production from macrophage: Possible link between MAP and immune response in Crohn's disease, in Inflammatory Bowel Diseases, 2011, DOI:10.1002/ibd.21750, PMID 21990211.
- ^ Baumgart, Martin; Dogan, Belgin; Rishniw, Mark; Weitzman, Gil; Bosworth, Brian; Yantiss, Rhonda; Orsi, Renato H; Wiedmann, Martin et al., Culture independent analysis of ileal mucosa reveals a selective increase in invasive Escherichia coli of novel phylogeny relative to depletion of Clostridiales in Crohn's disease involving the ileum, in The ISME Journal, 2007, DOI:10.1038/ismej.2007.52, PMID 18043660.
- ^ Sasaki, M; Sitaraman, SV; Babbin, BA; Gerner-Smidt, P; Ribot, EM; Garrett, N; Alpern, JA; Akyildiz, A et al., Invasive Escherichia coli are a feature of Crohn's disease. Laboratory investigation; a journal of technical methods and pathology, 2007, DOI:10.1038/labinvest.3700661, PMID 17660846.
- ^ Darfeuille-Michaud, A; Boudeau, J; Bulois, P; Neut, C; Glasser, AL; Barnich, N; Bringer, MA; Swidsinski, A et al., High prevalence of Adherent-invasive Escherichia coli associated with ileal mucosa in Crohn's disease, in Gastroenterology, 2004, DOI:10.1053/j.gastro.2004.04.061, PMID 15300573.
- ^ Baumgart, M; Dogan, B; Rishniw, M; Weitzman, G; Bosworth, B; Yantiss, R; Orsi, RH; Wiedmann, M et al., Culture independent analysis of ileal mucosa reveals a selective increase in invasive Escherichia coli of novel phylogeny relative to depletion of Clostridiales in Crohn's disease involving the ileum, in The ISME Journal, 2007, DOI:10.1038/ismej.2007.52, PMID 18043660.
- ^ Nickerson, K. P.; McDonald, C., Crohn's Disease-Associated Adherent-Invasive Escherichia coli Adhesion is Enhanced by Exposure to the Ubiquitous Dietary Polysaccharide Maltodextrin, in Mizoguchi, Emiko. PLoS ONE, 2012, DOI:10.1371/journal.pone.0052132, PMID 23251695.
- ^ Martinez-Medina, Margarita; Naves, Plínio; Blanco, Jorge; Aldeguer, Xavier; Blanco, Jesus E; Blanco, Miguel; Ponte, Carmen; Soriano, Francisco et al., Biofilm formation as a novel phenotypic feature of adherent-invasive Escherichia coli (AIEC), in BMC Microbiology, 2009, DOI:10.1186/1471-2180-9-202, PMID 19772580.
- ^ Abderrahman Chargui, Annabelle Cesaro, Sanda Mimouna, Mohamed Fareh, Patrick Brest, Philippe Naquet, Arlette Darfeuille-Michaud, Xavier Hébuterne, Baharia Mograbi, Valérie Vouret-Craviari, Paul Hofman, Subversion of Autophagy in Adherent Invasive Escherichia coli-Infected Neutrophils Induces Inflammation and Cell Death, in PLoS ONE, 2012, DOI:10.1371/journal.pone.0051727.
- ^ Melanie Craven, Charlotte E. Egan, Scot E. Dowd, Sean P. McDonough, Belgin Dogan, Eric Y. Denkers, Dwight Bowman, Ellen J. Scherl, Kenneth W. Simpson, Inflammation Drives Dysbiosis and Bacterial Invasion in Murine Models of Ileal Crohn’s Disease, in PLoS ONE, 2012, DOI:10.1371/journal.pone.0041594.
- ^ Barnich, N; Darfeuille-Michaud, A, Adherent-invasive Escherichia coli and Crohn's disease, in Current Opinion in Gastroenterology, 2007, DOI:10.1097/MOG.0b013e3280105a38, PMID 17133079.
- ^ Hugot, Jean-Pierre; Alberti, Corinne; Berrebi, Dominique; Bingen, Edouard; Cézard, Jean-Pierre, Crohn's disease: The cold chain hypothesis (PDF), in The Lancet, 2003, DOI:10.1016/S0140-6736(03)15024-6, PMID 14683664.
- ^ Forbes, Alastair; Kalantzis, Tommy, Crohn's disease: The cold chain hypothesis, in International Journal of Colorectal Disease, 2005, DOI:10.1007/s00384-005-0003-7, PMID 16059694.
- ^ Subramanian, S.; Roberts, C. L.; Hart, C. A.; Martin, H. M.; Edwards, S. W.; Rhodes, J. M.; Campbell, B. J., Replication of Colonic Crohn's Disease Mucosal Escherichia coli Isolates within Macrophages and Their Susceptibility to Antibiotics, in Antimicrobial Agents and Chemotherapy, 2007, DOI:10.1128/AAC.00375-07, PMID 18070962.
- ^ Chiedzo M. Mpofu, Barry J. Campbell, Sreedhar Subramanian, Stuart Marshall–Clarke, C. Anthony Hart, Andy Cross, Carol L. Roberts, Adrian McGoldrick, Steven W. Edwards, Jonathan M. Rhodes, Microbial Mannan Inhibits Bacterial Killing by Macrophages: A Possible Pathogenic Mechanism for Crohn's Disease, in Gastroenterology, 2007, DOI:10.1053/j.gastro.2007.08.004, PMID 17919633.
- ^ New insights into Crohn's Disease, in Research Intelligence, University of Liverpool, 2008 (archiviato dall'url originale il 23 settembre 2013).
- ^ European Commission Directorate-General Health & Consumer Protection, Possible links between Crohn's disease and Paratuberculosis (PDF), 2000 (archiviato dall'url originale il 17 dicembre 2008).
- ^ Gui, G. P.; Thomas, P. R.; Tizard, M. L.; Lake, J.; Sanderson, J. D.; Hermon-Taylor, J., Two-year-outcomes analysis of Crohn's disease treated with rifabutin and macrolide antibiotics, in Journal of Antimicrobial Chemotherapy, 1997, DOI:10.1093/jac/39.3.393, PMID 9096189.
- ^ Cobrin GM, Abreu MT, Defects in mucosal immunity leading to Crohn's disease, in Immunol. Rev., vol. 206, 2005, pp. 277–95, DOI:10.1111/j.0105-2896.2005.00293.x, PMID 16048555.
- ^ Charles O. Elson, Yingzi Cong e Casey T. Weaver, Monoclonal Anti–Interleukin 23 Reverses Active Colitis in a T Cell–Mediated Model in Mice, in Gastroenterology, vol. 132, n. 7, 2007-06, pp. 2359–2370, DOI:10.1053/j.gastro.2007.03.104. URL consultato il 18 luglio 2021.
- ^ Prescott NJ, Fisher SA, Franke A, et al., A nonsynonymous SNP in ATG16L1 predisposes to ileal Crohn's disease and is independent of CARD15 and IBD5, in Gastroenterology, vol. 132, n. 5, 2007, pp. 1665–71, DOI:10.1053/j.gastro.2007.03.034, PMID 17484864.
- ^ Marks DJ, Segal AW., Innate immunity in inflammatory bowel disease: a disease hypothesis, in J Pathol., vol. 214, n. 2, gennaio 2008, pp. 260–6, DOI:10.1002/path.2291, PMC 2635948, PMID 18161747. URL consultato il 4 novembre 2009.
- ^ Dessein R, Chamaillard M, Danese S, Innate immunity in Crohn's disease: the reverse side of the medal, in J Clin Gastroenterol, vol. 42, Suppl 3 Pt 1, settembre 2008, pp. S144–7, DOI:10.1097/MCG.0b013e3181662c90, PMID 18806708. URL consultato il 4 novembre 2009.
- ^ a b Mark Pimentel, Michael Chang, Evelyn J. Chow, Siamak Tabibzadeh, Viorelia Kirit-Kiriak, Stephan R. Targan, Henry C. Lin, Identification of a prodromal period in Crohn's disease but not ulcerative colitis, in American Journal of Gastroenterology, vol. 95, n. 12, 2000, pp. 3458–62, DOI:10.1111/j.1572-0241.2000.03361.x, PMID 11151877.
- ^ (EN) Crohn's Disease Symptoms, Diet, Pictures, Drugs, Life Expectancy, su eMedicineHealth. URL consultato il 18 luglio 2021.
- ^ David Zieve, George F Longstreth, Crohn's Disease, su healthline.com, ADAM Health Illustrated Encyclopedia, 18 ottobre 2009. URL consultato il 16 agosto 2010 (archiviato dall'url originale il 27 agosto 2010).
- ^ a b c Daniel K. Podolsky, Inflammatory bowel disease, in New England Journal of Medicine, vol. 346, n. 6, 2002, pp. 417–29, DOI:10.1056/NEJMra020831, PMID 12167685. URL consultato il 2 luglio 2006.
- ^ M. H. Mueller, M. E. Kreis, M. L. Gross, H. D. Becker, T. T. Zittel & E. C. Jehle, Anorectal functional disorders in the absence of anorectal inflammation in patients with Crohn's disease, in British Journal of Surgery, vol. 89, n. 8, 2002, pp. 1027–31, DOI:10.1046/j.1365-2168.2002.02173.x, PMID 12153630.
- ^ a b c d e f internetmedicin.se > Inflammatorisk tarmsjukdom, kronisk, IBD By Robert Löfberg. Retrieved Oct 2010 Translate.
- ^ a b c d e Stephen B. Hanauer, William Sandborn, Management of Crohn's disease in adults (PDF), in American Journal of Gastroenterology, vol. 96, n. 3, 1º marzo 2001, pp. 635–43, DOI:10.1111/j.1572-0241.2001.03671.x, PMID 11280528. URL consultato il 7 novembre 2009 (archiviato dall'url originale il 27 settembre 2011).
- ^ Ramzi S. Cotran, Tucker Collins e Stanley L. Robbins, Robbins pathologic basis of disease., 6th ed., Saunders, 1999, ISBN 0-7216-7335-X, OCLC 39465455. URL consultato il 18 luglio 2021.
- ^ Taylor B, Williams G, Hughes L, Rhodes J, The histology of anal skin tags in Crohn's disease: an aid to confirmation of the diagnosis, in Int J Colorectal Dis, vol. 4, n. 3, 1989, pp. 197–9, DOI:10.1007/BF01649703, PMID 2769004.
- ^ Oren K. Fix, Jorge A. Soto, Charles W. Andrews and Francis A. Farraye, Gastroduodenal Crohn's disease, in Gastrointestinel Endoscopy, vol. 60, n. 6, 2004, p. 985, DOI:10.1016/S0016-5107(04)02200-X, PMID 15605018.
- ^ a b H.A. Büller, Problems in diagnosis of IBD in children, in The Netherlands Journal of Medicine, vol. 50, n. 2, 1997, pp. S8–S11, DOI:10.1016/S0300-2977(96)00064-2, PMID 9050326.
- ^ R.M. Beattie, N. M. Croft, J. M. Fell, N. A. Afzal and R. B. Heuschkel, Inflammatory bowel disease, in Archives of Disease in Childhood, vol. 91, n. 5, 2006, pp. 426–32, DOI:10.1136/adc.2005.080481, PMC 2082730, PMID 16632672.
- ^ S. J. O'Keefe, Nutrition and gastrointestinal disease, in Scandinavian Journal of Gastroenterology Supplement, vol. 31, n. 220, 1996, pp. 52–9, DOI:10.3109/00365529609094750, PMID 8898436.
- ^ Silvio Danese, Stefano Semeraro, Alfredo Papa, Italia Roberto, Franco Scaldaferri, Giuseppe Fedeli, Giovanni Gasbarrini, Antonio Gasbarrini, Extraintestinal manifestations in inflammatory bowel disease, in World Journal of Gastroenterology, vol. 11, n. 46, 2005, pp. 7227–36, PMID 16437620. URL consultato il 7 novembre 2009 (archiviato dall'url originale il 7 luglio 2007).
- ^ Arthritis, su healthline.com, Healthline Networks, Inc., 10 ottobre 2008. URL consultato il 16 agosto 2010 (archiviato dall'url originale il 21 luglio 2010).
- ^ Michael Bernstein, Sue Irwin and Gordon R. Greenberg, Maintenance infliximab treatment is associated with improved bone mineral density in Crohn's disease, in The American Journal of Gastroenterology, vol. 100, n. 9, 2005, pp. 2031–5., DOI:10.1111/j.1572-0241.2005.50219.x, PMID 16128948.
- ^ a b Crohn's disease. professionals.epilepsy.com. Retrieved on July 13, 2007.
- ^ Zadik Y, Drucker S, Pallmon S, Migratory stomatitis (ectopic geographic tongue) on the floor of the mouth, in J Am Acad Dermatol, vol. 65, n. 2, agosto 2011, pp. 459-60, PMID 21763590.
- ^ Ekbom A, Helmick C, Zack M, Adami H, Increased risk of large-bowel cancer in Crohn's disease with colonic involvement, in Lancet, vol. 336, n. 8711, 1990, pp. 357–9, DOI:10.1016/0140-6736(90)91889-I, PMID 1975343.
- ^ Collins P, Mpofu C, Watson A, Rhodes J, Strategies for detecting colon cancer and/or dysplasia in patients with inflammatory bowel disease, in Alastair J Watson (a cura di), Cochrane Database Syst Rev, n. 2, 2006, pp. CD000279, DOI:10.1002/14651858.CD000279.pub3, PMID 16625534.
- ^ Evans J, Steinhart A, Cohen Z, McLeod R, Home total parenteral nutrition: an alternative to early surgery for complicated inflammatory bowel disease, in J Gastrointest Surg, vol. 7, n. 4, 2003, pp. 562–6, DOI:10.1016/S1091-255X(02)00132-4, PMID 12763417.
- ^ C Kaplan, IBD and Pregnancy: What You Need to Know, su ccfa.org, Crohn's and Colitis Foundation of America, 21 ottobre 2005. URL consultato il 7 novembre 2009 (archiviato dall'url originale il 17 febbraio 2012).
- ^ Rita Del Pinto, Davide Pietropaoli e Apoorva K. Chandar, Association Between Inflammatory Bowel Disease and Vitamin D Deficiency: A Systematic Review and Meta-analysis, in Inflammatory Bowel Diseases, 12 agosto 2015, DOI:10.1097/MIB.0000000000000546. URL consultato il 26 settembre 2015.
- ^ (EN) HCP: Pill Cam, Capsule Endoscopy, Esophageal Endoscopy, su givenimaging.com. URL consultato il 27 gennaio 2012.
- ^ a b Amy K. Hara, Jonathan A. Leighton, Russell I. Heigh, Virender K. Sharma, Alvin C. Silva, Giovanni De Petris, Joseph G. Hentz and David E. Fleischer, Crohn disease of the small bowel: preliminary comparison among CT enterography, capsule endoscopy, small-bowel follow-through, and ileoscopy, in Radiology, vol. 238, n. 1, gennaio 2006, pp. 128–34, DOI:10.1148/radiol.2381050296, PMID 16373764. URL consultato il 4 novembre 2009.
- ^ Stuart L. Triester, Jonathan A. Leighton, Grigoris I. Leontiadis, Suryakanth R. Gurudu, David E. Fleischer, Amy K. Hara, Russell I. Heigh, Arthur D. Shiff, and Virender K. Sharma, A meta-analysis of the yield of capsule endoscopy compared to other diagnostic modalities in patients with non-stricturing small bowel Crohn's disease, in The American Journal of Gastroenterology, vol. 101, n. 5, 2006, pp. 954–64, DOI:10.1111/j.1572-0241.2006.00506.x, PMID 16696781. URL consultato il 4 novembre 2009.
- ^ P.M. Dixon, M.E. Roulston and D.J. Nolan, The small bowel enema: a ten year review, in Clinical Radiology, vol. 47, n. 1, 1993, pp. 46–8, DOI:10.1016/S0009-9260(05)81213-9, PMID 8428417.
- ^ L. R. Carucci, M. S. Levine, Radiographic imaging of inflammatory bowel disease, in Gastroenterology Clinics of North America, vol. 31, n. 1, 2002, pp. 93–117, DOI:10.1016/S0889-8553(01)00007-3, PMID 12122746.
- ^ A. Rajesh, D.D.T. Maglinte, Multislice CT enteroclysis: technique and clinical applications, in Clinical Radiology, vol. 61, n. 1, 2006, pp. 31–9, DOI:10.1016/j.crad.2005.08.006, PMID 16356814.
- ^ Rivka Zissin, Marjorie Hertz, Alexandra Osadchy, Ben Novis and Gabriela Gayer, Computed Tomographic Findings of Abdominal Complications of Crohn's Disease—Pictorial Essay, in Canadian Association of Radiologists Journal, vol. 56, n. 1, 2005, pp. 25–35, PMID 15835588.
- ^ B. A. MacKalski, C. N. Bernstein, New diagnostic imaging tools for inflammatory bowel disease, in Gut, vol. 55, n. 5, 2005, pp. 733–41, DOI:10.1136/gut.2005.076612, PMC 1856109, PMID 16609136.
- ^ Luciene G Mota, Leukocyte-technetium-99m uptake in Crohn’s disease: Does it show subclinical disease?, in World Journal of Gastroenterology, vol. 16, n. 3, 2010, pp. 365, DOI:10.3748/wjg.v16.i3.365. URL consultato il 18 luglio 2021.
- ^ a b c Asher Kornbluth, David B. Sachar, Ulcerative colitis practice guidelines in adults (update): American College of Gastroenterology, Practice Parameters Committee (PDF), in American Journal of Gastroenterology, vol. 99, n. 7, luglio 2004, pp. 1371–85, DOI:10.1111/j.1572-0241.2004.40036.x, PMID 15233681. URL consultato il 7 novembre 2009 (archiviato dall'url originale il 6 aprile 2008).
- ^ Ulrika Broomé, Annika Bergquist, Primary sclerosing cholangitis, inflammatory bowel disease, and colon cancer, in Seminars in Liver Disease, vol. 26, n. 1, febbraio 2006, pp. 31–41, DOI:10.1055/s-2006-933561, PMID 16496231.
- ^ NA. Shepherd, Granulomas in the diagnosis of intestinal Crohn's disease: a myth exploded?, in Histopathology, vol. 41, n. 2, agosto 2002, pp. 166–8, DOI:10.1046/j.1365-2559.2002.01441.x, PMID 12147095.
- ^ U. Mahadeva, JP. Martin, NK. Patel e AB. Price, Granulomatous ulcerative colitis: a re-appraisal of the mucosal granuloma in the distinction of Crohn's disease from ulcerative colitis., in Histopathology, vol. 41, n. 1, luglio 2002, pp. 50–5, DOI:10.1046/j.1365-2559.2002.01416.x, PMID 12121237.
- ^ a b Pages 152-156 (Section: Inflammatory bowel disease(IBD)) in: Elizabeth D Agabegi; Agabegi, Steven S., Step-Up to Medicine (Step-Up Series), Hagerstwon, MD, Lippincott Williams & Wilkins, 2008, ISBN 0-7817-7153-6.
- ^ Martin Feller, Karin Huwiler e Alain Schoepfer, Long-term antibiotic treatment for Crohn's disease: systematic review and meta-analysis of placebo-controlled trials, in Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 50, n. 4, 15 febbraio 2010, pp. 473–480, DOI:10.1086/649923, PMID 20067425. URL consultato il 18 luglio 2021.
- ^ (EN) Antibiotics and Probiotics in IBD: Why, When, and How, su Medscape. URL consultato il 18 luglio 2021.
- ^ Cosimo Prantera e Maria Lia Scribano, Antibiotics and probiotics in inflammatory bowel disease: why, when, and how, in Current Opinion in Gastroenterology, vol. 25, n. 4, 2009-07, pp. 329–333, DOI:10.1097/MOG.0b013e32832b20bf. URL consultato il 18 luglio 2021.«Section "Antibiotics and Ulcerative Colitis"»
- ^ Clinical Research Alliance Update (PDF), su ccfa.org, Crohn's and Colitis Foundation of America, 1º maggio 2007. URL consultato il 14 febbraio 2008 (archiviato dall'url originale il 16 febbraio 2008).
- ^ a b WS Fries e B Nazario, Crohn's Disease: 54 Tips to Help You Manage, su webmd.com, WebMD, 16 maggio 2007. URL consultato il 14 febbraio 2008.
- ^ Brown AC, Rampertab SD, Mullin GE, Existing dietary guidelines for Crohn's disease and ulcerative colitis, in Expert Rev Gastroenterol Hepatol, giugno 2011, PMID 21651358.
- ^ van der Heide F, Dijkstra A, Albersnagel FA, Kleibeuker JH, Dijkstra G, Active and passive smoking behaviour and cessation plans of patients with Crohn's disease and ulcerative colitis, in van der Heide F, Dijkstra A, Albersnagel FA, Kleibeuker JH, Dijkstra G, giugno 2010, PMID 21122495.
- ^ Cosnes J, Smoking, physical activity, nutrition and lifestyle: environmental factors and their impact on IBD, in Cosnes J, 2010, PMID 20926865.
- ^ Allaire Schneider, Ivy Hossain e Julia VanderMolen, Comparison of remicade to curcumin for the treatment of Crohn's disease: A systematic review, in Complementary Therapies in Medicine, vol. 33, agosto 2017, pp. 32–38, DOI:10.1016/j.ctim.2017.06.002. URL consultato il 12 dicembre 2017.
- ^ E’ necessaria una terapia di mantenimento nel Crohn?, su ig-ibd.com, Gruppo Italiano per lo studio delle Malattie Infiammatorie Croniche Intestinali. URL consultato il 29 aprile 2012 (archiviato dall'url originale il 20 marzo 2014).
- ^ Fergus Shanahan, Crohn's disease, in The Lancet, vol. 359, n. 9300, Elsevier Science, 2002, p. 67.
- ^ PL. Lakatos, Z. Czegledi; T. Szamosi; J. Banai; G. David; F. Zsigmond; T. Pandur; Z. Erdelyi; O. Gemela; J. Papp; L. Lakatos, Perianal disease, small bowel disease, smoking, prior steroid or early azathioprine/biological therapy are predictors of disease behavior change in patients with Crohn's disease., in World J Gastroenterol, vol. 15, n. 28, luglio 2009, pp. 3504-10, PMID 19630105.
- ^ Nielsen OH, Vainer B, Rask-Madsen J, Review article: the treatment of inflammatory bowel disease with 6-mercaptopurine or azathioprine [collegamento interrotto], in Aliment. Pharmacol. Ther., vol. 15, n. 11, novembre 2001, pp. 1699–708, PMID 11683683.
- ^ Levesque BG, Loftus EV Jr, Initiating azathioprine for Crohn's disease, in Clin Gastroenterol Hepatol, maggio 2012, PMID 22330233.
- ^ Z. Lin, Y. Bai; P. Zheng, Meta-analysis: efficacy and safety of combination therapy of infliximab and immunosuppressives for Crohn's disease., in Eur J Gastroenterol Hepatol, vol. 23, n. 12, novembre 2011, pp. 1100-10, DOI:10.1097/MEG.0b013e32834b9544, PMID 21971373.
- ^ FDA Approves Cimzia to Treat Crohn's Disease, su fda.gov, Food and Drug Administration, 22 aprile 2008. URL consultato l'11 aprile 2009.
- ^ Sandborn, W.J., Colombel, J.F.; Enns, R.; Feagan, B.G.; Hanauer, S.B.; Lawrance, I.C.; Panaccione, R.; Sanders, M.; Schreiber, S.; Targan, S.; Others,, Natalizumab Induction and Maintenance Therapy for Crohn's Disease, in New England Journal of Medicine, vol. 353, n. 18, 2005, pp. 1912–25, DOI:10.1056/NEJMoa043335, PMID 16267322.
- ^ JK MacDonald e JWD McDonald, Natalizumab for induction of remission in Crohn's disease, in Cochrane Database of Systematic Reviews, John Wiley & Sons, Ltd, 19 luglio 2006, DOI:10.1002/14651858.cd006097. URL consultato il 18 luglio 2021.
- ^ Murray Longmore, Ian Wilkinson, Tom Turmezei, Chee Kay Cheung, Oxford Handbook of Clinicial Medicine, 7th edition, Oxford University Press, 2007, pp. 266–7, ISBN 0-19-856837-1.
- ^ Naftali T, Lev LB, Yablecovitch D, Half E, Konikoff FM., Treatment of Crohn's disease with cannabis: an observational study (PDF), in Isr Med Assoc J. 2011; 13(8):455-8.
- ^ Timna Naftali, Lihi Bar-Lev Schleider e Iris Dotan, Cannabis induces a clinical response in patients with Crohn's disease: a prospective placebo-controlled study, in Clinical Gastroenterology and Hepatology: The Official Clinical Practice Journal of the American Gastroenterological Association, vol. 11, n. 10, ottobre 2013, pp. 1276–1280.e1, DOI:10.1016/j.cgh.2013.04.034. URL consultato il 12 dicembre 2017.
- ^ AJ Tresca, Resection Surgery for Crohn's Disease, su ibdcrohns.about.com, About.com, 12 gennaio 2007. URL consultato il 14 febbraio 2008 (archiviato dall'url originale il 13 novembre 2007).
- ^ Ozuner G, Fazio VW, Lavery IC, Milsom JW, Strong SA, Reoperative rates for Crohn's disease following strictureplasty. Long-term analysis, in Dis. Colon Rectum, vol. 39, n. 11, 1996, pp. 1199–203, DOI:10.1007/BF02055108, PMID 8918424.
- ^ Short Bowel Syndrome Archiviato il 21 marzo 2014 in Internet Archive. as defined by the National Institute of Diabetes and Digestive and Kidney Diseases
- ^ M Rhodes, Intestinal transplant for Crohn's disease, su revolutionhealth.com, Everyday Health, 24 ottobre 2006. URL consultato il 22 marzo 2009.
- ^ Caprilli R, Gassull M, Escher J et al., European evidence based consensus on the diagnosis and management of Crohn's disease: special situations, in Gut, 55 Suppl 1, 2006, pp. i36–58, DOI:10.1136/gut.2005.081950c, PMC 1859996, PMID 16481630.
- ^ Review on efficacy and health services research studies of complementary and alternative medicine in inflammatory bowel disease.
- ^ D. Duricova, N. Pedersen; M. Elkjaer; M. Gamborg; P. Munkholm; T. Jess, Overall and cause-specific mortality in Crohn's disease: a meta-analysis of population-based studies., in Inflamm Bowel Dis, vol. 16, n. 2, febbraio 2010, pp. 347-53, DOI:10.1002/ibd.21007, PMID 19572377.
Bibliografia[modifica | modifica wikitesto]
Testi in italiano[modifica | modifica wikitesto]
- Ermes Orlandelli, Malattie infiammatorie croniche intestinali: il morbo di Crohn nel modello psiconeuroendocrinoimmunologico, Roma, Società Editrice Universo, 2002, ISBN 88-87753-71-7.
- E. Polli, [et al.], La malattia di Crohn, in Relazione all’85. Congresso della Società italiana di medicina interna ed all’86. Congresso della Società italiana di chirurgia, Roma, 1984, ISBN 88-7025-051-2.
- Bryan N. Brooke, La malattia di Crohn, a cura di Carlo Cafaro, Roma, Il pensiero scientifico, 1972. ISBN non esistente
- Robbins, Cotran, Le basi patologiche delle malattie, VII edizione, Ed. Elsevier e Masson, ISBN 978-88-214-3175-3.
- Harrison, Principi di Medicina Interna (il manuale - 16ª edizione), New York - Milano, McGraw-Hill, 2006, ISBN 88-386-2459-3.
- Claudio Rugarli, Medicina interna sistematica, 5ª ed., Milano, Elsevier - Masson, 2010, ISBN 88-214-3109-6.
Testi in inglese[modifica | modifica wikitesto]
Patofisiologia[modifica | modifica wikitesto]
- Joseph C. Sengen, Concise Dictionary of Modern Medicine, New York, McGraw-Hill, ISBN 978-88-386-3917-3.
- Stefan Silbernagl e Florian Lang, Color Atlas of Pathophysiology, Thieme, 20 dicembre 2009, pp. 32–, ISBN 978-3-13-116552-7.
- Lippincott Williams & Wilkins, Pathophysiology: A 2-In-1 Reference for Nurses, Lippincott Williams & Wilkins, 10 marzo 2004, pp. 363–, ISBN 978-1-58255-317-7.
- S. Rose, Gastrointestinal And Hepatobiliary Pathophysiology[collegamento interrotto], Hayes Barton Press, 31 ottobre 2004, pp. 310–, ISBN 978-1-59377-181-2.
- Professional Guide to Pathophysiology, Lippincott Williams & Wilkins, 7 gennaio 2010, pp. 330–, ISBN 978-1-60547-766-4.
Terapia[modifica | modifica wikitesto]
- Theodore M. Bayless e Stephen B. Hanauer, Advanced Therapy of Inflammatory Bowel Disease, PMPH-USA, 2001, pp. 465–, ISBN 978-1-55009-122-9.
- Russell D. Cohen, Inflammatory Bowel Disease: Diagnosis and Therapeutics, Springer, 16 marzo 2011, pp. 64–, ISBN 978-1-60327-432-6.
- Bayless e Stephen B Hanauer, Advanced Therapy of Inflammatory Bowel Disease, Volume 2: IBD and Crohn's Disease, PMPH-USA, 1º novembre 2011, pp. 728–, ISBN 978-1-60795-035-6.
- Pierre Michetti, Therapy of Crohn's Disease, Karger Publishers, 2005, ISBN 978-3-8055-7931-5.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su malattia di Crohn
Wikimedia Commons contiene immagini o altri file su malattia di Crohn
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) Crohn disease, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Crohn Online, su crohnonline.net.
- (EN) www.webmd.com - Crohn's disease, su webmd.com.
- (EN) www.mayoclinic.com - Crohn's disease, su mayoclinic.com.
- (EN) emedicine.medscape.com - Crohn's disease, su emedicine.medscape.com.
- (EN) digestive.niddk.nih.gov - Crohn's disease, su digestive.niddk.nih.gov. URL consultato il 19 luglio 2011 (archiviato dall'url originale il 9 giugno 2014).
| Controllo di autorità | Thesaurus BNCF 6362 · NDL (EN, JA) 00561182 |
|---|
