Cortisone
| Cortisone | |
|---|---|
 | |
 | |
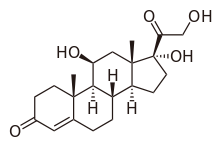
| Nome IUPAC | |
| 17,21-diidrossipregn-4-en-3,11,20-trione | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C21H28O5 |
| Massa molecolare (u) | 360,46 |
| Numero CAS | |
| Numero EINECS | 200-162-4 |
| PubChem | 222786 |
| DrugBank | DB14681 |
| SMILES | CC12CCC(=O)C=C1CCC3C2C(=O)CC4(C3CCC4(C(=O)CO)O)C |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 220-224 °C (493,15-497,15 K) |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | ---[1] |
Il cortisone è un ormone usato come farmaco.
Chimicamente è un corticosteroide di formula C21H28O5 strettamente correlato al corticosterone.
Corticosteroidi e adrenalina sono ormoni rilasciati nel sangue dalle ghiandole surrenali in situazioni di stress. Essi elevano la pressione arteriosa e preparano l'organismo alla reazione di lotta o fuga.
Il cortisone è il precursore inerte della molecola del cortisolo. Esso viene attivato per riduzione dell'11-cheto gruppo mediante un enzima chiamato 11-β-steroide-deidrogenasi. La forma attiva del cortisone è il cortisolo, detto anche idrocortisone.
In chimica farmaceutica il cortisone è usato nel trattamento di diversi disturbi, somministrato per via orale o parenterale. Uno degli effetti del cortisone sull'organismo, potenzialmente dannoso per certi aspetti, è di deprimere il sistema immunitario.
Il cortisone fu scoperto per primo dal chimico statunitense Edward Calvin Kendall al quale venne attribuito nel 1950 il Premio Nobel per la medicina e la fisiologia - insieme a Philip S. Hench e Tadeusz Reichstein - per la scoperta degli ormoni della corteccia surrenale, delle loro strutture e funzioni.
Storia[modifica | modifica wikitesto]

Edward Calvin Kendall, ricercatore della Mayo Clinic di Rochester (Stati Uniti), si interessò agli effetti di questi estratti e condusse ricerche sulla componente corticale delle ghiandole surrenali.
Isolò così da questi tessuti otto composti cristallini, assegnando a ciascuno una lettera dell'alfabeto. Il composto isolato come quinto in ordine di tempo, chiamato per questo "E", possedeva un elevato potere antinfiammatorio. Dopo complessi processi produttivi, Lewis H. Sarett nel 1944 arrivò alla sintesi del composto E, chiamandolo cortisone.
Nel 1949 fa il giro del mondo la notizia di un "artritico in bicicletta". In seguito infatti a una intuizione, Philip S. Hench, ex medico militare, usò il cortisone in un paziente affetto da artrite reumatoide, consentendogli di ritrovare la mobilità perduta.
A metà ottocento Thomas Addison, un medico inglese, aveva descritto dei particolari casi di persone colpite da una strana malattia mortale. Eseguendo delle autopsie, scoprì che tutti questi pazienti avevano le surrenali semidistrutte. A quei tempi pochi conoscevano o avevano sentito parlare delle ghiandole surrenali.
Nel 1716 l'Académie des Sciences de Bordeaux aveva bandito un concorso, con tanto di premio finale, il titolo “Qual è l'importanza delle surrenali?”, ma nessun concorrente aveva presentato qualcosa di serio e meritevole (https://philo-labo.fr/fichiers/Montesquieu%20-%2013%20Discours%20academiques.pdf - pag. 15)
. Delle surrenali si sapeva soltanto che erano ghiandole senza condotto, cioè quelle che riversano il loro prodotto direttamente nel sangue, oggi chiamate “ghiandole endocrine”. Ebbe così inizio una ricerca affannosa dei principi attivi prodotti dalle ghiandole.
Si vide che nelle surrenali erano distinguibili due parti, la midollare e la corticale, che la prima produceva un ormone detto adrenalina, ma che fosse la corticale ad essere di vitale importanza per l'organismo. Molti laboratori stavano facendo ricerche per trovare il principio attivo della corticale, da più parti erano arrivate notizie circa la produzione di un estratto rilevatosi utile in pazienti colpiti dalla malattia di Addison.
Alla fine degli anni trenta si arrivò alla conclusione che la corticale liberava sia ormoni regolatori dell'equilibrio salino, o minerale, dunque chiamata mineralcorticoidi, sia ormoni che controllavano il metabolismo degli zuccheri, o glucidi, detti per questo glucocorticoidi. La corticale produceva una miscela di composti diversi, che studiarono Edward Kendall (USA) e Tadeus Reichstein (Basilea). Scoprirono che queste sostanze erano degli steroidi che chiamarono composto A, B, C, ecc. Kendall scoprì che i composti A, B, E e F restituivano agli animali privi di surrenali la possibilità di resistere a particolari situazioni di stress.
Durante la seconda guerra mondiale i servizi segreti statunitensi scoprirono che alcune delle sostanze studiate da Kendall, in particolare il composto E, veniva somministrato agli aviatori della Luftwaffe, e li faceva sentire a proprio agio anche oltre i 13.000 metri di altezza. Questo fece in modo che ci fosse una brusca accelerata delle indagini, era necessario che il composto E fosse disponibile anche per gli aviatori statunitensi.
All'inizio del 1941, al termine di un convegno, Kendall e Hench (un altro medico che analizzava le sostanze, cercando di aiutare i pazienti che soffrivano di artrite reumatoide), presero il formale impegno di provare il composto E nei pazienti con artrite reumatoide non appena la sostanza fosse stata disponibile. Nel 1944, Lewis Sarett, un chimico della casa farmaceutica Merck, era riuscito a sintetizzare in laboratorio il composto E, a partire da un'altra molecola, l'acido deossicolico, ricavato dalla bile dei bovini macellati. Così Hench chiese alla casa farmaceutica di sperimentare la nuova sostanza su una ventinovenne affetta da una grave forma di artrite reumatoide. La risposta fu affermativa, e così il 28 settembre 1948 fu fatta la prima storica iniezione del farmaco. La risposta fu immediata, dopo appena tre giorni la signora era già migliorata e continuò a migliorare ulteriormente nei giorni successivi. La sostanza fu poi sperimentata anche su pazienti affetti dalla malattia di Addison e gli effetti furono ottimi. Le notizie girarono per tutto il mondo, ma ci fu una confusione, molti pensarono che il composto E e la vitamina E fossero la stessa cosa, così per evitare ogni equivoco, Kendall e Hench decisero di chiamare la sostanza cortisone. Mentre il cortisone liberava da infiammazione le doloranti articolazioni dei malati, la scoperta del cortisone fu paragonata a quella della penicillina. Il cortisone fu poi prodotto in diversi modi, da patate dolci messicane a ormoni femminili, ecc. Nel 1950, Kendall, Hench e Reichstein vinsero il premio Nobel per la fisiologia e la medicina.
Avvertenze[modifica | modifica wikitesto]
Osteoporosi: la somministrazione di corticosteroidi, in particolare a dosaggi elevati e/o per tempi prolungati, può indurre perdita di massa ossea con un aumento del rischio di frattura. Valutare, sulla base del dosaggio e della durata del trattamento, la necessità di un monitoraggio periodico della densità ossea, tramite esame radiografico della colonna vertebrale. Alcuni autori raccomandano nei pazienti in terapia corticosteroidea superiore a 3 mesi, per la prevenzione dell'osteoporosi, oltre alla supplementazione di calcio, vitamina D, dieta proteica e regolare esercizio fisico, l'uso di bifosfonati o di analoghi dell'ormone paratiroideo nei pazienti con rischio elevato di frattura ossea[2][3].
Effetti e usi[modifica | modifica wikitesto]
Uno degli effetti potenzialmente dannosi del cortisone è però quello di sopprimere il sistema immunitario (una possibile spiegazione della correlazione tra stress e malattie), ma appunto per questo motivo è usato per sopprimere le risposte autoimmuni in persone sottoposte a trapianti di organi, al fine di prevenirne il rigetto.
Il cortisone è un farmaco oggi usato in una numerosa varietà di trattamenti, e può essere somministrato per via orale o parenterale.
Effetti collaterali[modifica | modifica wikitesto]
Il cortisone e i corticosteroidi possono avere vari effetti collaterali[4] e, anche se usati topicamente o per inalazione, possono incrementare il rischio di diabete[5] e osteoporosi[6]. Altri effetti collaterali comuni sono immunosoppressione, infezioni, disfunzioni sessuali, ipertensione, leucopenia, depressione, malattie cardiocircolatorie.
Ha importanti effetti catabolici con accumulo di adipe e perdita di massa magra, contrastati con la prescrizione medica di DHEA.
Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. dell'11.10.2012
- ^ Trombetti A. et al., Praxis (Bern 1994), 2004, 93 (11), 407
- ^ Aubry-Rozier B. et al., Rev. Med. Suisse, 2010, 6 (235), 307
- ^ Use of oral corticosteroids and risk of fractures. [J Bone Miner Res. 2000] - PubMed result
- ^ Topical corticosteroids and the risk of diabetes m... [Drug Saf. 2009] - PubMed result
- ^ Systemic adverse effects of inhaled corticosteroid... [Arch Intern Med. 1999] - PubMed result
Bibliografia[modifica | modifica wikitesto]
- Kruse DW, Intraarticular cortisone injection for osteoarthritis of the hip. Is it effective? Is it safe?, in Curr Rev Musculoskelet Med, vol. 1, n. 3-4, dicembre 2008, pp. 227–33, DOI:10.1007/s12178-008-9029-0, PMC 2682414, PMID 19468910.
- Woodward R. B., Sondheimer F., Taub D., The Total Synthesis of Cortisone, in Journal of the American Chemical Society, vol. 73, 1951, pp. 4057–4057, DOI:10.1021/ja01152a551.
- Ingle DJ, The biologic properties of cortisone: a review [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 10, n. 10, ottobre 1950, pp. 1312–54, PMID 14794756.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «cortisone»
Wikizionario contiene il lemma di dizionario «cortisone» Wikimedia Commons contiene immagini o altri file su cortisone
Wikimedia Commons contiene immagini o altri file su cortisone
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) cortisone, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 20981 · LCCN (EN) sh85033100 · GND (DE) 4131407-4 · BNF (FR) cb119816608 (data) · J9U (EN, HE) 987007567887605171 |
|---|