Dengue
| Dengue | |
|---|---|
| Specialità | infettivologia |
| Eziologia | infettiva |
| Classificazione e risorse esterne (EN) | |
| ICD-10 | A97 |
| OMIM | 614371 |
| MeSH | D003715 |
| MedlinePlus | 001374 |
| eMedicine | 215840 |
| Sinonimi | |
| Febbre spaccaossa Febbre dandy | |
La febbre dengue, più conosciuta semplicemente come dengue, è una malattia infettiva tropicale causata dal Dengue virus. Il virus esiste in cinque sierotipi differenti (DENV-1, DENV-2, DENV-3, DENV-4, DENV-5) e generalmente l'infezione con un tipo garantisce un'immunità a vita per quel tipo, mentre comporta solamente una breve immunità nei confronti degli altri. L'ulteriore infezione con un altro sierotipo comporta un aumento del rischio di complicanze gravi.
La malattia è trasmessa da zanzare del genere Aedes, in particolar modo la specie Aedes aegypti. Si presenta con febbre, cefalea, dolore muscolare e articolare, oltre al caratteristico esantema simile a quello del morbillo. In una piccola percentuale dei casi si sviluppa una febbre emorragica pericolosa per la vita, con trombocitopenia, emorragie e perdita di liquidi, che può evolvere in shock circolatorio e morte. La prevenzione si ottiene mediante l'eliminazione delle zanzare e del loro habitat, per limitare l'esposizione al rischio di trasmissione.[1][2]
La terapia è di supporto e si basa sull'idratazione in caso di una forma lieve-moderata di malattia e, nei casi più gravi, sulla somministrazione endovenosa di liquidi e sull'emotrasfusione. La prima descrizione della malattia è del 1779 e la sua eziologia è stata dimostrata nei primi anni del XX secolo. L'incidenza della dengue è cresciuta molto rapidamente a partire dagli anni sessanta, con circa 50-100 milioni di persone infettate ogni anno, e risulta endemica in 110 paesi.[3][4]
Epidemiologia e storia[modifica | modifica wikitesto]
Le origini del termine dengue non sono note, ma una delle teorie più accreditate vuole che derivi dalla frase in lingua swahili Ka-dinga pepo, che descrive una malattia causata da uno spirito maligno[5]. Il termine swahili dinga potrebbe derivare dalla parola spagnola dengue, che significa fastidioso, attento, termini che descrivono l'andatura di una persona che soffre il caratteristico dolore osseo dovuto alla malattia[6]. È tuttavia possibile che sia il termine spagnolo a derivare da una parola simile in lingua swahili[5]. Gli schiavi delle Indie Occidentali erano chiamati dandy (damerino in italiano) a causa della postura e dell'andatura, pertanto la malattia è conosciuta anche come febbre dandy[7][8]. Il termine febbre spaccaossa fu invece utilizzato per la prima volta durante l'epidemia del 1789-90 a Filadelfia[9][10]. Il termine dengue divenne il più utilizzato solo a partire dal 1828[8].
Storia[modifica | modifica wikitesto]
Il primo caso di dengue mai documentato risale probabilmente all'enciclopedia medica cinese realizzata durante la dinastia Jìn, tra il 265 e il 420, in riferimento a un "veleno acquoso" associato a insetti volanti[5][11]. Numerose epidemie sono state descritte durante il XVII secolo, ma la prima documentata è quella che, tra il 1779 e il 1780 colpì Africa, America settentrionale e gran parte dell'Asia. Nel 1906 fu confermata la trasmissione della malattia mediata da zanzare del genere Aedes e, nel 1907, la dengue divenne la seconda malattia dopo la febbre gialla dove fosse stata dimostrata un'eziologia virale[12].
Fino agli anni quaranta del XX secolo, le epidemie furono infrequenti[11]. La grande diffusione della dengue durante e dopo la seconda guerra mondiale è stata attribuita al dissesto ecologico causato dalla guerra stessa, che portò alla diffusione della malattia in varie aree del mondo prima risparmiate e alla comparsa della sua forma emorragica. Questa forma fu descritta per la prima volta nelle Filippine nel 1953, diventando, a partire dagli anni settanta, una delle principali cause di mortalità infantile nelle Americhe e nelle isole dell'oceano Pacifico[11]. Nel 1981 si venne a sviluppare un'epidemia da virus DENV-2 in pazienti dell'America centrale e meridionale che avevano contratto il DENV-1 diversi anni prima e fece per la prima volta la sua comparsa lo shock caratteristico della fase critica della malattia[13].
Epidemiologia[modifica | modifica wikitesto]

La maggior parte di chi contrae la dengue si riprende senza problemi[14], mentre la mortalità è dell'1–5% qualora non venga instaurato alcun regime terapeutico[4] e inferiore all'1% nel caso di trattamento adeguato[14]. Tuttavia le forme più gravi della malattia conducono a morte nel 26% dei casi[4][15]. La dengue è endemica in 110 paesi[4] e infetta dai 50 ai 100 milioni di individui ogni anno, con circa mezzo milione di persone che necessitano di ospedalizzazione[1][16][17] e 12 500-25 000 decessi[18][19]. La dengue, oltre a essere la più comune malattia virale trasmessa da artropodi[20], ha un impatto sulla popolazione valutabile in 1 600 DALY ogni milione di abitanti, del tutto simile a quello della tubercolosi[21]. Come malattia tropicale la dengue è ritenuta seconda in importanza solo alla malaria[4], e l'Organizzazione mondiale della sanità la considera una delle sedici malattie tropicali neglette[22].
Tra il 1960 e il 2010, l'incidenza della dengue è aumentata di circa trenta volte[3], si crede in conseguenza dell'urbanizzazione, della crescita della popolazione e dei movimenti migratori[1]. La distribuzione geografica della malattia è nella zona equatoriale, dove vive il 70% dei due miliardi e mezzo di persone che abitano nelle aree endemiche dell'Asia e dei paesi che si affacciano sull'oceano Pacifico[3]. Negli Stati Uniti il tasso di infezione presso gli individui di ritorno da un soggiorno in un paese endemico è del 2,9–8,0%[23], secondo solamente a quello per la malaria[24]. Fino al 2003 si è ritenuto che la dengue potesse rappresentare una potenziale arma biologica, ma studi successivi hanno rigettato questa possibilità, poiché si ritiene che il virus sia troppo difficile da trasferire e dal momento che la malattia grave si presenta in una percentuale relativamente piccola di popolazione[9].
Eziologia[modifica | modifica wikitesto]
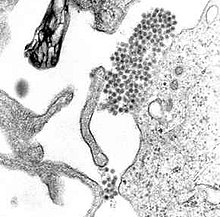
Quello responsabile della febbre dengue è un virus a RNA appartenente alla famiglia delle Flaviviridae, genere Flavivirus chiamato Dengue virus. Di questa famiglia fanno parte numerosi altri virus responsabili di febbre emorragica, tra cui quelli responsabili della febbre gialla, dell'encefalite di Saint-Louis, dell'encefalite giapponese e il virus del Nilo occidentale[13]. Tutte queste malattie sono trasmesse da artropodi, soprattutto zanzare e zecche, e i virus responsabili sono anche conosciuti come Arbovirus, dall'acronimo in lingua inglese arthropod borne virus (virus portato da artropodi)[13].
Come molti arbovirus, il virus della dengue permane in natura perché utilizza vettori ematofagi e ospiti vertebrati, mantenendosi soprattutto nelle foreste del Sud-est asiatico e dell'Africa. Nelle zone rurali la trasmissione avviene solitamente tramite puntura da parte di Aedes aegypti e altre del genere Aedes, tra le quali Aedes albopictus (zanzara tigre), mentre nelle città avviene quasi esclusivamente tramite Aedes aegypti, che risulta molto addomesticata[25]. Il ciclo vitale del vettore nelle aree urbane è generalmente limitato all'area in questione, ma la crescita incontrollata delle città nelle aree endemiche per la dengue ha portato a un aumento delle epidemie e della quantità di virus circolante, permettendone la diffusione anche in zone originariamente risparmiate e potrebbe, in futuro, rappresentare una minaccia per l'Europa[25].
Il genoma del virus contiene 11 000 paia di basi e codifica per tre proteine che formano il virione (C, prM, E) e sette diverse proteine che si ritrovano nella cellula ospite e sono necessarie per la replicazione virale (NS1, NS2a, NS2b, NS3, NS4a, NS4b, NS5)[20][21]. Il virus esiste in cinque diversi sierotipi, denominati DENV-1, DENV-2, DENV-3, DENV-4 e DENV-5[16][26], ciascuno dei quali può essere ugualmente causa della malattia[20]. Si ritiene che l'infezione con un sierotipo conferisca un'immunità a vita per il sierotipo in questione, ma solo a breve termine nei confronti degli altri[16][24]. La forma severa della malattia in caso di infezione secondaria avviene in particolar modo per gli individui esposti a DENV-1 che contraggano l'infezione da DENV-2 o DENV-3, oppure in persone esposte prima a DENV-3 e poi a DENV-2[21].
Trasmissione[modifica | modifica wikitesto]
Il Dengue virus è trasmesso soprattutto dalle zanzare del genere Aedes, in particolar modo la specie Aedes aegypti[16], che si trovano normalmente a una latitudine compresa tra il 35º parallelo nord e il 35º parallelo sud e a un'altitudine inferiore ai 1 000 metri s.l.m.[16], nutrendosi soprattutto durante il giorno[27]. Altre zanzare in grado di trasmettere la malattia sono Aedes albopictus, Aedes polynesiensis e Aedes scutellaris[16]. Gli esseri umani sono gli ospiti primari del virus[13][16], il quale può però essere rinvenuto anche in altri primati[28]; l'infezione può essere trasmessa con una singola puntura da parte del vettore[23].
Una femmina di zanzara che acquisisca sangue umano infetto diventa a sua volta infetta, con il virus localizzato a livello dell'apparato digerente. Circa 8-10 giorni dopo il virus invade e colonizza le cellule di altri tessuti, in particolar modo le ghiandole salivari, dalle quali è espulso insieme alla saliva. L'infezione non sembra avere effetti sulla zanzara, che rimane portatrice della malattia per il resto della propria vita. Aedes aegypti, a differenza delle altre, preferisce vivere e deporre le proprie uova in stretto rapporto con gli esseri umani, che rappresentano la sua fonte preferenziale di nutrimento rispetto ad altri vertebrati[29].
La dengue può essere trasmessa anche tramite infusione di emocomponenti o emoderivati e attraverso il trapianto di organi[30][31]. In paesi dove la malattia è endemica, come nel caso di Singapore, il rischio di infezione è compreso tra 1,6 e 6 ogni 10 000 trasfusioni di sangue[32], mentre la trasmissione verticale durante la gravidanza o l'allattamento è stata documentata[33].
Altre modalità di trasmissione interumana sono state descritte, ma sono tuttavia estremamente rare[24].
Patogenesi[modifica | modifica wikitesto]

Quando la zanzara infetta punge un essere umano, il virus penetra la cute insieme alla saliva dell'insetto. Una volta all'interno dell'organismo, si lega ai leucociti, vi penetra e si riproduce al loro interno. In particolare il virus dengue lega le cellule di Langerhans[34], entrandovi tramite endocitosi mediata dall'interazione tra proteine virali e specifiche proteine di membrana della cellula, la lectina DC-SIGN, CLEC5A e il recettore per il mannosio[20]. Il leucocita si sposta verso il linfonodo più vicino, mentre al suo interno il virus replica in vescicole legate al reticolo endoplasmatico, dove il genoma virale viene copiato e vengono prodotte le proteine virali. Il virione immaturo si sposta dunque all'apparato di Golgi dove avviene la maturazione definitiva grazie alla glicosilazione delle proteine virali ed esce dalla cellula mediante esocitosi. Oltre alle cellule di Langerhans, altri leucociti che vengono infettati sono i monociti e i macrofagi[20].
I leucociti infetti rispondono con la produzione di numerosi fattori, tra cui l'interferone, responsabili della maggior parte delle manifestazioni cliniche, quali la febbre, il dolore e gli altri sintomi simil-influenzali. La produzione di interferone fa parte del sistema immunitario innato e aumenta il livello di difesa da infezioni virali, favorendo la produzione di proteine del sistema di trasduzione mediato da JAK; alcuni sierotipi di Dengue virus sembrano avere la capacità di inibire questo segnale. La produzione di interferone attiva anche la produzione di anticorpi diretti contro antigeni virali, che mediano l'attivazione dei linfociti T contro le cellule infette[20]. Gli anticorpi permettono l'opsonizzazione e la conseguente fagocitosi da parte di cellule specializzate; alcuni di essi però, non legando ottimamente l'antigene, trasportano il virus lontano dai lisosomi del fagocita, in modo che esso non sia distrutto ma possa, bensì, continuare a replicare[20].
Nelle infezioni gravi la replicazione virale è molto aumentata, avviene anche in organi quali il fegato e il midollo osseo, e causa il passaggio di liquidi dal torrente circolatorio alle cavità corporee, attraverso l'endotelio dei piccoli vasi sanguigni in conseguenza di una sua disfunzione[18]. Ciò causa una riduzione del sangue circolante e la conseguente riduzione della pressione arteriosa, che può rivelarsi non sufficiente per le necessità dell'organismo e portare a uno stato di shock ipovolemico. D'altro canto la replicazione virale a livello del midollo osseo causa una disfunzione dell'emopoiesi, cui consegue la piastrinopenia responsabile delle emorragie tipiche della dengue[34]; la morte delle cellule infette a livello di questi organi può portare a un grande rilascio di citochine e fattori fibrinolitici, che peggiorano il quadro emorragico e favoriscono ulteriormente il danno endoteliale[34]. Non è del tutto chiaro perché un'infezione secondaria dovuta a un diverso sierotipo del virus porti a sviluppare un rischio sensibilmente aumentato di forma grave della malattia. L'ipotesi maggiormente condivisa si basa su un potenziamento mediato da anticorpi che si suppone possa essere causato dallo scarso legame di anticorpi non neutralizzanti e un direzionamento dei virioni verso il compartimento cellulare errato nei globuli bianchi che hanno fagocitato il virus per permetterne la distruzione[20][21]. Si ritiene tuttavia che questo possa non essere l'unico meccanismo patogenetico delle formi gravi di dengue[1]; altri possibili fattori che potrebbero avere un ruolo sono i linfociti T, alcune citochine e proteine del sistema del complemento[34].
In alcuni pazienti la malattia progredisce in una fase critica, successiva alla normalizzazione della temperatura corporea, che dura tipicamente uno o due giorni[35]. Durante questa fase si può presentare un accumulo di liquidi nel torace (versamento pleurico) e nell'addome (ascite) in conseguenza dell'aumento della permeabilità dei capillari. Questo può generare una condizione di ipovolemia e di scarsa perfusione degli organi vitali[35], spesso associata a disfunzione organica ed emorragie, in particolar modo digestive[4][35]. La condizione di shock o di febbre emorragica si manifesta in meno del 5% dei pazienti[4] e sono in particolar modo quelli infettati una seconda volta da un diverso sierotipo del Dengue virus a essere a rischio[4][20].
Complicanze[modifica | modifica wikitesto]
La forma grave della malattia è più comune nell'infanzia e, a differenza di molte altre malattie infettive, si presenta in bambini relativamente ben nutriti[4]. Le donne sono più colpite degli uomini[21] e la malattia può risultare particolarmente pericolosa in individui affetti da malattie croniche, quali il diabete mellito e l'asma bronchiale[21].
Occasionalmente il Dengue virus può infettare altri organi[35], sia in concomitanza al corteo sintomatologico classico, sia come unica manifestazione clinica[18]. Nello 0,5-6% dei casi si può presentare una riduzione dello stato di coscienza, imputabile a un'encefalite virale o, indirettamente, come conseguenza di un'insufficienza epatica[13][18]. Altre complicanze sono la mielite trasversa e la sindrome di Guillain-Barré[18], mentre le miocarditi sono rare[4][35].
Il polimorfismo di alcuni geni umani risulta correlato a maggior rischio di malattia grave. Tra questi sono compresi mutazioni del TNFα[1], del CTLA-4, del TGFβ[20] e particolari forme alleliche del complesso maggiore di istocompatibilità[21]; la carenza di glucosio-6-fosfato deidrogenasi, molto comune nei paesi africani, sembra anch'essa aumentare i rischi[34].
Clinica[modifica | modifica wikitesto]
La classificazione stilata nel 2009 dall'Organizzazione mondiale della sanità divide la dengue in due gruppi: non complicata e grave[1][14]. Questa sostituisce la classificazione del 1997, stilata dalla stessa organizzazione, che necessitava di maggior semplificazione essendo ritenuta troppo restrittiva (ma ancora utilizzata diffusamente)[14]. Essa prevedeva la suddivisione della malattia in febbre indifferenziata, febbre dengue e febbre emorragica dengue[4][15]. La forma emorragica era a sua volta suddivisa in quattro gradi di gravità: il grado I, caratterizzato da ecchimosi e positività alla prova del laccio in un paziente con febbre; il grado II, per pazienti con emorragia spontanea a carico di cute o altri organi; il grado III in presenza di shock; il grado IV in caso di shock grave con polso e pressione arteriosa non rilevabili[15]. I gradi III e IV sono definiti "sindrome da shock dengue"[14][15].
Segni e sintomi[modifica | modifica wikitesto]

Tipicamente i soggetti infettati con il virus della dengue sono asintomatici (80%) oppure hanno solo manifestazioni cliniche leggere, quale la febbre non complicata[1]. Circa il 5% dei pazienti va incontro a una forma più grave della malattia e solo in una piccola parte di essi la dengue può essere pericolosa per la vita[1][17]. Il periodo di incubazione dura tra i 3 e i 14 giorni, ma è solitamente compreso tra i 4 e i 7 giorni[36]; per questo motivo è possibile escludere la presenza della malattia in pazienti che manifestino sintomi oltre due settimane dopo il ritorno da un soggiorno in un'area endemica[4]. I bambini presentano sintomi simili a quelli del raffreddore comune e della gastroenterite (vomito e diarrea)[18], generalmente meno importanti rispetto agli adulti[37], sebbene siano maggiormente suscettibili a complicanze gravi[4].
La presentazione clinica tipica della dengue include febbre a esordio improvviso, cefalea tipicamente retrooculare, mialgia, artralgia ed esantema[1][24]. Il decorso della malattia può essere suddiviso in tre fasi: febbrile, critica e di recupero[35].
La fase febbrile è caratterizzata da febbre elevata, spesso superiore ai 40 °C, associata a dolore generalizzato e cefalea e dura solitamente tra i 2 e i 7 giorni[24][35]. Durante questa fase, il 50-80% dei pazienti con sintomi presenta un esantema cutaneo[24][38], che inizia tipicamente durante il 1º o 2º giorno di sintomi come un eritema, per assumere tra il 4º e il 7º giorno un aspetto morbilliforme[38][39]. A questo punto possono comparire petecchie[35] e si possono verificare piccoli episodi emorragici alla mucosa del naso e della bocca[4][24]. La febbre ha classicamente un andamento bifasico, ripresentandosi per un paio di giorni dopo la risoluzione iniziale, anche se il fenomeno ha una durata e delle tempistiche molto variabili[13][39].
Esami di laboratorio e strumentali[modifica | modifica wikitesto]
La prima alterazione visibile agli esami di laboratorio è il ridotto numero di globuli bianchi, condizione spesso seguita da riduzione del numero di piastrine e acidosi metabolica[4]. Nella forma grave la perdita di liquidi porta a emoconcentrazione, con aumento dell'ematocrito, e a riduzione dell'albumina circolante[4]. Versamento pleurico e ascite possono essere rilevati clinicamente solo quando importanti[4], mentre l'ecografia permette una diagnosi più precoce[1][4], anche se il suo utilizzo è limitato dalla scarsa disponibilità delle apparecchiature in alcuni paesi[1].
La dengue può essere diagnosticata anche mediante esami microbiologici[14], in particolar modo tramite l'isolamento del virus sul terreni di coltura, rilevamento del RNA virale dopo espansione tramite PCR, esami sierologici per la rilevazione di antigeni virali o anticorpi diretti verso di essi[21][40]. L'isolamento del virus e del suo genoma sono test più accurati di quelli sierologici, ma non sono diffusamente disponibili per via del loro costo elevato[40], mentre quest'ultimo e la PCR sono più accurati in particolar modo nella prima settimana di malattia[37], anche se tutti gli esami possono rivelarsi negativi nelle fasi precoci[4][21].
Tutti questi esami di laboratorio hanno un valore diagnostico solamente durante la fase acuta della malattia, eccezion fatta per la sierologia. La ricerca delle IgG e IgM, normalmente prodotte 5-7 giorni dopo l'infezione, può essere utilizzata per confermare la diagnosi di dengue anche nelle fasi tardive. Il titolo più elevato di IgM è rilevato dopo l'infezione primaria, ma esse sono prodotte anche in caso di infezione secondaria o terziaria; diventano non rilevabili 30-90 giorni dopo l'infezione primaria, ma, in caso di infezioni successive, scompaiono più rapidamente. Le IgG invece rimangono rilevabili per più di sessant'anni, anche in assenza di sintomi, e quindi risultano un ottimo indicatore di infezioni pregresse. Dopo l'infezione primaria raggiungono il loro picco dopo 2-3 settimane, mentre in corso di infezioni successive il picco è raggiunto prima e il titolo è solitamente più alto. Sia le IgG, sia le IgM provvedono all'immunità nei confronti di un determinato sierotipo. In laboratorio queste immunoglobuline possono legare altri Flavivirus, come quello della febbre gialla, rendendo difficile l'interpretazione dell'esame[21][24][41]. La rilevazione unicamente delle IgG non è considerata diagnostica a meno che il loro titolo non quadruplichi in campioni di sangue raccolti ad almeno due settimane di distanza dalla precedente raccolta. In una persona sintomatica, la rilevazione delle sole IgM è considerata diagnostica[41].
Diagnosi differenziale[modifica | modifica wikitesto]
Segnali d'allarme[14]
| ||||
| Dolore addominale | ||||
| Vomito in corso | ||||
| Epatomegalia | ||||
| Emorragia delle mucose | ||||
| Aumento dell'ematocrito con piastrinopenia | ||||
| Letargia | ||||
La diagnosi di dengue è solitamente clinica, basata sui sintomi riferiti e sull'esame obiettivo; questo è vero in particolar modo per le aree endemiche[1]. Tuttavia nelle fasi precoci è difficile da distinguere da altre infezioni virali[4]. La diagnosi è probabile se vengono rilevati in un paziente residente in un'area endemica, oltre alla febbre elevata, due tra i seguenti: nausea e vomito, esantema, dolore generalizzato, leucopenia, positività alla prova del laccio e uno qualsiasi dei segnali d'allarme riportati in tabella[14]. I segnali d'allarme si presentano tipicamente prima dell'esordio della forma grave di dengue[35]. La prova del laccio, particolarmente utile quando non sono disponibili esami di laboratorio, si esegue con l'applicazione per cinque minuti di uno sfigmomanometro al braccio e tramite la conta delle emorragie petecchiali che si presentano. Maggiore è il loro numero, più probabile è la diagnosi di malattia[35].
La dengue entra in diagnosi differenziale in ciascun individuo che manifesti febbre entro due settimane da un soggiorno in aree tropicali e subtropicali[37]. È difficilmente distinguibile dalla chikungunya, una malattia virale simile alla dengue sia per manifestazioni cliniche, sia per localizzazione delle aree endemiche[24]. Spesso l'iter diagnostico è orientato a escludere altre malattie simili, quali malaria, leptospirosi, febbre tifoide e meningite meningococcica[4].
Trattamento[modifica | modifica wikitesto]
Non esistono terapie specifiche per la dengue[1]. Le modalità di trattamento dipendono dalle manifestazioni cliniche, e possono andare dalla semplice idratazione orale a domicilio al ricovero con somministrazione di liquidi per via parenterale o emotrasfusioni[42]. La necessità di ricovero viene normalmente determinata sulla base dei segnali di allarme, soprattutto in presenza di comorbilità[4].
L'idratazione endovenosa si rende necessaria di solito per un paio di giorni[42] e la quantità di liquido da infondere è calcolata per garantire un'eliminazione renale di 0,5-1 mL/kg/h di urina, segni vitali stabili e una normalizzazione dell'ematocrito[4]. Procedure più invasive quali l'inserimento di un sondino nasogastrico, l'iniezione intramuscolare e le punture arteriose devono essere evitate a causa del rischio di sanguinamento[4]. Il paracetamolo viene utilizzato per il trattamento sintomatico della febbre e del dolore, mentre i FANS come l'aspirina o l'ibuprofene vanno evitati per non peggiorare il rischio di emorragia[42]. La trasfusione di sangue è richiesta precocemente nei pazienti con segni vitali instabili e a fronte di una tendenza dell'ematocrito a calare. Sebbene l'ematocrito non sia un indicatore dell'entità dell'emorragia buono quanto la concentrazione di emoglobina, si preferisce utilizzare questo indicatore piuttosto che attendere che l'emoglobina raggiunga un valore soglia per iniziare la trasfusione[43]. Possono essere somministrati sangue intero o globuli rossi concentrati, mentre non sono normalmente utilizzate trasfusioni di piastrine o di plasma fresco congelato[43].
Durante la fase di recupero dalla malattia la terapia idratante viene di solito sospesa per evitare una condizione di ipervolemia[4]; in caso si presenti tale condizione il trattamento prevede, in presenza di segni vitali stabili, la sola sospensione della somministrazione di liquidi[43] eventualmente associata a un diuretico dell'ansa quale la furosemide[43].
Prognosi[modifica | modifica wikitesto]
La fase di recupero, che dura circa 2-3 giorni[4], è caratterizzata dal riassorbimento dei liquidi e dal ripristino della volemia[35]. Il miglioramento è spesso sorprendente, ma si possono presentare bradicardia e prurito importante[4][35], oltre a un'eruzione cutanea maculo-papulare o di aspetto vasculitico, con successiva desquamazione cutanea[37]. Durante questa fase si può manifestare una condizione di sovraccarico di liquidi che, qualora evolva in edema cerebrale, può comportare alterazioni dello stato di coscienza e convulsioni[4]. Una condizione di affaticamento può permanere anche per settimane dopo la risoluzione clinica della malattia[37].
Prevenzione[modifica | modifica wikitesto]
Mutazioni del recettore della vitamina D e del frammento cristallizzabile delle IgG sembrano avere effetti protettivi, in particolar modo nelle forme gravi da infezione secondaria[21].

La prevenzione della malattia si basa quindi sul controllo della popolazione della zanzara vettrice e sulla protezione dal contatto dei residenti delle zone endemiche[2][44]. L'OMS raccomanda l'adozione di un programma integrato di controllo del vettore basato su cinque punti[2]:
- Patrocini, mobilitazioni sociali e legislazione al fine di assicurare il rinforzo degli organismi sanitari pubblici e delle comunità;
- Collaborazione tra sanità e altri ambiti, pubblici e privati;
- Approccio integrato al controllo della malattia per ottimizzare l'utilizzo delle risorse;
- Decisioni basate sull'evidenza clinica in modo da garantire che gli interventi siano mirati e appropriati;
- Rafforzamento delle capacità per garantire una risposta adeguata alla situazione locale.

Il principale metodo di controllo di Aedes aegypti consiste nell'eliminazione del suo habitat[2]. Questa può essere ottenuta nelle aree endemiche mediante lo svuotamento dei contenitori di acqua e l'utilizzo di agenti di controllo, ovvero specie animali la cui presenza riduca quella del vettore, o di insetticidi[2], anche se la spruzzatura di organofosfati o piretroidi non risulta efficace[17]. La riduzione delle raccolte di acqua all'aria aperta attraverso interventi ambientali è il metodo più utilizzato, date le preoccupazioni per eventuali effetti negativi sulla salute da parte degli insetticidi e le maggiori difficoltà logistiche per l'uso gli agenti di controllo[2]. La popolazione può prevenire le punture da parte del vettore utilizzando abiti che coprano completamente la cute, zanzariere o repellenti per insetti, in particolar modo il dietiltoluamide che si è rivelato essere il più efficace[23].
Dal 2016 è in uso un vaccino per il virus, approvato da FDA ed EMA[45].
Ricerca scientifica[modifica | modifica wikitesto]
Gli sforzi della ricerca scientifica per prevenire e trattare la dengue si basano sulla creazione di metodi di controllo del vettore[46], sullo sviluppo di un vaccino efficace e sullo studio di farmaci antivirali[44].
Per quanto riguarda il controllo del vettore sono stati sviluppati nuovi metodi per ridurre il numero di zanzare, ad esempio mediante l'introduzione nelle raccolte di acqua di Poecilia reticulata o Copepoda che si nutrono delle loro larve[46]. Sono in corso tentativi di infettare la popolazione di zanzare con batteri del genere Wolbachia, che sembrano rendere le zanzare parzialmente resistenti al virus[37].
Ci sono programmi in corso sullo sviluppo di un vaccino in grado di coprire tutti e quattro i sierotipi del dengue virus[44]. Uno dei problemi è che un vaccino potrebbe aumentare il rischio di malattia grave attraverso il meccanismo del potenziamento mediato da anticorpi[47]. Il vaccino ideale dovrebbe essere sicuro, accessibile e conveniente in termini di costo-beneficio, efficace dopo una o due somministrazioni, facile da trasportare e immagazzinare, non attivare il meccanismo del potenziamento mediato da anticorpi e coprire tutti i sierotipi[47]. A partire dal 2009, una serie di vaccini è entrata in una fase di studio e sperimentazione[9][21][47] e si ritiene che il primo possa essere introdotto in commercio a partire dal 2015[44].
Oltre al controllo del vettore e alla creazione di un vaccino efficace, sono presenti sforzi per sviluppare nuovi farmaci antivirali che siano efficaci nel trattamento della dengue e nella prevenzione delle forme gravi[48][49]. La determinazione della struttura delle proteine virali potrebbe essere d'aiuto nella realizzazione di farmaci efficaci[49]. Tra le possibili molecole bersaglio vi è la RNA polimerasi RNA-dipendente, codificata dal gene NS5 e responsabile della duplicazione del genoma virale. Altri approcci includono la creazione di specifici inibitori della proteasi vitale, codificata da NS3 e responsabile dello splicing delle proteine virali[50], di farmaci che inibiscano l'ingresso del virione nella cellula o di inibitori del processo di rivestimento in 5', necessario per la replicazione virale[48].
Note[modifica | modifica wikitesto]
- ^ a b c d e f g h i j k l m (EN) Whitehorn J, Farrar J, Dengue, in Br. Med. Bull., vol. 95, 2010, pp. 161–73, DOI:10.1093/bmb/ldq019, PMID 20616106.
- ^ a b c d e f WHO, pp. 59-60, 2009.
- ^ a b c WHO, p. 3, 2009.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab (EN) Ranjit S, Kissoon N, Dengue hemorrhagic fever and shock syndromes, in Pediatr. Crit. Care Med., vol. 12, n. 1, gennaio 2011, pp. 90–100, DOI:10.1097/PCC.0b013e3181e911a7, PMID 20639791.
- ^ a b c (EN) Etymologia: dengue, in Emerg. Infec. Dis., vol. 12, n. 6, giugno 2006, p. 893.
- ^ (EN) Harper D, Etymology: dengue, su Online Etymology Dictionary, 2001. URL consultato il 21 luglio 2012.
- ^ (EN) Definition of Dandy fever, su medterms.com, MedicineNet.com, 15 giugno 1998. URL consultato il 21 luglio 2012 (archiviato dall'url originale il 5 giugno 2011).
- ^ a b (EN) Halstead SB, Dengue (Tropical Medicine: Science and Practice), River Edge, N.J, Imperial College Press, 2008, pp. 1–10, ISBN 1-84816-228-6.
- ^ a b c (EN) Barrett AD, Stanberry LR, Vaccines for biodefense and emerging and neglected diseases, San Diego, Academic, 2009, pp. 287–323, ISBN 0-12-369408-6.
- ^ (EN) Rush AB, An account of the bilious remitting fever, as it appeared in Philadelphia in the summer and autumn of the year 1780, in Medical enquiries and observations, Philadelphia, Prichard and Hall, 1789, pp. 104–117.
- ^ a b c (EN) Gubler DJ, Dengue and dengue hemorrhagic fever, in Clin. Microbiol. Rev., vol. 11, n. 3, luglio 1998, pp. 480–96, PMC 88892, PMID 9665979. URL consultato il 21 luglio 2012 (archiviato dall'url originale il 25 ottobre 2011).
- ^ (EN) Henchal EA, Putnak JR, The dengue viruses, in Clin. Microbiol. Rev., vol. 3, n. 4, ottobre 1990, pp. 376–96, DOI:10.1128/CMR.3.4.376, PMC 358169, PMID 2224837. URL consultato il 21 luglio 2012 (archiviato dall'url originale il 25 luglio 2011).
- ^ a b c d e f (EN) Gould EA, Solomon T, Pathogenic flaviviruses, in The Lancet, vol. 371, n. 9611, febbraio 2008, pp. 500–9, DOI:10.1016/S0140-6736(08)60238-X, PMID 18262042.
- ^ a b c d e f g h WHO, p. 10, 2009.
- ^ a b c d (EN) WHO, Chapter 2: clinical diagnosis (PDF), in Dengue haemorrhagic fever: diagnosis, treatment, prevention and control, 2ª ed., Ginevra, World Health Organization, 1997, pp. 12–23, ISBN 92-4-154500-3.
- ^ a b c d e f g WHO, p. 14, 2009.
- ^ a b c (EN) Reiter P, Yellow fever and dengue: a threat to Europe?, in Euro Surveill, vol. 15, n. 10, 11 marzo 2010, p. 19509, PMID 20403310.
- ^ a b c d e f (EN) Varatharaj A, Encephalitis in the clinical spectrum of dengue infection, in Neurol. India, vol. 58, n. 4, 2010, pp. 585–91, DOI:10.4103/0028-3886.68655, PMID 20739797.
- ^ (EN) WHO media centre, Dengue and dengue haemorrhagic fever, su who.int, World Health Organization, marzo 2009. URL consultato il 21 luglio 2012.
- ^ a b c d e f g h i j (EN) Rodenhuis-Zybert IA, Wilschut J, Smit JM, Dengue virus life cycle: viral and host factors modulating infectivity, in Cell. Mol. Life Sci., vol. 67, n. 16, agosto 2010, pp. 2773–86, DOI:10.1007/s00018-010-0357-z, PMID 20372965.
- ^ a b c d e f g h i j k l (EN) Guzman MG, Halstead SB, Artsob H, et al., Dengue: a continuing global threat, in Nat. Rev. Microbiol., vol. 8, 12 Suppl, dicembre 2010, pp. S7–S16, DOI:10.1038/nrmicro2460, PMID 21079655.
- ^ (EN) WHO, Neglected tropical diseases, su who.int, World Health Organization. URL consultato il 21 luglio 2012.
- ^ a b c (EN) Center for Disease Control and Prevention, Chapter 5 – dengue fever (DF) and dengue hemorrhagic fever (DHF), su 2010 Yellow Book. URL consultato il 21 luglio 2012.
- ^ a b c d e f g h i (EN) Chen LH, Wilson ME, Dengue and chikungunya infections in travelers, in Curr. Opin. Infect. Dis., vol. 23, n. 5, ottobre 2010, pp. 438–44, DOI:10.1097/QCO.0b013e32833c1d16, PMID 20581669.
- ^ a b Gubler, pp. 376-377, 2010.
- ^ MS. Mustafa, V. Rasotgi; S. Jain; V. Gupta, Discovery of fifth serotype of dengue virus (DENV-5): A new public health dilemma in dengue control., in Med J Armed Forces India, vol. 71, n. 1, gennaio 2015, pp. 67-70, DOI:10.1016/j.mjafi.2014.09.011, PMID 25609867.
- ^ WHO, p. 59, 2009.
- ^ (EN) Vector-borne viral infections, su who.int, World Health Organization. URL consultato il 21 luglio 2012.
- ^ Gubler, pp. 377-378, 2010.
- ^ (EN) Wilder-Smith A, Chen LH, Massad E, Wilson ME, Threat of dengue to blood safety in dengue-endemic countries, in Emerg. Infect. Dis., vol. 15, n. 1, gennaio 2009, pp. 8–11, DOI:10.3201/eid1501.071097, PMC 2660677, PMID 19116042.
- ^ (EN) Stramer SL, Hollinger FB, Katz LM, et al., Emerging infectious disease agents and their potential threat to transfusion safety, in Transfusion, 49 Suppl 2, agosto 2009, pp. 1S–29S, DOI:10.1111/j.1537-2995.2009.02279.x, PMID 19686562.
- ^ (EN) Teo D, Ng LC, Lam S, Is dengue a threat to the blood supply?, in Transfus Med, vol. 19, n. 2, aprile 2009, pp. 66–77, DOI:10.1111/j.1365-3148.2009.00916.x, PMC 2713854, PMID 19392949.
- ^ (EN) Wiwanitkit V, Unusual mode of transmission of dengue, in Journal of Infection in Developing Countries, vol. 4, n. 1, gennaio 2010, pp. 51–4, PMID 20130380.
- ^ a b c d e (EN) Martina BE, Koraka P, Osterhaus AD, Dengue virus pathogenesis: an integrated view, in Clin. Microbiol. Rev., vol. 22, n. 4, ottobre 2009, pp. 564–81, DOI:10.1128/CMR.00035-09, PMC 2772360, PMID 19822889. URL consultato il 21 luglio 2012 (archiviato dall'url originale il 18 maggio 2011).
- ^ a b c d e f g h i j k l WHO, p. 25, 2009.
- ^ Gubler, p. 379, 2010.
- ^ a b c d e f (EN) Simmons CP, Farrar JJ, Nguyen vV, Wills B, Dengue, in N Engl J Med, vol. 366, n. 15, aprile 2012, pp. 1423–32, DOI:10.1056/NEJMra1110265, PMID 22494122.
- ^ a b (EN) Wolff K, Johnson RA (eds.), Viral infections of skin and mucosa, in Fitzpatrick's color atlas and synopsis of clinical dermatology, 6ª ed., New York, McGraw-Hill Medical, 2009, pp. 810–2, ISBN 978-0-07-159975-7.
- ^ a b (EN) Knoop KJ, Stack LB, Storrow A, Thurman RJ (eds.), Tropical medicine, in Atlas of emergency medicine, 3ª ed., New York, McGraw-Hill Professional, 2010, pp. 658–9, ISBN 0-07-149618-1.
- ^ a b WHO, pp. 90-95, 2009.
- ^ a b Gubler, p. 380, 2010.
- ^ a b c WHO, pp. 32-37, 2009.
- ^ a b c d WHO, pp. 40-43, 2009.
- ^ a b c d WHO, pp. 137-146, 2009.
- ^ (EN) Dengue Vaccine, su cdc.gov. URL consultato il 6 febbraio 2021.
- ^ a b WHO, p. 71, 2009.
- ^ a b c (EN) Webster DP, Farrar J, Rowland-Jones S, Progress towards a dengue vaccine, in Lancet Infect Dis, vol. 9, n. 11, novembre 2009, pp. 678–87, DOI:10.1016/S1473-3099(09)70254-3, PMID 19850226.
- ^ a b (EN) Sampath A, Padmanabhan R, Molecular targets for flavivirus drug discovery, in Antiviral Res., vol. 81, n. 1, gennaio 2009, pp. 6–15, DOI:10.1016/j.antiviral.2008.08.004, PMC 2647018, PMID 18796313.
- ^ a b (EN) Noble CG, Chen YL, Dong H, et al., Strategies for development of Dengue virus inhibitors, in Antiviral Res., vol. 85, n. 3, marzo 2010, pp. 450–62, DOI:10.1016/j.antiviral.2009.12.011, PMID 20060421.
- ^ (EN) Tomlinson SM, Malmstrom RD, Watowich SJ, New approaches to structure-based discovery of dengue protease inhibitors, in Infectious Disorders Drug Targets, vol. 9, n. 3, giugno 2009, pp. 327–43, PMID 19519486.
Bibliografia[modifica | modifica wikitesto]
- (EN) Gubler DJ, Dengue viruses, in Mahy BWJ, Van Regenmortel MHV (a cura di), Desk Encyclopedia of Human and Medical Virology, Boston, Academic Press, 2010, pp. 372–382, ISBN 0-12-375147-0.
- Harrison, Principi di medicina interna, 16ª ed., Milano, McGraw-Hill, 2005, ISBN 88-386-2999-4.
- Murray, Rosenthal, Microbiologia, Napoli, EdiSES, 2007, ISBN 88-7959-262-9.
- Robbins & Cotran, La basi patologiche delle malattie, Milano, Elsevier Italia, 2006, ISBN 88-85675-53-0.
- (EN) WHO, Dengue Guidelines for Diagnosis, Treatment, Prevention and Control (PDF), Ginevra, World Health Organization, 2009, ISBN 92-4-154787-1.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su febbre dengue
Wikimedia Commons contiene immagini o altri file su febbre dengue
Collegamenti esterni[modifica | modifica wikitesto]
- dengue, su sapere.it, De Agostini.
- (EN) dengue, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN) Opere riguardanti Dengue, su Open Library, Internet Archive.
- (EN) World Community Grid: Discovering Dengue Drugs – Together, su worldcommunitygrid.org. URL consultato il 21 luglio 2012 (archiviato dall'url originale il 15 aprile 2009).
- (EN) A worldwide mapping of dengue antiviral research (2010), su denguedrugs.com. URL consultato il 21 luglio 2012 (archiviato dall'url originale il 24 luglio 2012).
- (EN) Dengue, su who.int, Organizzazione mondiale della sanità. URL consultato il 21 luglio 2012.
- (EN) Dengue, su cdc.gov, U.S. Centers for Disease Control and Prevention. URL consultato il 21 luglio 2012.
- (EN) Dengue fever, su hpa.org.uk, UK Health Protection Agency. URL consultato il 21 luglio 2012.
- (EN) DengueMap, su healthmap.org, U.S. Centers for Disease Control and Prevention/HealthMap. URL consultato il 21 luglio 2012.
| Controllo di autorità | Thesaurus BNCF 49095 · LCCN (EN) sh85036728 · GND (DE) 4149075-7 · BNE (ES) XX535983 (data) · BNF (FR) cb11946040c (data) · J9U (EN, HE) 987007547997205171 · NSK (HR) 006463860 · NDL (EN, JA) 00561310 |
|---|
