Amminoglicosidi
Gli amminoglicosidi sono una classe di antibiotici battericidi formati da un gruppo glicosidico e uno amminico. Tale struttura conferisce loro proprietà basiche, elevata solubilità in acqua e di conseguenza idrofilia. A causa di questo, la loro capacità di diffusione attraverso le membrane è molto bassa (infatti solitamente richiedono il trasporto attivo).
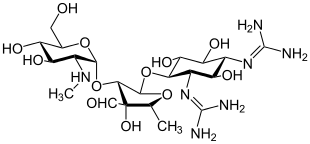
Il primo amminoglicoside descritto, la streptomicina, fruttò al suo scopritore, l'ucraino Selman Abraham Waksman, il Premio Nobel per la medicina nel 1952[1]. Questo antibiotico fu isolato dall'actinomicete Streptomyces griseus, da cui prende il nome; comunque tutta la classe deriva da due generi: Streptomicina, Neomicina, Kanamicina e Tobramicina furono isolate dal genere Streptomyces; mentre la Gentamicina e la Sisomicina sono state isolate da appartenenti al genere Micromonospora.
Meccanismo di azione
[modifica | modifica wikitesto]Gli amminoglicosidi esercitano la loro funzione legandosi a proteine specifiche della subunità 30S del ribosoma, inibendo la sintesi proteica del batterio[2][3] in almeno tre modi:
- blocco della formazione del complesso ribosoma-RNA messaggero;
- induzione di errori nella lettura del messaggero stesso, con l'incorporazione di amminoacidi errati provocando la sintesi di proteine anormali e/o non funzionali;
- impedimento della traslocazione del peptidil-tRNA dal sito A al sito P del ribosoma.
Tradizionalmente, le proprietà antibatteriche degli amminoglicosidi erano attribuite unicamente alla loro capacità di inibire la sintesi proteica legandosi irreversibilmente alla subunità minore del ribosoma. Questa spiegazione però non può giustificare, da sola, la potente attività battericida di questa classe di antibiotici, poiché altri antibiotici in grado di inibire la sintesi proteica -come le tetracicline- non sono battericidi. Recenti studi sembrano dimostrare che la loro azione litica incomincia a livello della membrana batterica.
Infatti sembra che gli amminoglicosidi abbiano la capacità di distruggere o causare la formazione di pori a livello della membrana cellulare batterica[4]. Comunque il meccanismo preciso di azione non è ancora completamente noto ma sembra che gli amminoglicosidi siano in grado di competere chimicamente con gli ioni Mg2+ e Ca2+ che collegano tra loro i polisaccaridi di due lipopolisaccaridi adiacenti; questo provoca la formazione transiente di pori nella parete batterica modificando la normale permeabilità della membrana stessa[5]. Un'altra possibilità suggerisce che l'azione di proteine anomale create dall'azione degli antibiotici stessi alteri la permeabilità della membrana. Comunque attraverso questi pori il ceppo batterico perde componenti essenziali per la sopravvivenza come nucleotidi e altri.
Spettro di azione
[modifica | modifica wikitesto]Gli amminoglicosidi sono attivi principalmente contro batteri aerobici Gram negativi come Pseudomonas, Acinetobacter e Enterobacter. Inoltre alcune specie di Micobatteri, incluso quello che provoca la tubercolosi, sono suscettibili a questi antibiotici (gli aminoglicosidi sono utilizzati come antitubercolari di 2° linea (cioè vengono considerati quando il paziente resiste agli antitubercolari di 1° linea) ) . La relativa inefficienza contro i batteri anaerobi è probabilmente dovuta al fatto che l'assorbimento di questi antibiotici richiede un enzima della catena respiratoria della cellula , che nei batteri anaerobi non è presente , impossibilitando quindi l'entrata dell'antibiotico all'interno della cellula .
L'uso più frequente di questi composti si ha nel trattamento di infezioni gravi, quali la setticemia, infezioni gravi del tratto urinario, eccetera. Questa limitazione è dovuta alla tossicità di tali composti, ma la loro forza ne fa gli antibiotici di elezione nel primo trattamento di queste infezioni. Tuttavia, una volta che si è risaliti al batterio causa di tali infezioni, il trattamento con gli amminoglicosidi viene spesso interrotto a favore dell'utilizzo di antibiotici meno tossici.
È possibile trattare anche infezioni di batteri Gram-positivi (tra cui gli stafilococchi) con gli amminoglicosidi, ma in questo caso vengono utilizzati in associazione con altri antibiotici inibitori della parete cellulare (spesso le penicilline) per il loro effetto sinergico.
Studi preliminari hanno mostrato risultati incoraggianti per il trattamento della fibrosi cistica. Questa è causata dalla mutazione di un gene codificante per una proteina di membrana. In circa il 10% di casi, le mutazioni in questo gene causano una terminazione prematura della proteina, portando alla formazione di una proteina tronca e non funzionale. Si pensa che l'azione della gentamicina sia in grado di distorcere la struttura del complesso ribosoma-RNA, portando al non-riconoscimento del codone di stop e quindi facendo in modo da far procedere il ribosoma attraverso questo punto fino alla sintesi della proteina normale. Il trattamento è solo nella fase sperimentale ma sembra abbia portato a benefici nelle cellule di pazienti malati[6].
Vie di somministrazione e tossicità
[modifica | modifica wikitesto]Gli amminoglicosidi vengono scarsamente assorbiti per via orale dalla mucosa gastrica, pertanto, nelle infezioni sistemiche, devono essere impiegati per via parenterale (intravenosa e intramuscolare); vengono assorbiti attraverso la cute lesionata (ad esempio da ustioni) e in questi casi vengono utilizzati per via topica. Gli amminoglicosidi vengono escreti nell'urina in forma inalterata. Essi hanno tutti la stessa emivita plasmatica di 2-3 h, che risulta notevolmente prolungata in caso di insufficienza renale
Tutti gli amminoglicosidi -specialmente kanamicina e neomicina- sono nefrotossici e ototossici, il che ne limita molto l'utilizzo. Questa tossicità è sia tempo sia concentrazione dipendente, per cui la quantità di antibiotico viene calcolata in base al peso dell'individuo. I danni provocati da queste sostanze possono includere problemi alla coclea (con perdita di udito), all'apparato vestibolare (perdita di equilibrio) e alle funzioni renali (sangue nell'urina, blocco renale). Inoltre possono provocare un blocco neuromuscolare, una parestesia e una neuropatia periferica oltre a uno shock anafilattico. La tossicità dipende molto dal modo di somministrazione (per uso topico normalmente possono dare solo fenomeni di ipersensibilità), e i casi di utilizzo parenterale sono dovuti alla gravità dei sintomi.
Meccanismi di resistenza
[modifica | modifica wikitesto]Finora sono stati identificati tre tipi principali di meccanismi di resistenza contro questi antibiotici:
- ridotta penetrazione dell'antibiotico; essendo idrosolubile per poter attraversare le membrane necessita di trasporto attivo con purine e ATP, meccanismo bloccato da: cationi bivalenti (calcio e magnesio), iperosmolarità, pH eccessivamente acido, anaerobiosi;
- modificazione enzimatica dell'amminoglicoside stesso a opera di enzimi batterici (transferasi) mediante adenilazione, acetilazione o fosforilazione;
- mutazione del sito legante il ribosoma.
Note
[modifica | modifica wikitesto]- ^ Nobelprize.com https://www.nobelprize.org/nobel_prizes/medicine/laureates/1952/waksman-bio.html
- ^ Aminoglycosides: Bacteria and Antibacterial Drugs: Merck Manual Professional http://www.merck.com/mmpe/sec14/ch170/ch170b.html
- ^ Pharmamotion Copia archiviata, su pharmamotion.com.ar. URL consultato il 13 maggio 2009 (archiviato dall'url originale il 9 settembre 2009).
- ^ Shakil et al Aminoglycosides versus bacteria-a description of the action, resistance mechanism, and nosocomial battleground https://www.ncbi.nlm.nih.gov/pubmed/17657587
- ^ Lorian, Victor. "Antibiotics in Laboratory Medicine". Williams & Wilkins Press, 1996 (pp.589-590)
- ^ (EN) Gentamicin-induced correction of CFTR function in patients with cystic fibrosis and CFTR stop mutations, su content.nejm.org (archiviato dall'url originale il 18 giugno 2010).
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Amminoglicosidi
Wikimedia Commons contiene immagini o altri file su Amminoglicosidi
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) amminoglicosidi, su nlm.nih.gov.
- Amminoglicosidi dal manuale Merck (archiviato dall'url originale il 1º maggio 2009).