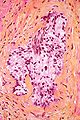
Carcinoma della prostata
| Carcinoma della prostata | |
|---|---|
 Microfotografia di un adenocarcinoma a cellule acinarie della prostata. | |
| Tipo | Maligno |
| Cellula di origine | Principalmente le cellule basali |
| Fattori di rischio | · Età · Dieta · Familiarità |
| Età media alla diagnosi | 70 anni |
| Classificazione e risorse esterne | |
| ICD-9-CM | (EN) 185 |
| ICD-10 | (EN) C61 |
Per carcinoma della prostata s'intende una categoria diagnostica che annovera le neoplasie maligne che si originano dalle cellule epiteliali della prostata, una ghiandola dell'apparato genitale maschile. Questa neoplasia può dare luogo a metastasi, con predilezione per le ossa e i linfonodi loco-regionali. Il tumore alla prostata può causare dolore, difficoltà alla minzione, disfunzione erettile e altri sintomi.
Il tumore alla prostata si sviluppa più frequentemente negli ultracinquantenni; è il secondo più comune tipo di tumore negli Stati Uniti, dove è responsabile del maggior numero di morti da tumore, dopo il tumore del polmone.[1] Molti fattori, compresa la genetica e la dieta, si ritiene siano implicati nello sviluppo del carcinoma prostatico.
Il tumore prostatico viene più spesso scoperto all'esame obiettivo o per il tramite di esami ematici, come la misurazione del PSA (antigene prostatico specifico). Un sospetto tumore alla prostata è tipicamente confermato tramite l'asportazione (biopsia) di un frammento di tessuto, e il successivo esame istologico. Si può ricorrere a ulteriori test come l'ecografia, la radiografia e la scintigrafia, per determinarne la diffusione e se il tumore abbia o meno originato metastasi.
Il tumore prostatico si può trattare con la chirurgia, la radioterapia, la terapia ormonale, occasionalmente la chemioterapia, o combinazioni di queste. L'età e lo stato di salute del paziente, così come la diffusione del tumore, l'aspetto microscopico e la risposta al trattamento iniziale, sono importanti per determinare la prognosi. Poiché il tumore della prostata è una malattia tipica degli uomini anziani, molti di essi potranno andare incontro a morte prima che il tumore possa espandersi o causare sintomi; ciò rende difficoltosa una selezione del trattamento.[2] La decisione se trattare o meno un tumore localizzato (ossia completamente confinato all'interno della prostata) implica un bilancio tra i benefici attesi e gli effetti negativi in termini di sopravvivenza del paziente e della sua qualità della vita.
Storia[modifica | modifica wikitesto]
Sebbene la prostata sia stata descritta per la prima volta dall'anatomista veneziano Niccolò Massa nel 1536, e illustrata dal fiammingo Andrea Vesalio nel 1538, il tumore prostatico non venne identificato prima del 1853.[3]

Inizialmente venne classificato come malattia rara, per gli scarsi metodi di indagine e la ridotta speranza di vita media dell'epoca. I primi trattamenti messi in atto furono interventi chirurgici per risolvere l'ostruzione urinaria.[4] La prostatectomia radicale perineale venne eseguita per la prima volta nel 1904 da Hugh Young al Johns Hopkins Hospital[5]. La rimozione chirurgica dei testicoli, orchiectomia, come trattamento venne eseguita nel 1890 (infra Terapia ormonale), ma con successo limitato. La resezione transuretrale della prostata rimpiazzò la prostatectomia radicale per la disostruzione dell'uretra nella metà del XX secolo. La prostatectomia radicale retropubica venne messa a punto nel 1983 da Patrick Walsh.[6] Questo approccio chirurgico consentì la rimozione della prostata e dei linfonodi col mantenimento della funzionalità erettile del pene.
Nel 1941 Charles B. Huggins pubblicò uno studio di utilizzo di estrogeni per contrastare la produzione di testosterone in pazienti con tumore prostatico metastatico. La scoperta di questa terapia valse a Huggins nel 1966 il Nobel per la Medicina.[7] Il ruolo del GnRH in ambito riproduttivo venne stabilito da Andrzej W. Schally e Roger Guillemin, che per questo vinsero il Nobel per la Medicina nel 1977; vennero quindi sviluppati e utilizzati in terapia gli agonisti per i recettori del GnRH.[8][9]
La radioterapia per il tumore prostatico venne sviluppata agli inizi del XX secolo e inizialmente consisteva nell'impianto intraprostatico di radio. La radioterapia a fascio esterno fu più utilizzata quando alla metà del XX secolo divennero disponibili fonti di radiazioni più potenti. La brachiterapia con l'impianto di "semi" fu descritta per la prima volta nel 1983.[10] La chemioterapia sistemica per il tumore della prostata venne studiata per la prima volta negli anni settanta. Al protocollo iniziale con ciclofosfamide 5-fluorouracile ben presto si aggiunsero molteplici altri con un'ampia gamma di farmaci sistemici.[11]
Epidemiologia[modifica | modifica wikitesto]

Nessun dato
meno di 4
4-8
8-12
12-16
16-20
20-24
24-28
28-32
32-36
36-40
40-44
più di 44
La frequenza del carcinoma prostatico nel mondo è largamente variabile.[13] È meno diffuso nell'Asia meridionale e orientale, più comune in Europa, con ampie differenze tra paese e paese e ancor di più negli Stati Uniti.[14] Secondo l'American Cancer Society, vi sono forti differenze geografiche ed etniche nella frequenza; infatti, il carcinoma prostatico è meno comune tra gli uomini asiatici, più comune tra gli uomini di colore, l'incidenza tra gli uomini europei è intermedia rispetto alle due precedenti popolazioni.[15][16][17] Secondo dati del 2002 il tasso d'incidenza annuale in Asia Centrale è inferiore a 3/100 000 abitanti, mentre nel continente nordamericano si hanno più di 160/100 000 abitanti registrati.[18][19] Tuttavia la rilevazione di queste maggiori frequenze può essere stata influenzata dai maggiori tassi di diagnosi dovuti al progresso diagnostico e alle politiche di prevenzione[20].
Le cause specifiche della neoplasia sono sconosciute.[21] Il rischio di sviluppare il tumore è correlato all'età[22], alla genetica,[23] alla razza,[24] alla dieta,[25] allo stile di vita, all'assunzione di farmaci e ad altri fattori. Il fattore primario è l'età. Il tumore della prostata è raro negli uomini al di sotto dei 45 anni, ma diventa sempre più frequente con l'invecchiamento. L'età media al momento della diagnosi è di 70 anni[26]. Molti soggetti colpiti, tuttavia, non manifestano in vita segni di malattia: studi autoptici su uomini cinesi, tedeschi, israeliani, giamaicani, svedesi e ugandesi, morti per altre cause, sono stati individuati tumori alla prostata nel trenta per cento dei cinquantenni e nell'ottanta per cento dei settantenni.[27] Nel 2005 negli Stati Uniti sono stati stimati 230 000 nuovi casi e 30 000 decessi[28]. Essendo una neoplasia tipica dell'età avanzata, può infatti accadere che sopraggiunga il decesso della persona colpita, per vecchiaia o altre cause, prima che il tumore mostri sintomi o segni che rivelino la sua presenza.
La familiarità e il corredo genetico di un uomo contribuiscono al rischio di sviluppare il tumore. Ciò è suggerito da un aumento dell'incidenza riscontrato in certi gruppi razziali, nei gemelli identici e in uomini portatori di certi geni. Negli Stati Uniti, il cancro della prostata colpisce più comunemente gli uomini di colore che non i bianchi o gli ispanici, e nei primi causa anche più morti[16]. Gli uomini con un fratello o un padre colpiti dal tumore corrono un rischio doppio del normale di svilupparlo anch'essi[29]. Studi su gemelli condotti in Scandinavia suggeriscono che il quaranta per cento del rischio può essere attribuito a fattori ereditari[30]. Tuttavia nessun gene preso singolarmente è responsabile del tumore, sono anzi sospettati molti geni differenti. Due geni (BRCA1 e BRCA2), che sono pure importanti fattori di rischio per il tumore dell'ovaio e il tumore della mammella, sono anche coinvolti nel tumore della prostata[31].
L'assunzione con la dieta di certi cibi, vitamine, e minerali possono contribuire al rischio. Gli uomini con maggiori livelli sierici di acido α-linolenico, un acido grasso polinsaturo a catena corta, sono a maggior rischio di tumore della prostata. Tuttavia gli stessi studi dimostrarono che negli uomini con livelli elevati di acidi grassi a catena lunga (EPA e DHA) diminuisce l'incidenza.[32] Altri fattori dietetici in grado di aumentare il rischio includono un basso apporto di vitamina E (reperibile nei vegetali a foglie verdi), di licopene (presente nei pomodori), di acidi grassi omega-3[33] (reperibili nei pesci a carne grassa[33][34] come il salmone o il pesce azzurro), e di selenio.[35] Anche bassi livelli ematici di vitamina D possono aumentare il rischio di sviluppare un tumore; ciò può essere correlato a una minore esposizione ai raggi ultravioletti[36][37].
Esistono anche dei legami tra tumore della prostata e assunzione di farmaci, procedure e condizioni mediche. L'utilizzo giornaliero di farmaci antinfiammatori non steroidei (FANS) come l'aspirina può ridurre il rischio[38]. Farmaci ipolipidemizzanti come le statine possono anch'essi ridurlo[39]. La sterilizzazione tramite vasectomia può aumentare il rischio di tumore della prostata, ma i dati sono contraddittori[40]. Eiaculazioni più frequenti possono abbassare il rischio; uno studio mostrò che gli uomini che eiaculano cinque volte a settimana dai venti a trent'anni di età, vedono ridotto il rischio di tumore[41]. Un'infezione o un'infiammazione della prostata (prostatite) può aumentare le probabilità di tumore. In particolare, infezioni sessualmente trasmesse come la clamidia, la gonorrea, e la sifilide sembrano aumentare il rischio[42], così come l'obesità[43].
In passato si credeva che elevati valori di testosterone causassero o facilitassero il cancro alla prostata, in realtà sono i bassi livelli di quest'ormone a essere correlati a questo tumore, inoltre persino l'uso di testosterone in soggetti ipogonadici non aumenta questo rischio[44].
Inoltre è appurato che gli uomini affetti dalla sindrome di Klinefelter abbiano un'incidenza sensibilmente inferiore di tumore prostatico rispetto agli uomini sani[45]
Anatomia[modifica | modifica wikitesto]

La prostata è un organo parte dell'apparato genitale maschile che interviene nella produzione del liquido spermatico. In un uomo adulto la prostata misura circa tre centimetri e pesa circa venti grammi.[46] È localizzata nella pelvi, al di sotto della vescica e anteriormente al retto; circonda parzialmente l'uretra.[47] A causa della sua posizione, le malattie della prostata spesso interferiscono con la minzione, l'eiaculazione o la defecazione. La prostata contiene molte piccole ghiandole che producono circa il venti per cento della parte liquida dello sperma.[48] Nel carcinoma prostatico le cellule di queste ghiandole mutano in cellule cancerose. Per funzionare la prostata ha bisogno di ormoni maschili, noti come androgeni; gli androgeni includono il testosterone, prodotto nei testicoli, il deidroepiandrosterone, prodotto dalle ghiandole surrenali, e il diidrotestosterone, prodotto dalla prostata stessa.
Eziologia[modifica | modifica wikitesto]
Le cause specifiche del cancro alla prostata rimangono ancora sconosciute.[49] I primi fattori di rischio sono comunque l'età e la storia familiare. Il cancro alla prostata è molto raro negli uomini sotto i 45 anni, ma diventa più frequente all'aumentare dell'età. L'età media dei pazienti al momento della diagnosi è di 70 anni.[50] Comunque molti uomini non vengono mai a conoscenza di avere questo tipo di tumore. Gli esami autoptici effettuati su uomini cinesi, tedeschi, israeliani, giamaicani, svedesi e ugandesi, morti per cause differenti, hanno evidenziato la presenza di un cancro alla prostata nel 30% dei casi sotto i 50 anni e nell'80% sopra i 70.[51] Gli uomini che hanno un familiare di primo grado che ha avuto questo tipo di tumore, hanno il doppio del rischio di svilupparlo rispetto agli uomini che non hanno avuto malati in famiglia.[52] Il rischio appare maggiore per gli uomini che hanno un fratello con questo cancro rispetto a quelli che hanno solo il padre.
Negli Stati Uniti, nel 2005, si sono stimati 230 000 nuovi casi di tumori alla prostata e 30 000 morti a causa di esso.[53] Uomini con pressione sanguigna elevata sono, inoltre, più propensi a sviluppare il cancro prostatico.[54] Uno studio del 2010 ha messo in mostra come le cellule basali prostatiche sono il sito dove più comunemente origina il cancro.[55]
Anatomia patologica[modifica | modifica wikitesto]
L'adenocarcinoma acinare (il tumore che si sviluppa dalle strutture acinari, a forma di acino d'uva, della prostata) rappresenta l'istotipo più frequente tra le neoplasie prostatiche. Tuttavia, esistono alcuni altri istotipi che vanno riconosciuti e segnalati, per la differente presentazione clinica e decorso prognostico.
- Adenocarcinoma duttale, origina dalle cellule dei dotti prostatici. Nel caso in cui originino dai dotti periuretrali danno una sintomatologia assimilabile ai carcinomi di origine uroteliale. È bene riconoscere questo tipo di carcinoma per la prognosi peggiore rispetto all'adenocarcinoma classico.
- Carcinoma adenosquamoso o squamoso, per la metaplasia epitelioide spontanea di una neoplasia a differenziazione ghiandolare o in seguito a trattamento ormonale.
- Carcinomi mucinosi della prostata, neoplasie che si caratterizzano per la produzione di muco, talora in elevate quantità.
- Carcinoma a piccole cellule, istotipo più aggressivo, origina da cellule neuroendocrine intercalate nel contesto del parenchima prostatico.
- Neoplasie mesenchimali, come i sarcomi o i liposarcomi, molto rari.
- Linfomi.
Nel 70% dei casi l'adenocarcinoma acinare origina dalla porzione periferica, con tipica localizzazione posteriore.[56] Su questa caratteristica si fonda il razionale dell'esplorazione rettale come esame di approccio e completamento diagnostico nella visita di un paziente con corredo clinico ascrivibile a patologia prostatica. Nell'ultimo decennio, il miglioramento delle metodiche diagnostiche ha permesso una sempre più precoce individuazione delle masse confinate al parenchima, rendendo difficile per l'anatomo-patologo il riconoscimento macroscopico della neoplasia nel pezzo operatorio attraverso la sola ispezione visiva; molto spesso infatti, le piccole neoplasie vengono riconosciute palpatoriamente come masse duro lignee all'interno della ghiandola. Alla superficie di taglio, la neoplasia si presenta di colore bianco o giallo-aranciato, compatta, con margini spiculati o policiclici e penetranti il parenchima circostante. La naturale evoluzione della neoplasia prevede l'espansione locale nel contesto della ghiandola e la successiva infiltrazione delle vescicole seminali, del collo vescicale e dell'uretra prostatica, evento che comporta manifestazioni ostruttive con disuria, pollachiuria e stranguria, talora emospermia[57]. Negli stadi avanzati si ha inoltre infiltrazione del pavimento pelvico e del retto con conseguente tenesmo. Le vie linfatiche più frequentemente coinvolte sono in ordine di frequenza:[58]
- Linfonodi otturatori
- Linfonodi perivescicali
- Linfonodi ipogastrici
- Linfonodi iliaci
- Linfonodi presacrali
- Linfonodi paraortici
La metastatizzazione ematica coinvolge tipicamente le ossa, in particolare la colonna lombare (più raramente toracica, del femore, della pelvi e delle coste).[58]
Aspetto microscopico[modifica | modifica wikitesto]
Le ghiandole neoplastiche sono tipicamente più piccole, affollate e rigide delle normali; presentano iperplasia massiva, con perdita delle papille e dello strato basale esterno. Le normali colorazioni evidenziano un nucleo grande, provvisto di nucleolo, contornato da citoplasma chiaro o talora intensamente eosinofilo (con caratteristica colorazione rosa-violacea omogenea).[56] Benché queste isole neoplastiche siano di facile individuazione, la diagnosi istologica potrebbe rendersi difficile per la mancanza di pleomorfismo e di figure mitotiche atipiche, tuttavia l'elevato monomorfismo e la rigidità dell'aspetto degli acini affollati, con cellule e nuclei posti in posizioni monotone all'interno del focolaio di adenocarcinoma, permettono un'agevole distinzione dalle ghiandole normali, tipicamente più variegate nell'aspetto, con profili tortuosi e cellule disposte in modo fisiologicamente disordinato, con citoplasmi chiari secretivi e nuclei piccoli e allungati, affusolati, blu-viola scuri, diversi da quelli rigidamente tondi e nucleolati del carcinoma. Talora però i focolai neoplastici rilevati nei frustoli bioptici ottenuti con ago tranciante sono molto piccoli e con caratteristiche valutabili su un ristretto numero di acini sospetti. Normali colorazioni con ematossilina-eosina che mostrino ghiandole piccole, affollate di cellule con perdita delle papille possono in questi casi essere solo suggestive di carcinoma prostatico; la diagnosi viene avvalorata qualora si presentino una o più di queste caratteristiche:[56]
- Nuclei grandi e amorfi, citoplasma scuro, nucleoli prominenti.
- Assenza di cellule basali nel contesto delle ghiandole basali (ricercate con marcatori immunologici)
- Invasione perineurale (vedi immagine)
Un'entità istologica di notevole importanza è la neoplasia intraepiteliale prostatica di alto grado o PIN, caratterizzata da ampie formazioni ghiandolari con protrusioni papillari (primo elemento di distinzione con le neoplasie maligne), proliferazione intra-acinare non invasiva, anaplasia nucleare e prominenti nucleoli (in più del 10% delle cellule). Altra importante caratteristica da ricercare nella PIN è la presenza di cellule basali, assenti nel carcinoma, qui solo attenuate. La PIN è un'importante lesione che deve essere seguita nel tempo per la possibile trasformazione maligna.[59][60][61][62][63]
-
Frustolo bioptico, colorazione cromo-ematossilina-floxina. In alto a destra si evidenzia un aggregato ghiandolare iperplasico, con ghiandole piccole e stipate. Sono evidenti ghiandole normali in basso.
-
Frustolo bioptico, alto ingrandimento, colorazione cromo-ematossilina-floxina che evidenzia ghiandole normali (in basso e a sinistra) e ghiandole neoplastiche (in alto a destra). Si noti come le ghiandole neoplastiche siano più piccole e stipate e presentino grandi nuclei amorfi.
-
Frustolo bioptico, colorazione cromo-ematossilina-floxina. Nella porzione centrale, il frustolo è attraversato perpendicolarmente da un nervo, infiltrato da un piccolo gruppo ghiandolare neoplastico in basso. Questo è un tipico esempio di invasione perineurale.
-
Frustolo bioptico, colorazione cromo-ematossilina-floxina, altro esempio di invasione perineurale da parte di gruppi ghiandolari neoplastici.
-
Neoplasia intraepiteliale prostatica di alto grado (PIN), colorazione con ematossilina-eosina, basso ingrandimento.
-
Neoplasia intraepiteliale prostatica di alto grado (PIN), colorazione con ematossilina-eosina, ingrandimento intermedio.
-
Neoplasia intraepiteliale prostatica di alto grado (PIN), colorazione con ematossilina-eosina, alto ingrandimento.
Profilo clinico[modifica | modifica wikitesto]
Un carcinoma della prostata in fase precoce di solito non dà luogo a sintomi. Spesso viene diagnosticato in seguito al riscontro di un livello elevato di PSA durante un controllo di routine. Talvolta, tuttavia, il carcinoma causa dei problemi, spesso simili a quelli che intervengono nella iperplasia prostatica benigna; essi includono pollachiuria, nicturia, difficoltà a iniziare la minzione e a mantenere un getto costante, ematuria, stranguria. Può anche causare problemi nella funzione sessuale, come difficoltà a raggiungere l'erezione, e eiaculazione dolorosa.[64]
In stadio avanzato può causare sintomi addizionali quando si diffonde ad altre parti del corpo. Il sintomo più comune è il dolore osseo, spesso localizzato alle vertebre, alla pelvi o alle costole, e causato da metastasi in queste sedi. La localizzazione vertebrale può indurre compressione al midollo spinale, causando debolezza alle gambe e incontinenza urinaria e fecale.[65]
Profilo diagnostico[modifica | modifica wikitesto]
Lo screening oncologico è un metodo per scoprire tumori non diagnosticati. I test di screening possono indurre a ricorrere a esami più specifici, come la biopsia. Le scelte diagnostiche di screening nel caso del tumore della prostata comprendono l'esame rettale e il dosaggio del PSA.
È controversa la validità degli esami di screening, poiché non è chiaro se i benefici che ne derivano sopravanzino i rischi degli esami diagnostici successivi e della terapia antitumorale. Il tumore della prostata è un tumore a crescita lenta, molto comune fra gli uomini anziani. Infatti in maggioranza i tumori della prostata non crescono abbastanza per dare luogo a sintomi, e i pazienti muoiono per cause diverse. Il dosaggio del PSA può svelare questi piccoli tumori che non avrebbero altrimenti avuto modo di manifestarsi; uno screening del genere può quindi condurre a un numero eccessivo di diagnosi, con la relativa sequela di test ulteriori e di terapie. La biopsia può causare dolore, sanguinamento e infezioni; le terapie possono causare incontinenza urinaria e disfunzioni erettili. Dunque è essenziale che vengano considerati i rischi e i benefici prima di intraprendere uno screening utilizzando il dosaggio del PSA[66].
In genere gli screening iniziano dopo i 50 anni di età, ma possono essere proposti prima negli uomini di colore e in quelli con una forte storia familiare di tumori alla prostata.[67][68]
Krilaviciute et al. (2023)[69] ha esaminato l'efficacia dell'esame rettale digitale (DRE) come test di screening isolato per il cancro alla prostata nei giovani uomini. È stato riscontrato che il DRE ha un tasso di rilevazione molto più basso per il cancro alla prostata rispetto allo screening PSA. Pertanto, si raccomanda di non utilizzare il DRE come test di screening per il cancro alla prostata nei giovani uomini, poiché non fornisce un miglioramento nella rilevazione rispetto allo screening PSA.
Esame rettale[modifica | modifica wikitesto]

L'esame rettale digitale è una procedura in cui l'esaminatore inserisce un dito guantato e lubrificato nel retto del paziente, allo scopo di valutare le dimensioni, la forma e la consistenza della prostata: zone irregolari, dure o bozzolute devono essere sottoposte a ulteriori valutazioni, perché potrebbero essere indicative di tumore. L'esame rettale è in grado di valutare solo la parte posteriore della prostata, ma fortunatamente l'85% dei tumori ha origine proprio in questa parte. In genere dà modo di apprezzare tumori già in stadio avanzato.[70]
Non è mai stato dimostrato che, come unico test di screening, l'esame rettale sia in grado di ridurre il tasso di mortalità.[71]
Dosaggio del PSA[modifica | modifica wikitesto]
Il dosaggio del PSA misura il livello ematico di un enzima prodotto dalla prostata. Livelli di PSA sotto 4 ng/mL (nanogrammi per millilitro) sono generalmente considerati normali, mentre livelli sopra i 4 ng/mL sono considerati anormali (sebbene negli uomini oltre i 65 anni livelli fino a 6,5 ng/mL possono essere accettabili, in dipendenza dai parametri di riferimento di ciascun laboratorio). Livelli di PSA tra 4 e 10 ng/mL indicano un rischio di tumore più alto del normale, ma il rischio stesso non sembra direttamente proporzionale al livello. Quando il PSA è sopra i 10 ng/mL, l'associazione col tumore diventa più forte, tuttavia quello del PSA non è un test perfetto. Alcuni uomini con tumore prostatico in atto non hanno livelli elevati di PSA, e la maggioranza di uomini con un elevato PSA non ha un tumore. Oggi è possibile dosare un ulteriore marcatore per il carcinoma prostatico, il PCA3 (prostate cancer gene 3); l'iperespressione di questo gene (valutabile mediante dosaggio del mRNA nelle urine) è strettamente associata alla trasformazione maligna delle cellule della prostata. Il dosaggio è quindi particolarmente utile nei pazienti già sottoposti a biopsia, per predire l'evoluzione del tumore.[72][73][74][75][76][77][78]
Conferma diagnostica[modifica | modifica wikitesto]

Quando si sospetta un carcinoma prostatico, o un esame di screening è indicativo di un rischio aumentato, si prospetta una valutazione più invasiva. L'unico esame in grado di confermare pienamente la diagnosi è la biopsia, ossia l'asportazione di piccoli frammenti di tessuto per l'esame al microscopio. Tuttavia, prima che alla biopsia, si può ricorrere a metodiche meno invasive per raccogliere informazioni riguardo alla prostata e al tratto urinario: la cistoscopia mostra il tratto urinario a partire dall'interno della vescica usando un piccolo endoscopio inserito nell'uretra; l'ecografia transrettale disegna un'immagine della prostata tramite gli ultrasuoni emessi da una sonda inserita nel retto.

Se si sospetta un tumore si ricorre alla biopsia. Con essa si ottengono campioni di tessuto dalla prostata tramite il retto: una pistola da biopsia inserisce e quindi rimuove speciali aghi a punta cava (di solito da tre a sei per ogni lato della prostata) in meno di un secondo. I campioni di tessuto vengono quindi esaminati al microscopio per determinare la presenza di tumore, valutarne gli aspetti istomorfologici (grading secondo il Gleason score system). In genere le biopsie prostatiche vengono eseguite ambulatorialmente e di rado richiedono l'ospedalizzazione. Il 55% degli uomini riferisce malessere durante la procedura.[79]

Uno studio portato a termine nel 2003 dall'Istituto scientifico universitario San Raffaele.[80][81] ha dimostrato l'efficacia dell'utilizzo della tomografia a emissione di positroni (PET) con il tracciante C-Colina, come esame per individuare recidive del tumore alla prostata. Questo esame è consigliato nei pazienti che hanno già subito un trattamento radicale del tumore e a cui si è rilevato un valore del marcatore PSA tale da far pensare a una ripresa della malattia. Più recentemente è possibile eseguire la PET nei pazienti con carcinoma prostatico anche utilizzando come traccianti i liganti del PSMA (PSMA-PET), proteina di superficie abbondantemente espressa dalle cellule di carcinoma. Tale metodica presenta un'accuratezza maggiore della PET con colina[82] ed inoltre può essere utilizzata per effettuare una terapia radiometabolica mirata (approccio teranostico)[83]
Grazie alla PET è possibile, inoltre, differenziare una diagnosi di cancro alla prostata da una iperplasia benigna, da una prostatite cronica e da un tessuto prostatico sano.[84]
Stadiazione[modifica | modifica wikitesto]
Una parte importante della valutazione diagnostica è la stadiazione, ossia il determinare le strutture e gli organi interessati dal tumore. Determinare lo stadio aiuta a definire la prognosi e a selezionare le terapie. Il sistema più comune è il sistema a quattro stadi TNM (abbreviazione da Tumore/LinfoNodi/Metastasi), che prevede di considerare le dimensioni del tumore, il numero di linfonodi coinvolti e la presenza di metastasi.
La distinzione più importante operata da qualsiasi sistema di stadiazione è se il tumore è o meno confinato alla prostata. Diversi esami sono disponibili per evidenziare una valutazione in questo senso, e includono la TAC per valutare la diffusione nella pelvi, la scintigrafia per le ossa, e la risonanza magnetica per valutare la capsula prostatica e le vescicole seminali.
I risultati possono poi essere classificati grazie alla stadiazione TNM o di Whitmore-Jewett:
| Stadio | Descrizione |
|---|---|
| T1a | tumore in meno del 5% del parenchima (corrisponde allo stadio A1 di WJ). |
| T1b | tumore in più del 5% del parenchima. |
| T1c | come 1b + PSA elevato (questi 2 stadi corrispondono allo stadio A2 di WJ) |
| T2a | coinvolge 1 lobo (comprende gli stadi B1 e B2 di WJ) |
| T2b | coinvolge entrambi i lobi (stadio B3 di WJ) |
| T3a | oltrepassa la capsula prostatica da un solo lobo (stadio C1 di WJ) |
| T3b | oltrepassa la capsula da entrambi i lobi |
| T3c | invade le vescichette seminali (stadio C2 di WJ) |
| T4 | invade organi adiacenti (stadio D di WJ, diviso in ormono-sensibile e insensibile) |
| N1a | metastasi linfonodali non rilevabili |
| N1b | una sola minore o uguale a 2 cm |
| N1c | una sola fra 2 e 5 cm |
| N2a | oltre 5 cm o multiple |
| MX | metastasi a distanza non rilevabili |
| M0 | assenza di metastasi a distanza |
| M1a | linfonodi extraregionali |
| M1b | scheletro |
| M1c | altri siti |
Dopo una biopsia prostatica, un patologo esamina il campione al microscopio. Se è presente un tumore il patologo ne indica il grado; questo indica quanto il tessuto tumorale differisce dal normale tessuto prostatico, e suggerisce quanto velocemente il tumore stia crescendo. Il grado di Gleason assegna un punteggio da 2 a 10, dove 10 indica le anormalità più marcate; il patologo assegna un numero da 1 a 5 alle formazioni maggiormente rappresentate, poi fa lo stesso con le formazioni immediatamente meno comuni; la somma dei due numeri costituisce il punteggio finale. Il tumore è definito ben differenziato se il punteggio è fino 4, mediamente differenziato se 5 o 6, scarsamente differenziato se maggiore di 6. È da notare che non solo è importante la somma algebrica ma anche come è stata ottenuta, ovvero un 4+2 è sicuramente più grave di un 2+4, perché questo indica che nel primo caso ci siano soprattutto formazioni scarsamente differenziate, mentre nel secondo caso soprattutto ben differenziate.
| Grado | Descrizione |
|---|---|
| Grado 1: | altamente differenziato |
| Grado 2: | ben differenziato: |
| Grado 3: | moderatamente differenziato |
| Grado 4: | scarsamente differenziato |
| Grado 5: | altamente indifferenziato (cellule infiltranti) |
Un'appropriata definizione del grado di malignità del tumore è di importanza fondamentale, in quanto è uno dei fattori utilizzati per guidare le scelte terapeutiche.
Terapia[modifica | modifica wikitesto]
La terapia del carcinoma prostatico può comprendere: l'osservazione in assenza di trattamento, la chirurgia, la radioterapia, gli ultrasuoni focalizzati ad alta intensità HIFU, la chemioterapia, la criochirurgia, la terapia ormonale, o una combinazione di queste. La scelta dell'opzione migliore dipende dallo stadio della malattia, dal punteggio secondo la scala Gleason, e dai livelli di PSA. Altri fattori importanti sono l'età del paziente, il suo stato generale, e il suo pensiero riguardo alla terapia proposta e agli eventuali effetti collaterali. Poiché tutte le terapie possono indurre significativi effetti collaterali, come le disfunzione erettile e l'incontinenza urinaria, discutere col paziente circa la possibile terapia spesso aiuta a bilanciare gli obiettivi terapeutici coi rischi di alterazione dello stile di vita.[88][89][90]
Se il tumore si è diffuso esternamente alla prostata, le opzioni terapeutiche cambiano. La terapia ormonale e la chemioterapia sono spesso riservate ai casi in cui la malattia si è estesa esternamente alla prostata; tuttavia esistono delle eccezioni: la radioterapia può essere impiegata per alcuni tumori in fase avanzata, e la terapia ormonale per alcuni in fase precoce. La crioterapia, la terapia ormonale e la chemioterapia possono inoltre essere utilizzate se il trattamento iniziale fallisce e il tumore progredisce.[91][92][93]
Osservazione[modifica | modifica wikitesto]
L'osservazione, una "sorveglianza attiva", prevede il regolare monitoraggio della malattia in assenza di un trattamento invasivo. Spesso vi si ricorre quando si riscontra, in pazienti anziani, un tumore in stadio precoce e a crescita lenta. Può essere consigliabile anche quando i rischi connessi alla chirurgia, alla radioterapia, o alla terapia ormonale sopravanzino i possibili benefici. Si possono intraprendere gli altri trattamenti se si manifestano sintomi, o se appaiono indizi di un'accelerazione nella crescita del tumore. La maggioranza degli uomini che optano per l'osservazione di tumori in stadi precoci vanno incontro alla possibilità di manifestare segni di progressione del tumore, ed entro tre anni hanno necessità di intraprendere una terapia.[94] Sebbene tale scelta eviti i rischi connessi alla chirurgia e alle radiazioni, il rischio di metastasi si può innalzare. I problemi di salute connessi all'avanzare dell'età durante il periodo di osservazione possono anch'essi complicare la chirurgia e la radioterapia.[95]
Chirurgia[modifica | modifica wikitesto]
La rimozione chirurgica della prostata, o prostatectomia, è un trattamento comune sia per i tumori prostatici in stadi precoci, sia per i tumori non rispondenti alla radioterapia. Il tipo più comune è la prostatectomia retropubica radicale, in cui si rimuove la prostata tramite un'incisione addominale. Un altro tipo è la prostatectomia perineale radicale, in cui l'incisione è praticata a livello del perineo, la regione fra lo scroto e l'ano. La prostatectomia può risolvere, a cinque anni, circa il 70% dei casi di tumore della prostata;[96] tassi di sopravvivenza più alti si sono trovati con un Gleason score inferiore a 3.[97]
La prostatectomia radicale è molto efficace per i tumori limitati alla prostata, tuttavia può causare danni ai nervi in grado di alterare significativamente la qualità della vita dei pazienti.
I nervi deputati all'erezione e alla minzione sono immediatamente adiacenti alla prostata, per cui le complicazioni più importanti sono l'incontinenza urinaria e l'impotenza. Circa il 40% degli uomini residuano incontinenza urinaria, di solito sotto forma di perdite quando starnutiscono, tossiscono o ridono. L'impotenza è anch'essa un problema comune: sebbene la sensibilità sul pene e la capacità di raggiungere l'orgasmo rimangano intatte, l'erezione e l'eiaculazione sono spesso compromesse; farmaci come il sildenafil (Viagra), il tadalafil (Cialis), o il vardenafil (Levitra) possono ristabilire un certo grado di potenza. In alcuni uomini con tumori più piccoli, una tecnica chirurgica meno invasiva può essere d'aiuto per evitare queste complicazioni.[98]
La prostatectomia radicale è stata tradizionalmente usata come unico trattamento per un tumore di piccole dimensioni. Tuttavia cicli di terapia ormonale prima della chirurgia possono migliorare le percentuali di successo, e sono correntemente oggetto di studio[99]. La chirurgia può essere intrapresa anche quando il tumore non risponde alla radioterapia, tuttavia, poiché le radiazioni causano modifiche dei tessuti, in questa situazione aumentano i rischi di complicazioni.
Da uno studio comparativo condotto nel 2009 su un totale di 8 837[100] interventi di chirurgia radicale per tumore alla prostata, l'incidenza dell'incontinenza urinaria e impotenza ha evidenziato che:
- Chirurgia con robot/laparoscopia:
- 15,9% di incontinenza urinaria
- 26,8% di impotenza e disfunzioni erettili.
- Chirurgia classica-tradizionale a "cielo aperto":
- 12,2% di incontinenza urinaria
- 19,2% di impotenza e disfunzioni erettili.
La resezione transuretrale della prostata è una procedura chirurgica messa in atto quando l'uretra è ostruita a causa dell'ingrossamento prostatico; generalmente è riservata alle malattie prostatiche benigne e non è intesa come trattamento definitivo del tumore. Consiste nell'inserimento nell'uretra di un piccolo endoscopio, tramite il quale, con apposito strumento, si taglia via la parte di prostata che occlude il lume.
Radioterapia[modifica | modifica wikitesto]
La radioterapia utilizza i raggi X per uccidere le cellule tumorali; i raggi X sono un genere di radiazione ionizzante in grado di danneggiare o distruggere il DNA delle cellule in crescita. Due differenti tipi di radioterapia sono utilizzati nel trattamento del carcinoma prostatico: la radioterapia a fascio esterno e la brachiterapia.
La radioterapia a fascio esterno utilizza un acceleratore lineare per produrre raggi X ad alta energia che vengono raggruppati in un fascio diretto contro la prostata. Una tecnica chiamata Radioterapia a Intensità Modulata (IMRT) può essere utilizzata per adattare il fascio radiante alla forma del tumore, permettendo di somministrare dosi maggiori con minor danno per la vescica e il retto. La radioterapia a fascio esterno viene in genere somministrata per diverse settimane, con visite giornaliere ai centri di radioterapia.[101]
La brachiterapia prevede il posizionamento di circa 100 piccoli "semi" contenenti materiale radioattivo (come lo iodio 125 o il palladio 103) tramite un ago attraverso la cute del perineo direttamente nel tumore. Questi semi emettono radiazioni ionizzanti a bassa energia, in grado di percorrere solo una breve distanza; sono permanenti ma non comportano rischi di emissioni all'esterno.[102][103]
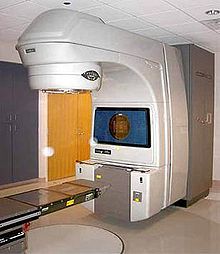
La radioterapia è di uso comune nel trattamento del carcinoma prostatico. Può essere utilizzata al posto della chirurgia nei tumori in fase precoce, così come in quelli in fase avanzata per trattare le dolorose metastasi ossee; può essere associata alla terapia ormonale per i casi a rischio intermedio, quando la radioterapia da sola ha meno probabilità di essere risolutiva. Alcuni oncologi associano radioterapia a fascio esterno e la brachiterapia per casi con rischio da intermedio a elevato. Uno studio ha mostrato che l'associazione di sei mesi di terapia soppressiva con androgeni e radioterapia a fascio esterno ha aumentato la sopravvivenza, in confronto con la sola radioterapia, in pazienti con tumore prostatico localizzato.[104] Altri oncologi utilizzano una tripla combinazione di radioterapia a fascio esterno, brachiterapia e terapia ormonale.
Applicazioni meno comuni per la radioterapia si hanno quando il tumore comprime il midollo spinale, o talvolta dopo la chirurgia, quando il tumore per esempio si trova nelle vescicole seminali, nei linfonodi, al di fuori della capsula prostatica, o ai margini della biopsia.
La radioterapia viene spesso utilizzata per quei pazienti in cui lo stato di salute aumenta il rischio chirurgico. Sembra in grado di curare i piccoli tumori confinati alla prostata quasi quanto la chirurgia. Tuttavia, al 2006, alcune questioni rimangono irrisolte, ossia se le radiazioni debbano essere somministrate al resto della pelvi, quale debba essere la dose assorbita, e la terapia ormonale debba essere effettuata contemporaneamente.
Gli effetti collaterali della radioterapia possono presentarsi dopo poche settimane dall'inizio del trattamento. Entrambi i tipi di radioterapia possono causare diarrea e sanguinamento gastrointestinale dovuti a una proctite da radiazioni, così come incontinenza urinaria e impotenza. I sintomi tendono a migliorare nel corso del tempo.[105] I pazienti sottoposti a radioterapia a fascio esterno vedono aumentato il rischio di sviluppare in seguito tumore del colon e della vescica.[106]
Criochirurgia[modifica | modifica wikitesto]
La criochirurgia è un altro metodo di trattamento del tumore della prostata. È meno invasivo della prostatectomia radicale, e richiede meno frequentemente l'anestesia generale. Sotto guida ecografica vengono inserite delle barrette metalliche attraverso la cute del perineo sino alla prostata. Le barrette vengono raffreddate con azoto liquido, portando i tessuti circostanti a −196 °C. L'acqua contenuta nelle cellule della prostata congela e le cellule muoiono. L'uretra viene protetta dal freddo con un catetere Foley riempito di acqua calda. La criochirurgia in genere comporta meno problemi sul controllo dell'urinazione rispetto ad altri trattamenti, ma nel 90% dei casi residua impotenza. Quando utilizzata come trattamento iniziale, la criochirurgia non ha l'efficacia della chirurgia tradizionale o della radioterapia,[107] tuttavia è potenzialmente preferibile alla prostatectomia radicale nel caso di recidive tumorali dopo radioterapia.
Terapia ormonale[modifica | modifica wikitesto]

La terapia ormonale utilizza i farmaci o la chirurgia per impedire alle cellule tumorali della prostata di assumere diidrotestosterone (DHT), un ormone prodotto dai testicoli e dalla prostata stessa, e necessario alla maggioranza dei tumori per accrescersi. Bloccare il DHT spesso fa sì che il tumore smetta di crescere e anche diminuisca di volume. Tuttavia la terapia ormonale di rado è curativa, perché il tumore di solito sviluppa resistenza nell'arco di uno o due anni. La terapia ormonale è dunque di solito impiegata quando il tumore si è espanso oltre la prostata; può impiegarsi anche in alcuni pazienti sottoposti a radioterapia o chirurgia per prevenire recidive.[108]
La terapia ormonale colpisce le vie metaboliche che l'organismo utilizza per produrre DHT, a qualche livello del circuito di feedback endocrino che coinvolge i testicoli, l'ipotalamo, l'ipofisi, i surreni e la prostata. Innanzitutto bassi livelli ematici di DHT stimolano l'ipotalamo a produrre GnRH (ormone rilasciante le gonadotropine). Il GnRH stimola l'ipofisi a produrre ormone luteinizzante (LH), il quale fa produrre ai testicoli testosterone. Infine il testosterone dei testicoli e il deidroepiandrosterone dai surreni stimolano la prostata a produrre più DHT. La terapia ormonale può ridurre i livelli di DHT interrompendo questo percorso in qualche punto.
Esistono varie forme di terapia ormonale:
- L'orchiectomia è la rimozione chirurgica dei testicoli. Poiché i testicoli producono la maggioranza del testosterone, dopo l'orchiectomia i livelli di testosterone cadono.
- Gli antiandrogeni sono farmaci come la flutamide, bicalutamide, nilutamide, e il ciproterone acetato che bloccano direttamente l'azione del testosterone e del DHT all'interno delle cellule tumorali.
- I farmaci bloccanti la produzione di androgeni nei surreni, come il DHEA, comprendono il ketoconazolo e l'amminoglutetimide. Poiché i surreni producono solo il 5% circa degli androgeni circolanti, questi farmaci si usano in genere in combinazione con altri metodi, in grado di bloccare la produzione testicolare di androgeni.
- L'azione del GnRH può essere interrotta in due modi. Gli antagonisti del GnRH sopprimono direttamente la produzione del GnRH, mentre gli agonisti del GnRH agiscono con una downregulation dopo un iniziale effetto stimolante. Degarelix e abarelix sono esempi di GnRH-antagonisti, mentre gli agonisti comprendono la leuprolide, la goserelina, la triptorelina, e la buserelina. Inizialmente questi farmaci aumentano la produzione di LH, tuttavia, poiché la somministrazione del farmaco non segue il ritmo giornaliero di produzione dell'ormone, i livelli di LH e GnRH decrescono dopo poche settimane.[109]
A oggi 2006 la terapia ormonale di maggior efficacia sono l'orchiectomia e i GnRH-agonisti. Nonostante i loro elevati costi, i GnRH-agonisti sono scelti più spesso dell'orchiectomia per ragioni estetiche ed emotive.[110]
Ogni trattamento ha degli svantaggi che ne limitano gli impieghi in certe circostanze. Sebbene l'orchiectomia sia una chirurgia a basso rischio, l'aspetto psicologico della rimozione dei testicoli può essere significativo. Il calo di testosterone può anche causare vampate, aumento di peso, calo della libido, ginecomastia, impotenza e osteoporosi. I GnRH-agonisti possono causare gli stessi effetti dell'orchiectomia ma sintomi peggiori all'inizio del trattamento; quando vi si ricorre in prima istanza l'impennata nei livelli di testosterone causa aumento del dolore dalle metastasi ossee, così spesso vi si accompagnano gli antiandrogeni per mitigarne questi effetti collaterali. Gli estrogeni non si usano comunemente, perché aumentano il rischio di malattie cardiovascolari, e trombosi. Gli antiandrogeni non causano in genere impotenza e danno luogo a minore perdita di massa muscolare e densità ossea. Il chetoconazolo può causare danni epatici con l'uso prolungato, e l'amminoglutetimide rash cutaneo.[110]
Le terapie possono anche essere neoadiuvanti (pre-operatorie per ridurre lo stadio prima della prostatectomia) o adiuvanti (post-operatoria per ridurre il rischio di recidive).
Recidiva biochimica[modifica | modifica wikitesto]
Per recidiva biochimica si intende un innalzamento dei valori di PSA successivo alla prostatectomia radicale (che, essendo prodotto dalle cellule neoplastiche, indica una ripresa della crescita tumorale). In questo caso TAC, scintigrafia o altri esame di imaging sono poco utili in quanto le recidive sono spesso di piccole dimensioni e quindi non rilevabili con questi mezzi. Il metodo migliore per capire se la recidiva è localizzata nella loggia prostatica o è sistemica consiste nell'analizzare la presenza di alcuni fattori di rischio (sotto elencati quelli per recidiva locale, la recidiva sistemica è presunta dai parametri opposti):
- Grado di Gleason <7
- non invasione delle vescichette seminali
- linfonodi pelvici negativi
- PSA dosabile oltre un anno dall'intervento
- PSA velocity <0,74 ng/mL/mese
- tempo di raddoppiamento >6 mesi
La terapia è solamente radioterapica (66 Gy) o associata a ormonoterapia.
Carcinoma della prostata resistente alla castrazione[modifica | modifica wikitesto]
Il carcinoma della prostata può progredire con aumento del PSA, comparsa o progressione delle metastasi durante o dopo la terapia ormonale classica. Si parla in questi casi di carcinoma della prostata resistente alla castrazione. In questa fase di malattia il tumore è in grado di crescere e progredire anche in presenza di basse dosi di testosterone circolante.[111]
Tra i chemioterapici utilizzabili, il docetaxel mostra un aumento della sopravvivenza di circa 2-3 mesi.[112][113] Un farmaco di seconda linea è rappresentato dal cabazitaxel,[114] mentre una certa efficacia è dimostrata dalla combinazione di bevacizumab, docetaxel, talidomide e prednisone.[115]
L'immunoterapia con sipuleucel-T nei pazienti con carcinoma resistente alla castrazione può aumentare la sopravvivenza di circa 4 mesi,[116] mentre il trattamento di seconda linea può essere effettuato con abiraterone, che mostra un aumento della sopravvivenza di 4 mesi e mezzo,[117] o con enzalutamide, una molecola organica, a struttura non steroidea capace di inibire il recettore per gli ormoni androgeni con potenziale attività antitumorale[118][119] che mostra un aumento della sopravvivenza di 5 mesi.[120][121][122]
La terapia radiometabolica delle metastasi ossee con 223Ra ha dimostrato un allungamento della sopravvivenza nei pazienti con tumore resistente alla castrazione[123]. Studi recenti[124] dimostrano come il vaccino GX301 a base di telomerasi, attualmente (2021) ancora in fase di sperimentazione, sia sicuro e induca una buona risposta immunitaria.
La positività delle lesioni metastatiche da carcinoma prostatico alla PSMA-PET può anch'essa essere utilizzata per pianificare una terapia radiometabolica mirata.[83]
Cure palliative[modifica | modifica wikitesto]
Una cura palliativa per i tumori prostatici in fase avanzata è rivolta al migliorare la qualità della vita attenuando i sintomi delle metastasi. La chemioterapia può utilizzarsi per ridurre la progressione della malattia e procrastinarne i sintomi.[125]
Il regime terapeutico usato più di frequente combina il chemioterapico docetaxel con un corticosteroide come il prednisone.[126]
I bifosfonati come l'acido zoledronico si sono dimostrati in grado di posticipare le complicazioni a carico dello scheletro come le fratture; inoltre inibiscono direttamente la crescita delle cellule neoplastiche. L'utilizzo della radioterapia in pazienti con metastasi di carcinoma prostatico refrattarie alla terapia ormonale.[125][127]
Il dolore osseo dovuto alle metastasi viene trattato in prima istanza con analgesici oppioidi come la morfina e l'ossicodone. La radioterapia a fascio esterno diretta sulle metastasi ossee assicura una diminuzione del dolore ed è indicata in caso di lesioni isolate, mentre la terapia radiometabolica è impiegabile nella palliazione della malattia ossea secondaria più diffusa[128][129]
Prognosi[modifica | modifica wikitesto]
Nelle società occidentali i tassi di tumori della prostata sono più elevati, e le prognosi più sfavorevoli che nel resto del mondo. Molti dei fattori di rischio sono maggiormente presenti in Occidente, tra cui la maggior durata di vita e il consumo di grassi animali. Inoltre, dove sono più accessibili i programmi di screening, v'è un maggior tasso di diagnosi. Il tumore della prostata è il nono più frequente tumore nel mondo, e il primo, a parte i tumori cutanei, negli Stati Uniti per quanto riguarda gli uomini, dove nel 2005 ha colpito il 18% degli uomini, e causa di morte per il 3%.[28] In Giappone, il tasso di morte per tumore della prostata era da un quinto alla metà rispetto agli Stati Uniti e all'Europa negli anni novanta;[130] in India nello stesso periodo metà delle persone con tumore della prostata non invasivo morivano entro dieci anni.[131] Gli afroamericani contraggono il tumore e ne muoiono 50-60 volte più frequentemente rispetto agli uomini di Shanghai, Cina.[132] In Nigeria il 2% degli uomini sviluppano tumore prostatico e il 64% di essi muoiono entro due anni.[133]
Nei pazienti sottoposti a trattamento gli indicatori prognostici più importanti sono lo stadio di malattia, i livelli pre-terapia di PSA e l'indice di Gleason. In generale maggiore il grado e lo stadio peggiore è la prognosi. Si può ricorrere ad algoritmi per calcolare il rischio stimato in un determinato paziente. Le predizioni sono basate sull'esperienza su ampi gruppi di pazienti affetti da tumori in vari stadi.[134]
Prevenzione[modifica | modifica wikitesto]
Il rischio di tumore prostatico può ridursi modificando fattori di rischio conosciuti, come l'assunzione di grassi animali. Diversi farmaci e vitamine possono anch'essi aiutare nella prevenzione: due supplementi dietetici, la vitamina E e il selenio; così gli estrogeni ricavati dalla soia e altre fonti vegetali (fitoestrogeni). Il toremifene, modulatore selettivo dei recettori per gli estrogeni, si è dimostrato promettente in test preliminari,[135] così come due farmaci in grado di bloccare la conversione del testosterone in diidrotestosterone, la finasteride[136] e la dutasteride.[137]
Frequenza di eiaculazioni[modifica | modifica wikitesto]
Uno studio del 2003[138] indica che eiaculazioni regolari possono avere un ruolo nella prevenzione del tumore della prostata. Altri studi, tuttavia:[139] non rilevano un'associazione significativa tra i due fattori.[140][141] Questi risultati hanno comunque contraddetto precedenti studi i quali suggerivano che aver avuto numerosi partner sessuali o comunque un'elevata attività sessuale incrementerebbe il rischio di carcinoma prostatico del 40%. Una differenza chiave può essere che questi precedenti studi definivano l'attività sessuale come il rapporto sessuale, mentre quelli più recenti si sono concentrati più sul numero di eiaculazioni avvenute con o senza rapporti sessuali.[142]
Un ulteriore studio risalente al 2004 riporta che: "La maggior parte delle categorie di persone con una elevata frequenza di eiaculazione si sono dimostrate non correlate al rischio di cancro alla prostata. Tuttavia, la frequenza di eiaculazione alta è correlata a diminuzione del rischio totale di cancro alla prostata". L'abstract della relazione ha concluso che: "I nostri risultati suggeriscono che la frequenza di eiaculazione non è correlata a un aumento del rischio di cancro alla prostata".[143]
Note[modifica | modifica wikitesto]
- ^ (EN) Prostate cancer - UK mortality statistics, su info.cancerresearchuk.org. URL consultato il 7 gennaio 2012 (archiviato dall'url originale il 4 gennaio 2012).
- ^ American Cancer Society webpage - (EN) Detailed Guide: prostate cancer, su cancer.org. URL consultato il 26 dicembre 2010.
- ^ Adams, J. The case of scirrhous of the prostate gland with corresponding affliction of the lymphatic glands in the lumbar region and in the pelvis. Lancet 1, 393 (1853).
- ^ Lytton, B. Prostate cancer: a brief history and the discovery of hormonal ablation treatment. J. Urol. 165, 1859-1862
- ^ Young, H. H. Four cases of radical prostatectomy. Johns Hopkins Bull. 16, 315 (1905).
- ^ Walsh, P. C., Lepor, H. & Eggleston, J. C. Radical prostatectomy with preservation of sexual function: anatomical and pathological considerations. Prostate 4, 473-485 (1983). PMID 6889192
- ^ Huggins, C. B. & Hodges, C. V. Studies on prostate cancer: 1. The effects of castration, of estrogen and androgen injection on serum phosphatases in metastatic carcinoma of the prostate. Cancer Res. 1, 203 (1941).
- ^ AV. Schally, AJ. Kastin; A. Arimura, Hypothalamic follicle-stimulating hormone (FSH) and luteinizing hormone (LH)-regulating hormone: structure, physiology, and clinical studies., in Fertil Steril, vol. 22, n. 11, novembre 1971, pp. 703-21, PMID 4941683.
- ^ G. Tolis, D. Ackman; A. Stellos; A. Mehta; F. Labrie; AT. Fazekas; AM. Comaru-Schally; AV. Schally, Tumor growth inhibition in patients with prostatic carcinoma treated with luteinizing hormone-releasing hormone agonists., in Proc Natl Acad Sci U S A, vol. 79, n. 5, marzo 1982, pp. 1658-62, PMID 6461861.
- ^ SR. Denmeade, JT. Isaacs, A history of prostate cancer treatment., in Nat Rev Cancer, vol. 2, n. 5, maggio 2002, pp. 389-96, DOI:10.1038/nrc801, PMID 12044015.
- ^ WW. Scott, DE. Johnson; JE. Schmidt; RP. Gibbons; GR. Prout; JR. Joiner; J. Saroff; GP. Murphy, Chemotherapy of advanced prostatic carcinoma with cyclophosphamide or 5-fluorouracil: results of first national randomized study., in J Urol, vol. 114, n. 6, dicembre 1975, pp. 909-11, PMID 1104900.
- ^ WHO Disease and injury country estimates, su World Health Organization, 2009. URL consultato l'11 novembre 2009.
- ^ Matsuda T, Saika K, Comparison of time trends in prostate cancer incidence (1973-2002) in Asia, from cancer incidence in five continents, Vols IV-IX, in Jpn. J. Clin. Oncol., vol. 39, n. 7, luglio 2009, pp. 468–9, DOI:10.1093/jjco/hyp077, PMID 19553401.
- ^ (EN) web.archive.org, su jncicancerspectrum.oxfordjournals.org (archiviato dall'url originale il 5 febbraio 2006).
- ^ (EN) What causes prostate cancer?, su cancer.org. URL consultato il 26 dicembre 2010 (archiviato dall'url originale il 14 dicembre 2010).
- ^ a b RM. Hoffman, FD. Gilliland; JW. Eley; LC. Harlan; RA. Stephenson; JL. Stanford; PC. Albertson; AS. Hamilton; WC. Hunt; AL. Potosky, Racial and ethnic differences in advanced-stage prostate cancer: the Prostate Cancer Outcomes Study., in J Natl Cancer Inst, vol. 93, n. 5, marzo 2001, pp. 388-95, PMID 11238701.
- ^ (EN) What causes prostate cancer?, su cancer.org, American Cancer Society. URL consultato il 27 gennaio 2012 (archiviato dall'url originale il 22 gennaio 2012).
- ^ Shin HR, Masuyer E, Ferlay J, Curado MP, Cancer in Asia - Incidence rates based on data in cancer incidence in five continents IX (1998-2002), in Asian Pac. J. Cancer Prev., 11 Suppl 2, 2010, pp. 11–6, PMID 20553065.
- ^ International Agency for Research on Cancer
- ^ (EN) The Role of Increasing Detection in the Rising Incidence of Prostate Cancer, su jama.ama-assn.org. URL consultato il 26 dicembre 2010.
- ^ Ann W. Hsing and Anand P. Chokkalingam, Prostate cancer epidemiology, in Frontiers in Bioscience, n. 11, 1º maggio 2006, pp. 1388-1413.
- ^ Djulbegovic M, Beyth RJ, Neuberger MM, et al., Screening for prostate cancer: systematic review and meta-analysis of randomised controlled trials, in BMJ, vol. 341, 2010, pp. c4543, PMC 2939952, PMID 20843937.
- ^ Liu H, Wang B, Han C, Meta-analysis of genome-wide and replication association studies on prostate cancer, in Prostate, vol. 71, n. 2, febbraio 2011, pp. 209–24, DOI:10.1002/pros.21235, PMID 20690139.
- ^ Albain KS, Unger JM, Crowley JJ, Coltman CA, Hershman DL, Racial disparities in cancer survival among randomized clinical trials patients of the Southwest Oncology Group, in J. Natl. Cancer Inst., vol. 101, n. 14, luglio 2009, pp. 984–92, DOI:10.1093/jnci/djp175, PMC 2724852, PMID 19584328.
- ^ Alexander DD, Mink PJ, Cushing CA, Sceurman B, A review and meta-analysis of prospective studies of red and processed meat intake and prostate cancer, in Nutr J, vol. 9, 2010, p. 50, DOI:10.1186/1475-2891-9-50, PMC 2987772, PMID 21044319.
- ^ BF. Hankey, EJ. Feuer; LX. Clegg; RB. Hayes; JM. Legler; PC. Prorok; LA. Ries; RM. Merrill; RS. Kaplan, Cancer surveillance series: interpreting trends in prostate cancer--part I: Evidence of the effects of screening in recent prostate cancer incidence, mortality, and survival rates., in J Natl Cancer Inst, vol. 91, n. 12, giugno 1999, pp. 1017-24, PMID 10379964.
- ^ N. Breslow, CW. Chan; G. Dhom; RA. Drury; LM. Franks; B. Gellei; YS. Lee; S. Lundberg; B. Sparke; NH. Sternby; H. Tulinius, Latent carcinoma of prostate at autopsy in seven areas. The International Agency for Research on Cancer, Lyons, France., in Int J Cancer, vol. 20, n. 5, novembre 1977, pp. 680-8, PMID 924691.
- ^ a b A. Jemal, T. Murray; E. Ward; A. Samuels; RC. Tiwari; A. Ghafoor; EJ. Feuer; MJ. Thun, Cancer statistics, 2005., in CA Cancer J Clin, vol. 55, n. 1, pp. 10-30, PMID 15661684.
- ^ GD. Steinberg, BS. Carter; TH. Beaty; B. Childs; PC. Walsh, Family history and the risk of prostate cancer., in Prostate, vol. 17, n. 4, 1990, pp. 337-47, PMID 2251225.
- ^ P. Lichtenstein, NV. Holm; PK. Verkasalo; A. Iliadou; J. Kaprio; M. Koskenvuo; E. Pukkala; A. Skytthe; K. Hemminki, Environmental and heritable factors in the causation of cancer--analyses of cohorts of twins from Sweden, Denmark, and Finland., in N Engl J Med, vol. 343, n. 2, luglio 2000, pp. 78-85, DOI:10.1056/NEJM200007133430201, PMID 10891514.
- ^ JP. Struewing, P. Hartge; S. Wacholder; SM. Baker; M. Berlin; M. McAdams; MM. Timmerman; LC. Brody; MA. Tucker, The risk of cancer associated with specific mutations of BRCA1 and BRCA2 among Ashkenazi Jews., in N Engl J Med, vol. 336, n. 20, maggio 1997, pp. 1401-8, DOI:10.1056/NEJM199705153362001, PMID 9145676.
- ^ Chan JM, Gann PH, Giovannucci EL., Role of diet in prostate cancer development and progression, in Journal of Clinical Oncology, 2005, PMID 16278466.
- ^ a b Szymanski KM, Wheeler DC, Mucci LA, Fish consumption and prostate cancer risk: a review and meta-analysis, in Am. J. Clin. Nutr., vol. 92, n. 5, novembre 2010, pp. 1223–33, DOI:10.3945/ajcn.2010.29530, PMID 20844069.
- ^ Reese AC, Fradet V, Witte JS, Omega-3 fatty acids, genetic variants in COX-2 and prostate cancer, in J Nutrigenet Nutrigenomics, vol. 2, n. 3, 2009, pp. 149–58, DOI:10.1159/000235565, PMC 2820568, PMID 19776642.
- ^ Ledesma MC, Jung-Hynes B, Schmit TL, Kumar R, Mukhtar H, Ahmad N, Selenium and vitamin E for prostate cancer: post-SELECT (Selenium and Vitamin E Cancer Prevention Trial) status, in Mol. Med., vol. 17, n. 1-2, 2011, pp. 134–43, DOI:10.2119/molmed.2010.00136, PMC 3022975, PMID 20882260.
- ^ CC. Schulman, S. Ekane; AR. Zlotta, Nutrition and prostate cancer: evidence or suspicion?, in Urology, vol. 58, n. 3, settembre 2001, pp. 318-34, PMID 11549473.
- ^ Choo CS, Mamedov A, Chung M, Choo R, Kiss A, Danjoux C, Vitamin D insufficiency is common in patients with nonmetastatic prostate cancer, in Nutr Res, vol. 31, n. 1, gennaio 2011, pp. 21–6, DOI:10.1016/j.nutres.2010.12.007, PMID 21310302.
- ^ EJ. Jacobs, C. Rodriguez; AM. Mondul; CJ. Connell; SJ. Henley; EE. Calle; MJ. Thun, A large cohort study of aspirin and other nonsteroidal anti-inflammatory drugs and prostate cancer incidence., in J Natl Cancer Inst, vol. 97, n. 13, luglio 2005, pp. 975-80, DOI:10.1093/jnci/dji173, PMID 15998950.
- ^ J. Shannon, S. Tewoderos; M. Garzotto; TM. Beer; R. Derenick; A. Palma; PE. Farris, Statins and prostate cancer risk: a case-control study., in Am J Epidemiol, vol. 162, n. 4, agosto 2005, pp. 318-25, DOI:10.1093/aje/kwi203, PMID 16014776.
- ^ E. Giovannucci, TD. Tosteson; FE. Speizer; A. Ascherio; MP. Vessey; GA. Colditz, A retrospective cohort study of vasectomy and prostate cancer in US men., in JAMA, vol. 269, n. 7, febbraio 1993, pp. 878-82, PMID 8123059.
- ^ GG. Giles, G. Severi; DR. English; MR. McCredie; R. Borland; P. Boyle; JL. Hopper, Sexual factors and prostate cancer., in BJU Int, vol. 92, n. 3, agosto 2003, pp. 211-6, PMID 12887469.
- ^ LK. Dennis, CF. Lynch; JC. Torner, Epidemiologic association between prostatitis and prostate cancer., in Urology, vol. 60, n. 1, luglio 2002, pp. 78-83, PMID 12100928.
- ^ EE. Calle, C. Rodriguez; K. Walker-Thurmond; MJ. Thun, Overweight, obesity, and mortality from cancer in a prospectively studied cohort of U.S. adults., in N Engl J Med, vol. 348, n. 17, aprile 2003, pp. 1625-38, DOI:10.1056/NEJMoa021423, PMID 12711737.
- ^ Raynaud JP., Prostate cancer risk in testosterone-treated men, in The Journal of Steroid Biochemistry and Molecular Biology, vol. 102, dicembre 2006, pp. 261-266, PMID 17113983.
- ^ (EN) Adrian Burton, Klinefelter's syndrome changes cancer risk, in The Lancet Oncology, vol. 6, n. 10, 1º ottobre 2005, pp. 741, DOI:10.1016/S1470-2045(05)70375-2. URL consultato il 3 luglio 2021.
- ^ Aumüller, G. Prostate Gland and Seminal Vesicles. Springer-Verlag Berlin-Heidelberg. 1979.
- ^ Moore, K., Dalley, A. Clinically Oriented Anatomy. Lippincott Williams & Wilkins, Baltimore, Maryland. 1999.
- ^ Steive, H. Männliche Genitalorgane. In: Handbuch der mikroskopischen Anatomie des Menschen. Vol. VII Part 2, pp. 1-399. Berlin: Springer 1930.
- ^ Hsing AW, Chokkalingam AP, Prostate cancer epidemiology, in Frontiers in Bioscience, vol. 11, 2006, pp. 1388–413, DOI:10.2741/1891, PMID 16368524.
- ^ BF Hankey, Feuer EJ, Clegg LX, Hayes RB, Legler JM, Prorok PC, Ries LA, Merrill RM, Kaplan RS, Cancer surveillance series: interpreting trends in prostate cancer—part I: Evidence of the effects of screening in recent prostate cancer incidence, mortality, and survival rates, in J Natl Cancer Inst, vol. 91, n. 12, 16 giugno 1999, pp. 1017–24, DOI:10.1093/jnci/91.12.1017, PMID 10379964.
- ^ N Breslow, Chan CW, Dhom G, Drury RA, Franks LM, Gellei B, Lee YS, Lundberg S, Sparke B, Sternby NH, Tulinius H., Latent carcinoma of prostate at autopsy in seven areas. The International Agency for Research on Cancer, Lyons, France, in Int J Cancer, vol. 20, n. 5, 15 novembre 1977, pp. 680–8, DOI:10.1002/ijc.2910200506, PMID 924691.
- ^ Zeegers MP, A Jellema e H Ostrer, Empiric risk of prostate carcinoma for relatives of patients with prostate carcinoma: a meta-analysis, in Cancer, vol. 97, n. 8, 2003, pp. 1894–903, DOI:10.1002/cncr.11262, PMID 12673715.
- ^ A Jemal A, Murray T, Ward E, Samuels A, Tiwari RC, Ghafoor A, Feuer EJ, Thun MJ, Cancer statistics, 2005, in CA Cancer J Clin, vol. 55, n. 1, Jan-February 2005, pp. 10–30, DOI:10.3322/canjclin.55.1.10, PMID 15661684. Erratum in: CA Cancer J Clin. 2005 Jul-Aug;55(4):259
- ^ Martin RM, Vatten L, Gunnell D, Romundstad P, Blood pressure and risk of prostate cancer: cohort Norway (CONOR), in Cancer Causes Control, vol. 21, n. 3, marzo 2010, pp. 463–72, DOI:10.1007/s10552-009-9477-x, PMID 19949849.
- ^ (EN) Witte ON, et al., Growth Regulation of Hematopoietic and Epithelial Cancers and the Immune Response, in Science, vol. 329, n. 5991, luglio 2010, pp. 568–571, DOI:10.1126/science.1189992, PMC 2917982, PMID 20671189.
- ^ a b c Robbins e Cotran, 2008, pp. 1050-1056.
- ^ Albertazzi-Porena, 2003, pp. 691-704.
- ^ a b Harrison, 2006, pp. 623-632.
- ^ Busch PC, Egevad L, Haggman M., Precancer of the prostate, in Cancer Surv., vol. 32, 1998, pp. 149-79., PMID 10489627.
- ^ McNeal JE., Origin and development of carcinoma in the prostate., in Cancer, vol. 23, n. 1, 1969 Jan, pp. 24-34, PMID 576325.
- ^ Wang X, Hickey RJ, Malkas LH, Koch MO, Li L, Zhang S, Sandusky GE, Grignon DJ, Eble JN, Cheng L., Elevated expression of cancer-associated proliferating cell nuclear antigen in high-grade prostatic intraepithelial neoplasia and prostate cancer, in Prostate, 28 ottobre 2010., PMID 21031434.
- ^ Kronz JD, Allan CH, Shaikh AA, Epstein JI., Predicting cancer following a diagnosis of high-grade prostatic intraepithelial neoplasia on needle biopsy: data on men with more than one follow-up biopsy., in Am J Surg Pathol, vol. 25, n. 8, 2001 Aug, pp. 107-85., PMID 1147429.
- ^ Häggman MJ, Macoska JA, Wojno KJ, Oesterling JE., The relationship between prostatic intraepithelial neoplasia and prostate cancer: critical issues., in J Urol., vol. 158, n. 1, 1997 Jul, pp. 12-22, PMID 9186314.
- ^ DC. Miller, KS. Hafez; A. Stewart; JE. Montie; JT. Wei, Prostate carcinoma presentation, diagnosis, and staging: an update form the National Cancer Data Base., in Cancer, vol. 98, n. 6, settembre 2003, pp. 1169-78, DOI:10.1002/cncr.11635, PMID 12973840.
- ^ IW. van der Cruijsen-Koeter, AN. Vis; MJ. Roobol; MF. Wildhagen; HJ. de Koning; TH. van der Kwast; FH. Schröder, Comparison of screen detected and clinically diagnosed prostate cancer in the European randomized study of screening for prostate cancer, section rotterdam., in J Urol, vol. 174, n. 1, luglio 2005, pp. 121-5, DOI:10.1097/01.ju.0000162061.40533.0f, PMID 15947595.
- ^ Salute internazionale, su saluteinternazionale.info.
- ^ RL. Grubb, KA. Roehl; JA. Antenor; WJ. Catalona, Results of compliance with prostate cancer screening guidelines., in J Urol, vol. 174, n. 2, agosto 2005, pp. 668-72; discussion 672, PMID 16006944.
- ^ S. Giusti, D. Caramella; E. Fruzzetti; M. Lazzereschi; A. Tognetti; C. Bartolozzi, Peripheral zone prostate cancer. Pre-treatment evaluation with MR and 3D ¹H MR spectroscopic imaging: correlation with pathologic findings., in Abdom Imaging, vol. 35, n. 6, dicembre 2010, pp. 757-63, DOI:10.1007/s00261-009-9577-9, PMID 19756851.
- ^ https://doi.org/10.1016/j.euo.2023.09.008
- ^ GW. Chodak, P. Keller; HW. Schoenberg, Assessment of screening for prostate cancer using the digital rectal examination., in J Urol, vol. 141, n. 5, maggio 1989, pp. 1136-8, PMID 2709500.
- ^ MD. Krahn, JE. Mahoney; MH. Eckman; J. Trachtenberg; SG. Pauker; AS. Detsky, Screening for prostate cancer. A decision analytic view., in JAMA, vol. 272, n. 10, settembre 1994, pp. 773-80, PMID 7521400.
- ^ Hessels D, Schalken JA, The use of PCA3 in the diagnosis of prostate cancer., in Nat Rev Urol., vol. 5, n. 6, maggio 2009, pp. 255-61, PMID 19424173.
- ^ (EN) Laxman B, Morris DS, Yu J, et al., A first-generation multiplex biomarker analysis of urine for the early detection of prostate cancer, in Cancer Res., vol. 68, n. 3, febbraio 2008, pp. 645–9, DOI:10.1158/0008-5472.CAN-07-3224, PMID 18245462.
- ^ (EN) de la Taille A, Progensa PCA3 test for prostate cancer detection, in Expert Rev. Mol. Diagn., vol. 7, n. 5, settembre 2007, pp. 491–7, DOI:10.1586/14737159.7.5.491, PMID 17892357.
- ^ (EN) Bussemakers MJ, van Bokhoven A, Verhaegh GW, et al., DD3: a new prostate-specific gene, highly overexpressed in prostate cancer, in Cancer Res., vol. 59, n. 23, dicembre 1999, pp. 5975–9, PMID 10606244.
- ^ (EN) Neves AF, Araújo TG, Biase WK, et al., Combined analysis of multiple mRNA markers by RT-PCR assay for prostate cancer diagnosis, in Clin. Biochem., vol. 41, n. 14-15, luglio 2008, p. 1191, DOI:10.1016/j.clinbiochem.2008.06.013, PMID 18640109.
- ^ Haese A, de la Taille A, van Poppel H, et al., Clinical Utility of the PCA3 Urine Assay in European Men Scheduled for Repeat Biopsy, in Eur. Urol., vol. 54, n. 5, giugno 2008, p. 1081, DOI:10.1016/j.eururo.2008.06.071, PMID 18602209.
- ^ Marks LS, Fradet Y, Deras IL, et al., PCA3 molecular urine assay for prostate cancer in men undergoing repeat biopsy, in Urology, vol. 69, n. 3, marzo 2007, pp. 532–5, DOI:10.1016/j.urology.2006.12.014, PMID 17382159.
- ^ ML. Essink-Bot, HJ. de Koning; HG. Nijs; WJ. Kirkels; PJ. van der Maas; FH. Schröder, Short-term effects of population-based screening for prostate cancer on health-related quality of life., in J Natl Cancer Inst, vol. 90, n. 12, giugno 1998, pp. 925-31, PMID 9637143.
- ^ Sanraffaele.org - Nuovo esame per tumore alla prostata, su sanraffaele.org. URL consultato il 28 marzo 2021 (archiviato dall'url originale il 10 settembre 2012).
- ^ M. Picchio, C. Messa; C. Landoni; L. Gianolli; S. Sironi; M. Brioschi; M. Matarrese; DV. Matei; F. De Cobelli; A. Del Maschio; F. Rocco, Value of [11C]choline-positron emission tomography for re-staging prostate cancer: a comparison with [18F]fluorodeoxyglucose-positron emission tomography., in J Urol, vol. 169, n. 4, aprile 2003, pp. 1337-40, DOI:10.1097/01.ju.0000056901.95996.43, PMID 12629355.
- ^ https://pubmed.ncbi.nlm.nih.gov/35486169/
- ^ a b https://pubmed.ncbi.nlm.nih.gov/31440799/
- ^ B. Scher, M. Seitz; W. Albinger; R. Tiling; M. Scherr; HC. Becker; M. Souvatzogluou; FJ. Gildehaus; HJ. Wester; S. Dresel, Value of 11C-choline PET and PET/CT in patients with suspected prostate cancer., in Eur J Nucl Med Mol Imaging, vol. 34, n. 1, gennaio 2007, pp. 45-53, DOI:10.1007/s00259-006-0190-7, PMID 16932935.
- ^ Prostatakrebs-Kodierhilfe. Tumorzentrum Freiburg 2007 Archiviato il 9 ottobre 2007 in Internet Archive. (PDF)
- ^ Christian Wittekind, Hans-Joachim Meyer (Hrsg.): TNM: Klassifikation maligner Tumoren. Wiley-VCH Verlag, 7. Auflage 2010, ISBN 3-527-32759-2
- ^ Cheng L, Montironi R, Bostwick DG, Lopez-Beltran A, Berney DM, Staging of prostate cancer, in Histopathology, gennaio 2012, PMID 22212080.
- ^ Wagner W, Bölling T, Hambruegge C, Hartlapp J, Krukemeyer MG, Patients' satisfaction with different modalities of prostate cancer therapy--a retrospective survey among 634 patients, in Anticancer Res, novembre 2011, PMID 22110217.
- ^ Corcoran NM, Gleave ME, Targeted therapy in prostate cancer, in Histopathology, gennaio 2012, PMID 22212088.
- ^ Bach P, Döring T, Gesenberg A, Möhring C, Goepel M, Psychological aspects of prostate cancer: a clinical review, gennaio 2012, PMID 22212706.
- ^ Treatments for Clinically Localized Prostate Cancer, PMID 21938810.
- ^ S. Gupta, M. Varghese; MM. Shareef; MM. Ahmed, Human Prostate Cancer Cells Secrete Neuro-Protective Factors in Response to Cryotherapy., in Mol Cell Pharmacol, vol. 1, n. 4, gennaio 2009, pp. 200-206, PMID 20401329.
- ^ DS. Finley, AS. Belldegrun, Salvage cryotherapy for radiation-recurrent prostate cancer: outcomes and complications., in Curr Urol Rep, vol. 12, n. 3, giugno 2011, pp. 209-15, DOI:10.1007/s11934-011-0182-4, PMID 21394596.
- ^ H. Wu, L. Sun; JW. Moul; HY. Wu; DG. McLeod; C. Amling; R. Lance; L. Kusuda; T. Donahue; J. Foley; A. Chung, Watchful waiting and factors predictive of secondary treatment of localized prostate cancer., in J Urol, vol. 171, n. 3, marzo 2004, pp. 1111-6, DOI:10.1097/01.ju.0000113300.74132.8b, PMID 14767282.
- ^ Klotz L., Active surveillance for prostate cancer: a review, ottobre 2011, PMID 22052761.
- ^ Aldo Zangara, Terapia medica ragionata, PICCIN, 2002, pp. 1105–, ISBN 978-88-299-1649-8.
- ^ H. Zincke, JE. Oesterling; ML. Blute; EJ. Bergstralh; RP. Myers; DM. Barrett, Long-term (15 years) results after radical prostatectomy for clinically localized (stage T2c or lower) prostate cancer., in J Urol, vol. 152, 5 Pt 2, novembre 1994, pp. 1850-7, PMID 7523733.
- ^ GS. Gerber, RA. Thisted; PT. Scardino; HG. Frohmuller; FH. Schroeder; DF. Paulson; AW. Middleton; DB. Rukstalis; JA. Smith; PF. Schellhammer; M. Ohori, Results of radical prostatectomy in men with clinically localized prostate cancer., in JAMA, vol. 276, n. 8, agosto 1996, pp. 615-9, PMID 8773633.
- ^ Ward JF, Zincke H, Radical prostatectomy for the patient with locally advanced prostate cancer, in Curr Urol Rep, vol. 4, n. 3, 2003, pp. 196-204, PMID 12756082.
- ^ Dott. J.C. HU, Urologo all'ospedale di Boston, su JAMA (American Medical Association, Vol.302, nº14, 2009
- ^ Radioterapia a fasci esterni, su aimac.it, AIMaC. URL consultato il 25 gennaio 2012.
- ^ CA. Perez, GE. Hanks; SA. Leibel; AL. Zietman; Z. Fuks; WR. Lee, Localized carcinoma of the prostate (stages T1B, T1C, T2, and T3). Review of management with external beam radiation therapy., in Cancer, vol. 72, n. 11, dicembre 1993, pp. 3156-73, PMID 7694785.
- ^ Bice WS, Prestidge BR, Kurtzman SM, et al., Recommendations for permanent prostate brachytherapy with (131)Cs: a consensus report from the Cesium Advisory Group, in Brachytherapy, vol. 7, n. 4, 2008, pp. 290–6, DOI:10.1016/j.brachy.2008.05.004, PMID 18782682.
- ^ AV. D'Amico, J. Manola; M. Loffredo; AA. Renshaw; A. DellaCroce; PW. Kantoff, 6-month androgen suppression plus radiation therapy vs radiation therapy alone for patients with clinically localized prostate cancer: a randomized controlled trial., in JAMA, vol. 292, n. 7, agosto 2004, pp. 821-7, DOI:10.1001/jama.292.7.821, PMID 15315996.
- ^ CA. Lawton, M. Won; MV. Pilepich; SO. Asbell; WU. Shipley; GE. Hanks; JD. Cox; CA. Perez; WT. Sause; SR. Doggett, Long-term treatment sequelae following external beam irradiation for adenocarcinoma of the prostate: analysis of RTOG studies 7506 and 7706., in Int J Radiat Oncol Biol Phys, vol. 21, n. 4, settembre 1991, pp. 935-9, PMID 1917622.
- ^ DJ. Brenner, RE. Curtis; EJ. Hall; E. Ron, Second malignancies in prostate carcinoma patients after radiotherapy compared with surgery., in Cancer, vol. 88, n. 2, gennaio 2000, pp. 398-406, PMID 10640974.
- ^ DK. Bahn, F. Lee; R. Badalament; A. Kumar; J. Greski; M. Chernick, Targeted cryoablation of the prostate: 7-year outcomes in the primary treatment of prostate cancer., in Urology, vol. 60, 2 Suppl 1, agosto 2002, pp. 3-11, PMID 12206842.
- ^ M. Robson, N. Dawson, How is androgen-dependent metastatic prostate cancer best treated?, in Hematol Oncol Clin North Am, vol. 10, n. 3, giugno 1996, pp. 727-47, PMID 8773508.
- ^ DA. Loblaw, DS. Mendelson; JA. Talcott; KS. Virgo; MR. Somerfield; E. Ben-Josef; R. Middleton; H. Porterfield; SA. Sharp; TJ. Smith; ME. Taplin, American Society of Clinical Oncology recommendations for the initial hormonal management of androgen-sensitive metastatic, recurrent, or progressive prostate cancer., in J Clin Oncol, vol. 22, n. 14, luglio 2004, pp. 2927-41, DOI:10.1200/JCO.2004.04.579, PMID 15184404.
- ^ a b T. Tammela, Endocrine treatment of prostate cancer., in J Steroid Biochem Mol Biol, vol. 92, n. 4, novembre 2004, pp. 287-95, DOI:10.1016/j.jsbmb.2004.10.005, PMID 15663992.
- ^ CL. Derleth, EY. Yu, Targeted therapy in the treatment of castration-resistant prostate cancer., in Oncology (Williston Park), vol. 27, n. 7, luglio 2013, pp. 620-8, PMID 23977754.
- ^ Clarke NW, Docetaxel for the Treatment of Hormone Refractory Prostate Cancer (PDF), su nice.org.uk, 2005. URL consultato il 6 ottobre 2013 (archiviato dall'url originale il 12 luglio 2012).
- ^ Prostate cancer (hormone-refractory) - docetaxel, su nice.org.uk, National Institute for Health and Clinical Excellence, 10 dicembre 2010. URL consultato il 6 ottobre 2013.
- ^ JS. de Bono, S. Oudard; M. Ozguroglu; S. Hansen; JP. Machiels; I. Kocak; G. Gravis; I. Bodrogi; MJ. Mackenzie; L. Shen; M. Roessner, Prednisone plus cabazitaxel or mitoxantrone for metastatic castration-resistant prostate cancer progressing after docetaxel treatment: a randomised open-label trial., in Lancet, vol. 376, n. 9747, ottobre 2010, pp. 1147-54, DOI:10.1016/S0140-6736(10)61389-X, PMID 20888992.
- ^ YM. Ning, JL. Gulley; PM. Arlen; S. Woo; SM. Steinberg; JJ. Wright; HL. Parnes; JB. Trepel; MJ. Lee; YS. Kim; H. Sun, Phase II trial of bevacizumab, thalidomide, docetaxel, and prednisone in patients with metastatic castration-resistant prostate cancer., in J Clin Oncol, vol. 28, n. 12, aprile 2010, pp. 2070-6, DOI:10.1200/JCO.2009.25.4524, PMID 20308663.
- ^ PW. Kantoff, CS. Higano; ND. Shore; ER. Berger; EJ. Small; DF. Penson; CH. Redfern; AC. Ferrari; R. Dreicer; RB. Sims; Y. Xu, Sipuleucel-T immunotherapy for castration-resistant prostate cancer., in N Engl J Med, vol. 363, n. 5, luglio 2010, pp. 411-22, DOI:10.1056/NEJMoa1001294, PMID 20818862.
- ^ FDA approves Zytiga for late-stage prostate cancer, su fda.gov, U.S. Food and Drug Administration, 28 aprile 2011. URL consultato il 6 ottobre 2013.
- ^ (FR) Noel-Wekstein S, Turpin G, De Gennes JL, [Magnetic resonance imaging in the follow-up of craniopharyngioma surgically treated], in Presse Med, vol. 19, n. 1, 1990, p. 32, PMID 2137222.
- ^ Scher HI, Beer TM, Higano CS, et al., Antitumour activity of MDV3100 in castration-resistant prostate cancer: a phase 1-2 study, in Lancet, vol. 375, n. 9724, aprile 2010, pp. 1437–46, DOI:10.1016/S0140-6736(10)60172-9, PMC 2948179, PMID 20398925.
- ^ FDA approves new treatment for a type of late stage prostate cancer, su fda.gov, United States Food and Drug Administration, 31 agosto 2012. URL consultato il 6 ottobre 2013.
- ^ Anna Azvolinsky, FDA Approves Enzalutamide (Xtandi) for Late-Stage Prostate Cancer, su cancernetwork.com, CancerNetwork, 4 settembre 2012. URL consultato il 6 ottobre 2013.
- ^ (EN) Search of: MDV3100 - List Results - ClinicalTrials.gov, su clinicaltrial.gov (archiviato dall'url originale il 25 febbraio 2014).
- ^ PR. Sieber, Emerging Therapeutic for the Treatment of Skeletal-related Events Associated With Metastatic Castrate-resistant Prostate Cancer., in Rev Urol, vol. 16, n. 1, 2014, pp. 10-20, PMID 24791151.
- ^ Gilberto Filaci, Daniela Fenoglio e Franco Nolè, Telomerase-based GX301 cancer vaccine in patients with metastatic castration-resistant prostate cancer: a randomized phase II trial, in Cancer immunology, immunotherapy: CII, vol. 70, n. 12, 2021-12, pp. 3679–3692, DOI:10.1007/s00262-021-03024-0. URL consultato il 26 novembre 2021.
- ^ a b RK. Portenoy, Treatment of cancer pain., in Lancet, vol. 377, n. 9784, giugno 2011, pp. 2236-47, DOI:10.1016/S0140-6736(11)60236-5, PMID 21704873.
- ^ J. Yaneva, J. Zlatanova, Histone H1 interacts specifically with certain regions of the mouse alpha-globin gene., in DNA Cell Biol, vol. 11, n. 2, marzo 1992, pp. 91-9, PMID 1547021.
- ^ Saad F, Gleason DM, Murray R, Tchekmedyian S, Venner P, Lacombe L, Chin JL, Vinholes JJ, Goas JA, Chen B, A randomized, placebo-controlled trial of zoledronic acid in patients with hormone-refractory metastatic prostate carcinoma, in J Natl Cancer Inst, vol. 94, n. 19, 2002, pp. 1458-68, PMID 12359855.
- ^ E. Seregni, B. Padovano; A. Coliva; E. Zecca; E. Bombardieri, State of the art of palliative therapy., in Q J Nucl Med Mol Imaging, vol. 55, n. 4, agosto 2011, pp. 411-9, PMID 21738114.
- ^ DJ. Hillegonds, S. Franklin; DK. Shelton; S. Vijayakumar; V. Vijayakumar, The management of painful bone metastases with an emphasis on radionuclide therapy., in J Natl Med Assoc, vol. 99, n. 7, luglio 2007, pp. 785-94, PMID 17668645.
- ^ K. Wakai, [Descriptive epidemiology of prostate cancer in Japan and Western countries]., in Nihon Rinsho, vol. 63, n. 2, febbraio 2005, pp. 207-12, PMID 15714967.
- ^ M. Jaubert de Beaujeu, Y. Chavrier, [Deformations of the anterior thoracic wall (author's transl)]., in Ann Chir Thorac Cardiovasc, vol. 15, n. 1, gennaio 1976, pp. 1-6, PMID 1259345.
- ^ AW. Hsing, L. Tsao; SS. Devesa, International trends and patterns of prostate cancer incidence and mortality., in Int J Cancer, vol. 85, n. 1, gennaio 2000, pp. 60-7, PMID 10585584.
- ^ DN. Osegbe, Prostate cancer in Nigerians: facts and nonfacts., in J Urol, vol. 157, n. 4, aprile 1997, pp. 1340-3, PMID 9120935.
- ^ Di Blasio CJ, Rhee AC, Cho D, Scardino PT, Kattan MW, Predicting clinical end points: treatment nomograms in prostate cancer, in Semin Oncol, vol. 30, n. 5, 2003, pp. 567-86, PMID 14571407.
- ^ MS. Steiner, CR. Pound, Phase IIA clinical trial to test the efficacy and safety of Toremifene in men with high-grade prostatic intraepithelial neoplasia., in Clin Prostate Cancer, vol. 2, n. 1, giugno 2003, pp. 24-31, PMID 15046680.
- ^ IM. Thompson, PJ. Goodman; CM. Tangen; MS. Lucia; GJ. Miller; LG. Ford; MM. Lieber; RD. Cespedes; JN. Atkins; SM. Lippman; SM. Carlin, The influence of finasteride on the development of prostate cancer., in N Engl J Med, vol. 349, n. 3, luglio 2003, pp. 215-24, DOI:10.1056/NEJMoa030660, PMID 12824459.
- ^ RJ. Hamilton, SJ. Freedland, 5-α reductase inhibitors and prostate cancer prevention: where do we turn now?, in BMC Med, vol. 9, 2011, p. 105, DOI:10.1186/1741-7015-9-105, PMID 21920036.
- ^ Giles GG, Severi G, English DR, et al., Sexual factors and prostate cancer, in BJU Int., vol. 92, n. 3, agosto 2003, pp. 211–6, PMID 12887469.
- ^ Leitzmann MF, Platz EA, Stampfer MJ, Willett WC, Giovannucci E, Ejaculation frequency and subsequent risk of prostate cancer, in JAMA, vol. 291, n. 13, aprile 2004, pp. 1578–86, DOI:10.1001/jama.291.13.1578, PMID 15069045.
- ^ Giles GG, Severi G, English DR, McCredie MR, Borland R, Boyle P, Hopper JL, Sexual factors and prostate cancer, in BJU Int., vol. 92, n. 3, agosto 2003, pp. 211–6, DOI:10.1046/j.1464-410X.2003.04319.x, PMID 12887469.
- ^ Leitzmann MF, Platz EA, Stampfer MJ, Willett WC, Giovannucci E, Ejaculation frequency and subsequent risk of prostate cancer, in JAMA, vol. 291, n. 13, aprile 2004, pp. 1578–86, DOI:10.1001/jama.291.13.1578, PMID 15069045.
- ^ Douglas Fox, Masturbating may protect against prostate cancer, su newscientist.com, New Scientist, 16 luglio 2003.
- ^ Dimitropoulou P, Lophatananon A, Easton D, Pocock R, Dearnaley DP, Guy M, Edwards S, O'Brien L, Hall A, Wilkinson R, Eeles R, Muir KR, Sexual activity and prostate cancer risk in men diagnosed at a younger age, in BJU Int., vol. 103, n. 2, gennaio 2009, pp. 178–85, DOI:10.1111/j.1464-410X.2008.08030.x, PMID 19016689.
Bibliografia[modifica | modifica wikitesto]
- (EN) Position of the American Dietetic Association and Dietitians of Canada: Vegetarian diets, in J Am Diet Assoc, vol. 103, n. 6, 2003, pp. 748-65, PMID 12778049.
- (EN) Strom SS, Yamamura Y, Duphorne CM, Spitz MR, Babaian RJ, Pillow PC, Hursting SD. Phytoestrogen intake and prostate cancer: a case-control study using a new database. Nutr Cancer. 1999;33(1):20-5. Erratum in: Nutr Cancer 2000;36(2):243. PMID 10227039
- (EN) Clinically localised prostate cancer , Timothy J Wilt, Ian M Thompson, BMJ 2006;333:1102-1106
- (EN) Emil A. Tanagho, Jack W. McAninch: Smith's General Urology. Appleton & Lange, Norwalk 1995. ISBN 0-8385-8612-0.
- (DE) Hans Ulrich Schmelz, Christoph Sparwasser, Wolfgang Weidner: Facharztwissen Urologie. Springer, Heidelberg 2006. ISBN 3-540-20009-6.
- (DE) Herbert Rübben: Uroonkologie. Springer, Berlin 2001. ISBN 3-540-67310-5.
- (DE) Jürgen Sökeland: Urologie. Thieme, Stuttgart 1993. ISBN 3-13-300611-8.
- (DE) M. Kessler: Kleintieronkologie. Parey-Verlag, München 2005. ISBN 3-8304-4103-7.
Testi di oncologia e patologia generale[modifica | modifica wikitesto]
- Gianni Bonadonna, Gioacchino Robustelli Della Cuna, Pinuccia Valgussa, Medicina oncologica, 8ª ed., Milano, Elsevier Masson, 2007, ISBN 978-88-214-2814-2.
- Pontieri, Russo, Frati, Patologia generale, 3ª ed., Padova, Piccin, 2005, ISBN 88-299-1734-6.
Testi di anatomia patologica[modifica | modifica wikitesto]
- Robbins e Cotran, Le basi patologiche delle malattie, 7ª ed., Torino-Milano, Elsevier Masson, 2008, ISBN 978-88-85675-53-7.
- Mariuzzi, Anatomia patologica e correlazioni anatomo-cliniche, Padova, Piccin, 2006, ISBN 978-88-299-1769-3.
- James O'D. McGee, Peter G. Isaacson, Nicholas A. Wright, Heather M. Dick, Mary P. E. Slack, Oxford Textbook of Pathology, New York, Oxford University Press, USA, 2007, ISBN 978-0-19-261972-3.
Testi di medicina interna e urologia[modifica | modifica wikitesto]
- Harrison, Principi di Medicina Interna - 16ª edizione, New York - Milano, McGraw-Hill, 2006, ISBN 978-88-386-3929-6.
- Claudio Rugarli, Medicina interna sistematica, 5ª ed., Masson, 2005, ISBN 978-88-214-2792-3.
- Albertazzi-Porena, Malattie del rene, delle vie urinarie e dell'apparato genitale maschile, Padova, Piccin, 2003, ISBN 88-299-1742-7.
Testi di diagnostica per immagini e radioterapia[modifica | modifica wikitesto]
- Giorgio Cittadini, Diagnostica per immagini e radioterapia, ECIG, 2008, ISBN 978-88-7544-138-8.
- Angelelli, AA.VV., Diagnostica per immagini per studenti e medici di medicina generale, Napoli, Idelson-Gnocchi, 2008, ISBN 978-88-7947-489-4.
Testi di farmacologia e chemioterapia[modifica | modifica wikitesto]
- Brunton, Lazo, Parker, Goodman & Gilman - Le basi farmacologiche della terapia, 11ª ed., McGraw Hill, 2006, ISBN 978-88-386-3911-1.
- Bertram G. Katzung, Farmacologia generale e clinica, Padova, Piccin, 2006, ISBN 88-299-1804-0.
Pubblicazioni (peer-review)[modifica | modifica wikitesto]
Linee guida (2005 - 2010)[modifica | modifica wikitesto]
- Wolf AM, Wender RC, Etzioni RB, et al., American Cancer Society guideline for the early detection of prostate cancer: update 2010, in CA Cancer J Clin, vol. 60, n. 2, 2010, pp. 70–98, DOI:10.3322/caac.20066, PMID 20200110.
- Horwich A, Parker C, Bangma C, Kataja V, Prostate cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up, in Ann. Oncol., 21 Suppl 5, maggio 2010, pp. v129–33, DOI:10.1093/annonc/mdq174, PMID 20555062.
- Heidenreich A, Albers P, Classen J, et al., Imaging studies in metastatic urogenital cancer patients undergoing systemic therapy: recommendations of a multidisciplinary consensus meeting of the Association of Urological Oncology of the German Cancer Society, in Urol. Int., vol. 85, n. 1, luglio 2010, pp. 1–10, DOI:10.1159/000318985, PMID 20693823.
- Mohler J, Bahnson RR, Boston B, et al., NCCN clinical practice guidelines in oncology: prostate cancer, in J Natl Compr Canc Netw, vol. 8, n. 2, febbraio 2010, pp. 162–200, PMID 20141676.
- Kawachi MH, Bahnson RR, Barry M, et al., NCCN clinical practice guidelines in oncology: prostate cancer early detection, in J Natl Compr Canc Netw, vol. 8, n. 2, febbraio 2010, pp. 240–62, PMID 20141680.
- (FR) Mongiat-Artus P, Peyromaure M, Richaud P, et al., [Recommendations for the treatment of prostate cancer in the elderly man: A study by the oncology committee of the French association of urology], in Prog. Urol., vol. 19, n. 11, dicembre 2009, pp. 810–7, DOI:10.1016/j.purol.2009.02.008, PMID 19945664.
- (ES) Heidenreich A, Aus G, Bolla M, et al., [EAU guidelines on prostate cancer], in Actas Urol Esp, vol. 33, n. 2, febbraio 2009, pp. 113–26, PMID 19418833.
- Hamashima C, Nakayama T, Sagawa M, Saito H, Sobue T, The Japanese guideline for prostate cancer screening, in Jpn. J. Clin. Oncol., vol. 39, n. 6, giugno 2009, pp. 339–51, DOI:10.1093/jjco/hyp025, PMID 19346535.
- Kramer BS, Hagerty KL, Justman S, et al., Use of 5-alpha-reductase inhibitors for prostate cancer chemoprevention: American Society of Clinical Oncology/American Urological Association 2008 Clinical Practice Guideline, in J. Clin. Oncol., vol. 27, n. 9, marzo 2009, pp. 1502–16, DOI:10.1200/JCO.2008.16.9599, PMC 2668556, PMID 19252137.
- Sturgeon CM, Duffy MJ, Stenman UH, et al., National Academy of Clinical Biochemistry laboratory medicine practice guidelines for use of tumor markers in testicular, prostate, colorectal, breast, and ovarian cancers, in Clin. Chem., vol. 54, n. 12, dicembre 2008, pp. e11–79, DOI:10.1373/clinchem.2008.105601, PMID 19042984.
- Lin K, Lipsitz R, Miller T, Janakiraman S, Benefits and harms of prostate-specific antigen screening for prostate cancer: an evidence update for the U.S. Preventive Services Task Force, in Ann. Intern. Med., vol. 149, n. 3, agosto 2008, pp. 192–9, PMID 18678846.
- Borneman T, Piper BF, Sun VC, Koczywas M, Uman G, Ferrell B, Implementing the Fatigue Guidelines at one NCCN member institution: process and outcomes, in J Natl Compr Canc Netw, vol. 5, n. 10, novembre 2007, pp. 1092–101, PMC 2515169, PMID 18053431.
Linee guida italiane[modifica | modifica wikitesto]
- Ist. toscano tumori, 5. Carcinoma della Prostata (PDF), su ittumori.it, www.ittumori.it.
- Bianchi G, Bracarda S, Bruzi P, et al., [Guidelines for prostate biopsy], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 63–5, PMID 16402733.
- De Luca S, Bertaccini A, Galetti TP, [Prostate biopsy: staging values], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 57–62, PMID 16402732.
- Bertè R, [Prostate biopsy: re-biopsy after prostatectomy], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 53–6, PMID 16402731.
- Bortolus R, [Prostate biopsy: re-biopsy after radiotherapy], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 50–2, PMID 16402730.
- Fandella A, Bertaccini A, Consonni P, Introini C, Gunelli R, [Prostate biopsy: re-biopsy after first negative biopsy], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 39–49, PMID 16402729.
- Galosi AB, Maruzzi D, Milani C, Nava L, Scattoni V, Zambolin T, [Prostate biopsy: number and places of sampling], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 33–8, PMID 16402728.
- De Matteis A, Bollito E, Galosi AB, Gardiman M, Montironi R, Sentinelli S, [Prostate biopsy: characteristics of the histological sample], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 28–32, PMID 16402727.
- Bertaccini A, Consonni P, Schiavina R, et al., [Prostate biopsy: approaches], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 24–7, PMID 16402726.
- Ferrante GL, Manferrari F, Maruzzi D, [Prostate biopsy: patient preparation and anesthesia], in Arch Ital Urol Androl, vol. 77, 3 Suppl 1, settembre 2005, pp. 17–23, PMID 16402725.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su carcinoma della prostata
Wikimedia Commons contiene immagini o altri file su carcinoma della prostata
Collegamenti esterni[modifica | modifica wikitesto]
- AIRC – Associazione Italiana Ricerca sul cancro Scheda Tumori: Tumore alla prostata, su airc.it.
- Cancro della prostata approfondimenti circa l'adenocarcinoma prostatico
- Progetto Oncologia del CNR, che illustra, tra le altre cose, l'epidemiologia, la diagnosi, la sintomatologia, le terapie e opzioni alternative, Follow-up e una lunga bibliografia.
- Sito italiano sulla brachiterapia a cura dell'Ospedale San Raffaele di Milano, su brachiterapia.it.
- (EN) urologychannel.com, dai sintomi ai trattamenti.
- (EN) Prostate Cancer Foundation, su prostatecancerfoundation.org.
- (EN) American Cancer Society, su cancer.org.
- (EN) National Kidney and Urologic Diseases Information Clearinghouse, su kidney.niddk.nih.gov. URL consultato il 29 gennaio 2006 (archiviato dall'url originale l'8 febbraio 2006).
- (EN) Studies of capsicina by AACR
- (EN) deCODE scopre fattori di rischio genetico considerevoli per il carcinoma prostatico, su prnewswire.com. URL consultato il 26 dicembre 2010 (archiviato dall'url originale il 25 luglio 2014).
- (EN) Stadiazione del carcinoma prostatico, su doctorslounge.com. URL consultato il 26 dicembre 2010 (archiviato dall'url originale il 6 febbraio 2012).
Supporto per i pazienti (siti in inglese):
- (EN) Newsgroup
- (EN) Sito non-profit aggiornato settimanalmente, su malecare.org.
| Classificazione e risorse esterne (EN) |
ICD-9-CM: 185; ICD-10: C6161.; ICD-10-CM: C61; OMIM: 176807, 300147, 300704, 601518, 602759, 608656, 608658, 609299, 609558, 610321, 610997, 611100, 611868, 611928, 611955, 611958 e 611959; DiseasesDB: 10780; |
| Controllo di autorità | LCCN (EN) sh85107606 · GND (DE) 4047511-6 · BNF (FR) cb12647583w (data) · J9U (EN, HE) 987007541096505171 · NDL (EN, JA) 00575400 |
|---|