Ebolavirus: differenze tra le versioni
→Riserve virali: ins. testo |
→Riserve virali: ins. testo e ref. |
||
| Riga 102: | Riga 102: | ||
Nel 2012 è stato scoperto in [[Cina]] il primo isolamento da pipistrelli del filovirus ceppo Reston a seguito di [[sierologia|esami sierologici]] condotti in una popolazione di pipistrelli cinesi. Il ceppo Reston ebolavirus, scoperto nelle Filippine, è l'unica specie ebolavirus identificata in Asia fino ad oggi.<ref name="Yuan-2012">{{Cita pubblicazione | cognome = Yuan | nome = J. | coauthors = Y. Zhang; J. Li; Y. Zhang; LF. Wang; Z. Shi | titolo = Serological evidence of ebolavirus infection in bats, China. | rivista = Virol J | volume = 9 | numero = | pagine = 236 | mese = | anno = 2012 | doi = 10.1186/1743-422X-9-236 | id = PMID 23062147 }}</ref> |
Nel 2012 è stato scoperto in [[Cina]] il primo isolamento da pipistrelli del filovirus ceppo Reston a seguito di [[sierologia|esami sierologici]] condotti in una popolazione di pipistrelli cinesi. Il ceppo Reston ebolavirus, scoperto nelle Filippine, è l'unica specie ebolavirus identificata in Asia fino ad oggi.<ref name="Yuan-2012">{{Cita pubblicazione | cognome = Yuan | nome = J. | coauthors = Y. Zhang; J. Li; Y. Zhang; LF. Wang; Z. Shi | titolo = Serological evidence of ebolavirus infection in bats, China. | rivista = Virol J | volume = 9 | numero = | pagine = 236 | mese = | anno = 2012 | doi = 10.1186/1743-422X-9-236 | id = PMID 23062147 }}</ref> |
||
Inoltre, in 353 oranghi sani [[Borneo]] ([[Pongo pygmaeus]]) nell'isola [[Kalimantan]] in [[Indonesia]], nel periodo dal dicembre 2005 al dicembre 2006, si è trovata una posività sierologica pari al 18,4% (65/353) e al 1,7% (6/353) dei campioni esaminati rispettivamente per EBOV (Ebola) e MARV (Marburg). La maggior parte dei sieri EBOV-positivi ha mostrato una somiglianza sierologica per i ceppi trovati in [[Zaire]], [[Sudan]], [[Costa d'Avorio]], o per i virus Bundibugyo, che sono stati trovati finora solo in Africa. Gli autori della ricerca suggeriscono l'esistenza di molteplici specie di filovirus, o di virus sconosciuti correlati ai filovirus, in [[Indonesia]], alcuni dei quali sono sierologicamente simili ai virus EBOV africani, indicando così una possibile presenza di serbatoi di virus non ancora identificati tra le popolazioni di orango indonesiane.<ref name="Nidom-2012">{{Cita pubblicazione | cognome = Nidom | nome = CA. | coauthors = E. Nakayama; RV. Nidom; MY. Alamudi; S. Daulay; IN. Dharmayanti; YP. Dachlan; M. Amin; M. Igarashi; H. Miyamoto; R. Yoshida | titolo = Serological evidence of Ebola virus infection in Indonesian orangutans. | rivista = PLoS One | volume = 7 | numero = 7 | pagine = e40740 | mese = | anno = 2012 | doi = 10.1371/journal.pone.0040740 | id = PMID 22815803 }}</ref> |
|||
== Ceppi virali == |
== Ceppi virali == |
||
Versione delle 10:58, 13 apr 2014
| Ebola virus | |
|---|---|
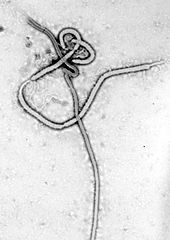 Fotografia al microscopio elettronico della struttura del filovirus. I filamenti hanno un diametro di 60 - 80 nm | |
| Stato di conservazione | |
| Classificazione dei virus | |
| Dominio | Acytota |
| Gruppo | Gruppo V (Virus a RNA) |
| Famiglia | Filoviridae |
| Genere | Filovirus |
L'ebola è un virus appartenente alla famiglia Filoviridae estremamente aggressivo per l'uomo, che causa una febbre emorragica. Il primo ceppo di tale virus fu scoperto nel 1976, nella Repubblica Democratica del Congo (ex Zaire). Finora sono stati isolati quattro ceppi del virus, di cui tre letali per l'uomo. Fin dalla sua scoperta, il virus ebola è stato responsabile di un elevato numero di morti.[1] Verosimilmente il virus viene trasmesso all'uomo tramite contagio animale. Il virus si diffonde tra coloro che sono entrati in contatto con il sangue e i fluidi corporei di soggetti infetti. Considerati l'alto tasso di letalità, la rapidità del decesso, la localizzazione geografica delle infezioni (frequentemente in regioni isolate), il potenziale epidemiologico tuttavia è considerato di basso livello.
L'ebola pare essere un virus zoonotico fra le popolazioni di gorilla di pianura dell'Africa centrale. Nel 2005, tre specie di pipistrelli sono state identificate come portatrici del virus ma, non mostrando i sintomi, sono state ritenute ospiti naturali, o riserve virali.[2]
La febbre emorragica dell'ebola è potenzialmente mortale e comprende una gamma di sintomi quali febbre, vomito, diarrea, dolore o malessere generalizzato e a volte emorragia interna e esterna. Il tasso di mortalità è estremamente alto, variabile dal 50 al 89% secondo il ceppo virale, e un trattamento tramite vaccino non è tuttora disponibile.[3] La causa della morte è solitamente dovuta a shock ipovolemico o sindrome da disfunzione d’organo multipla.
Potenzialmente il virus potrebbe essere utilizzato come arma biologica: come agente di bioterrorismo, il virus è classificato di categoria A.[4] La sua efficacia come agente di guerra biologica tuttavia è compromessa proprio dall'elevata mortalità e dal livello di contagio: un'epidemia tipica potrebbe diffondersi attraverso un piccolo villaggio o ospedale, contagiando l'intera comunità senza poter trovare altri ospiti potenziali, morendo quindi prima di raggiungere una comunità più ampia.
È significativo che nessuno dei ceppi di ebola noti abbia una trasmissibilità di tipo aerea; solo il tipo ebola Reston (dalla città di Reston, Virginia, dove fu identificato in un tipo di scimmia) sembra sia di tipo aereo.
Etimologia
Il virus prende il nome dalla valle dell'Ebola nella Repubblica Democratica del Congo (ex Zaïre), dal sito della prima epidemia scoppiata nel 1976, in un ospedale missionario condotto da suore olandesi.[5]
Virologia
Morfologia

L'indagine al microscopio elettronico di ceppi di ebolavirus mostra la caratteristica struttura filamentosa dei filovirus.[6] Il virus EBOV VP30 è costituito da una catena di 288 amminoacidi.[6] I virioni generalmente hanno una struttura tubolare che può variare nella forma: possono assumere la forma di bastone pastorale, di occhiello, di U o di 6, arrotolata, circolare o ramificata. Tuttavia, le tecniche di laboratorio di purificazione come la centrifugazione potrebbero influenzarne l'aspetto morfologico.[6] I virioni misurano generalmente 80 nm in diametro.[6] Hanno misure variabili, tipicamente attorno ai 1000 nm, ma possono raggiungere i 1400 nm di lunghezza. Nel centro del virione è presente una struttura chiamata nucleocapside, che è costituita dal RNA genomico virale e un complesso proteico NP, VP35, VP30 e L. Il virione ha un diametro di 40-50 nm e un canale centrale di 20–30 nm di diametro. Una glicoproteina (GP) virale è presente sulla membrana virale, derivata dalla membrana cellulare ospite. Tra membrana e nucleocapside, nella cosiddetta matrice, sono allocate le proteine virali VP40 e VP24.
Genoma
Ciascun virione contiene una molecola lineare anti-senso di RNA, di circa 18.959 nucleotidi di lunghezza fino anche a 18.961. L'estremità 3′ non è poliadenilata, e 5′ è priva di cappuccio. È stato accertato che 472 nucleotidi a partire dal 3' UTR, e 731 nucleotidi dal 5' UTR sono sufficienti per la replicazione.[6] È in grado di codificare sette proteine strutturali ed una non strutturale. La regione codificante è 3′ - leader - NP - VP35 - VP40 - GP/sGP - VP30 - VP24 - L - trailer - 5′; leader e trailer essendo regioni non trascritte trasportano segnali importanti per il controllo della trascrizione, replicazione e assemblaggio del genoma virale nel nuovo virione. Il materiale genomico in sé non è infettivo a causa delle proteine virali, ma all'RNA polimerasi RNA dipendente, sono necessarie per la trascrizione del genoma virale nel mRNA, così come per la replicazione del genoma virale.
Ciclo vitale
- Il virus attacca i recettori dell'ospite mediante il peplomero glicoproteico veicolandosi in vescicole per endocitosi nella cellula ospite.
- Fusione della membrana virale con la membrana vescicolare; il nucleocapside è rilasciato nel citoplasma.
- L'ssRNA anti-senso incapsidato, è usato come stampo per la sintesi (3' - 5') di mRNA poliadenilato, monocistronico.
- Traduzione dell'mRNA nelle proteine virali utilizzando le strutture della cellula ospite.
- Elaborazione post-traduttiva delle proteine virali. Dal clivaggio di GP0 (precursore glicoproteico) derivano GP1 e GP2, che vengono abbondantemente glicosilate. L'assemblaggio di queste due molecole, prima in eterodimeri, e poi in trimeri costituisce la superficie del peplomero. Un precursore glicoproteico di secrezione subisce un clivaggio in SGP e delta peptide, entrambi i quali rilasciati dalla cellula.
- Con l'aumento del livello proteico virale, dalla traduzione si passa alla replicazione. Usando l'RNA anti-senso come stampo, viene sintetizzato un +ssRNA complementare; questo viene usato come stampo ulteriore per la sintesi del nuovo (-) ssRNA genomico, che viene rapidamente incapsidato.
- Il nucleocapside neoformato e le proteine envelope si associano alla membrana plasmatica della cellula ospite; il rilascio dei virioni avviene per gemmazione.
Riserve virali
Nonostante numerosi studi, la riserva naturale di ebolavirus non è ancora stata identificata. Tra il 1976 e il 1998, nessun "ebolavirus" è stato riscontrato nelle 30.000 specie fra mammiferi, uccelli, rettili, anfibi ed artropodi prelevate nelle regioni colpite,[7] fatta eccezione per del materiale genetico ritrovato in sei roditori (Mus setulosus e specie Praomys) e in un toporagno (Sylvisorex ollula) reperito nella Repubblica Centro Africana nel 1998.[8] Ebolavirus furono scoperti in carcasse di gorilla, scimpanzé e gazzelle durante l'epidemia del 2001 e del 2003 (le carcasse erano la fonte dell'epidemia umana iniziale), ma l'elevata mortalità dell'infezione preclude a queste specie la possibilità di tramutarsi in riserva.[7]
Anche piante, artropodi e uccelli sono stati considerati riserve virali; tuttavia, i pipistrelli sono considerati i candidati migliori.[9] Taluni pipistrelli erano noti per risiedere nella fabbrica di cotone nella quale i pazienti indiziati per le epidemie del 1976 e del 1979 lavoravano e che furono inoltre implicati nelle epidemie di Marburg nel 1975 e nel 1980.[7] Tra le 24 specie di piante e le 19 specie di vertebrati inoculati sperimentalmente con ebolavirus, solo nei pipistrelli si è verificata l'infezione.[10] L'assenza di segni clinici in questi pipistrelli è caratteristica delle specie-riserva. Nel 2002-03, un'indagine su 1.030 animali provenienti dal Gabon e dalla Repubblica del Congo che includeva 679 pipistrelli ha identificato RNA proveniente da ebolavirus in 13 di questi (Hyspignathus monstrosus, Epomops franquetti e Myonycteris torquata).[11] I pipistrelli sono anche noti per essere la riserva virale di numerosi virus come nipahvirus, hendravirus e lyssavirus. Di recente[quando?] è stato identificato[senza fonte] uno dei recettori sfruttato dal virus, TIM-1, che sarebbe importante per l'attacco ad alcune cellule epiteliali (possibili via d'ingresso del virus). Sembra che il virus ebola si sia sviluppato in alcune caverne del Kenya.[12].
Nel 2012 è stato scoperto in Cina il primo isolamento da pipistrelli del filovirus ceppo Reston a seguito di esami sierologici condotti in una popolazione di pipistrelli cinesi. Il ceppo Reston ebolavirus, scoperto nelle Filippine, è l'unica specie ebolavirus identificata in Asia fino ad oggi.[13] Inoltre, in 353 oranghi sani Borneo (Pongo pygmaeus) nell'isola Kalimantan in Indonesia, nel periodo dal dicembre 2005 al dicembre 2006, si è trovata una posività sierologica pari al 18,4% (65/353) e al 1,7% (6/353) dei campioni esaminati rispettivamente per EBOV (Ebola) e MARV (Marburg). La maggior parte dei sieri EBOV-positivi ha mostrato una somiglianza sierologica per i ceppi trovati in Zaire, Sudan, Costa d'Avorio, o per i virus Bundibugyo, che sono stati trovati finora solo in Africa. Gli autori della ricerca suggeriscono l'esistenza di molteplici specie di filovirus, o di virus sconosciuti correlati ai filovirus, in Indonesia, alcuni dei quali sono sierologicamente simili ai virus EBOV africani, indicando così una possibile presenza di serbatoi di virus non ancora identificati tra le popolazioni di orango indonesiane.[14]
Ceppi virali
I microbiologi hanno descritto diverse sottospecie di ebola. L'elenco seguente non è esaustivo. Un nuovo ceppo di ebolavirus è stato identificato in Uganda durante un'epidemia e non sembra avere corrispondenze con nessuno delle quattro specie identificate in precedenza dagli studiosi.[15].
Zaïre ebolavirus (ZEBOV)

Questo ceppo virale ha il tasso più elevato di mortalità: oltre il 90%, con una media approssimativa dell'83% in 27 anni. Gli indici di mortalità erano dell'88% nel 1976, 100% nel 1977, 59% nel 1994, 81% nel 1995, 73% nel 1996, 80% nel 2001-2002 e 90% nel 2003.
La prima epidemia è avvenuta il 26 agosto, 1976, a Yambuku, una città a nord dello Zaire. Il primo caso registrato fu un insegnante di 44 anni, Mabalo Lokela, che era di ritorno da un viaggio nel nord dello stato. La sua febbre era altissima e gli fu inizialmente diagnosticata la malaria, quindi gli fu somministrato del chinino. Lokela si recava in ospedale ogni giorno; una settimana dopo i suoi sintomi comprendevano vomito incontrollabile, feci diarroiche miste a sangue, cefalea, vertigini, problemi respiratori. Più tardi cominciò a sanguinare dal naso, dalla bocca e dall'ano. Lokela spirò l'8 settembre del 1976, circa 14 giorni dopo la comparsa dei sintomi. Successivamente, numerosi pazienti mostrarono sintomi analoghi come febbre, cefalea, dolori muscolo-scheletrici, stanchezza, nausea e vertigini fino a mostrare i sintomi finali del primo paziente colpito. Inizialmente si pensò che la diffusione virale fosse dovuta all'uso ripetuto degli aghi non sterili utilizzati per Lokela. Successivamente si pensò anche allo scarso rispetto dei protocolli di sicurezza nell'assistenza dei pazienti colpiti da malattie infettive e ai riti funebri tradizionali che prevedono, prima della sepoltura, il lavaggio del tratto gastrointestinale. Due infermiere che lavoravano a Yambuku morirono nella medesima epidemia.[16] Tale variante del virus sembra quella che ha scatenato nella primavera 2014 la nuova epidemia in Guinea[17]).
Sudan ebolavirus (SEBOV)

Il ceppo Sudan ebolavirus fu il secondo ceppo di ebola scoperto nel 1976. Apparentemente sembrava originarsi tra i lavoratori del cotone della città di Nzara, in Sudan. Il primo caso riportato fu quello di un lavoratore esposto probabilmente ad una riserva virale naturale nell'azienda cotoniera. I ricercatori testarono ogni animale ed insetto per comprovare l'ipotesi, tuttavia nessuno risultò positivo al virus. Il portatore è tuttora sconosciuto. Il secondo caso coinvolse il proprietario di un nightclub a Nzara, Sudan. L'ospedale locale, Maridi, sperimentò un tentativo per curare il paziente che risultò inutile. L'ospedale, comunque, non sostenne alcuna procedura di sicurezza nella disinfezione e sterilizzazione dello strumentario utilizzato sul paziente, facilitando il contagio nel nosocomio. L'epidemia più recente di Sudan ebolavirus è stata nel maggio del 2004. 20 casi di Sudan ebolavirus furono registrati a Yambio, nel Sudan, con cinque decessi. Il Centro per il controllo e prevenzione delle malattie confermò la presenza del virus qualche giorno dopo. I paesi confinanti come l'Uganda e la Repubblica Democratica del Congo hanno incrementato la sorveglianza dei confini per il controllo dell'epidemia. Il tasso di mortalità per il Sudan ebolavirus è stato del 54% nel 1976, 68% nel 1979 e 53% nel 2000/2001. La media si aggira intorno al 54%.
Reston ebolavirus
Il ceppo Reston ebolavirus è sospettato di essere sia una sottospecie di ebola che un nuovo tipo di filovirus di origine asiatica. Fu scoperto in una specie di macaco nei Laboratori Hazleton (ora Covance) nel 1989. Questa scoperta attrasse significativamente l'attenzione dei media e portò alla pubblicazione del libro The Hot Zone (Area di contagio, di Richard Preston). Nonostante lo stato di pericolosità biologica (livello 4), il ceppo Reston ebolavirus non è patologico per gli esseri umani ed è solo mediamente mortale per le scimmie;[18] la percezione intorno la mortalità del virus venne alterata dal fatto che ci fu una coinfezione di scimmie con il Simian virus(SHFV).[19]
Nel corso della scoperta, sei tecnici che maneggiavano gli animali divennero sieropositivi, uno di loro si tagliò mentre stava praticando una necroscopia sul fegato di una scimmia infetta. Quando il tecnico non si ammalò, gli studiosi conclusero che il virus avesse una bassa patogenicità negli uomini.[20] Altre scimmie colpite dal ceppo Reston ebolavirus furono spedite nuovamente a Reston e ad Alice, nel Texas, nel febbraio 1990. Altri casi di Reston ebolavirus presente in scimmie infette furono scoperti a Siena, nel 1992 e ancora in Texas nel marzo 1996.
Tai ebolavirus o Costa d'Avorio
Questo ceppo di ebola fu inizialmente scoperto tra gli scimpanzé della foresta Tai in Costa d'Avorio. Il 1º novembre, 1994, i cadaveri di due scimpanzé furono trovati nella foresta. L'autopsia mostrò che nel cuore vi era del sangue fluido e marrone, nessun segno evidente sugli organi e, inoltre, anche i polmoni erano ripieni di sangue molto fluido. Studi sui tessuti mostrarono risultati simili ai casi umani riportati durante l'epidemia di ebola nel 1976 avvenuta in Zaïre e in Sudan. Successivamente nel 1994, furono scoperti altri cadaveri di scimpanzé positivi all'ebola esaminati mediante tecniche molecolari. Si suppose che la fonte del contagio fosse la carne infetta di scimmie del tipo Red Colobus, che venivano predate dagli scimpanzé.[21]
Uno degli scienziati che effettuò l'autopsia sugli scimpanzé infetti, contrasse l'ebola e sviluppò sintomi simili alla febbre dengue approssimativamente una settimana dopo l'autopsia; venne così trasportata in Svizzera per effettuare una terapia. Dopo due settimane fu dimessa dall'ospedale e si riprese completamente a distanza di sei settimane dopo l'infezione.
Bundibugyo ebolavirus
Il 24 novembre, 2007, il Ministero Ugandese per la Sanità confermò un'epidemia di ebola nel distretto di Bundibugyo. In seguito, tramite l'esame di campioni effettuati da laboratori statunitensi, dal Centro di Controllo per le Malattie e dall'Organizzazione mondiale della sanità (OMS), si ebbe la conferma della presenza di una nuova specie di ebolavirus. Il 20 febbraio 2008, il Ministero ugandese ufficialmente annunciò la fine dell'epidemia di Bundibugyo con l'ultima persona infettata dimessa l'8 gennaio 2008.[22] Funzionari ugandesi confermarono un totale di 149 casi di questo nuovo ceppo di ebola, responsabile di 37 decessi.[23]
Febbre emorragica dell'ebola
Sintomi
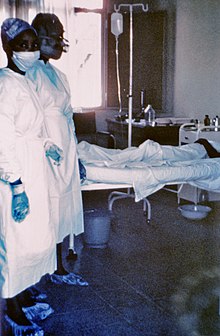
I sintomi sono variabili e compaiono improvvisamente. La sintomatologia iniziale comprende febbre alta (almeno 38,8 °C), cefalea, mialgia, artralgia, dolori addominali, astenia, faringite, nausea e vertigini.[24] Prima che venga presa in considerazione un'epidemia virale, questi sintomi precoci vengono confusi facilmente con le manifestazioni della malaria, della febbre tifoide, della dissenteria, dell'influenza, o di altre molteplici infezioni batteriche, le quali provengono da fonti molto meno letali. L'ebola progressivamente è in grado di causare sintomi di più grave entità, come diarrea, feci scure o sanguinolente, vomito scuro dall'aspetto a "fondo di caffè", occhi rossi dilatati con presenza di aree emorragiche sulla sclera, petecchie, rash maculopapulare e porpora. Altri sintomi secondari includono ipotensione, ipovolemia, tachicardia, danni agli organi (soprattutto a reni, milza e fegato) come risultato di una necrosi sistemica disseminata e proteinuria. L'emorragia interna è causata da una reazione tra il virus e le piastrine che dà luogo a varie rotture nelle pareti dei vasi capillari. Dopo 5–7 giorni l'individuo colpito muore.[senza fonte] Occasionalmente si presentano sanguinamenti interni o emorragie esterne orali e nasali e, in alcuni casi, provenienti dai fori d'accesso degli aghi per siringhe non ancora completamente chiusi. L'ebola virus può influenzare il numero di globuli bianchi e piastrine, innescando fenomeni trombotici.[senza fonte] Più del 50% dei pazienti svilupperà pertanto fenomeni emorragici.[senza fonte] La metodologia diagnostica relativa all'ebola include test urinari e sulla saliva. Il margine di tempo tra l'insorgenza dei sintomi e la morte si aggira intorno ai 7-14 giorni. A partire dalla seconda settimana di infezione, si assiste ad una riduzione dell'iperpiressia o all'innescarsi di una sindrome da disfunzione multiorgano. Il tasso di mortalità è alto, tra il 50 e il 90%.[24] Le cause principali di morte sono lo shock ipovolemico e la MODS (Multiple Organ Dysfunction Syndrome).[25]
La replicazione dei filovirus viene favorita da un'ampia tipologia di organi e strutture cellulari quali gli epatociti, le cellule epiteliali, i fibroblasti, le cellule reticolari e le cellule adrenocorticali.[6] Più in particolare, la sensibilità delle cellule endoteliali è verosimilmente la causa dei sintomi tardivi dell'infezione, come l'emorragia e lo shock ipovolemico.[6]
Diagnosi
L'ebola è diagnosticata tramite test ELISA (Enzyme-Linked ImmunoSorbent Assay). Tuttavia il metodo diagnostico produce risultati ambigui durante le fasi non epidemiche.
Dopo il caso di Reston, il Dr. Carl Johnson del CDC analizzò gli indiani San Blas dell'America Centrale, i quali non avevano nessuna storia di infezioni virali di ebola, ma che mostrarono il 2% di positività. Ulteriori ricerche effettuate sui nativi americani dell'Alaska mostrarono una percentuale di positivi analoga. Per contrastare i falsi positivi un test più complesso basato sul sistema ELISA fu sviluppato da Tom Kzaisek negli USAMRIID che venne in seguito migliorato con l'analisi mediante anticorpi in immunofluorescenza.[32]
Trasmissione
Tra gli esseri umani, il virus viene trasmesso mediante il contatto diretto con i fluidi corporei infetti, oppure, in minor proporzione, per via epidermica o per contatto con le membrane mucose. Il periodo di incubazione può variare dai 2 ai 21 giorni, ma generalmente è di 5–10 giorni.
Sebbene la trasmissione virale per via aerea tra le scimmie sia stata dimostrata nel corso di un'epidemia accidentale verificatasi in laboratori americani situati in Virginia, vi è una scarsa evidenza di trasmissioni aeree da uomo a uomo in ciascuna delle epidemie registrate. L'infermiera Mayinga N'Seka rappresenta un caso isolato. L'occasione in cui contrasse il virus rimane tuttora sconosciuta. Le infezioni di ebolavirus su pazienti umani sono state documentate in casi di contatto con scimpanzé infetti, gorilla e antilopi della foresta, avvenuti in Costa d'Avorio, nella repubblica congolese e in Gabon. Anche la trasmissione virale del tipo ebola Reston è stata registrata a causa del contatto con scimmie cynomolgus (Macaca fascicularis).[24]
Finora, tutte le epidemie di ebola sono avvenute in strutture ospedaliere inadeguate, dove i protocolli di igiene e sterilizzazione sono un lusso o rappresentano pratiche sconosciute al personale, e dove gli aghi monouso e le autoclavi non esistono a causa dei costi eccessivi. Nei moderni ospedali, forniti di strumentario monouso e favoriti dalla conoscenza dei protocolli di base in ambito igienico-sanitario, l'ebola non si è mai manifestato su vasta scala.
Nelle prime fasi l'ebola sembra non essere estremamente contagioso. Il contatto in fase precoce con individui colpiti sembra non causare la malattia. Come la malattia progredisce, i fluidi corporei presenti nella diarrea, nel vomito e nel sangue rappresentano un rischio biologico estremo. A causa della carenza di strumentario appropriato e di protocolli igienico-sanitari, le epidemie su vasta scala scoppiano nelle aree più povere ed isolate prive di ospedali moderni e di personale addestrato. Molte delle aree dove persistono le riserve virali hanno queste caratteristiche. In alcuni ambienti basterebbe cessare la condivisione degli aghi o il loro riutilizzo senza le adeguate procedure di sterilizzazione, isolare i pazienti e osservare rigidamente le procedure infermieristiche che prevedono l'uso di mascherine, guanti, occhiali e camici monouso. Procedure igieniche, queste, che dovrebbero obbligatoriamente essere fatte osservare a tutto il personale medico e a chiunque abbia a che fare con il paziente.
È piuttosto improbabile che l'ebola possa svilupparsi con caratteristiche pandemiche a livello mondiale, per via della sua difficoltà a diffondersi per via aerea e a causa del lasso di tempo in cui il virus assume caratteristiche contagiose atte alla diffusione, in comparazione con altre malattie infettive. In situazioni di isolamento come nelle aree ospedaliere di quarantena o nei villaggi remoti, la maggior parte delle vittime vengono infettate rapidamente a seguito della presenza del primo caso infettivo. Inoltre, l'instaurarsi di sintomi precoci dal momento in cui la malattia diviene contagiosa rende remota l'eventualità che un individuo colpito sia in grado di effettuare viaggi permettendo lo spostamento del contagio. Poiché i cadaveri sono infetti, alcuni medici adottano misure preventive affinché le sepolture avvengano in sicurezza contrariamente ai rituali funebri tradizionali diffusi in quelle aree.[26]
Terapia

Non esiste un protocollo standardizzato di trattamento per la febbre emorragica da ebolavirus. La terapia primaria è unicamente di supporto e comprende procedure invasive ridotte al minimo: bilancio degli elettroliti, poiché i pazienti sono frequentemente disidratati, ripristino dei fattori di coagulazione per arrestare il sanguinamento, mantenimento dei parametri ematici e di ossigenazione, trattamento delle complicanze infettive. Il plasma dei convalescenti (coloro che sono sopravvissuti all'infezione di ebola) sembra essere promettente come terapia. [senza fonte]. La Ribavirina è inefficace. Anche l'Interferone non pare dare risultati. Nelle scimmie, la somministrazione di un inibitore dell'emocoagulazione (rNAPc2) ha mostrato qualche beneficio, preservando il 33% degli animali infettati da una infezione al 100% letale per le scimmie (sfortunatamente, questa terapia è inefficace sugli umani). Agli inizi del 2006, studiosi dell'USAMRIID (Istituto statunitense di ricerche mediche sulle malattie infettive dell'esercito) annunciarono il 75% delle guarigioni in scimmie rhesus infettate con ebolavirus a cui era stata somministrata terapia antisenso.[27]
Il 7 aprile 2014 un gruppo di ricerca dell' Istituto di Biologia molecolare della Facoltà di Medicina dell'Università di Hannover in Germania, pubblica uno studio dove suggerisce l'uso dei farmaci: amiodarone, dronedarone e verapamil come possibili bloccanti l'ingresso del virus nella cellula umana. Infatti, l'amiodarone è un inibitore dei canali multi-ionici e anche un antagonista adrenergico, mostrando per questo di essere un potente inibitore dell'ingresso nella cellula dei filovirus a concentrazioni che sono regolarmente raggiungibili nel siero umano durante la somministrazione con farmaci farmaci antiaritmici. L'amiodarone agirebbe anche sugli arenavirus come il virus Guanarito. Un meccanismo simile è stato ipotizzato anche per il verapamil e il dronedarone.[28]
Vaccini
Sono stati prodotti vaccini sia per l'ebola[29] che per il Marburg virus[30] che al 99% sono risultati efficaci nella riduzione degli effetti dell'infezione virale nelle scimmie. Questi vaccini sono derivati da DNA ricombinante, virus della stomatite vescicolare o da Adenovirus ricombinante[31] che trasportano le proteine virali sulla loro superficie. Recenti sperimentazioni nella produzione di vaccini umani, come quello del NIAID nel 2003, non hanno sortito alcun successo.[32] Il problema maggiore con i vaccini è che fintanto che la somministrazione avviene nel corso dell'esordio sintomatologico (1-4 giorni dopo la manifestazione), la compromissione organica sarà sempre troppo avanzata affinché possa avvenire una guarigione: la rottura di arterie e capillari e altri sintomi potrebbero causare danni mortali o traumatizzare seriamente il paziente.
Epidemie recenti

Focolai del 1976
Focolai dal 1977 al 2012
Focolai del 2014
Il 30 agosto 2007, 103 individui (100 adulti e 3 bambini) furono infettati da una sospetta febbre emorragica nel villaggio di Kampungu, nella Repubblica Democratica del Congo. L'epidemia scoppiò dopo i funerali di due capo-villaggio e 217 individui di 4 villaggi si ammalarono. L'OMS inviò un team per prelevare campioni ematici da analizzare e in seguito confermò che molti dei casi erano il risultato di un contagio di ebolavirus.[33] La più vasta epidemia congolese uccise 245 individui nel 1995 a Kikwit, ad appena 200 miglia dalla fonte epidemica dell'agosto del 2007.[34].
Il 30 novembre 2007, il Ministro della Sanità ugandese confermò un'epidemia di ebola nel distretto di Bundibugyo. A seguito della conferma sui campioni testati dai Laboratori Nazionali Statunitensi e dal Centro di Controllo per le Malattie, l'OMS confermò la presenza di una nuova specie di ebolavirus.[35] L'epidemia cessò ufficialmente il 20 febbraio 2008. Finché durò, furono registrati 149 casi di questo nuovo ceppo, 37 dei quali morirono.
Un caso registrato di ebola è stato comunicato ufficialmente dal Ministero della Salute Ugandese il 28 luglio 2012. Colpite 20 persone di cui 14 decedute (alla data 31 luglio). Si è sviluppato a Kibaale. Nove dei deceduti erano familiari entrati in contatto diretto con i malati durante la malattia (inizialmente non identificata come ebola) o durante la sepoltura. Gli altri colpiti sono stati il personale sanitario e pochi altri poi monitorati.
Nel settembre 2012, il portavoce dell'Organizzazione mondiale della sanità a Kinshasa, Eugene Kabambi, ufficializza la notizia di un'epidemia fuori controllo nella Repubblica Democratica del Congo. Nel giorno 13 del mese, i morti sono già 31.[36]
Il 22 marzo 2014 è confermata la notizia di una epidemia di ebola in Guinea[37], che ha in brevissimo tempo raggiunto la capitale Conakry[38]; la gravità e l'estensione del contagio ha indotto l'Europa prima (che ha inviato anche un team di specialisti dell'Istituto per le malattie infettive Spallanzani di Roma[39])[40] e poi gli Stati Uniti (che hanno inviato un team di specialisti dell'Istituto malattie infettive di Atlanta-Georgia[41]) a intervenire per arginare l'infezione. Medici senza frontiere parla di "epidemia senza precedenti", tale da suscitare timori di possibile diffusione al di fuori dell'Africa[42]. L'analisi genetica del virus indica che è più strettamente correlato (98% match) al virus Ebola (specie Zaire ebolavirus ) ultimo registrato nel 2009 nella Repubblica Democratica del Congo[43].
Bioterrorismo
L'alta mortalità e la scarsità di vaccini e terapie adeguate, classificano l'ebola come un agente di rischio biologico di livello 4, così come agente bioterroristico di categoria A[44].
Come arma terroristica, l'ebola è stato preso in considerazione dai membri della setta giapponese Aum Shinrikyo, il cui leader, Shoko Asahara, inviò circa 40 membri in Zaire nel 1992 i quali si finsero di supporto medico alle vittime dell'ebola, presumibilmente nel tentativo di acquisire un campione virale.[45]
Utilizzo in prodotti della cultura di massa
I virus di ebola e marburg sono stati una generosa fonte di idee e soggetti per spettacoli e opere di vario genere della cultura di massa e nella narrativa di genere. Il fascino per il virus è dovuto probabilmente all'alto tasso di mortalità fra i soggetti colpiti, alla sua natura misteriosa e alla sua tendenza a provocare raccapriccianti perdite di sangue dagli orifizi corporei. Infatti questo virus ha acquisito anche una discreta popolarità, specialmente in Europa, tra gli amanti del genere cinematografico denominato gore.
Cinema
Nel film Virus letale, il virus protagonista, il fittizio "Motaba" descritto dalla pellicola, è strettamente ispirato al virus africano.[46] Anche i sintomi e l'area dell'infezione sono pertinenti.
Esistono quattro film che trattano di un'epidemia del Virus ebola:
- Virus letale (Outbreak) (1995)
- Ebola: Area di contagio (Virus) (1995) Film TV
- Yi boh laai beng duk (1996)
- Plague Fighters (1996) Film TV
In Resident Evil, il Virus T è una versione modificata del Virus Progenitore, creato modificando geneticamente il virus ebola.[47] Anche Tomb Raider: La culla della vita rappresenta un'arma biologica[48] che consiste in una forma di ebola molto potenziata, capace di provocare la morte in pochi minuti.
Parossismi ed esagerazioni nella rappresentazione cinematografica
Molte rappresentazioni del virus di ebola nella narrativa e nei media sono considerate esagerate o mitizzanti.[senza fonte] Una diffusa leggenda vuole che il virus uccida così in fretta da avere poco tempo per diffondersi. Le vittime muoiono molto presto dopo il contatto con l'agente infettivo. In realtà, il tempo di incubazione è di circa una settimana. L'intervallo medio fra la comparsa dei primi sintomi e la morte varia dai 3 ai 21 giorni, con una media di 10,1. Sebbene ciò ostacoli la propagazione in massa, è un tempo già abbastanza lungo perché alcune persone contraggano la malattia.
Un altro mito vuole che il virus faccia sciogliere, liquefare o sanguinare copiosamente i pazienti. In rappresentazioni di questo tipo, le vittime dell'ebola presentano sangue che spruzza, carni in liquefazione, volto da zombi e drammatici conati con espulsione di vomito ematico, che fuoriesce a volte anche dai corpi appena deceduti. Nei fatti, solo una parte delle vittime dell'ebola presenta sanguinamento copioso, e la maggior parte dei resoconti sul corso della malattia descrivono pazienti ottusi e letargici. Circa il 10% dei pazienti soffre di qualche emorragia, ma è generalmente interna o lieve, come il sanguinamento delle gengive. I sintomi dell'ebola sono generalmente limitati ad estrema spossatezza, vomito, diarrea, dolori addominali, febbre alta, cefalea e altri dolori.
Quello che segue è l'estratto di un'intervista al primario epidemiologo Philippe Calain, del Centro di controllo e prevenzione malattie, reparto agenti patogeni speciali, di Kikwit (1996):
«At the end of the disease the patient does not look, from the outside, as horrible as you can read in some books. They are not melting. They are not full of blood. They're in shock, muscular shock. They are not unconscious, but you would say 'obtunded', dull, quiet, very tired. Very few were hemorrhaging. Hemorrhage is not the main symptom. Less than half of the patients had some kind of hemorrhage. But the ones that had bled, died.»
«Nell'ultima fase della malattia i pazienti non appaiono, dall'esterno, orripilanti come si legge in certi libri. Non si sciolgono. Non sono pieni di sangue. Sono in stato di shock: shock muscolare. Non sono incoscienti, ma si potrebbero definire "ottusi", fiacchi, apatici, stremati. Pochissimi perdono sangue. L'emorragia non è il sintomo principale. Meno della metà dei pazienti ha qualche tipo di sanguinamento. Ma quelli che hanno perso sangue, sono morti.»
Narrativa di genere
Nel romanzo Contagio di Robin Cook, il virus ebola è usato come una possibile arma, con intento criminale.
Nel romanzo Nel Bianco di Ken Follett, una variante del virus ebola, dal nome Madoba-2, viene rubata, con intento criminale, da un laboratorio di ricerca in Scozia.
La guerra biologica con virus di ebola modificati, trasportati per via aerea, è stata un tema centrale nei romanzi di Tom Clancy Potere esecutivo e Rainbow Six. In quest'ultimo l'autore inserisce una variante più aggressiva del virus ebola denominato "Shiva" creato artificialmente in laboratorio ed in grado di diffondersi per via aerea.
Il virus Reston è il soggetto del libro di Richard Preston, Area di contagio. Ha anche portato allo sviluppo del film Outbreak (1995).
Note
- ^ Ebola Cases and Outbreaks - CDC Special Pathogens Branch, su cdc.gov, Centers for Disease Control and Prevention. URL consultato l'8 dicembre 2007.
- ^ X. Pourrut, A. Délicat, PE Rollin, TG Ksiazek, J-P Gonzalez, EM Leroy (2007) "Spatial and temporal patterns of Zaire ebolavirus antibody prevalence in the possible reservoir bat species" Journal of Infectious Diseases 196: 176–183.
- ^ Rouquet P, Froment JM, Bermejo M, et al, Wild animal mortality monitoring and human Ebola outbreaks, Gabon and Republic of Congo, 2001-2003, in Emerging Infect. Dis., vol. 11, n. 2, 2005, pp. 283–90, PMID 15752448.
- ^ Borio L, Inglesby T, Peters CJ, et al, Hemorrhagic fever viruses as biological weapons: medical and public health management, in JAMA, vol. 287, n. 18, 2002, pp. 2391–405, PMID 11988060.
- ^ Jason Socrates Bardi, Death Called a River, in Scribbs Research Institute, vol. 2, n. 1, 2002. URL consultato l'8 dicembre 2006.
- ^ a b c d e f g Hans-Dieter Klenk, Feldmann, Heinz, Ebola and Marburg Viruses, Molecular and Cellular Biology, Wymondham, Norfolk, Horizon Bioscience, 2004, ISBN 0-9545232-3-7.
- ^ a b c Pourrut X, Kumulungui B, Wittmann T, et al, The natural history of Ebola virus in Africa, in Microbes Infect., vol. 7, n. 7-8, 2005, pp. 1005–14, DOI:10.1016/j.micinf.2005.04.006, PMID 16002313.
- ^ Morvan JM, Deubel V, Gounon P, et al, Identification of Ebola virus sequences present as RNA or DNA in organs of terrestrial small mammals of the Central African Republic, in Microbes Infect., vol. 1, n. 14, 1999, pp. 1193–201, DOI:10.1016/S1286-4579(99)00242-7, PMID 10580275.
- ^ Fruit bats may carry Ebola virus, in BBC News, 11 dicembre 2005. URL consultato il 25 febbraio 2008.
- ^ Swanepoel R, Leman PA, Burt FJ,et al, Experimental inoculation of plants and animals with Ebola virus, in Emerging Infect. Dis., vol. 2, n. 4, 1996, pp. 321–5, PMID 8969248.
- ^ Leroy EM, Kumulungui B, Pourrut X, et al, Fruit bats as reservoirs of Ebola virus, in Nature, vol. 438, n. 7068, 2005, pp. 575–6, DOI:10.1038/438575a, PMID 16319873.
- ^ Focus n.223, maggio 2011, p.116
- ^ J. Yuan, Serological evidence of ebolavirus infection in bats, China., in Virol J, vol. 9, 2012, p. 236, DOI:10.1186/1743-422X-9-236, PMID 23062147.
- ^ CA. Nidom, Serological evidence of Ebola virus infection in Indonesian orangutans., in PLoS One, vol. 7, n. 7, 2012, pp. e40740, DOI:10.1371/journal.pone.0040740, PMID 22815803.
- ^ New subtype of Ebola suspected in Uganda, in USA Today, 30 novembre 2007. URL consultato il 25 febbraio 2008.
- ^ Margaretha Isaacson, et al., Two Belgian nurses died of Ebola.
- ^ http://www.cdc.gov/vhf/ebola/outbreaks/guinea/
- ^ Level 4: Virus Hunters of the CDC (1999), p.300. Quotation: "Mentre è vero che dovremmo essere molto confortati dal fatto che il virus di Reston non è patologico per l'uomo - non fa ammalare nessuno - c'è ancora la minaccia di un ulteriore ceppo nelle scimmie importato da chissà dove, che potrebbe essere dannoso per l'uomo."
- ^ Level 4: Virus Hunters of the CDC (1999), ppgs.307-309.
- ^ Level 4: Virus Hunters of the CDC (1999), ppgs.298-299.
- ^ Ebola Cote d'Ivoire Outbreaks
- ^ End of Ebola outbreak in Uganda, su who.int, World Health Organization, 20 febbraio 2008.
- ^ Tim Cocks, Uganda confirms 113 suspected Ebola cases, Reuters, 11 dicembre 2007. URL consultato il 25 febbraio 2008.
- ^ a b c WHO Fact Sheet Ebola haemorrhagic fever
- ^ Bray M, Geisbert TW, Ebola virus: the role of macrophages and dendritic cells in the pathogenesis of Ebola hemorrhagic fever, in Int. J. Biochem. Cell Biol., vol. 37, n. 8, 2005, pp. 1560–6, DOI:10.1016/j.biocel.2005.02.018, PMID 15896665.
- ^ Blaine Harden, Dr. Matthew's Passion, in New York Times Magazine, 18 febbraio 2001. URL consultato il 25 febbraio 2008.
- ^ USAMRIID press release (PDF), su usamriid.army.mil.
- ^ G. Gehring, The clinically approved drugs amiodarone, dronedarone and verapamil inhibit filovirus cell entry., in J Antimicrob Chemother, Apr 2014, DOI:10.1093/jac/dku091, PMID 24710028.
- ^ Jones SM, Feldmann H, Ströher U, et al, Live attenuated recombinant vaccine protects nonhuman primates against Ebola and Marburg viruses, in Nat. Med., vol. 11, n. 7, 2005, pp. 786–90, DOI:10.1038/nm1258, PMID 15937495.
- ^ Hevey M, Negley D, Pushko P, Smith J, Schmaljohn A, Marburg virus vaccines based upon alphavirus replicons protect guinea pigs and nonhuman primates, in Virology, vol. 251, n. 1, 1998, pp. 28–37, DOI:10.1006/viro.1998.9367, PMID 9813200.
- ^ Sullivan NJ, Geisbert TW, Geisbert JB, et al, Accelerated vaccination for Ebola virus haemorrhagic fever in non-human primates, in Nature, vol. 424, n. 6949, 2003, pp. 681–4, DOI:10.1038/nature01876, PMID 12904795.
- ^ NIAID Ebola Vaccine Enters Human Trial, su www3.niaid.nih.gov, National Institute of Allergy and Infectious Diseases, 18 novembre 2003.
- ^ Ebola Outbreak Confirmed in Congo, in NewScientist.com, 11 settembre 2007. URL consultato il 25 febbraio 2008.
- ^ Mystery DR Congo fever kills 100, in BBC News, 31 agosto 2007. URL consultato il 25 febbraio 2008.
- ^ Uganda: Deadly Ebola Outbreak Confirmed - UN, in UN News Service, 30 novembre 2007. URL consultato il 25 febbraio 2008.
- ^ Ebola fuori controllo in Congo, 31 morti, in ANSA, 13 settembre 2012.
- ^ http://www.repubblica.it/solidarieta/emergenza/2014/03/22/news/epidemia_di_ebola_in_guinea_34_morti_in_un_mese_l_esperto_europa_non_rischia-81642127/
- ^ http://notizie.virgilio.it/notizie/esteri/2014/03_marzo/23/guinea_virus_ebola_raggiunge_capitale,42149718.html
- ^ quotidiano "la stampa"-->esteri- 27/03/2014
- ^ la missione dello European Mobile Laboratory gestirà due laboratori di alta sicurezza per la diagnosi della malattia; del team, che è arrivato in Guinea il 27.03.2014, faranno parte, oltre ai ricercatori italiani, anche personale del Bernhard-Nocht Institute di Amburgo e dell’Institut Pasteur di Lione, a cui si aggiungeranno esperti britannici, in collaborazione con le autorità locali e con l’organizzazione Medici Senza Frontiere, che ha circa 30 esperti nella zona
- ^ http://www.cdc.gov/vhf/ebola/outbreaks/guinea/
- ^ http://www.theguardian.com/world/2014/mar/31/guinea-ebola-epidemic-medecins-sans-frontieres
- ^ http://www.cdc.gov/vhf/ebola/outbreaks/guinea/
- ^ Hoenen T, Groseth A, Falzarano D, Feldmann H, Ebola virus: unravelling pathogenesis to combat a deadly disease, in Trends Mol Med, vol. 12, n. 5, 2006, pp. 206–15, DOI:10.1016/j.molmed.2006.03.006, PMID 16616875.
- ^ Chronology of Aum Shinrikyo's CBW Activities (PDF), Monterey Institute for International Studies.
- ^ Articolo su Corriere della Sera.it
- ^ Capcom.co.jp "Wesker's Report II", su www3.capcom.co.jp. URL consultato il 12 aprile 2008.
- ^ (EN) Lara Croft Tomb Raider: The Cradle of Life su jesusfreakhideout.com
Bibliografia
- Joseph B. McCormick M.D., Fisher-Hoch M.D., Susan, Level 4: Virus Hunters of the CDC, Horvitz, Leslie Alan, "Updated edition" 3rd, Barnes & Noble, 1999 [1996], ISBN 978-0-7607-1208-5.
- Richard Preston, The Hot Zone, A Terrifying True Story, Anchor Books (Random House), Sagebrush Education Resources, Tandem Library Books, 20 luglio 1995 [1994], ISBN 0-385-47956-5.
- Tara Waterman, Ebola Reston Outbreak Standford Honors Thesis, su stanford.edu, Stanford University, 1999. URL consultato il 2 agosto 2008.
Altri progetti
 Wikimedia Commons contiene immagini o altri file su Ebolavirus
Wikimedia Commons contiene immagini o altri file su Ebolavirus Wikispecies contiene informazioni su Ebolavirus
Wikispecies contiene informazioni su Ebolavirus
Collegamenti esterni
- Febbre emorragica Ebola - Istituto Superiore di sanità (EpiCentro)
- Template:Thesaurus BNCF
Fonti
- Database entry on genus Ebolavirus - ICTVdB
- Ebola Virus Haemorrhagic Fever - Proceedings of an International Colloquium on Ebola Virus Infection and Other Haemorrhagic Fevers held in Antwerp, Belgium, 6-8 December, 1977
- Questions and Answers about Ebola Hemorrhagic Fever - Center for Disease Control (CDC), retrieved 10 July 2006
- WHO Factsheet - retrieved 10 July 2006
- Template:ECDC
- Vaccine Research Center (VRC) - Informazioni relative alle ricerche per un vaccino sull'Ebola
- www.healthocrates.com - Articolo sulla febbre emorragica dell'Ebola
Epidemie
- Ebola outbreak in Congo, CBC News, 12 settembre 2007.
- Ebola 'kills over 5,000 gorillas', BBC News, 8 dicembre 2006.
- History of Ebola Outbreaks - Centers for Disease Control Special Pathogens Branch, retrieved 2006-07-10.
- Infection Control for Viral Hemorrhagic Fevers in the African Health Care Setting - Center for Disease Control and Prevention, Atlanta, December 1998.
- Filovirus Global Symposium - Filomeeting 2008
Ciclo vitale
- Biomarker Database - informazioni sull'Ebola
Contagiosità
- U.S. Army Medical Research Institute of Infectious Diseases: Gene-Specific Ebola Therapies Protect Nonhuman Primates from Lethal Disease
- Jaax NK, Davis KJ, Geisbert TJ, et al, Lethal experimental infection of rhesus monkeys with Ebola-Zaire (Mayinga) virus by the oral and conjunctival route of exposure, in Arch. Pathol. Lab. Med., vol. 120, n. 2, 1996, pp. 140–55, PMID 8712894.
- Johnson E, Jaax N, White J, Jahrling P, Lethal experimental infections of rhesus monkeys by aerosolized Ebola virus, in Int J Exp Pathol, vol. 76, n. 4, 1995, pp. 227–36, PMID 7547435.
- Leffel EK, Reed DS, Marburg and Ebola viruses as aerosol threats, in Biosecur Bioterror, vol. 2, n. 3, 2004, pp. 186–91, PMID 15588056.
- Salvaggio MR, Baddley JW, Other viral bioweapons: Ebola and Marburg hemorrhagic fever, in Dermatol Clin, vol. 22, n. 3, 2004, pp. 291–302, vi, DOI:10.1016/j.det.2004.03.003, PMID 15207310.
- Jaax N, Jahrling P, Geisbert T, et al, Transmission of Ebola virus (Zaire strain) to uninfected control monkeys in a biocontainment laboratory, in Lancet, vol. 346, n. 8991-8992, 1995, pp. 1669–71, PMID 8551825.
- What is the probability of a dangerous strain of Ebola mutating and becoming airborne? Brett Russel, retrieved 2006-07-10.

