Superossido di potassio
| Superossido di potassio | |
|---|---|
 | |
| Caratteristiche generali | |
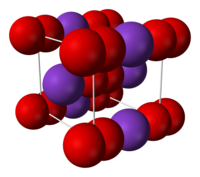
| Formula bruta o molecolare | KO2 |
| Massa molecolare (u) | 71,10 g/mol |
| Aspetto | solido giallo |
| Numero CAS | |
| Numero EINECS | 234-746-5 |
| PubChem | 61541 |
| SMILES | [O-]=O.[K+] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,14 g/cm3 |
| Temperatura di fusione | 425 °C decomposizione |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 271 - 314 |
| Consigli P | 220 - 280 - 305+351+338 - 310 [1] |
Il superossido di potassio è il composto chimico con formula KO2. Questo raro sale dello ione superossido è prodotto dalla combustione del potassio fuso in puro ossigeno. Il superossido di potassio è usato come agente ossidante nell'industria chimica.
L'Agenzia Spaziale Russa ha avuto successo nell'usare il superossido di potassio nei generatori chimici di ossigeno per le tute spaziali ed il velivolo spaziale Sojuz. KO2 è stato anche utilizzato nelle bombole dei respiratori per i vigili del fuoco nelle operazioni di salvataggio nelle miniere, ma ha avuto uso limitato nei respiratori scuba per il pericolo di reazioni esplosive con l'acqua. La capacità teorica del KO2 è l'assorbimento di 0,309 kg di CO2 per kg di assorbente, mentre 0,45 kg di O2 sono generati per ogni kg di assorbente. Il corpo umano però produce più CO2 dell'ossigeno assorbito, così può rivelarsi necessario un dispositivo o assorbente specificamente per il CO2.
Pericoli[modifica | modifica wikitesto]
Il superossido di potassio è un potente ossidante, e può produrre reazioni esplosive quando combinato con una varietà di sostanze, compresa l'acqua, acidi, sostanze organiche o grafite in polvere. Anche il superossido secco può produrre un composto esplosivo sensibile agli urti in combinazione con sostanze come cherosene, e oli minerali.[2] Nel 1999 presso l'Oak Ridge National Laboratory, un'esplosione fu causata dall'impatto di uno strumento metallico su una miscela sensibile agli urti di superossido di potassio (KO2) e olio minerale. [3]
Note[modifica | modifica wikitesto]
- ^ scheda del superossido di potassio su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ Aerojet Nuclear Company (1975), "An Explosives Hazards Analysis of the Eutectic Solution of NaK and KO2". Idaho National Engineering Laboratory..
- ^ U.S. Department of Energy, Y-12 NaK Accident Investigation, su hss.energy.gov, February 2000 (archiviato dall'url originale il 28 maggio 2010).
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Superossido di potassio
Wikimedia Commons contiene immagini o altri file su Superossido di potassio
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) potassium superoxide, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.