Storia della pandemia di AIDS
| Storia della pandemia di AIDS epidemia | |
|---|---|
 | |
| Patologia | AIDS |
| Origine | |
| Periodo | 1981[1] - in corso |
| Dati statistici globali[2] | |
| Numero di casi | 37,9 milioni (2018) |
| Numero di morti | 32 milioni (2018[3]) |

La storia della diffusione dell'AIDS su scala pandemica (o "epidemia globale")[4] viene solitamente fatta incominciare nel 1981, quando fu riconosciuta l'esistenza di una nuova malattia in alcuni pazienti negli Stati Uniti: in realtà l'infezione esisteva già da molti anni, ma era stata sempre scambiata per altro.
Diffusasi in maniera esponenziale in tutto il mondo, diventando una vera e propria pandemia,[5][6][7][8][9] a differenza di tutte le altre epidemie fino ad allora conosciute, fu a lungo mortale in percentuali vicine al 100% dei casi diagnosticati (pur nella variabilità dei tempi di sviluppo dei sintomi). Inoltre, la connessione presto dimostrata con la sfera sessuale e con l'uso di sostanze stupefacenti (eroina) legò indissolubilmente il contagio, nell'opinione generale, a comportamenti stigmatizzabili, in quanto "trasgressivi": la sieropositività è ancora oggi vissuta come una condizione potenzialmente discriminatoria, che talvolta ha anche richiesto specifici interventi legislativi.[10]
Dal 1996 una combinazione di farmaci riesce a "immobilizzare" il virus negli individui, bloccando lo sviluppo della sindrome immunodepressiva, ma non a eradicarlo, cronicizzando quindi l'infezione. Tutt'altro che debellata, la sindrome da HIV è diventata endemica nei paesi sviluppati, dove è crollato il numero di decessi, ma non quello dei contagi, mentre è ancora uno dei più gravi fattori di mortalità nei paesi in via di sviluppo, all'origine di gravi problematiche sociali, etiche, economiche e organizzative.
Origini[modifica | modifica wikitesto]
L'esistenza di virus che inducono uno stato di progressiva immunodeficienza è documentata in natura in varie specie animali, tra i quali sono più noti il FIV (Feline Immunodeficiency Virus), legato ai felini e in particolare al gatto, e il SIV (Simian Immunodeficiency Virus), legato a varie specie di scimmie.[10]
Passaggio di specie[modifica | modifica wikitesto]

È ormai accertato che il virus umano dell'HIV (Human Immunodeficiency Virus) derivi da mutazioni di vari ceppi del SIV, con il salto di specie in un'epoca imprecisata in alcune regioni dell'Africa occidentale sub-sahariana.[10] I primi studi degli anni ottanta indicavano come possibile zona d'origine del contagio la zona dei grandi laghi,[11] mentre gli studi più moderni propendono per un'area più a ovest, nel Camerun. Dal virus SIVcpz dello scimpanzé Pan troglodytes troglodytes deriverebbe il ceppo HIV-1, responsabile dell'attuale pandemia, mentre dal virus SIVsmm, che colpisce le scimmie Sooty Mangabey, deriverebbe il ceppo HIV-2, dotato di patogenicità e contagiosità più limitate, che è rimasto confinato nei luoghi di origine, con l'eccezione di alcuni soggetti infettati nelle proprie aree endemiche e poi trasferitisi in paesi occidentali.
La trasmissione uomo/scimmia dovette avvenire tramite il contatto tra liquidi biologici (ad esempio morso).[12] Vi sono prove che gli esseri umani che partecipano ad attività di caccia e di vendita di carne e pelli di scimmia abbiano contratto il SIV ("teoria del cacciatore");[13] tuttavia, solo alcune di queste infezioni sono state in grado di causare epidemie nell'uomo, e tutte si sono verificate tra la fine del XIX secolo e l'inizio del XX secolo.
Il primo caso di sieropositività accertato risale al 1959, quando venne prelevato da un uomo di Leopoldville (oggi Kinshasa) un campione di sangue che, analizzato trent'anni dopo, dimostrò di contenere anticorpi all'HIV-1.[14] All'anno successivo appartiene un campione di tessuti di linfonodi di una donna della stessa città, pure infettato dal virus.[15]
Non è chiaro perché pratiche di caccia e macellazione in atto da secoli abbiano prodotto un'epidemia che si è sviluppata documentatamente solo sul finire degli anni cinquanta, magari facilitata dal crearsi di più stretti contatti ambientali tra uomo e scimmia, a seguito della progressiva coltivazione della savana.[16] Agli inizi degli anni novanta fu proposta una teoria del vaccino orale antipolio sull'origine dell'AIDS, ma rimasta sempre in ambito speculativo e che non ha mai ricevuto conferme né un significativo consenso in ambito scientifico.
Diversi laboratori di microbiologia (fra cui il Los Alamos National Laboratory) hanno effettuato confronti filogenetici e datazioni della sequenza "progenitrice" del gruppo principale dell'HIV-1 (HIV-1 Gruppo M), concludendo tutte che l'introduzione dell'HIV-1 nell'uomo è avvenuta nella prima metà del XX secolo (1915-1941 circa o, secondo altri studi del 2008, entro il 1908-1930).[17][18][19][20] Nel 1931 è infatti individuabile una prima descrizione dei sintomi della sindrome dell'immunodeficienza umana acquisita, sebbene non riconosciuta come tale e classificata come degenerazione o complicazione di malattie note.[12] Nel 2014, una ricerca sulla genesi e la storia iniziale dell'epidemia di AIDS condotta da un gruppo internazionale di virologi, genetisti e biologi, diretti da Oliver G. Pybus, dell'università di Oxford, e da Philippe Lemey, dell'università di Lovanio, ha stabilito che la prima infezione potrebbe essere avvenuta nel 1920 circa nel tratto camerunese del fiume Sangha, un affluente del Congo, dove un cacciatore in viaggio verso Léopoldville (l'attuale Kinshasa) sarebbe stato infettato, probabilmente durante una battuta di caccia, da uno scimpanzé portatore del ceppo di SIV.[21]
L'analisi nel 2019 da parte di un team di ricerca sempre dell'università di Lovanio assieme a ricercatori di diversi altri istituti di ricerca internazionali, di un campione di tessuto del 1966 proveniente dalla Repubblica del Congo, da cui è stato possibile estrarre una copia del genoma completo dell'HIV, ha potuto retrodatare la prima infezione tra il 1881 e il 1918.[22][23]
La fase nascosta dell'epidemia[modifica | modifica wikitesto]
Il primo ceppo responsabile del contagio in Africa fu HIV-2, più simile al SIV, che cominciò a diffondersi lungo la costa occidentale dell'Africa. In seguito fece la sua comparsa il tipo HIV-1, lungo i paesi centro-equatoriali.[16]
Nella seconda metà del XX secolo è stata diagnosticato in Africa un cosiddetto slim disease ("mal sottile"), che portava misteriosamente a morte i malati per una progressiva consunzione e che probabilmente era l'AIDS. Il virus si dovette diffondere in aree urbane dell'Africa (come Kinshasa), quasi esclusivamente tramite contagi eterosessuali, per poi travalicare l'oceano alla fine degli anni sessanta. Sporadiche manifestazioni della sindrome di immunodeficienza, riconosciuta come tale solo nei decenni successivi, sono state infatti riscontrate nei tessuti conservati di persone decedute fin dal 1969 in America (caso di Robert R.) e in Europa (casi di Arvid Noe e di Grethe Rask).[12]
Negli anni settanta, favorita dalla promiscuità legata alla rivoluzione sessuale e altri fenomeni connessi,[24] ebbe inizio la seconda fase della malattia, che interessò prima Haiti, poi New York e il Brasile.[16] Haiti aveva particolari relazioni con l'Africa centrale e il virus qui trovò un bacino di contagio vantaggioso favorito sia dalla massiccia raccolta di plasma tra la popolazione povera locale, sia dall'essere meta del turismo gay statunitense, e comunità omosessuali maschili, facendo da ponte tra l'Africa e l'America[16][25][26]
Il virus negli USA[modifica | modifica wikitesto]
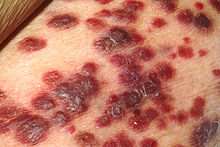
Soltanto quando il virus incominciò a colpire con forza alcuni specifici gruppi di individui, i sospetti di essere di fronte a una nuova patologia non poterono più essere ignorati. Grazie alla particolare forza contagiosa dei soggetti maschi e grazie alle condizioni particolarmente favorevoli al contagio dei rapporti di tipo anale, il virus trovò infatti un vantaggioso bacino di infezione nella comunità omosessuale maschile di alcune grandi città statunitensi.[12]
Alla fine del 1980 un ricercatore dell'Università della California, Michael Gottlieb, nell'ambito di uno studio sui deficit del sistema immunitario si imbatté in un ospedale nel caso di un giovane paziente che soffriva di un raro tipo di polmonite dovuta al protozoo Pneumocystis carinii, che di solito colpiva quasi esclusivamente i neonati prematuri e i pazienti dal sistema immunitario molto indebolito (malati oncologici, o esposti a farmaci molto potenti, o trapiantati).[27] Nei mesi successivi Gottlieb scoprì in altri tre pazienti, tutti omosessuali attivi, un basso livello di linfociti T.[25]
Considerando i lunghi tempi di incubazione del virus prima dell'arrivo dei sintomi, l'epidemia doveva essere arrivata già a uno stadio talmente avanzato dall'essere ormai impossibile continuare a ignorarne i segnali. Il 5 giugno 1981 infatti i Centri per la prevenzione e il controllo delle malattie di Atlanta pubblicarono nel bollettino Morbidity and mortality weekly report un improvviso aumento di diagnosi di casi di polmonite da Pneumocystis carinii e di un raro tumore dei vasi sanguigni, il sarcoma di Kaposi, in alcuni giovani omosessuali gravitanti nelle aree metropolitane di Los Angeles, San Francisco e New York. Il fatto non destò particolare allarme, ma le segnalazioni di nuovi casi aumentarono vertiginosamente, tanto che già nel luglio di quell'anno il New York Times pubblicò le constatazioni allarmanti legate a tale notizia: i casi erano ormai centinaia (422), colpivano soggetti molto più giovani di quanto non avvenisse normalmente, e avevano un decorso clinico estremamente grave, con un alto numero di decessi (159).[28] Pochi giorni dopo i CDC costituirono una task force dedicata espressamente alla ricerca sul sarcoma di Kaposi e sulle altre infezioni opportunistiche:[25] si iniziò a parlare di epidemia e venne associata all'omosessualità.[28]
La ricerca di un paziente zero negli Stati Uniti, sebbene in passato abbia prodotto il nome di Gaëtan Dugas, non ebbe esito, anche per il lungo periodo di incubazione del virus.[29]
Nel 1981, nell'oscurità legata alle forme di trasmissione contagio, cominciano a nascere le prime teorie sulle cause delle infezioni e dei tumori: infezione da Cytomegalovirus, uso di droghe, stimolazione eccessiva del sistema immunitario. Il ricordo di alcune centinaia di morti verificatesi in Spagna per una sindrome tossica da olio adulterato fece sospettare di non essere in presenza di una patologia contagiosa, ma di un'intossicazione legata magari a sostanze in uso tra la comunità omosessuale, come il nitrito d'amile (popper) utilizzato come potenziatore dell'orgasmo.[16] Alla fine dell'anno si registrano i primi casi tra eterosessuali e il primo contagio in Europa, in Inghilterra.[25]
La malattia non aveva ancora un nome e incominciarono a circolare sulla carta stampata le definizioni più disparate: "Gay compromise sindrome", su The Lancet, "immunodeficienza gay-correlata" (Gay-related immune deficiency, GRID), "cancro dei gay", "disfunzione immunitaria acquisita".[25]
Debutto ufficiale di una nuova epidemia[modifica | modifica wikitesto]

La notizia di una "nuova" malattia trasmissibile fu accolta nella generale incredulità, anche perché appena quattro anni prima (nel 1977) era entrato negli annali lo straordinario traguardo sanitario mondiale dell'eradicazione definitiva del vaiolo: per la prima volta nella storia della medicina si era definitivamente debellata una patologia che da millenni mieteva alti numeri di vittime all'anno. Dal dopoguerra, in effetti, le migliorate condizioni abitative, alimentari e di gestione delle acque avevano drasticamente ridotto nei paesi sviluppati l'incidenza di patologie fino ad allora endemiche come la malaria, il tifo, la tubercolosi, le salmonellosi, mentre la diffusione delle vaccinazioni aveva estinto di fatto infezioni gravi e frequenti come il tetano, la difterite e la poliomielite. Inoltre, la comparsa degli antibiotici negli anni quaranta aveva reso improvvisamente guaribili patologie infettive come le polmoniti, gli ascessi, le sepsi e persino la peste e il colera.[10]
In tale contesto il rischio di un'epidemia nuova e inarrestabile non figurava in nessuna previsione della fine degli anni settanta, un periodo in cui la società concentrava le sue preoccupazioni su temi come l'inquinamento, l'esaurimento delle fonti energetiche, i conflitti atomici e l'effetto serra[Ma se negli anni '70 e '80 la teoria scientifica generale andava ancora verso una nuova "era glaciale" (e le temperature medie globali cominciarono ad aumentare solo dal 1978-'79) e se ne continuò un po' ancora a parlare persino con la pubblicizzazione del buco nell'ozono dal 1986...]. Le epidemie fino ad allora conosciute erano infatti di tipo strutturale, cioè legate a carenze o inefficienze nella gestione di particolari elementi della salute sociale (acque, alimenti, rifiuti, animali, insetti), risolvibili con interventi strutturali e farmacologici, mentre si andavano affacciando sulla scena le epidemie cosiddette comportamentali, legate cioè agli errori nei comportamenti degli individui, tra le quali quella da HIV rappresentava la più estesa e pericolosa, anche perché legata alla sfera irrazionale ed emotiva dei rapporti sessuali e della tossicodipendenza.[10]
Nel 1982 alcuni primi casi si verificarono tra gli emofiliaci, obbligati a ricevere continue trasfusioni, e cominciò a farsi strada l'idea che il contagio fosse legato a un'anomalia del sangue,[28] svanendo presto l'illusione del contagio chimico.
Nell'agosto di quell'anno, durante un congresso della Food and Drug Administration sugli emocomponenti, Bruce Voeller propose di chiamare la nuova malattia Acquired Immune-Deficiency Syndrome (AIDS),[28] basandosi sulla comparsa di una serie di patologie nei pazienti, tra cui infezioni opportunistiche e neoplasie (il sarcoma di Kaposi, il linfoma di Burkitt, il linfoma primitivo cerebrale e alcuni linfomi dei linfonodi a grado alto e intermedio) altrimenti molto rare in giovani adulti non immunodepressi.[16]
A fine anno morì un primo bambino emofiliaco per una trasfusione infetta e si registrò il primo caso documentato di trasmissione verticale materno-fetale:[25] per l'opinione pubblica fu un vero e proprio trauma.[16] La facilità degli spostamenti delle persone e le frequenti occasioni di viaggio resero rapidamente l'epidemia un fatto mondiale: nel 1982 si registrarono i primi casi in Italia, Canada e Brasile.[30][31] In Italia, in particolare, il primo caso era legato a un paziente omosessuale che si era recato più volte negli Stati Uniti; nel 1983 i casi erano 4, con caratteristiche simili, e nel 1984 18, tra cui un primo caso, a Milano, di un paziente tossicodipendente che non era mai stato all'estero.[32]
I casi negli USA nel 1982 salirono a 1 614 con 619 decessi.[28] Per il 1983 i dati individuavano 642 omosessuali maschi contagiati, 154 tossicodipendenti, 81 tossicodipendenti omosessuali, 50 soggetti haitiani immigrati e 61 a epidemiologia ignota.
L'alta prevalenza di omosessuali maschi focalizzò inizialmente l'attenzione sulla sola popolazione gay e il messaggio era arrivato anche all'opinione pubblica fin da quando il New York Times titolò «Raro cancro osservato in 41 omosessuali» (1981). Sebbene circoscrivere il rischio a un gruppo sociale ristretto e socialmente isolato fu in un certo senso di conforto per l'opinione pubblica, ciò fu fuorviante e per diversi anni distolse l'attenzione dal più concreto e reale rischio di diffusione nel mondo tramite i rapporti eterosessuali.[10]
Nel frattempo, soprattutto nella fascia mediterranea, il mezzo di diffusione più veloce e frequente fu quello del contatto ematico tra gruppi di eroinomani che condividevano la stessa siringa: in Italia, ad esempio, nei primi anni ottanta il consumo di eroina era un'occasione di incontro per molti giovani, tra i quali si condividevano sia la sostanza che la siringa.[10]
Per un certo periodo l'infezione fu chiamata "delle 4 H", poiché colpiva omosessuali, eterosessuali utilizzatori di droghe endovena, haitiani ed emofiliaci (in inglese "homosexuals, heterosexual intravenous drug users, Haitian immigrants" e "hemophiliacs").[33]
La scoperta del virus[modifica | modifica wikitesto]

Nel 1982 Robert Gallo, direttore del laboratorio di biologia cellulare dei tumori del National Cancer Institute di Bethesda in America, accertò l'origine virale dell'epidemia, riconoscendo l'azione di un retrovirus, appartenente a tale particolare famiglia da lui identificata qualche anno prima nei suoi studi sulla leucemia.[16]
Il 4 novembre 1983 Françoise Barré-Sinoussi, nel laboratorio di retrovirologia dell'Istituto Pasteur di Parigi diretto da Luc Montagnier vide al microscopio per la prima volta il virus HIV, nei tessuti di un linfonodo prelevato da una persona infetta, ma che non aveva ancora sviluppato la sindrome: si tratta di un paziente omosessuale che aveva come unico sintomo i linfonodi ingrossati.[10][25]
Circa sei mesi dopo, il 22 aprile 1984, i CDC dichiarano pubblicamente che il virus francese era stato definitivamente identificato come la causa dell'AIDS e il giorno successivo venne annunciato che Robert Gallo aveva a sua volta isolato un virus prelevato da pazienti malati di AIDS, e che per il virus sarebbe stato disponibile a breve un kit per riconoscere le persone infette, tramite l'individuazione nel sangue della presenza o meno di uno degli anticorpi prodotti dall'organismo contro l'infezione.[10][25] Il virus di Gallo, infettante i linfociti T umani, si rivelò poi lo stesso virus francese e tra i due istituti si avviò una vera e propria battaglia legale su chi dovesse rivendicare la scoperta, conclusa in un certo senso con il conferimento del premio Nobel per la medicina ai francesi nel 2008.[25]

La terza fase dell'epidemia[modifica | modifica wikitesto]

Dalla seconda metà degli anni ottanta l'epidemia entrò nel pieno della sua "terza fase"; dopo quella "nascosta" e quella americana e nordeuropea (quella legata prevalentemente agli omosessuali), esplose infatti il contagio per via parenterale tra tossicodipendenti nell'Europa centromeridionale e di nuovo negli USA, in Thailandia, in India e molte altre regioni asiatiche e africane, raggiungendo una diffusione veramente da pandemia mondiale. Si trattava di una via alternativa a quella sessuale (etero- e omosessuale), che si aggiungeva alle altre fonti di contagio.[16]
Nel 1985 si tenne ad Atlanta la prima Conferenza internazionale sull'AIDS, sponsorizzata dall'Organizzazione mondiale della sanità, alla quale partecipano circa duemila ricercatori provenienti da trenta paesi. Nelle successive conferenze, che si tennero a cadenza annuale fino al 1996, vennero via via resi noti i dati sulla diffusione dell'epidemia. Nel 1984 ad esempio negli Stati Uniti i casi di contagio erano arrivati a 22 996 e 12 592 i decessi, con un decorso della malattia che aveva ancora l'allarmante dato vicino al 100% di mortalità. Venne denunciata l'esistenza del focolaio africano, senza però avere dati certi, e si iniziò a parlare di trasmissione eterosessuale.[25] Dal 1985 in USA e Giappone si iniziò, con riluttanza,[34] a testare gli emoderivati, in Europa dall'anno successivo.[25]
La piena cognizione che sangue ed emoderivati trasmettessero l'AIDS avvenne tra molti ritardi, quando circa ottomila casi si erano verificati negli Stati Uniti e seimila in Europa, tra il 1985 e il 1992, nonostante dal 1985 si scaldassero gli emoderivati per la neutralizzazione del virus[35]. Ritardata fu l'esclusione dalle donazioni di alcune categorie a rischio (come i detenuti), così come l'applicazione dei test ELISA, specialmente in Francia[16]. Nel rapporto statunitense sull'epidemia del 1986 si richiamò la necessità di dare informazioni legate al sesso. La seconda conferenza mondiale si tenne a Parigi, durante la quale l'OMS fornì una stima di 5/10 milioni di sieropositivi[25]. Apparve chiaro come fosse necessario creare campagne d'informazione per arginare il contagio e cominciarono a circolare le prime notizie sulla ricerca legata a una possible cura. L'anno successivo registrò la conferenza a Washington, in cui l'Assemblea Mondiale della Sanità approvò una strategia globale per fronteggiare l'epidemia. Nel mondo si contavano ormai 50 000 casi (800 in Italia)[25].
I problemi sociali ed economici legati alla droga, la difficile emancipazione degli omosessuali incominciata proprio in quegli anni, l'imbarazzo legato ai temi sessuali, furono all'origine di atti di discriminazione e sottostima dei rischi. Emblematico è il caso dell'Italia, il cui Ministro della sanità, Carlo Donat-Cattin ritardò oltremodo i controlli sulle sacche di sangue (ben tre anni dopo altri paesi europei, nel 1988)[36] e le campagne di informazione pubbliche sull'epidemia (pure solo dal 1988, a fronte del 1985 in Gran Bretagna e del 1986 in paesi come Francia, Germania, Belgio, zona scandinava), vietando di fatto di citare l'uso del profilattico come metodo di prevenzione per evitare di "spiegarne l'uso nelle scuole" (a differenza ad esempio degli spot della TV svizzera)[37]. Oltre a tutto ciò si aggiunse una esagerata tendenza a sovrastimare nettamente i casi da parte sia del ministro Donat-Cattin che delle istituzioni italiane e Occidentali, preannunciando una vera e propria paralizzazione degli ospedali a causa di un'annunciata epidemia di ampia portata.[38]
I paesi dell'est europeo a causa del loro isolazionismo si mantennero pressoché esenti dal virus fino alla fine della cortina di ferro, in seguito alla quale e alla liberalizzazione degli spostamenti il virus arrivò anche lì e si diffuse molto rapidamente superando di gran lunga la diffusione in Occidente diventando in pochi anni una vera piaga per Russia e Ucraina[39].
Casi celebri, episodi di discriminazione e di solidarietà[modifica | modifica wikitesto]

La prima vittima celebre che ammise pubblicamente di essere affetta da AIDS fu il divo statunitense Rock Hudson, morto il 2 ottobre 1985. Il "caso Rock Hudson" portò alla coscienza degli USA, dell'Europa e delle popolazioni di molti altri Paesi l'esistenza della sindrome e di come essa non fosse un destino riservato a pochi emarginati, né una "prerogativa" del mondo omosessuale (in realtà il divo era gay, ma segretamente). La sua immagine di uomo virile, bianco, ricco e persino repubblicano (amico personale di Ronald Reagan), non sembrava avere nulla a che fare con lo stereotipo imperante circa la tipologia delle vittime del morbo, dimostrando così che le convinzioni confortate dalle statistiche sulle cosiddette "categorie a rischio" andavano senz'altro riviste.
Hudson visse sulla sua pelle la discriminazione e la psicosi legata a questa malattia di cui si sapeva poco e faceva paura: quando un comunicato stampa diffuse la sua reale situazione sanitaria, l'ospedale di Parigi in cui era ricoverato si svuotò immediatamente per il terrore del contagio. L'attore volle rientrare subito negli Stati Uniti, ma il suo staff incontrò notevoli problemi nel reperire un volo, poiché nessuna compagnia aerea voleva averlo come passeggero. L'attrice Linda Evans, che qualche anno prima aveva baciato Hudson sul set di Dynasty, si sottopose a controlli medici, risultando poi non infettata, non sapendo che il virus non si trasmette col bacio[12].
L'amicizia con l'attore e con altre persone ammalate spinse invece Elizabeth Taylor a impegnarsi attivamente, dedicando molto tempo e molte energie nella lotta all'AIDS, attraverso manifestazioni e raccolte fondi, culminate con la fondazione dell'American Foundation for AIDS Research (AmfAR). Si stima che la Taylor abbia aiutato alla raccolta di circa 50 000 000 $ per la lotta alla malattia[40]. Vittima della discriminazione fu anche il ragazzo emofiliaco Ryan White, che dopo un'iniezione di sangue contaminato contrasse il virus e, nel 1984, sebbene i medici avessero escluso il rischio di contaminazione, fu espulso dalla scuola, diventando un simbolo della lotta all'HIV/AIDS negli Stati Uniti: per lui intervennero Magic Johnson, Elton John e Michael Jackson.
Nel 1990, poco tempo dopo la morte di White, il Congresso degli Stati Uniti d'America proclamò il Ryan White Care Act, fondamentale per contrastare l'AIDS. Lo stesso anno l'epidemia mieteva un'altra vittima illustre, l'artista Keith Haring. Una delle prime vittime eterosessuali famose fu Arthur Ashe, tennista statunitense, che fu diagnosticato come positivo all'HIV il 31 agosto 1988, dopo aver contratto il virus da trasfusioni di sangue durante un intervento chirurgico al cuore; morì all'età di 49 anni, il 6 febbraio 1993[41]. Una vittima celebre nel Regno Unito fu Nicholas Eden, Lord Avon (m. 1985), membro gay della Camera dei lord e figlio del defunto Primo ministro del Regno Unito Anthony Eden[42]. Il virus provocò forse la sua più celebre vittima il 24 novembre 1991, quando la rockstar Freddie Mercury, cantante e frontman dei Queen, morì per una patologia correlata all'AIDS dopo aver annunciato la malattia soltanto il giorno precedente[43]. Poco dopo seguì quella del ballerino Rudol'f Nureev (1993).
In Francia Michel Foucault tenne rigorosamente nascosta la sua malattia, morendo nel 1984; nel 1987 invece Jean-Paul Aron decise di rompere il silenzio, primo nel suo paese, facendosi intervistare dal settimanale Nouvel Observateur in copertina e col titolo Mon Sida ("Il mio AIDS")[44]. In Italia ci fu più circospezione sull'argomento: la scomparsa dello scrittore Pier Vittorio Tondelli fu ad esempio un fatto privato, reso noto solo dopo l'esito fatale (1991)[45]; solo nel 1992 un personaggio pubblico fece sentire la sua voce, il giornalista Giovanni Forti, in una fase avanzata della malattia, facendosi intervistare su Rai 1 da Enzo Biagi e pubblicando una cronaca limpida, e insieme ottimista, del suo stato su L'Espresso del 16 febbraio 1992: i colleghi del settimanale gli dedicarono la copertina, prima di morire, il 4 aprile di quell'anno[46]. Il 18 novembre 1993 moriva anche, a 41 anni, Stefano Marcoaldi, giornalista de L'Espresso, che negli anni precedenti era stato tra i fondatori dell'ASA (Associazione Solidarietà AIDS) di Milano (e uno dei suoi primi presidenti) e aveva dato un volto e una voce alla HIV-sieropositività in Italia grazie alle sue frequenti apparizioni come ospite al Maurizio Costanzo Show.
La risposta farmacologica[modifica | modifica wikitesto]
La scoperta dell'AZT[modifica | modifica wikitesto]

Nel 1987, a tempo di record (entrando negli annali della storia della medicina), fu approvato un primo farmaco, la molecola dell'AZT, inibitrice dell'enzima della transcrittasi inversa virale[25]. Sebbene i risultati della terapia si sarebbero dimostrati non pienamente soddisfacenti, per la relativa facilità con cui il virus riusciva a sviluppare ceppi resistenti al farmaco, il farmaco dimostrò di prolungare la vita dei pazienti rallentando lo sviluppo della sindrome. Nonostante le difficoltà di assunzione e i pesanti effetti collaterali, il farmaco riaccese la speranza di decine di migliaia di contagiati, creando però anche inevitabili problemi gestionali nella sua erogazione, all'origine di disordini e di un vero e proprio mercato nero (come il caso di Ron Woodroof a Dallas)[47].
Alla conferenza del 1988, a Stoccolma, partecipò per la prima volta una nutrita rappresentanza di ricercatori da paesi in via di sviluppo. Seguì nel 1989 la conferenza di Montréal, in cui per la prima volta ci fu una forte contestazione da parte di attivisti che rivendicavano l'abbassamento del prezzo dell'AZT, arrivando al palco: negli USA la Burroughs Wellcome fu costretta a venire incontro a queste richieste[25]. Sempre nel 1988 venne istituita la Giornata mondiale contro l'AIDS, ogni anno il 1º dicembre: dietro tale data non c'è un evento particolarmente significativo, ma essa venne scelta in modo da ottenere la massima copertura mediatica, dopo le elezioni USA e prima del periodo natalizio[48].
In Italia, archiviato il lassismo di Donat-Cattin, il nuovo ministro Francesco De Lorenzo fece andare in onda nel 1989 la più efficace comunicazione di massa sull'AIDS nel pubblico italiano, con una serie di spot televisivi in cui venivano mostrati i modi di contagio (tra tossicodipendenti e con rapporti sessuali eterosessuali non protetti). In essi un alone viola circondava i contagiati, altrimenti invisibili, invitando a prendere misure precauzionali come l'evitare di utilizzare siringhe usate o come l'utilizzo del preservativo nei rapporti sessuali occasionali. Celebre lo slogan "AIDS, se lo conosci lo eviti"[49]. La VI conferenza internazionale AIDS si tenne a San Francisco (1990) e in quell'occasione furono migliaia gli attivisti scesi in campo, che manifestarono per richiamare l'attenzione sulla malattia e contestare le norme discriminatorie introdotte da George Bush, limitanti ad esempio la mobilità dei sieropositivi[25]. I dati di quell'anno parlavano di 254 000 casi di AIDS nel mondo (6 759 in Italia), con i sieropositivi stimati in circa 10 milioni[25].
Ulteriori progressi farmacologici[modifica | modifica wikitesto]

Nel 1991 venne approvato un nuovo farmaco anti AIDS, la DDI che, come l'AZT, mirava a impedire la trascrittasi inversa agendo sugli enzimi coinvolti, evitando alcuni degli effetti collaterali del precedente farmaco. Un anno dopo fu approvata la DDC, un altro inibitore, e prese avvio lo studio clinico sulla combinazione a due farmaci[25]. La conferenza del 1991 si tiene a Firenze e quella successiva, l'VIII, avrebbe dovuto tenersi a Boston, ma le norme restrittive del governo nordamericano resero necessario uno spostamento ad Amsterdam[25]. Simbolo della rinata speranza fu il cestista statunitense Magic Johnson: dopo aver ammesso di essere sieropositivo nel 1991, nello sconcerto generale (anche per la sua eterosessualità), la sua malattia non progredì mai a uno stadio grave grazie all'uso dei farmaci[50].
Nel 1993 scoppiò in Francia - e poi in altri paesi tra cui l'Italia - lo scandalo del sangue infetto che fece arrestare e condannare quattro funzionari della banca del sangue[25]. La IX conferenza si tenne a Berlino, in cui si registrò come l'epidemia si stesse diffondendo molto rapidamente nel sud est asiatico[25]. Lo stesso anno i CDC americani introdussero una nuova definizione di AIDS, non più basata sui sintomi, ma sul livello di linfociti T CD4+ al di sotto di 200/mm3; in Europa invece si continuò col metodo tradizionale, includendo nella conta nuove infezioni opportunistiche quali tubercolosi polmonare, polmonite ricorrente e carcinoma invasivo della cervice. Tale novità, legata a considerazioni di ordine assistenziale negli Stati Uniti, portò al raddoppio virtuale dell'incidenza di casi AIDS negli USA[16].
L'ingresso sul mercato del D4T si ebbe nel 1994, anno dell'ultima conferenza annuale, a Yokohama. In seguito le conferenze si tennero ogni due anni. Nel 1994 i malati di AIDS nel mondo erano saliti del 37%, con 985 119 casi complessivi, dei quali il 42% negli Stati Uniti, il 33,5% in Africa, l'11,5% in Europa, l'11,5% nelle Americhe, l'1% in Asia e lo 0,5% in Oceania; i sieropositivi erano stimati in 16 milioni, di cui un milione solo di bambini in Africa. In Italia i dati parlavano di un infettato ogni diecimila abitanti[25]. La progressione farmacologica aveva già intaccato la mortalità per la malattia, che dal 100% nel 1984 era scesa al 77,5%[10]. Ulteriori progressi, sebbene non ancora risolutivi, si registrarono nel 1995, quando fu approvato il saquinavir, il primo inibitore della proteasi, e il 3TC, un inibitore della trascrittasi inversa particolarmente sinergico con altri inibitori. Il 1995 fu anche l'anno che registrò il picco dell'epidemia, col massimo numero di nuovi casi: in Italia arrivarono a essere 4 515[25].

La svolta dell'HAART (1996)[modifica | modifica wikitesto]
Il 1996 fu l'anno della svolta che vide l'abbandono della monoterapia (AZT) e delle duplici terapie: a gennaio infatti furono presentati studi clinici sull'Haart (Highly Active Anti-Retroviral Therapy), che presto diventò lo standard mondiale nella cura dell'AIDS. Si tratta di una combinazione di due inibitori della trascrittasi inversa, il processo che permette al virus di trascrivere il proprio codice genetico (RNA) nello stesso linguaggio usato dal codice genetico delle cellule dell'uomo (DNA), impedendo di essere aggredito dai farmaci e dalla risposta immunitaria, e di un inibitore della proteasi, ovvero l'enzima che modella le macroproteine prodotte dalle cellule infettate in una forma idonea a dar vita a nuovi virus. Venne inoltre messo a punto un metodo per misurare la carica virale degli individui, ovvero la presenza di copie del virus nel sangue, in modo da capire l'efficacia delle terapie.

Lo scienziato taiwanese David Ho, sulla base di modelli matematici, sostenne che era vicina la possibilità di eradicare il virus e si guadagnò la copertina del TIME come "uomo dell'anno"[25]. Le possibilità terapeutiche si arricchìrono di nuovi farmaci, come la nevirapina, primo inibitore non nucleosidico della trascrittasi inversa, l'indinavir e il ritonavir, agenti contro la proteasi. L'XI Conferenza Internazionale AIDS a Vancouver si chiuse per la prima volta con la sensazione condivisa che si stesse intravedendo una luce in fondo al tunnel. I risultati delle nuove terapie non tardano infatti ad arrivare: la mortalità per AIDS calò in modo rapido e netto (negli Stati Uniti si dimezza già dal primo anno), i ricoveri diminuirono in modo drastico mentre la fiducia, l'ottimismo, e l'entusiasmo, tornarono tra medici e pazienti affetti da HIV[25].
Nuovi progressi e la catastrofe africana[modifica | modifica wikitesto]
I successivi sforzi della comunità sanitaria internazionale si spostarono quindi sull'accessibilità delle terapie per tutti, con una platea di destinatari stimata in 22 milioni di infettati nel mondo. Trattandosi di farmaci molto costosi, la cura rappresenta un problema anche per i bilanci dei paesi sviluppati del Nord del mondo e a maggior ragione per i paesi sottosviluppati e in via di sviluppo, nei quali l'accesso a tali terapie appare come una chimera irraggiungibile[25].
I risultati positivi delle ricerche sulle terapie di combinazione furono presentati alla XII Conferenza Internazionale AIDS di Ginevra (1998), sebbene l'entusiasmo fosse frenato dai primi fallimenti terapeutici dell'Haart: se infatti la terapia non azzera rapidamente la replicazione, il virus, con la sua alta mutabilità, sviluppa presto forme resistenti, per cui è necessario ricorrere a molecole differenti; capitavano inoltre resistenze incrociate[25]. Nonostante ciò la terapia segnò indiscutibili successi: i numeri di decessi e i casi di AIDS conclamato crollarono, generando però un pericoloso riflusso.
Il messaggio che prendeva piede nell'opinione pubblica era infatti che l'AIDS fosse battuto e l'epidemia arrestata, confondendo il dato del decrescere della mortalità con quello dei nuovi contagi, che invece restò stabile, anzi in aumento[25]. Inoltre si accrebbe il divario tra Nord e Sud del mondo[25]: per ridurre le diseguaglianze l'International AIDS Society (Ias) organizzò a Roma nel 1999 la State-of-the Art Conference on Treatment of Hiv Infection che lancia il progetto "Share" per una chiamata a una mobilitazione collettiva mondiale. La situazione in Africa era infatti più che mai drammatica: stime parlavano dell'8% della popolazione sudafricana infetta, con 3,6 milioni di persone ammalate di AIDS. Tali dati facevano del Sudafrica il paese più colpito al mondo, con circa un quinto della popolazione infetta[25].

Nel 1999 molti nuovi farmaci videro la luce: l'abacavir (inibitore della trascrittasi inversa), il nelfinavir (contro la proteasi), la delaviridina e l'efavirenz (inibitori non nucleosidici della trascrittasi inversa); inoltre negli Stati Uniti l'FDA garantì una procedura d'approvazione accelerata per l'inibitore della proteasi amprenavir e molte nuove molecole erano in procinto di registrazione[25]. Nel settembre del 2000 fu messo in commercio il lopinavir, potentissimo inibitore della proteasi. Nel 2000, a vent'anni dalla scoperta dell'epidemia, si calcolavano 16,3 milioni di decessi[25].
L'epidemia aveva ormai una dimensione geopolitica, e stimolava la solidarietà tra paesi ricchi e paesi poveri: a chi sosteneva che i brevetti dei farmaci dovessero essere sempre e comunque rispettati rispondeva chi sostiene che, davanti alla catastrofe sanitaria, fosse legittimo da parte dei paesi più poveri di accedere a diverse forme di approvvigionamento, compresi i cosiddetti farmaci generici prima dell'esauristi dei diritti. Alcune aziende farmaceutiche accettarono di ridurre significativamente il prezzo dei farmaci per il sud del mondo. Nel frattempo il presidente Bill Clinton riconobbe l'emergenza africana e varò una sorta di nuovo piano Marshall[25]. La nuova conferenza internazionale si tenne a Durban, con 12 700 delegati di cui 1 459 erano giornalisti. Dei 36,1 milioni di sieropositivi nel 2000 (di cui 1,4 di bambini sotto i 15 anni di età), oltre il 70% viveva nell'Africa sub-sahariana e il 16% nel sud-est asiatico[25].
Ricadute positive sulla virologia e l'assistenza sanitaria[modifica | modifica wikitesto]

La pandemia dell'AIDS ha sollevato tutta una serie di problematiche, stimolando la popolazione mondiale a trovare soluzioni, non del tutto prive di ricadute positive in generale. I migliori centri di ricerca del mondo si sono impegnati subito in approfondite ricerche sui virus e in particolare sui retrovirus, facendo nuove scoperte in campo epidemiologico, virologico, immunologico e clinico, con un'intensità senza precedenti nella storia della medicina. Di tali scoperte hanno beneficiato tutti i soggetti immunocompromessi in generale. Le conoscenze sui virus, sul loro aggancio alle cellule dell'ospite e sulla loro replicazione hanno subito un'impennata, dalle quali sono nati nuovi farmaci antivirali[10].
L'assistenza ai malati ha stimolato la nascita e la regolamentazione dei day-hospital e dell'assistenza domiciliare, utilizzati anche per altre forme di patologie croniche. Forme di volontariato organizzato sono sorte ovunque[10]. Nei paesi poveri l'epidemia di AIDS ha rivelato all'opinione pubblica lo stato di abbandono di interi sub-continenti, spingendo l'intervento di molte associazioni non-profit impegnate nella lotta all'AIDS, con risultati incoraggianti. In paesi dove ancora oggi si muore di malaria, tubercolosi, polmoniti e diarree, tutte malattie curabili con costi enormemente inferiori a quelli delle cure per l'AIDS, la diffusione di una cultura della salute, legata all'educazione, l'informazione, la prevenzione e la cura, può portare ricadute positive su tutte le patologie che affliggono i paesi poveri[10].
L'epidemia oggi[modifica | modifica wikitesto]
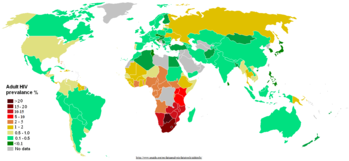
Oggi la situazione dell'epidemia nel mondo è complessa e articolata. Nel mondo occidentale categorie un tempo ad altissimo rischio, come eroinomani e omosessuali maschi, sono oggi interessate in maniera più limitata dal contagio. I primi si sono ormai circoscritti in limitate sacche di consumatori cronici, mentre i secondi hanno progressivamente preso atto dei rischi, utilizzando maggiormente il preservativo. Sebbene il consumo di eroina sia in crescita in paesi dal recente benessere, come l'Est europeo, l'Eurasia e il lontano Oriente, oggi la trasmissione eterosessuale è nettamente la prevalente causa di contagio nel mondo, quasi esclusiva in numerosi paesi. UNAIDS, organizzazione internazionale per il controllo dell'epidemia, stima le persone sieropositive in circa 39,5 milioni (2007), con 4,3 milioni di nuove infezioni nel 2006. I morti per l'epidemia quasi 3 milioni.
Nella sola Africa subsahariana sono stimati 24,7 milioni di persone HIV+ viventi, 460 000 nell'Africa settentrionale, 7,8 milioni nel sud-est asiatico, 740 000 in Europa, 1,7 milioni nell'Europa dell'Est e in Asia centrale, 1,7 milioni in America Latina, 1,4 milioni in America Settentrionale, 250 000 nei Caraibi e 81 000 in Australia[51]. Le nuove infezioni erano stimate nel 2006 a 2,8 milioni per l'Africa sub-sahariana, 860.000 per il Sud-Est e del Sud asiatici, 270 000 per l'Europa dell'Est e l'Asia centrale, 140 000 per l'America Latina, 43 000 per l'America Settentrionale e 22 000 per l'Europa occidentale[51]. Il problema legato all'HIV/AIDS nei paesi sviluppati è oggi rappresentato soprattutto da una pericolosa attenuazione progressiva della percezione del rischio nella collettività: l'AIDS non è più sentito come un'emergenza e l'attenzione di media, istituzioni e della stessa comunità scientifica è progressivamente crollata.
La morte per AIDS viene vista come un evento eccezionale, e il rischio di contagio è sistematicamente sottostimato, soprattutto nei giovani, che arrivano all'appuntamento con le prime esperienze sessuali privi delle adeguate conoscenze, e nella popolazione ultraquarantenne, soprattutto immigrata. Le conseguenze di questo stato si leggono nel numero costante dei contagi, che si è stabilizzato e non accenna a diminuire (soprattutto per le trasmissioni di tipo sessuale), e nella fase ormai avanzata della malattia a cui arriva una fetta sempre più larga di persone ignare del proprio contagio. Tra il 40 e il 50% di HIV+ scoprono di esserlo solo alla prima infezione opportunistica, dopo essere stati per mesi o anni possibili fonti di contagio e quando non possono ormai più godere i benefici di una diagnosi precoce, richiedendo un più difficile trattamento terapeutico[10].
La conferenza mondiale a Washington (23-26 luglio 2012) ha evidenziato soprattutto il problema dell'accesso ai farmaci nei paesi meno ricchi, dimostrando progressi incoraggianti in questo senso: oggi sono circa 8 milioni le persone HIV+ in Africa subsahariana che possono accedere a una terapia antiretrovirale[52]. La conferenza mondiale tenutasi a Melbourne nel luglio 2014 ha presentato, in particolare, le caratteristiche particolari del virus HIV nell'area asiatico-pacifica[53].
In Italia[modifica | modifica wikitesto]
In Italia, come nel resto del mondo occidentale, il contagio da HIV si è trasformato da epidemia (col picco endemico raggiunto all'inizio degli anni '80 con circa 18 000 nuove infezioni all'anno) a endemia. Le nuove infezioni all'anno si sono stabilizzate in circa 3 500-4 000[51], un numero che mostra una leggera riduzione solo tra i consumatori di sostanze per via iniettiva, mentre resta costante tra eterosessuali e omosessuali maschi. Nel 2010 i nuovi casi sono stati 5,5 ogni 100 000 residenti, con un'incidenza maggiore nel centro nord e minore al sud e nelle isole[54].
In particolare il contagio riguarda in percentuale maggiore gli stranieri residenti (un contagio su tre, 20 nuovi casi su 100 000 stranieri residenti)[54]. I rapporti sessuali non protetti sono all'origine dell'80,7% di tutte le segnalazioni (eterosessuali 49,8%, omosessuali 30,9%), l'età media di persone che scoprono il contagio è 39 anni per i maschi e 35 per le femmine, tra i quali oltre un terzo si accorge della malattia solo in una fase avanzata. A quest'ultima fascia appartengono soprattutto persone di età sopra i 40 anni, prevalentemente eterosessuali e più spesso stranieri[54]. Stime europee parlano di un sieropositivo su quattro che non sa di esserlo[54].
Le tendenze del XXI secolo riguardano essenzialmente:
- l'aumento delle infezioni contratte attraverso rapporti sessuali;
- la diminuzione di nuovi contagi attraverso il consumo di sostanze per via iniettiva;
- l'aumento di casi tra i residenti stranieri;
- la diminuzione delle infezioni tra le donne;
- l'aumento dell'età media e delle nuove infezioni in persone con oltre 50 anni di età[54]. È aumentata anche la percentuale di nuovi contagi sotto i 25 anni.[55]
Tra i sintomi che hanno portato alla diagnosi dell'AIDS sono diminuite la candidosi polmonare o esofagea, mentre sono aumentati i linfomi[54].
Dal 1982 in Italia sono stati segnalati circa 64 000 casi di AIDS, con quasi 40 000 decessi (2010)[54], i sieropositivi sono stimati in circa 130 000-140 000 (2006): non è obbligatoria la loro segnalazione da parte di province e regioni (le stime si basano sui modelli di UNAIDS), mentre è obbligatoria quella di casi di AIDS conclamato[10].
Note[modifica | modifica wikitesto]
- ^ 1° bollettino CDC. Il 1° campione di tessuto noto è del 1959.
- ^ Numero complessivo di casi confermati e sospetti.
- ^ Global HIV & AIDS statistics — 2019 fact sheet, su unaids.org, UNAIDS, 1º dicembre 2019.
- ^ (EN) HIV data and statistics, su who.int. URL consultato il 2 gennaio 2021.
- ^ WHO | The AIDS Pandemic: an update on the numbers and needs, su WHO. URL consultato il 2 gennaio 2021.
- ^ Robert Walter Eisinger e Anthony S. Fauci, Ending the HIV/AIDS Pandemic1, in Emerging Infectious Diseases, vol. 24, n. 3, 2018-03, pp. 413–416, DOI:10.3201/eid2403.171797. URL consultato il 2 gennaio 2021.
- ^ (EN) Myron S. Cohen, Nick Hellmann e Jay A. Levy, The spread, treatment, and prevention of HIV-1: evolution of a global pandemic, in Journal of Clinical Investigation, vol. 118, n. 4, 1º aprile 2008, pp. 1244–1254, DOI:10.1172/JCI34706. URL consultato il 2 gennaio 2021.
- ^ R. V. Short, The HIV/AIDS pandemic: new ways of preventing infection in men, in Reproduction, Fertility, and Development, vol. 16, n. 5, 2004, pp. 555–559, DOI:10.10371/RD03109. URL consultato il 2 gennaio 2021.
- ^ (EN) The AIDS Pandemic | ScienceDirect, su sciencedirect.com. URL consultato il 2 gennaio 2021.
- ^ a b c d e f g h i j k l m n o Il Libro dell'Anno 2007 su Treccani.it.
- ^ R.J. Biggar, M. Melbye, L. Kestens et al., Seroepidemiology of HTLV-III antibodies in a remote population of eastern Zaire, "Br.Med.J.", 290, 16 marzo 1985, 808-810. (R.J. Biggar, P.L. Gigase, M. Melbye, L. Kestens, P.S. Sarin, A.J. Bodner, P. Demedts, W.J. Stevens, L. Paluku, C. Delacollette et al., ELISA HTLV retrovirus antibody reactivity associated with malaria and immune complexes in healthy Africans, "Lancet", 2(8454), 7 settembre 1985, 520-523 e R.J. Biggar, Possible nonspecific association between malaria and HTLV-III/LAV, "N.Engl.J.Med.", 15(7), 14 agosto 1986, 457-458). (D.B. Hrdy, Cultural practices contributing to the transmission of human immunodeficiency virus in Africa, "Rev.Infect.Dis.", 9(6), 12 novembre 1987, 1109-1119).
- ^ a b c d e Storia dell’AIDS, su MEDICITALIA.it. URL consultato il 17 dicembre 2020.
- ^ Kalish ML, Wolfe ND, Ndongmo CD, McNicholl J, Robbins KE, M Aidoo, PN Fonjungo, G Alemnji e C Zeh, Central African hunters exposed to simian immunodeficiency virus, in Emerg Infect Dis, vol. 11, n. 12, 2005, pp. 1928–30, DOI:10.3201/eid1112.050394, PMID 16485481.
- ^ Zhu, T., Korber, B. T., Nahmias, A. J., Hooper, E., Sharp, P. M. and Ho, D. D., An African HIV-1 Sequence from 1959 and Implications for the Origin of the Epidemic, in Nature, vol. 391, n. 6667, 1998, pp. 594–7, Bibcode:1998Natur.391..594Z, DOI:10.1038/35400, PMID 9468138.
- ^ Michael Worobey, Marlea Gemmel, Dirk E. Teuwen, Tamara Haselkorn, Kevin Kunstman, Michael Bunce, Jean-Jacques Muyembe, Jean-Marie M. Kabongo e Raphaël M. Kalengayi, Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960, in Nature, vol. 455, n. 7213, 2008, pp. 661–4, Bibcode:2008Natur.455..661W, DOI:10.1038/nature07390, PMID 18833279.
- ^ a b c d e f g h i j k Universo del Corpo (1999) su Treccani.it.
- ^ Worobey M, Gemmel M, Teuwen DE, et al, Direct evidence of extensive diversity of HIV-1 in Kinshasa by 1960, in Nature, vol. 455, n. 7213, ottobre 2008, pp. 661–4, DOI:10.1038/nature07390, PMID 18833279.
- ^ News, su africa.reuters.com. URL consultato il 5 ottobre 2008 (archiviato dall'url originale il 5 ottobre 2008).
- ^ Korber B, Muldoon M, Theiler J, et al, Timing the ancestor of the HIV-1 pandemic strains, in Science, vol. 288, n. 5472, 2000, pp. 1789–96, DOI:10.1126/science.288.5472.1789, PMID 10846155.
- ^ Salemi M, Strimmer K, Hall WW, et al, Dating the common ancestor of SIVcpz and HIV-1 group M and the origin of HIV-1 subtypes using a new method to uncover clock-like molecular evolution, in Faseb J., vol. 15, n. 2, 2001, pp. 276–8, PMID 11156935.
- ^ Ricostruita la storia delle origini e della diffusione dell'HIV, in Le Scienze, 3 ottobre 2014.
- ^ Benjamin Ryan, Oldest Complete HIV Genome Found in 1966 Sample From Central Africa, in POZ, 8 giugno 2020.
- ^ Benjamin Ryan, A near full-length HIV-1 genome from 1966 recovered from formalin-fixed paraffin-embedded tissue, in Proceedings of the National Academy of Sciences, Brendan B. Larsen, Philippe Lemey, Jean-Jacques Muyembe-Tamfum, Dirk E. Teuwen, Michael Worobey, vol. 117, n. 22, giugno 2020, pp. 12222-12229, DOI:10.1073/pnas.1913682117.
- ^ Ne è indizio il boom di altre malattie veneree in quegli anni, cfr. Universo del Corpo (1999).
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah Storia dell'epidemia di Aids su Epicentro, sito del Centro Nazionale di Epidemiologia, Sorveglianza e Promozione della Salute
- ^ David Quammen, Spillover. L'evoluzione delle pandemie, traduzione di Luigi Civalleri, 12ª ed., Milano, Adelphi, 2014 [2012], ISBN 9788845932045.
- ^ AIDS in "Enciclopedia dei ragazzi", su treccani.it. URL consultato il 17 dicembre 2020.
- ^ a b c d e Vent'anni di AIDS sul sito Nova3, su nova3.com. URL consultato il 19 agosto 2012 (archiviato dall'url originale il 4 ottobre 2013).
- ^ Dina Fine Maron, New HIV Genetic Evidence Dispels "Patient Zero" Myth, in Scientific American.
- ^ Aids in Canada Archiviato il 9 luglio 2008 in Internet Archive.
- ^ Aids in Brasile, su avert.org.
- ^ Bruno de Michelis, Remo Modica, Giorgio Re et al.: Trattato di Clinica Odontostomatologica, Torino 1992, terza edizione
- ^ Centers for Disease Control (CDC), Opportunistic infections and Kaposi's sarcoma among Haitians in the United States, in MMWR Morb. Mortal. Wkly. Rep., vol. 31, n. 26, luglio 1982, pp. 353–4, 360–1, PMID 6811853.
- ^ 22 maggio 1984, un articolo sull'archivio di Repubblica.it
- ^ S. Franceschi, L. dal Maso, C. La Vecchia, Trends in incidence of AIDS associated with transfusion of blood and blood products in Europe and the United States, 1985-93, "British Medical Journal", 1995, 311, pp. 1534-1536.
- ^
 Storia proibita degli anni '80 - L'amore ai tempi dell'AIDS, su YouTube.
Storia proibita degli anni '80 - L'amore ai tempi dell'AIDS, su YouTube.
- ^ AIDS, il tragico ritardo, su radioradicale.it, su radioradicale.it. URL consultato il 31 agosto 2012 (archiviato dall'url originale il 7 febbraio 2012).
- ^ "L'Aids farà scoppiare gli ospedali", in La Stampa, 2 Dicembre 1988, p. 1.«Donat-Cattin annuncia che nel '92 i malati saranno 120 mila e la Sanità andrà in crisi»
- ^ Andkronos, su adnkronos.com.
- ^ Amfar.org
- ^ Tributes to Arthur Ashe, in The Independent, Londra, 8 febbraio 1993.
- ^ Anthony Eden, su nndb.com. URL consultato il 1º novembre 2011.
- ^ BBC ON THIS DAY | 24 | 1991: Giant of rock dies, BBC News, 24 novembre 1963. URL consultato il 1º novembre 2011.
- ^ Mon sida par Jean-Paul ARON (1925-1988)
- ^ Biografia nel sito ufficiale dedicato a Pier Vittorio Tondelli, su tondelli.comune.correggio.re.it (archiviato dall'url originale il 18 settembre 2018).
- ^ 4 aprile 1992, articolo sulla morte di Giovanni Forti sull'archivio di Repubblica.it.
- ^ The Dallas Buyer's Club Archiviato l'11 novembre 2012 in Internet Archive.
- ^ World Aids Day, sito ufficiale
- ^ Il video sul Youtube, su youtube.com.
- ^ (EN) Profilo biografico, su nba.com, NBA. URL consultato il 5 gennaio 2012.
- ^ a b c Dati del 2006, vedi Treccani.it
- ^ Aids2012, sito ufficiale
- ^ Sito ufficiale della conferenza mondiale 2014, su aids2014.org.
- ^ a b c d e f g Dati del Ministero della Salute Archiviato il 22 dicembre 2013 in Internet Archive. pubblicati per la giornata mondiale dell'Aids del 2011.
- ^ Giornata Mondiale contro l’AIDS (PDF), su salute.gov.it, Istituto Superiore di Sanità - Centro Operativo AIDS, 1º dicembre 2011.
Bibliografia[modifica | modifica wikitesto]
- M.D. Grmek, AIDS. Storia di una epidemia attuale, Roma-Bari, Laterza, 1989.
- S. Franceschi, L. dal Maso, C. La Vecchia, Trends in incidence of AIDS associated with transfusion of blood and blood products in Europe and the United States, 1985-93, British Medical Journal, 1995, n. 311.
Voci correlate[modifica | modifica wikitesto]
- HIV, AIDS
- Diffusione dell'HIV/AIDS in Africa
- Nastro rosso
- Sierofobia
- Cronologia dei primi casi di AIDS
Collegamenti esterni[modifica | modifica wikitesto]
- Vent'anni di epidemia di Aids, su nova3.com. URL consultato il 19 agosto 2012 (archiviato dall'url originale il 4 ottobre 2013).
- Storia dell'Aids su Medicitalia.it, su medicitalia.it.
- AIDS su "Il libro dell'anno" (2007) di Treccani.it, su treccani.it.
- Storia dell'epidemia di Aids su Epicentro, sito del Centro Nazionale di Epidemiologia, Sorveglianza e Promozione della Salute, su epicentro.iss.it.
- Dati su HIV/AIDS del Centro Operativo AIDS (COA) dell'Istituto Superiore di Sanità italiano.
- Un'intervista a un malato di AIDS nel 1985, su ricerca.repubblica.it.