AIDS: differenze tra le versioni
→Epidemiologia: Aggiorno con riferimenti |
+ Storia |
||
| Riga 21: | Riga 21: | ||
La [[sindrome]] è, allo stato attuale, curabile con numerosi [[farmaci]] ma non ancora guaribile, non è possibile infatti eradicare totalmente il virus dall'organismo che lo ospita. Le terapie odierne, di gran lunga meglio tollerabili di quelle usate al momento dell'emergenza nei primi [[anni 1980|anni ottanta]], riescono a ridurre la [[viremia]] (quantità di virus presente nel [[sangue]]) a livelli bassissimi o non rilevabili consentendo la rigenerazione dei linfociti e la prosecuzione di una vita esente dalle malattie opportunistiche che normalmente si presentano nelle persone non curate. L'andamento clinico-patologico della sindrome è estremamente variabile tra gli individui perché la progressione dell'infezione dipende dall'età, da fattori genetici del virus<ref>Campbell et al., [[2004]]; Campbell et al., [[2005]]; Senkaali et al., [[2005]]</ref> o dell'ospite<ref>Clerici et al., [[1996]]; Morgan et al., [[2002]]a; Tang et al., [[2003]]</ref>, dalle condizioni igieniche e dalla presenza di co-infezioni<ref>Morgan et al., [[2002]]b; Lawn et al., [[2004]]</ref>. |
La [[sindrome]] è, allo stato attuale, curabile con numerosi [[farmaci]] ma non ancora guaribile, non è possibile infatti eradicare totalmente il virus dall'organismo che lo ospita. Le terapie odierne, di gran lunga meglio tollerabili di quelle usate al momento dell'emergenza nei primi [[anni 1980|anni ottanta]], riescono a ridurre la [[viremia]] (quantità di virus presente nel [[sangue]]) a livelli bassissimi o non rilevabili consentendo la rigenerazione dei linfociti e la prosecuzione di una vita esente dalle malattie opportunistiche che normalmente si presentano nelle persone non curate. L'andamento clinico-patologico della sindrome è estremamente variabile tra gli individui perché la progressione dell'infezione dipende dall'età, da fattori genetici del virus<ref>Campbell et al., [[2004]]; Campbell et al., [[2005]]; Senkaali et al., [[2005]]</ref> o dell'ospite<ref>Clerici et al., [[1996]]; Morgan et al., [[2002]]a; Tang et al., [[2003]]</ref>, dalle condizioni igieniche e dalla presenza di co-infezioni<ref>Morgan et al., [[2002]]b; Lawn et al., [[2004]]</ref>. |
||
Nei paesi in cui le cure [[antiretrovirale|antiretrovirali]] e quelle per le infezioni opportunistiche e neoplastiche sono maggiormente disponibili, o, come in Italia, sostenute dal [[Servizio sanitario nazionale|SSN]], la [[mortalità]] dell'AIDS è ridotta<ref>Palella et al., 1998</ref>, non mancano però i problemi causati dagli effetti collaterali<ref>Montessori et al., 2004</ref>, dallo sviluppo della resistenza ai farmaci e dalla scarsa aderenza ai regimi terapeutici prescritti. |
Nei paesi in cui le cure [[antiretrovirale|antiretrovirali]] e quelle per le infezioni opportunistiche e neoplastiche sono maggiormente disponibili, o, come in Italia, sostenute dal [[Servizio sanitario nazionale|SSN]], la [[mortalità]] dell'AIDS è ridotta<ref>Palella et al., 1998</ref>, non mancano però i problemi causati dagli effetti collaterali<ref>Montessori et al., 2004</ref>, dallo sviluppo della resistenza ai farmaci e dalla scarsa aderenza ai regimi terapeutici prescritti. |
||
==Storia== |
|||
L'AIDS è stato riconosciuto per la prima volta il [[5 giugno]] [[1981]], quando il [[Centri per la prevenzione e il controllo delle malattie|CDC]] ha registrato un cluster di polmonite da ''[[Pneumocystis carinii]]'' in cinque uomini [[omosessualità|omosessuali]] a [[Los Angeles]].<ref name=MMWR2>{{Cite journal| author=Gottlieb MS| title=Pneumocystis pneumonia—Los Angeles. 1981| journal=Am J Public Health| volume=96| issue=6| pages=980–1; discussion 982–3| year=2006| pmid=16714472| url=http://www.cdc.gov/mmwr/preview/mmwrhtml/june_5.htm| accessdate=March 31, 2009 |
|||
| pmc=1470612| archiveurl= http://web.archive.org/web/20090422042240/http://www.cdc.gov/mmwr/preview/mmwrhtml/june_5.htm| archivedate=April 22 2009 <!--DASHBot-->| deadurl= no}}</ref> In principio, il CDC non aveva dato un nome ufficiale alla malattia e spesso faceva riferimento ad essa per mezzo delle malattie che sono state associate ad essa, ad esempio, [[linfoadenopatia]].<ref name=MMWR1982a/><ref name=Barre/> |
|||
In generale la stampa coniò il termine ''GRID'' che stava per ''Gay-related immune deficiency''.<ref name=Altman>{{Cite news |
|||
|author=Altman LK | url=http://www.nytimes.com/1982/05/11/science/new-homosexual-disorder-worries-health-officials.html?scp=1&sq=New%20homosexual%20disorder%20worries%20officials&st=cse | title=New homosexual disorder worries health officials | work=The New York Times | date=May 11, 1982 | accessdate =August 31, 2011}}</ref> Il CDC, in cerca di un nome, osservò che le comunità infette apparentemente fossero limitate a quelle degli [[haiti|haitiani]], degli omosessuali, degli [[emofilia|emofiliaci]] e dei conumatori di [[eroina]], coniò i termine di "malattia 4H".<ref name=SciRep470b>{{cite web| publisher=[[American Association for the Advancement of Science]]| date= July 28, 2006 |
|||
| url=http://www.scienceonline.org/cgi/reprint/313/5786/470b.pdf| title= Making Headway Under Hellacious Circumstances| accessdate =June 23, 2008| format=PDF}}</ref> Tuttavia, dopo aver stabilito che l'AIDS non era limitato a quelle sole comunità[159], il termine AIDS venne introdotto nel luglio 1982.<ref name=Kher>{{Cite news | author=Kher U |
|||
| title=A Name for the Plague| work=Time | date=July 27, 1982 | url=http://www.time.com/time/80days/820727.html |accessdate=March 10, 2008| archiveurl= http://web.archive.org/web/20080307015307/http://www.time.com/time/80days/820727.html| archivedate=March 7 2008 <!--DASHBot-->| deadurl= no}}</ref> Nel settembre 1982, il CDC iniziò ad usare i nomi di AIDS per la corretta definizione della malattia.<ref name=MMWR1982c>{{Cite journal |
|||
| author=Centers for Disease Control (CDC) | title=Update on acquired immune deficiency syndrome (AIDS)—United States | journal=MMWR Morb Mortal Wkly Rep. | year=1982 | pages=507–508; 513–514 | volume=31 | issue=37 | pmid=6815471}}</ref> |
|||
La identificazione positiva del virus HIV-1 viene dal [[Congo]] nel 1959 e gli studi genetici del 1960 indicano che il virus passato nella popolazione umana dagli scimpanzé circa cinquant'anni prima.<ref name=Worobey /> Uno studio del 2007 studio afferma che un ceppo di HIV- 1, probabilmente spostato dall'Africa ad Haiti, è entrato negli Stati Uniti intorno al [[1969]].<ref>{{Cite journal| author=Gilbert MT, Rambaut A, Wlasiuk G, Spira TJ, Pitchenik AE, Worobey M| title=The emergence of HIV/AIDS in the Americas and beyond| journal=Proc. Natl. Acad. Sci. U.S. A.| volume=104| issue=47| pages=18566–70| year=2007| pmid=17978186| doi=10.1073/pnas.0705329104| pmc=2141817| bibcode = 2007PNAS..10418566G }}</ref> |
|||
L'HIV deriva dal relativo [[virus di immunodeficienza delle scimmie]] (SIV), che infetta le scimmie in [[Africa]]. Vi sono prove che gli esseri umani che partecipano ad attività di caccia e di vendita di pelli di scimmia, abbiano contratto il SIV.<ref name=Kalish2005>{{cite journal |author=Kalish ML |title=Central African hunters exposed to simian immunodeficiency virus |journal=Emerg Infect Dis |volume=11 |issue=12 |pages=1928–30 |year=2005|pmid=16485481 |author-separator=, |author2=Wolfe ND |author3=Ndongmo CD |author4=McNicholl J |author5=Robbins KE '' |display-authors=5 |last6=Aidoo |first6=M |last7=Fonjungo |first7=PN |last8=Alemnji |first8=G |last9=Zeh |first9=C |doi=10.3201/eid1112.050394}}</ref> Tuttavia, solo alcune di queste infezioni è stata in grado di causare epidemie nell'uomo e tutte si sono verificate tra la fine del [[XIX secolo]] e l'inizio del [[XX secolo]]. Per spiegare la nascita di epidemie di HIV negli umani solo da quel momento, vi sono diverse teorie: cambiamenti sociali dopo il [[colonialismo]]<ref name=Sharp2001>{{cite journal|last1=Sharp |first1=P. M. |last2=Bailes |first2=E. |last3=Chaudhuri |first3=R. R. |last4=Rodenburg|first4=C. M. |last5=Santiago |first5=M. O. |last6=Hahn |first6=B. H. |title=The origins of acquired immune deficiency syndrome viruses: where and when? |journal=Philosophical Transactions of the Royal Society B: Biological Sciences |volume=356 |pages=867–76 |year=2001 |doi=10.1098/rstb.2001.0863 |pmid=11405934|pmc=1088480|issue=1410}}</ref> trasmissione tramite vaccinazioni contro il [[vaiolo]] con aghi non sterili<ref name=Marx2001>{{cite journal |author=Marx PA, Alcabes PG, Drucker E |title=Serial human passage of simian immunodeficiency virus by unsterile injections and the emergence of epidemic human immunodeficiency virus in Africa |volume=356 |pages=911–20 |year=2001 |journal=Philos Trans R Soc Lond B Biol Sci |pmc=1088484 |pmid=11405938 |doi=10.1098/rstb.2001.0867|url=http://rstb.royalsocietypublishing.org/content/356/1410/911.abstract |issue=1410}}</ref><ref name=Chitnis2000>{{cite journal |last1=Chitnis|first1=Amit |last2=Rawls |first2=Diana |last3=Moore |first3=Jim |title=Origin of HIV Type 1 in Colonial French Equatorial Africa? |journal=AIDS Research and Human Retroviruses |volume=16 |issue=1 |pages=5–8|year=2000 |pmid=10628811 |doi=10.1089/088922200309548}}</ref> e la [[prostituzione]] con la concomitante alta frequenza di malattie [[ulcera|ulcerative]] dei [[genitali]] (come la [[sifilide]]) nelle nascenti città coloniali.<ref name=Sousa2010>{{cite journal |last1=Sousa |first1=João Dinis de |last2=Müller |first2=Viktor |last3=Lemey|first3=Philippe |last4=Vandamme |first4=Anne-Mieke |last5=Vandamme |first5=Anne-Mieke |title=High GUD Incidence in the Early 20th Century Created a Particularly Permissive Time Window for the Origin and Initial Spread of Epidemic HIV Strains |journal=PLoS ONE |volume=5 |issue=4 |pages=e9936 |year=2010 |pmid=20376191|pmc=2848574 |doi=10.1371/journal.pone.0009936 |editor1-last=Martin |editor1-first=Darren P.}}</ref><ref name=McNeil>{{cite news |author=[[Donald McNeil, Jr.|Donald G. McNeil, Jr.]] |title=Precursor to H. I. V. Was in Monkeys for Millennia|url=http://www.nytimes.com/2010/09/17/health/17aids.html?_r=1&src=me&ref=general |quote=Dr. Marx believes that the crucial event was the introduction into Africa of millions of inexpensive, mass-produced syringes in the 1950s. ... suspect that the growth of colonial cities is to blame. Before 1910, no Central African town had more than 10,000 people. But urban migration rose, increasing sexual contacts and leading to red-light districts.|work=[[The New York Times|New York Times]] |date=September 16, 2010 |accessdate=September 17, 2010| archiveurl= http://web.archive.org/web/20100919223130/http://www.nytimes.com/2010/09/17/health/17aids.html?_r=1&src=me&ref=general| archivedate=September 19 2010 <!--DASHBot-->| deadurl= no}}</ref> |
|||
Una delle prime vittime famose di AIDS fu l'americano [[Rock Hudson]], un attore gay morto il 2 ottobre 1985 dopo aver annunciato che aveva contratto il virus. La malattia gli era stata diagnosticata nel 1984. [171] Un'altra vittima degna di nota fu [[Nicholas Eden]], membro gay del [[Parlamento inglese]] e figlio del defunto [[primo ministro inglese|primo ministro]] [[Anthony Eden]].<ref>{{cite web|url=http://www.nndb.com/people/817/000088553/ |title=Anthony Eden |publisher=Nndb.com |accessdate=November 1, 2011}}</ref><ref>{{cite web|last=Coleman |first=Brian |url=http://www.newstatesman.com/blogs/brian-coleman/2007/06/lady-thatcher-gay-tory |title=Thatcher the gay icon |work=New Statesman |date=June 25, 2007 |accessdate=November 1, 2011}}</ref> Il virus ha provocato forse la sua più celebre vittima il [[24 novembre]] [[1991]], quando la [[rock star]] [[Freddie Mercury]], cantante de [[frontman]] dei [[Queen]], morì per una malattia correlata all'AIDS dopo aver annunciato la malattia soltanto il giorno precedente.<ref>{{cite news|url=http://news.bbc.co.uk/onthisday/hi/dates/stories/november/24/newsid_2546000/2546945.stm |title=BBC ON THIS DAY | 24 | 1991: Giant of rock dies |publisher=BBC News |date=November 24, 1963 |accessdate=November 1, 2011}}</ref> Tuttavia la diagnosi gli era stata fatta già nel 1987.<ref>{{cite web|url=http://www.nndb.com/people/521/000044389/ |title=Freddie Mercury |publisher=Nndb.com |accessdate=November 1, 2011}}</ref> Una delle prime vittime [[eterosessuale|eterosessuali]] fu [[Arthur Ashe]], [[tennista]] americano. Diagnosticato come positivo all'HIV, il 31 agosto 1988, dopo aver contratto il virus da [[trasfusione di sangue|trasfusioni di sangue]] durante un [[intervento chirurgico]] al [[cuore]]. Morì all'età di 49 anni, il 6 febbraio 1993.<ref>{{cite news| url=http://www.independent.co.uk/news/tributes-to-arthur-ashe-1471622.html | location=London |work=The Independent | date=February 8, 1993}}</ref> |
|||
Una teoria controversa nota come [[teoria del vaccino orale antipolio sull'origine dell'AIDS]] suggerisce che l'epidemia di AIDS sia stata involontariamente avviata alla fine del 1950 nel [[Congo Belga]] dalla ricercatrice [[Hilary Koprowski]] che stava sperimentando un [[vaccino]] contro la [[poliomielite]].<ref name=Curtis>{{Cite news| author=Curtis T | title=The origin of AIDS| work=Rolling Stone | year=1992 | pages=54–59, 61, 106, 108 | issue=626 |url=http://www.uow.edu.au/arts/sts/bmartin/dissent/documents/AIDS/Curtis92.html|accessdate=March 10, 2008| archiveurl =http://web.archive.org/web/20080217014508/http://www.uow.edu.au/arts/sts/bmartin/dissent/documents/AIDS/Curtis92.html|archivedate = February 17, 2008}}</ref><ref name=Hooper>{{Cite book | author = Hooper E | year = 1999 | title = The River: A Journey to the Source of HIV and AIDS | edition = 1st |
|||
|pages = 1–1070 | publisher = Little Brown & Co | location = Boston, Massachusetts | isbn = 0-316-37261-7}}</ref> La comunità scientifica ha dichiarato che le prove disponibili non non supportano questa teoria.<ref name=refuted>{{Cite journal| author = Worobey M |title = Origin of AIDS: contaminated polio vaccine theory refuted|journal=Nature | year=2004 | page=820 | volume=428| issue=6985 | pmid=15103367 |doi=10.1038/428820a|bibcode = 2004Natur.428..820W| author-separator = ,| author2 = Santiago ML| author3 = Keele BF| display-authors = 3| last4 = Ndjango| first4 = Jean-Bosco N.| last5 = Joy| first5 = Jeffrey B.| last6 = Labama| first6 = Bernard L.| last7 = Dhed'a| first7 = Benoît D.| last8 = Rambaut| first8 = Andrew| last9 = Sharp| first9 = Paul M. }}</ref><ref name=Berry>{{Cite journal | author = Berry N |title = Mitochondrial DNA and retroviral RNA analyses of archival oral polio vaccine (OPV CHAT) materials: evidence of macaque nuclear sequences confirms substrate identity|journal=Vaccine | year=2005 | pages=1639–1648 | volume=23 | pmid=15705467 | doi=10.1016/j.vaccine.2004.10.038| issue = 14 | author-separator = , | author2 = Jenkins A | author3 = Martin J | display-authors = 3 | last4 = Davis | first4 = Clare | last5 = Wood | first5 = David | last6 = Schild | first6 = Geoffrey | last7 = Bottiger | first7 = Margareta | last8 = Holmes | first8 = Harvey | last9 = Minor | first9 = Philip}}</ref><ref name=VaccineQA>{{cite web| publisher=[[Centers for Disease Control and Prevention]]| date= March 23, 2004| url=http://www.cdc.gov/nip/vacsafe/concerns/aids/poliovac-hiv-aids-qa.htm| title= Oral Polio Vaccine and HIV / AIDS: Questions and Answers | accessdate =November 20, 2006}}</ref> |
|||
== Epidemiologia == |
== Epidemiologia == |
||
Versione delle 13:17, 30 apr 2012
| AIDS | |
|---|---|
 | |
| Specialità | infettivologia |
| Eziologia | HIV |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 042 |
| ICD-10 | B24 |
| OMIM | 609423 |
| MeSH | D000163 |
| MedlinePlus | 000594 |
| eMedicine | 211316 |
| Sinonimi | |
| Sindrome da immunodeficienza acquisita | |
La Sindrome da Immunodeficienza Acquisita (da cui l'acronimo SIDA in italiano, francese e spagnolo), o Acquired Immune Deficiency Syndrome (AIDS in inglese, utilizzato anche all'estero) è un insieme di manifestazioni dovute alla deplezione ossia la diminuzione del numero di linfociti T derivante da infezione con virus HIV-1 o HIV-2[1][2][3].
Descrizione

La malattia presenta diversi quadri clinici:
- AIDS (acquired immuno-deficiency syndrome): sindrome da immunodeficienza acquisita
- PLG o LAS (persistent generalized lymphadenopathy): linfadenopatia generalizzata persistente
- ARC (AIDS related complex): complesso di sintomi correlati all'AIDS
- ADC (AIDS dementia complex): demenza collegata all'AIDS
Tra queste manifestazioni sono comprese infezioni da microrganismi e l'insorgenza di tumori sia comuni nella popolazione generale sia caratteristici delle persone immunocompromesse. L'agente eziologico della patologia è il virus HIV.[4][5] La sindrome è, allo stato attuale, curabile con numerosi farmaci ma non ancora guaribile, non è possibile infatti eradicare totalmente il virus dall'organismo che lo ospita. Le terapie odierne, di gran lunga meglio tollerabili di quelle usate al momento dell'emergenza nei primi anni ottanta, riescono a ridurre la viremia (quantità di virus presente nel sangue) a livelli bassissimi o non rilevabili consentendo la rigenerazione dei linfociti e la prosecuzione di una vita esente dalle malattie opportunistiche che normalmente si presentano nelle persone non curate. L'andamento clinico-patologico della sindrome è estremamente variabile tra gli individui perché la progressione dell'infezione dipende dall'età, da fattori genetici del virus[6] o dell'ospite[7], dalle condizioni igieniche e dalla presenza di co-infezioni[8]. Nei paesi in cui le cure antiretrovirali e quelle per le infezioni opportunistiche e neoplastiche sono maggiormente disponibili, o, come in Italia, sostenute dal SSN, la mortalità dell'AIDS è ridotta[9], non mancano però i problemi causati dagli effetti collaterali[10], dallo sviluppo della resistenza ai farmaci e dalla scarsa aderenza ai regimi terapeutici prescritti.
Storia
L'AIDS è stato riconosciuto per la prima volta il 5 giugno 1981, quando il CDC ha registrato un cluster di polmonite da Pneumocystis carinii in cinque uomini omosessuali a Los Angeles.[11] In principio, il CDC non aveva dato un nome ufficiale alla malattia e spesso faceva riferimento ad essa per mezzo delle malattie che sono state associate ad essa, ad esempio, linfoadenopatia.[12][13]
In generale la stampa coniò il termine GRID che stava per Gay-related immune deficiency.[14] Il CDC, in cerca di un nome, osservò che le comunità infette apparentemente fossero limitate a quelle degli haitiani, degli omosessuali, degli emofiliaci e dei conumatori di eroina, coniò i termine di "malattia 4H".[15] Tuttavia, dopo aver stabilito che l'AIDS non era limitato a quelle sole comunità[159], il termine AIDS venne introdotto nel luglio 1982.[16] Nel settembre 1982, il CDC iniziò ad usare i nomi di AIDS per la corretta definizione della malattia.[17]
La identificazione positiva del virus HIV-1 viene dal Congo nel 1959 e gli studi genetici del 1960 indicano che il virus passato nella popolazione umana dagli scimpanzé circa cinquant'anni prima.[18] Uno studio del 2007 studio afferma che un ceppo di HIV- 1, probabilmente spostato dall'Africa ad Haiti, è entrato negli Stati Uniti intorno al 1969.[19]
L'HIV deriva dal relativo virus di immunodeficienza delle scimmie (SIV), che infetta le scimmie in Africa. Vi sono prove che gli esseri umani che partecipano ad attività di caccia e di vendita di pelli di scimmia, abbiano contratto il SIV.[20] Tuttavia, solo alcune di queste infezioni è stata in grado di causare epidemie nell'uomo e tutte si sono verificate tra la fine del XIX secolo e l'inizio del XX secolo. Per spiegare la nascita di epidemie di HIV negli umani solo da quel momento, vi sono diverse teorie: cambiamenti sociali dopo il colonialismo[21] trasmissione tramite vaccinazioni contro il vaiolo con aghi non sterili[22][23] e la prostituzione con la concomitante alta frequenza di malattie ulcerative dei genitali (come la sifilide) nelle nascenti città coloniali.[24][25]
Una delle prime vittime famose di AIDS fu l'americano Rock Hudson, un attore gay morto il 2 ottobre 1985 dopo aver annunciato che aveva contratto il virus. La malattia gli era stata diagnosticata nel 1984. [171] Un'altra vittima degna di nota fu Nicholas Eden, membro gay del Parlamento inglese e figlio del defunto primo ministro Anthony Eden.[26][27] Il virus ha provocato forse la sua più celebre vittima il 24 novembre 1991, quando la rock star Freddie Mercury, cantante de frontman dei Queen, morì per una malattia correlata all'AIDS dopo aver annunciato la malattia soltanto il giorno precedente.[28] Tuttavia la diagnosi gli era stata fatta già nel 1987.[29] Una delle prime vittime eterosessuali fu Arthur Ashe, tennista americano. Diagnosticato come positivo all'HIV, il 31 agosto 1988, dopo aver contratto il virus da trasfusioni di sangue durante un intervento chirurgico al cuore. Morì all'età di 49 anni, il 6 febbraio 1993.[30]
Una teoria controversa nota come teoria del vaccino orale antipolio sull'origine dell'AIDS suggerisce che l'epidemia di AIDS sia stata involontariamente avviata alla fine del 1950 nel Congo Belga dalla ricercatrice Hilary Koprowski che stava sperimentando un vaccino contro la poliomielite.[31][32] La comunità scientifica ha dichiarato che le prove disponibili non non supportano questa teoria.[33][34][35]
Epidemiologia

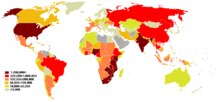
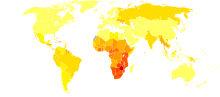
nessun dato
≤ 10
10–25
25–50
50–100
100–500
500–1000
1000–2500
2500–5000
5000–7500
7500-10000
10000-50000
≥ 50000
La pandemia di AIDS può anche essere vista come diverse epidemie di sottotipi distinti. I fattori principali della sua diffusione sono la trasmissione sessuale e la trasmissione verticale da madre a figlio alla nascita e attraverso il latte materno.[36] Nonostante il recente miglioramento all'accesso al trattamento antiretrovirale, in molte regioni del mondo, la pandemia di AIDS ha coinvolto circa 2,1 milioni (range tra gli 1.900.000 e i 2.400.000) di persone nel 2007, di cui circa 330.000 erano bambini sotto i 15 anni.[37] A livello globale, si stima che 33,2 milioni di persone vivevano con l'HIV nel 2007, di cui 2,5 milioni di bambini. Si stima che circa 2,5 milioni (range tra gli 1.800.000 e i 4.100.000) persone siano state contagiate nel 2007, tra cui 420.000 bambini.[37]
L'Africa subsahariana rimane di gran lunga la regione più colpita. Nel 2007 si stimava che li ci fossero il 68% di tutte le persone che vivono con l'AIDS e il 76% di tutte le morti per AIDS, con 1,7 milioni di nuove infezioni. A differenza di altre regioni, la maggior parte delle persone che vivevano con l'HIV nell'Africa sub-sahariana nel 2007 erano donne (61%). La prevalenza sugli adulti nel 2007 era stata stimata al 5,0% e l'AIDS continua ad essere la principale causa di mortalità in questa regione.[37]
Il Sud Africa ha la più grande popolazione di pazienti affetti da HIV nel mondo, seguito da Nigeria e India.[38] Il Sud e Sud-Est asiatico sono le seconde regioni più colpite.[37] L'India ha circa 2,5 milioni di infetti e la prevalenza negli adulti è stimata mnello 0,36%.[37] L'aspettativa di vita è diminuita drammaticamente negli paesi più colpiti, per esempio, nel 2006 è stato stimato che era scesa da 65 a 35 anni in Botswana.[36]
Negli Stati Uniti, le giovani donne afro-americane sono a rischio particolarmente elevato per l'infezione da HIV.[39] Gli afro-americani rappresentano il 10% della popolazione, ma possiedono circa la metà dei casi di HIV/AIDS a livello nazionale.[40] Questo è dovuto in parte alla mancanza di informazioni sull'AIDS , nonché di un accesso limitato alle risorse sanitarie e una maggiore probabilità di rapporti sessuali con partner di sesso maschile a rischio.[41]
Ci sono anche differenze geografiche nella prevalenza AIDS negli Stati Uniti, è infatti più comune nelle grandi aree metropolitane della costa orientale e nella California e nelle aree urbane del profondo sud.[41] Circa 1,1 milioni di persone vivono con l'HIV/AIDS negli Stati Uniti e più di 56.000 nuove infezioni si verificano ogni anno.[42]
Nei paesi dell'Europa dell'Est e dell'Asia Centrale l'epidemia è in espansione con 1,3 milioni di persone sieropositive contro le 160.000 del 1995.
Patogenesi
Ciò che l'infezione virale provoca è la comparsa di uno stato infiammatorio cronico che si risolve in un deficit funzionale e quantitativo del sistema immunitario. Sebbene una risposta immune particolarmente forte possa essere utile per controllare la replicazione virale, il mantenimento di un tale stato nel corso del tempo può portare a un progressivo esaurimento e deplezione cellulare.
Evento centrale nella patogenesi dell'infezione da HIV è l'interessamento della linea linfocitaria.
Effettivamente oltre alla riduzione numerica si notano anche vari fenomeni imputabili alla riduzione funzionale dei linfociti T:
- Riduzione della risposta proliferativa alla stimolazione antigenica,
- Sbilanciamento della risposta Th1 a favore di quella Th2. Ciò determina una riduzione dell'immunità cellulare a tutto vantaggio di quella umorale,
- Mancanza o riduzione della risposta T a opera di antigeni cui si era precedentemente suscettibili. Si ipotizza che ciò possa essere dovuto a una precoce deplezione dei linfociti CD4 di memoria probabilmente a causa della loro alta espressione del recettore CCR5.
Attualmente si ritiene che tutti questi fenomeni non abbiano una base univoca ma multifattoriale:
- è noto che l'HIV sia in grado di uccidere direttamente la cellula per lisi (effetto citopatico). Ciò potrebbe avvenire per accumulo eccessivo di particelle o materiale genetico o proteico di natura virale. Si pensa che a ciò si possa aggiungere un'inibizione eccedente dell'espressione proteica della cellula ospite
- l'HIV è in grado di generare sincizi per la fusione delle membrane cellulari di cellule infette tra loro oppure con cellule sane a causa del legame che si può formare tra gp120 e CD4. A seguito della fusione si determina un forte rigonfiamento e morte cellulare in poche ore. Sembrerebbe che la capacità di formare sincizi sia limitata solo ai ceppi T-tropici di HIV-1.
- la formazione di anticorpi contro proteine dell'envelope virale può essere responsabile della lisi di cellule esprimenti questi antigeni sulla loro superficie. Possono intervenire diversi fenomeni in quest'evento: la lisi mediata da linfociti T specifici o a opera di cellule citotossiche (NK, granulociti, fagociti mononucleati),
- apoptosi linfocitaria. Questo fenomeno coinvolgerebbe sia i linfociti T CD4+ sia quelli CD8+. Per i primi si sospetta il coinvolgimento del legame CD4-gp120 nella genesi del fenomeno cui si aggiunge l'attivazione linfocitaria per stimolazione del recettore per l'antigene (TCR) con conseguente aggregazione dei CD4 e scatenamento del fenomeno apoptotico. Nella genesi di questo fenomeno, tuttavia, sono coinvolti altri fattori. Varie proteine virali, env, vpr, nef, vpu e tat hanno dimostrato di indurre apoptosi in linfociti T non infetti sebbene tra essa si ritenga che in vivo l'azione più importante venga svolta da env. Anche l'attivazione del recettore CXCR4 riveste una certa importanza in quanto esso è in grado di indurre una cascata molecolare apoptotica indipendente dal recettore Fas. Altri studi, inoltre, hanno dimostrato che l'attivazione di CXCR4 è un evento importante nello sviluppo dell'apoptosi sia dei linfociti CD4+ sia CD8+.
- perdita dei precursori delle cellule immunitarie. Si ritiene che ciò possa avvenire o per infezione diretta delle o di cellule progenitrici situate nel timo o di cellule accessorie capaci di secernere citochine e fattori necessari al processo di differenziazione.
- si è notato un certo grado di omologia tra gp120, gp41 e gli antigeni HLA-DR e HLA-DQ. Ciò ha portato a ipotizzare che eventuali anticorpi contro le proteine virali possano cross-reagire con le proteine HLA espresse su linfociti specifici determinando, così, un blocco del legame di quest'ultimi con il recettore CD4 delle cellule infette cui segue un'inibizione di tipo funzionale,
- sembrerebbe che il legame di gp120 o gp41 sul CD4 sia in grado di inibire la funzione dei linfociti T helper rendendoli incapaci di rispondere alla stimolazione mediata da CD3,
- possibile legame di superantigeni di origine virale alla catena b del TCR con conseguente anergia linfocitaria.
In corso di infezione da HIV vengono a crearsi due compartimenti virologici distinti ma comunicanti:
- un compartimento attivo costituito dal virus libero nel sangue e da quello contenuto all'interno di linfociti caratterizzato da una replicazione virale elevata,
- un compartimento di latenza costituito da linee cellulari e zone anatomiche dell'organismo dove il virus resta in uno stato latente e che fungono, perciò, da serbatoi (reservoir).
Se il compartimento attivo gioca un ruolo importante nel danneggiare il sistema immunitario, quello di latenza è il principale responsabile della mancata eradicazione del virus dall'organismo.
I reservoir di HIV vengono suddivisi in cellulari e anatomici.
Quelli cellulari sono costituiti dalle cellule follicolari-dendritiche, dai linfociti CD4+ quiescenti e dai monociti-macrofagi.
Dei reservoir anatomici fanno parte, invece, il sistema nervoso centrale e i testicoli (sebbene altri compartimenti dell'organismo siano sospettati di avere una funzione simile).
Le cellule follicolari dendritiche sembrano avere un ruolo importante, almeno nelle prime fasi dell'infezione, a causa della loro funzione di presentazione dell'antigene, nel portare il virus a contatto con gli organi linfoidi o i linfociti CD4+. Oltre a ciò si è visto che sono capaci di trattenere sulla loro superficie un elevato quantitativo di virioni. Tuttavia in corso di terapia antiretrovirale tale numero si riduce drasticamente a tal punto che qualche autore sostiene che esse, in corso di terapia antiretrovirale efficace, perdano la loro funzione di reservoir o, al massimo, che diventi di secondo piano. È da notare, tuttavia, che tale conclusione non è unanimemente condivisa.
I linfociti CD4+ quiescenti possono essere infettati da HIV anche se le modalità di questo fenomeno non sono ancora chiare. I linfociti quiescenti vengono sottoposti a maturazione nel timo e da lì emergono rimanendo in uno stato latente fino all'incontro con l'antigene. Si ritiene che l'infezione col virus possa avvenire o nello stadio immaturo all'interno del timo (organo nel quale il virus è stato rintracciato) o nello stadio di quiescenza una volta completata la maturazione. In tal caso si ritiene che a causa dello stato di quiete della cellula il genoma virale si trovi nella forma non integrata. Un'altra ipotesi sostiene che il virus infetti linfociti attivi i quali, una volta concluso il loro stato di attività, possono andare incontro a uno stato di latenza, ammesso che siano riusciti a sopravvivere. In tal caso il genoma virale si trova nella forma integrata anche se non si ha produzione di virioni.
I monociti/macrofagi sono un compartimento sottoposto a un'infezione cronica e produttiva da parte di HIV, essendo poco sensibili agli effetti citopatici del virus. La continua produzione virale e la capacità dei monociti di veicolare il virus in quasi tutto l'organismo rendono tale compartimento il più importante nel mantenimento dell'infezione. È noto,inoltre, che i monociti/macrofagi sono la principale fonte di virus in caso di interruzione o fallimento della terapia antiretrovirale.
È noto che HIV si può ritrovare nel sistema nervoso centrale di individui infetti. Da alcuni dati si ipotizza che la penetrazione del virus possa avvenire in tempi molto precoci dopo l'ingresso nell'organismo. Nel sistema nervoso centrale l'infezione virale è limitata ai macrofagi e alle cellule della microglia mentre gli altri tipi cellulari non sembrano essere coinvolti (tranne gli astrociti la cui infezione, come si è affermato precedentemente, non è produttiva). L'assoluta particolarità del sistema nervoso centrale quale elemento di riserva di HIV la si evince anche dal fatto che il virus in esso presente è genotipicamente e
Il più delle volte l'exitus avviene a seguito delle infezioni opportunistiche tra cui più spesso per le polmoniti.
La terapia
Attualmente, l'infezione da HIV viene trattata con la cosiddetta highly active antiretroviral therapy (HAART) nella quale si utilizzano opportune combinazioni di farmaci antiretrovirali. Il suo utilizzo, a partire dal suo ingresso nel 1995, ha consentito di ridurre la morbilità e la mortalità degli individui che sono stati infettati dal virus. Tale terapia, inoltre, permette anche un miglioramento dei parametri immunitari con un netto aumento del linfociti CD4+ che sembra permanere fino a 4-5 anni cui si accompagna un abbassamento della carica virale plasmatica e liquorale.
L'utilizzo della HAART, tuttavia, in uno studio preliminare condotto su dieci persone infette da HIV-2 sembra avere una minore efficacia rispetto ai risultati che si ottengono con HIV-1.
Attualmente la terapia antiretrovirale utilizza farmaci appartenenti a quattro classi:
- gli inibitori della trascrittasi inversa, a loro volta distinti in inibitori nucleosidici, nucleotidici e non nucleosidici,
- gli inibitori della proteasi,
- gli inibitori della fusione,
- gli inibitori dell'integrasi.
Gli inibitori nucleosidici della trascrittasi inversa per esplicare la loro azione devono venir trifosforilati dalle chinasi endocellulari e successivamente competono con i desossinucleotidi endogeni durante il processo di retrotrascrizione. L'efficacia di tali composti dipende dalla concentrazione intracellulare loro e dei desossinucleotidi con cui si trovano a competere. Ciò significa che cellule come i macrofagi, che hanno un metabolismo limitato e in conseguenza di ciò una concentrazione molto bassa di desossinucleotidi, sono assai sensibili all'azione di tali farmaci.
Gli inibitori nucleotidici, di cui in Italia è registrato solo il Tenofovir si comportano come inibitori competitivi della trascrittasi inversa, come gli inibitori nucleosidici, ma, a differenza di quest'ultimi, presentano un gruppo fosfato legato a una purina o una pirimidina. Ciò permette l'eliminazione della prima tappa di fosforilazione semplificando le tappe di metabolizzazione riducendole a due. Anche tale categoria di farmaci, così come gli inibitori nucleosidici, presenta un'azione maggiore sui macrofagi che sui linfociti infettati. Si è visto che l'indice terapeutico del Tenofovir sui monociti/macrofagi si aggira intorno a 15000 mentre sui linfociti si situa su 20.
Gli inibitori non nucleosidici della trascrittasi inversa esplicano la loro attività legandosi direttamente al sito attivo dell'enzima determinandone il blocco dell'azione. Tali farmaci sono indipendenti dal metabolismo cellulare in quanto non necessitano di alcuna modificazione e non risentono della concentrazione di dessosinucleotidi. A seguito di ciò il loro effetto su monociti/macrofagi e linfociti sembra essere equivalente.
Gli inibitori della proteasi vanno a bloccare l'ultima parte del ciclo replicativo di HIV in quanto impediscono la maturazione delle proteine virali. Ciò determina un blocco dell'assemblaggio e del rilascio di nuovi virioni. Un tale meccanismo d'azione fa sì che gli inibitori della proteasi siano utili in tutte quelle situazioni in cui le fasi iniziali del ciclo virale sono già passate rendendo perciò inutile l'uso degli inibitori della trascrittasi inversa. Una simile situazione si rinviene nei macrofagi i quali, come si è visto precedentemente, fungono da reservoir di HIV ai cui effetti citopatici sono poco sensibili. In tali cellule il genoma virale è già integrato in quello dell'ospite per cui gli unici composti in grado di bloccare la replicazione virale a questo livello attualmente sono gli inibitori della proteasi. Sfortunatamente la concentrazione efficace di questi composti sui monociti/macrofagi e maggiore di quella dei linfociti CD4+ attivi e spesso sono equivalenti alle massime concentrazioni plasmatiche raggiungibili in vivo. Ciò non solo può favorire la comparsa di effetti avversi ma può anche rendere ragione del fatto che in alcuni distretti dell'organismo l'inibizione della replicazione virale nei monociti/macrofagi ottenuta in tal modo sia incompleta.
Gli inibitori della fusione sono una categoria di farmaci di cui, al momento, l'unico esponente è l'Enfuvirtide, determinano un blocco del processo di fusione del virus con la membrana della cellula ospite. Questo processo si articola in tre fasi: aggancio, legame ai corecettori e fusione delle membrane. Enfuvirtide è un peptide che mima un motivo della proteina gp41. Quando la proteina gp120 si aggancia ai suoi recettori, gp41 subisce una serie di cambiamenti conformazionali che culminano nella formazione di una struttura a tre foglietti β che funziona da ponte tra il virione e la cellula da infettare. Enfuvirtide determina un blocco della regione amino-terminale della gp41 impedendo la formazione dei tre foglietti.
Gli inibitori dell'integrasi rappresentano una nuova categoria di farmaci che agiscono nella fase cosiddetta di "integrazione", ossia la fase in cui il DNA sintetizzato del virus si inserisce nel genoma della cellula ospite. Un esempio di questa classe di farmaci è il Raltegavir, che è stato anche il primo farmaco di questa categoria.
Sintomatologia
I primi sintomi dell'AIDS sono simili a quelli che si sviluppano in soggetti con un normale sistema immunitario. La maggior parte sono infezioni causate da batteri, virus, funghi, parassiti e altri organismi[43]. Negli individui affetti da AIDS sono comuni le infezioni opportunistiche, e aumenta il rischio di sviluppare varie forme di tumore come il Sarcoma di Kaposi, tumori del cervello e linfomi. Sintomi comuni sono febbre, sudorazione specie notturna, ingrossamento ghiandolare, tremore, debolezza e perdita di peso[44]. Senza il supporto terapeutico la morte sopravviene entro un anno[45]. La maggior parte dei pazienti muore per infezioni opportunistiche dovute al progressivo indebolimento del sistema immunitario[46]. Si ritiene che il trattamento terapeutico denominato HAART consenta un incremento dell'aspettativa di vita medio attorno ai 30 anni[47] o, secondo alcuni studi, anche oltre[48].
Definizione di AIDS e infezione da HIV
Fin dal 1982 sono state coniate varie definizioni per il monitoraggio epidemiologico dell'infezione: tra queste la definizione Bangui e quella dell'Organizzazione Mondiale della Sanità datata 1994. Tuttavia, non sono da intendersi come utili per la classificazione clinica dei pazienti, in quanto non sono appropriate e specifiche. Il sistema di classificazione usato dall'Organizzazione Mondiale della Sanità e quello del CDC Centers for Disease Control può essere utilizzato solo nei paesi sviluppati.
Classificazione delle infezioni e malattie da HIV dell'OMS
Nel 1990, l'Organizzazione Mondiale della Sanità (OMS) ha raggruppato i diversi tipi di casi definendo una scala per i pazienti affetti da HIV-1. Questa è stata aggiornata nel settembre del 2005. La maggior parte di queste infezioni opportunistiche può essere facilmente curata in soggetti altrimenti sani.
- Stadio I: l'infezione da HIV è asintomatica e non categorizzata come AIDS
- Stadio II: include minori manifestazioni mucocutanee e ricorrenti infezioni del tratto respiratorio superiore
- Stadio III: include diarrea cronica prolungata per oltre un mese, gravi infezioni batteriche e tubercolosi
- Stadio IV: include toxoplasmosi del cervello, candidosi di esofago, trachea, bronchi o polmoni e sarcoma di Kaposi; queste patologie sono usate come indicatori dell'AIDS.
Sistema di Classificazione delle Infezioni da HIV secondo i CDC
Negli USA, la definizione di AIDS è governata dai Centers for Disease Control and Prevention (CDC). Nel 1993, i CDC allargarono la loro definizione di AIDS andando a includere persone sane ma positive al test per l'HIV, e con un numero di linfocitiT CD4+ inferiore a 200 per µl di sangue. La maggioranza dei nuovi casi di AIDS negli Stati Uniti sono diagnosticati quando si ha un basso numero di linfociti T ed è presente una infezione da HIV[49].
Manifestazioni cliniche dell'AIDS

Le principali patologie polmonari
- Polmonite da Pneumocystis jiroveci
- Tubercolosi
- Parotite
Le principali infezioni del tratto gastro-intestinale
Le principali patologie neurologiche
Trasmissione
Dagli inizi dell'epidemia, sono state individuate principalmente tre vie di trasmissioni dell'HIV:
- Sessualmente. La maggior parte delle infezioni del virus dell'HIV avvenne, e avviene tuttora, attraverso rapporti sessuali non protetti. La trasmissione sessuale può insorgere quando c'è contatto fra le secrezioni sessuali di un partner infetto con le mucose genitali, della bocca (cunnilingus e fellatio) o del retto dell'altro. Nonostante la probabilità di trasmissione non sia elevata, il grande numero di esposizioni di questo tipo fa sì che sia la causa prevalente della diffusione del virus.
- Sangue e suoi derivati. Questa via di trasmissione è particolarmente importante per gli utilizzatori di droghe introvenose, emofiliaci e riceventi di trasfusioni di sangue e suoi derivati. In particolare, la trasmissione si ha con lo stretto e diretto contatto tra ferite aperte e sanguinanti oppure in casi come lo scambio di siringhe infette,[50] quindi il virus non si trasmette tramite contatti come strette di mano, abbracci, baci, morsi, graffi[51] né tramite l'uso di rasoi o spazzolini da denti di persone sieropositive (se privi di tracce ematiche), anche se è comunque sempre consigliabile l'uso di strumenti di igiene personale individuali[52].
Anche gli operatori del settore sanitario (infermieri, tecnici di laboratorio, dottori etc) sono coinvolti, sebbene più raramente. È interessato da questa via di trasmissione anche chi pratica o si fa praticare tatuaggi e piercing. - Madre-figlio. La trasmissione del virus da madre a figlio può accadere in utero durante le ultime settimane di gestazione e alla nascita. Anche l'allattamento al seno presenta un rischio di infezione per il bambino. In assenza di trattamento, il tasso di trasmissione tra madre e figlio è del 25%. Tuttavia, dove un trattamento viene effettuato, combinandolo con la possibilità di un parto cesareo, il rischio è stato ridotto all'1%.
L'HIV è stato trovato nella saliva, lacrime e urina di individui infetti, ma vista la bassa concentrazione del virus in questi liquidi biologici, il rischio di trasmissione è considerato trascurabile. Lo stesso vale per tosse, sudore, muco e feci.[51]
Si noti che il virus non si trasmette tramite vestiti, asciugamani, lenzuola, né tramite bicchieri, piatti o posate.[51]
Le zanzare, da sempre sospettate di essere un possibile veicolo di infezione, in realtà sono sostanzialmente innocue, sia perché il virus non si può replicare all'interno delle ghiandole salivari dell'insetto (trasmissione biologica)[53] sia per via della bassissima probabilità di infezione: è stato calcolato che una persona dovrebbe essere punta da 10 milioni di zanzare (portatrici del virus) per avere una probabilità di essere infettato.[54] Questa falsa credenza è diffusa nei paesi meno sviluppati.[55] Le zanzare sono in effetti responsabili della trasmissione di altre patologie a eziologia virale come per esempio dengue e febbre gialla per le quali però si verificano epidemie stagionali.
La zanzara femmina (il maschio non punge) dopo aver nutrito le uova nel proprio addome con il sangue aspirato, riposa per circa 24 ore, tempo sufficiente alla scomparsa del virus dall'insetto madre. Anche qualora la zanzara punga due individui in successione di cui il primo sieropositivo, la possibilità di contagio (trasmissione meccanica) è nulla perché il canale attraverso cui viene iniettata la saliva e quello attraverso il quale viene prelevato il sangue sono due condotti differenti, non in comunicazione tra di loro. Un discorso analogo può essere fatto anche per altri artropodi ematofagi come pulci, zecche e cimici.
Prevenzione
Non esistono attualmente farmaci in grado di prevenire l'infezione del virus HIV quindi il miglior modo di prevenire l'AIDS è evitare tutte quelle situazioni che permettono la trasmissione del virus dell'immunodeficienza. In particolare per evitare il contatto fra le secrezioni sessuali di un partner infetto con le mucose genitali bisogna evitare i rapporti non protetti e, per fare ciò, è necessario l'uso del preservativo maschile e del Il preservativo femminile.
Profilassi post-esposizione
In caso di possibile esposizione al virus, subito dopo un evento a rischio in base alle vie di trasmissione appena descritte, è possibile sottoporsi a un particolare trattamento farmacologico noto come profilassi post-esposizione, in grado di ridurre notevolmente le probabilità di contagio, se applicato correttamente e nei tempi appropriati.
Cura
Al momento non si guarisce dall'HIV o dall'AIDS e non esistono vaccini. L'infezione da HIV porta all'AIDS ed, alla fine, al decesso. Tuttavia nei paesi occidentali la maggior parte dei pazienti sopravvive per molti anni dopo la diagnosi grazie alla disponibilità sul mercato della terapia antiretrovirale a elevata attività (Highly Active Antiretroviral Therapy o HAART[56]). In mancanza della HAART, il passaggio dall'infezione da HIV all'AIDS si verifica in un arco di tempo che va dai 9 ai dieci anni e il tasso medio di sopravvivenza dopo che si sviluppa l'AIDS è di 9.2 mesi (Morgan e altri, 2002b). La HAART aumenta notevolmente il tempo che intercorre dalla diagnosi alla morte mentre continua la ricerca volta allo sviluppo di nuovi farmaci e di vaccini.
Le migliori possibilità offerte attualmente dalla HAART consistono in combinazioni o "cocktail" di farmaci in gruppi di almeno tre medicinali appartenenti ad almeno due famiglie, o "classi" di agenti antiretrovirali. I regimi tipici consistono in due analoghi nucleosidici della trascrittasi inversa (nucleoside analogue reverse transcriptase inhibitors, NRTI) insieme a un inibitore della proteasi oppure un analogo non nucleosidico della trascrittasi inversa (non nucleoside reverse transcriptase inhibitor, NNRTI).
I trattamenti antiretrovirali, congiuntamente alle cure mirate alla prevenzione delle infezioni che approfittano delle vulnerabilità create dall'AIDS hanno avuto un certo ruolo nel ritardare l'insorgenza delle complicanze associate all'AIDS, riducendo i sintomi ed estendendo la vita dei pazienti. Negli ultimi dieci anni si è riusciti a prolungare e a migliorare la qualità di vita delle persone affette da AIDS con risultati notevoli. [1], [2].
Tuttavia, le linee guida per il trattamento cambiano costantemente. Le linee guida attuali per la terapia antiretrovirale dell'Organizzazione Mondiale della Sanità riflettono i cambiamenti apportati alle linee-guida nel 2003 poiché in strutture in cui le risorse a disposizione sono limitate (per es. nei paesi in via di sviluppo) ad adulti e adolescenti infettati dall'HIV si raccomanda di iniziare a sottoporsi alla terapia ARV (antiretrovirale) quando l'infezione da HIV sia confermata e sia presente una delle seguenti condizioni:
- Infezione da HIV in fase avanzata:
- Fase 4 dell'infezione da HIV (secondo le norme OMS), a prescindere dalla percentuale di linfociti T di tipo CD4+;
- Fase 3 dell'infezione da HIV (secondo le norme OMS) attuando trattamenti definiti in base al tasso rilevato di linfociti T di tipo CD4 quando questo risulti inferione ai 350/µl;
- Fase 1 o 2 dell'infezione da HIV (secondo le norme OMS) attuando trattamenti definiti in base al quantitativo rilevato di linfociti T di tipo CD4+, quando questo risulti inferiore a 200/µl.
Lo U.S. Department of Health and Human Services (Dipartimento della Sanità e dei Servizi Sociali degli Stati Uniti), l'agenzia federale responsabile del controllo delle politiche sull'HIV/AIDS negli Stati Uniti, ha reso noto in data 6 ottobre 2005 quanto segue:
- Tutti i pazienti con precedenti di patologie da cui si desume l'effetto dell'AIDS o con sintomi severi di infezione da HIV a prescindere dal loro tasso di linfociti T di tipo CD4+ devono venir trattati con la ART (terapia antiretrovirale).
- La terapia antiretrovirale è anche consigliata per i pazienti asintomatici con una conta di linfociti T tipo CD4+ inferiore a 200/µl;
- I pazienti asintomatici con percentuale di linfociti T tipo CD4+ maggiore di 201-350/µl debbono ricevere cure dopo una valutazione rischio-beneficio e in accordo con i desideri del paziente;
- Per i pazienti asintomatici con un tasso di linfociti T tipo CD4+ superiore a 350/µl e con HIV RNA nel plasma maggiore a 100,000 copie/ml la maggior parte dei medici rimandano le misure terapeutiche ma secondo alcuni si potrebbe dare il via al trattamento.
- Si raccomanda di differire la terapia per i pazienti con un tasso di linfociti T tipo CD4+ superiore a >350/µl con RNA HIV inferiore a 100.000 copie/ml.
Il regime preferenziale con cui iniziare è uno dei due seguenti:
- enfavirez + lamivudina o emtricitabina + zidovudina o tenofovir; altrimenti
- lopinavir rafforzato da ritonavir + zidovudina + lamivudina o emtricitabine.
Inoltre, il DHHS consiglia ai dottori di accertare la carica virale, la rapidità del declino dei linfociti CD4+ e il grado di risposta del paziente nel decidere quando iniziare il trattamento. [3]
Ci sono non poche preoccupazioni sui regimi antiretrovirali. Le medicine possono avere seri effetti collaterali[57]. I regimi possono essere complessi, e imporre al paziente di assumere pillole diverse volte al giorno. Se il paziente non assume la terapia correttamente, può svilupparsi una certa resistenza al farmaco[58]. Inoltre, i farmaci retrovirali sono costosi e la maggior parte degli individui infetti nel mondo non hanno accesso alle medicine e ai trattamenti per l'HIV e l'AIDS.
La ricerca volta a migliorare i trattamenti attuali si occupa di diminuire gli effetti collaterali degli attuali medicinali, semplificare i regimi farmacologici per migliorarne l'effetto e determinare l'ordine ottimale tra una cura e l'altra per contenere la resistenza ai farmaci.
In lingua italiana, è possibile scaricare anche il documento del Ministero della Salute di dicembre 2005
"Aggiornamento delle conoscenze in tema di terapia antiretrovirale" dal seguente indirizzo: http://www.ministerosalute.it/aids/resources/aids/documenti/terapiaAIDS.pdf
Da quando l'AIDS è entrato nella coscienza collettiva sono state utilizzate diverse forme di medicina alternativa per cercare di curare i suoi sintomi. Nel primo decennio dell'epidemia quando nessuna cura convenzionale era disponibile, molte persone affette da AIDS hanno sperimentato terapie alternative (massaggio, medicine a base di erbe e fiori, l'agopuntura). Tuttavia, nessuna di queste ha dimostrato di avere alcun effetto positivo nel trattamento dell'HIV.
Test HIV
Quasi la metà delle persone infette da HIV non sa di esserlo finché non viene loro diagnosticato l'AIDS. I kit per il test dell'HIV sono usati per monitorare il sangue dei donatori e i derivati dal sangue, ma anche per diagnosticare, curare e sottoporre a controlli pazienti con HIV. I test dell'HIV rilevano la presenza di anticorpi HIV, di antigeni HIV o dell'HIV nel siero, plasma, nei fluidi orali, su macchie di sangue essiccato o nell'urina dei pazienti.
Origine dell'HIV/AIDS
La data ufficiale che segna l'inizio dell'epidemia dell'AIDS è il 5 giugno 1981, quando il centro per il monitoraggio e la prevenzione delle malattie degli Stati Uniti identificò un'epidemia di pneumocistosi polmonare dovute a pneumocystis carinii (ora riclassificato come Pneumocystis jirovecii) in cinque uomini gay di Los Angeles. Benché la sindrome fosse stata chiamata inizialmente GRID, o Gay-Related Immune Deficiency (cioè immunodeficienza dei gay), le autorità sanitarie si accorsero ben presto che quasi metà[senza fonte] della popolazione in cui era stata riscontrata non era omosessuale. Nel 1982 il CDC introdusse il termine AIDS per descrivere più esaustivamente la sindrome appena scoperta.
Tre dei primi casi noti di infezione da HIV risalgono a:
- Un campione di plasma estratto nel 1959 da un adulto maschio residente nell'attuale Repubblica Democratica del Congo[59].
- Campioni di tessuto contenenti l'HIV, estratto da un adolescente di nazionalità statunitense morto a Saint Louis nel 1969.
- Campioni di tessuto contenenti l'HIV estratti da un marinaio norvegese morto intorno al 1976.
Sono due le specie di HIV che infettano gli esseri umani: l'HIV-1 e l'HIV-2. L'HIV-1 è più virulento e si trasmette più facilmente. L'HIV-1 è la fonte della maggioranza delle infezioni da HIV nel mondo, mentre l'HIV-2 si trasmette meno facilmente, è più antico ed è per lo più diffuso nell'Africa occidentale[60]. Sia l'HIV-1 sia l'HIV-2 derivano da virus analoghi che infettano i primati. L'HIV-1 deriva da un virus dello Scimpanzé comune (Pan troglodytes troglodytes). L'origine dell'HIV-2 è attribuita con certezza al Cercocebus atys (ing. Sooty Mangabey), un cercopiteco presente in Guinea Bissau, Gabon e Camerun
Ricerca
Ultime scoperte
Il 10% della popolazione europea presenta una variante genetica, la d32, che produce un numero scarso di proteine-recettori CCR5 sui globuli bianchi. Ciò non provoca nessun disturbo alla salute, tanto che la grande diffusione della variante d32 è stata notata solo dopo la comparsa dell'AIDS, in quanto chi ha meno recettori CCR5 sui globuli bianchi corre meno rischi di essere infettato dal virus HIV. La genetista Alison Galvani, della Yale University, ipotizza che la variante genetica che protegge dall'HIV protegga anche da un altro killer, il vaiolo, un virus che condivide importanti caratteristiche con l'HIV. Analizzando la diffusione del vaiolo in Europa la ricercatrice ha scoperto che essa coincide con l'attuale prevalenza della variante D32 nel continente. Questa mutazione, quindi, potrebbe essere stata selezionata in passato come difesa contro un virus per poi venire utile in seguito contro un altro.
Piante transgeniche
Le piante transgeniche che esprimono uno o più geni dei virus dell'AIDS possono rappresentare un'efficace strategia per produrre un vaccino contro questa malattia, di fatto sono state già prodotte piante che esprimono antigeni che si sono rivelate efficaci nell'indurre la sintesi di anticorpi specifici. Le piante transgeniche sono superiori rispetto ad altri metodi per produrre vaccini perché nel tempo sono più economiche e producono più antigeni[61][62]
Una guarigione
Timothy Ray Brown, paziente americano (residente in Germania) infettato dall'HIV e da leucemia sembra avere di recente ottenuto grandi benefici da un trapianto di midollo proveniente da un donatore della variante genetica delta 32. Dopo quasi due anni dal trapianto del midollo sia la leucemia che il virus sembrano scomparsi.[63]
Ipotesi alternative sull'Aids
Una piccola minoranza di autori ha messo in discussione, con argomentazioni che sono però state ripetutamente dimostrate essere prive di fondamento scientifico, biologico o clinico, la connessione tra HIV e AIDS, l'esistenza del virus, o la validità delle attuali metodologie diagnostiche. I cosiddetti "dissidenti" criticano l'attuale approccio all'AIDS basato su HIV, affermando che, a loro parere, avrebbe causato diagnosi inaccurate, trattamenti inadeguate e dispendio di fondi pubblici.
Queste considerazioni hanno ricevuto forti smentite dalla comunità medica internazionale e dall'evidenza scientifica oggettiva, dalla quale emerge come i cosiddetti "dissidenti" ignorino del tutto le chiare evidenze scientifiche sul ruolo causale dell'HIV nell'etiopatogenesi dell'AIDS, e di essere anzi loro a rappresentare, con le loro tesi indimostrate e palesemente incoerenti, una seria minaccia per la salute pubblica.
L'emergere di tali idee "negazioniste" ha portato quindi, da parte di oltre 5.000 tra medici e scienziati (tra cui 11 vincitori di Premio Nobel), alla sottoscrizione dell'importante documento noto come Dichiarazione di Durban, nel quale si afferma che il legame causale tra HIV e AIDS è chiaramente definito, esaustivo e univoco.
Le conseguenze pericolose del "negazionismo" si sono infatti manifestate in maniera lampante in Sudafrica, dove politiche sanitarie relative all'AIDS basate su un approccio negazionista, e sull'uso di inefficaci rimedi tradizionali, hanno portato a un'enorme diffusione del virus HIV: si stima che il 20% della popolazione adulta sia sieropositivo[5], contro il 6,1% medio dell'Africa subsahariana[64].
Note
- ^ Sepkowitz KA, AIDS—the first 20 years, in N. Engl. J. Med., vol. 344, n. 23, giugno 2001, pp. 1764–72, DOI:10.1056/NEJM200106073442306, PMID 11396444.
- ^ Weiss RA, How does HIV cause AIDS?, in Science, vol. 260, n. 5112, maggio 1993, pp. 1273–9, Bibcode:1993Sci...260.1273W, DOI:10.1126/science.8493571, PMID 8493571.
- ^ Russell Cecil, Textbook of Medicine, Philadelphia, Saunders, 1988, pp. 1523, 1799, ISBN 0721618480.
- ^ Robert Gallo. A caccia di virus. Milano, Rizzoli, 1992.
- ^ a b Michael Specter. AIDS. Le cure negate, Le Scienze, 468, 58.
- ^ Campbell et al., 2004; Campbell et al., 2005; Senkaali et al., 2005
- ^ Clerici et al., 1996; Morgan et al., 2002a; Tang et al., 2003
- ^ Morgan et al., 2002b; Lawn et al., 2004
- ^ Palella et al., 1998
- ^ Montessori et al., 2004
- ^ Gottlieb MS, Pneumocystis pneumonia—Los Angeles. 1981, in Am J Public Health, vol. 96, n. 6, 2006, pp. 980–1; discussion 982–3. URL consultato il March 31, 2009.
- ^ Errore nelle note: Errore nell'uso del marcatore
<ref>: non è stato indicato alcun testo per il marcatoreMMWR1982a - ^ Errore nelle note: Errore nell'uso del marcatore
<ref>: non è stato indicato alcun testo per il marcatoreBarre - ^ Altman LK, New homosexual disorder worries health officials, in The New York Times, May 11, 1982. URL consultato il August 31, 2011.
- ^ Making Headway Under Hellacious Circumstances (PDF), su scienceonline.org, American Association for the Advancement of Science, July 28, 2006. URL consultato il June 23, 2008.
- ^ Kher U, A Name for the Plague, in Time, July 27, 1982. URL consultato il March 10, 2008.
- ^ Centers for Disease Control (CDC), Update on acquired immune deficiency syndrome (AIDS)—United States, in MMWR Morb Mortal Wkly Rep., vol. 31, n. 37, 1982, pp. 507–508; 513–514.
- ^ Errore nelle note: Errore nell'uso del marcatore
<ref>: non è stato indicato alcun testo per il marcatoreWorobey - ^ Gilbert MT, Rambaut A, Wlasiuk G, Spira TJ, Pitchenik AE, Worobey M, The emergence of HIV/AIDS in the Americas and beyond, in Proc. Natl. Acad. Sci. U.S. A., vol. 104, n. 47, 2007, pp. 18566–70, DOI:10.1073/pnas.0705329104.
- ^ Kalish ML, Central African hunters exposed to simian immunodeficiency virus, in Emerg Infect Dis, vol. 11, n. 12, 2005, pp. 1928–30, DOI:10.3201/eid1112.050394.
- ^ The origins of acquired immune deficiency syndrome viruses: where and when?, in Philosophical Transactions of the Royal Society B: Biological Sciences, vol. 356, n. 1410, 2001, pp. 867–76, DOI:10.1098/rstb.2001.0863.
- ^ Marx PA, Alcabes PG, Drucker E, Serial human passage of simian immunodeficiency virus by unsterile injections and the emergence of epidemic human immunodeficiency virus in Africa, in Philos Trans R Soc Lond B Biol Sci, vol. 356, n. 1410, 2001, pp. 911–20, DOI:10.1098/rstb.2001.0867.
- ^ Origin of HIV Type 1 in Colonial French Equatorial Africa?, in AIDS Research and Human Retroviruses, vol. 16, n. 1, 2000, pp. 5–8, DOI:10.1089/088922200309548.
- ^ High GUD Incidence in the Early 20th Century Created a Particularly Permissive Time Window for the Origin and Initial Spread of Epidemic HIV Strains, in PLoS ONE, vol. 5, n. 4, 2010, pp. e9936, DOI:10.1371/journal.pone.0009936.
- ^ Donald G. McNeil, Jr., Precursor to H. I. V. Was in Monkeys for Millennia, in New York Times, September 16, 2010. URL consultato il September 17, 2010.
- ^ Anthony Eden, su nndb.com. URL consultato il November 1, 2011.
- ^ Brian Coleman, Thatcher the gay icon, in New Statesman, June 25, 2007. URL consultato il November 1, 2011.
- ^ BBC ON THIS DAY | 24 | 1991: Giant of rock dies, BBC News, November 24, 1963. URL consultato il November 1, 2011.
- ^ Freddie Mercury, su nndb.com. URL consultato il November 1, 2011.
- ^ The Independent, February 8, 1993, http://www.independent.co.uk/news/tributes-to-arthur-ashe-1471622.html.
- ^ Curtis T, The origin of AIDS, in Rolling Stone, p. 54–59, 61, 106, 108. URL consultato il March 10, 2008.
- ^ Hooper E, The River: A Journey to the Source of HIV and AIDS, 1st, Boston, Massachusetts, Little Brown & Co, 1999, pp. 1–1070, ISBN 0-316-37261-7.
- ^ Worobey M, Origin of AIDS: contaminated polio vaccine theory refuted, in Nature, vol. 428, n. 6985, 2004, DOI:10.1038/428820a.
- ^ Berry N, Mitochondrial DNA and retroviral RNA analyses of archival oral polio vaccine (OPV CHAT) materials: evidence of macaque nuclear sequences confirms substrate identity, in Vaccine, vol. 23, n. 14, 2005, pp. 1639–1648, DOI:10.1016/j.vaccine.2004.10.038.
- ^ Oral Polio Vaccine and HIV / AIDS: Questions and Answers, su cdc.gov, Centers for Disease Control and Prevention, March 23, 2004. URL consultato il November 20, 2006.
- ^ a b Kallings LO, The first postmodern pandemic: 25 years of HIV/AIDS, in J Intern Med, vol. 263, n. 3, 2008, pp. 218–43, DOI:10.1111/j.1365-2796.2007.01910.x.
- ^ a b c d e UNAIDS, WHO, 2007 AIDS epidemic update (PDF), su data.unaids.org, December 2007. URL consultato il March 12, 2008.
- ^ McNeil DG Jr, U. N. agency to say it overstated extent of H. I. V. cases by millions, in New York Times, November 20, 2007. URL consultato il March 18, 2008.
- ^ Report: Black U.S. AIDS rates rival some African nations
- ^ "DTL&feed=rss. news_politics White House summit on AIDS' impact on black men[collegamento interrotto]". San Francisco Chronicle. June 3, 2010.
- ^ a b http://www.cdc.gov/hiv/topics/surveillance/resources/reports/2005report/pdf/2005SurveillanceReport.pdf
- ^ "Obama Ends U.S. Travel Ban On Visitors, Immigrants With HIV-AIDS". ABC News. October 30, 2009.
- ^ Holmes et al., 2003
- ^ Guss, 1994a; 1994b
- ^ Morgan et al., 2002b
- ^ Lawn et al., 2004
- ^ Nell'era della HAART aspettativa di vita maggiore di 30 anni, 29 gennaio 2010
- ^ (EN) HAART increases HIV-positive people's life expectancy by average of 13 years, 29 luglio 2008. L'articolo stima in 43 anni l'aspettativa di vita.
- ^ MMWR, 1992
- ^ Ministero della Salute, Hiv e Aids - Come si trasmette il virus, su salute.gov.it. URL consultato il 1º dicembre 2011.
- ^ a b c Ministero della Salute, Hiv e Aids - Come non si trasmette il virus, su salute.gov.it. URL consultato il 1º dicembre 2011.
- ^ Ministero della Salute, Prevenzione e controlli - Promozione della salute - AIDS - Faq, su salute.gov.it. URL consultato il 1º dicembre 2011.
- ^ Iqbal MM., Can we get AIDS from mosquito bites?, in J La State Med Soc., vol. 151, agosto 1999.
- ^ Bockarie MJ, Paru R., Can mosquitoes transmit AIDS?, in P N G Med J., vol. 39, 1996, pp. 205-207.
- ^ Mazloomy SS, Baghianimoghadam MH., Knowledge and attitude about HIV/ AIDS of schoolteachers in Yazd, Islamic Republic of Iran., in East Mediterr Health J., vol. 14, marzo-aprile 2008, pp. 292-297..
- ^ Schneider e altri, 2005
- ^ Saitoh et al., 2005
- ^ Dybul et al., 2002
- ^ Zhu et al., 1998
- ^ Reeves and Doms, 2002
- ^ Plant-based anti-HIV-1 strategies: vacci... [Expert Rev Vaccines. 2010] - PubMed - NCBI
- ^ Is there a role for plant-made vaccines in... [Immunol Cell Biol. 2005] - PubMed - NCBI
- ^ German HIV patient cured after stem cell transplant - World news, News - Belfasttelegraph.co.uk
- ^ UNAIDS: 2006 Report on the global AIDS epidemic
Bibliografia
- Becker, S., Dezii, C. M., Burtcel, B., Kawabata, H. and Hodder, S. (2002) Young HIV-infected adults are at greater risk for medication nonadherence. MedGenMed. 4, 21 PMID 12466764
- Campbell, G. R., Pasquier, E., Watkins, J., Bourgarel-Rey, V., Peyrot, V., Esquieu, D., Barbier, P., de Mareuil, J., Braguer, D., Kaleebu, P., Yirrell, D. L. and Loret E. P. (2004) The glutamine-rich region of the HIV-1 Tat protein is involved in T-cell apoptosis. J. Biol. Chem. 279, 48197-48204 PMID 15331610
- Campbell, G. R., Watkins, J. D., Esquieu, D., Pasquier, E., Loret, E. P., Spector, S. A. (2005) The C terminus of HIV-1 Tat modulates the extent of CD178-mediated apoptosis of T cells. J. Biol. Chem. 280, 38376-39382 PMID 16155003
- Adachi A, Gendelman HE, Koenig S, Folks T, Willey R, Rabson A, Martin MA. (1986) Production of acquired immunodeficiency syndrome-associated retrovirus in human and nonhuman cells transfected with an infectious molecular clone. J Virol. 59, 284-291 PMID 3016298
- Aldrovandi GM, Feuer G, Gao L, Jamieson B, Kristeva M, Chen IS, Zack JA. (1993) The SCID-hu mouse as a model for HIV-1 infection. Nature 363, 732-736 PMID 8515816
- Baumann E, Bethell T, Bialy H, Duesberg PH, Farber C, Geshekter CL, Johnson PE, Maver RW, Schoch R, Stewart GT, et al. (1995) AIDS proposal. Group for the Scientific Reappraisal of the HIV/AIDS Hypothesis. Science 267, 945-946 PMID 7863335
- Busch MP, Eble BE, Khayam-Bashi H, Heilbron D, Murphy EL, Kwok S, Sninsky J, Perkins HA, Vyas GN. (1991) Evaluation of screened blood donations for human immunodeficiency virus type 1 infection by culture and DNA amplification of pooled cells. N Engl J Med 325, 1-5 PMID 2046708
- Canaani E, Tronick SR, Robbins KC, Andersen PR, Dunn CY, Aaronson SA. (1980) Cellular origin of the transforming gene of Moloney murine sarcoma virus. Cold Spring Harb Symp Quant Biol. 44 Pt 2, 727-734 PMID 6253207
- Ciesielski CA, Marianos DW, Schochetman G, Witte JJ, Jaffe HW. (1994) The 1990 Florida dental investigation. The press and the science. Ann Intern Med 121, 886-888 PMID 7978703
- Cohen J. (1994) The Duesberg phenomenon. Science 266, 1642-1644 PMID 7992043
- Cohen J. (1994a) Duesberg and critics agree: Hemophilia is the best test. Science 266, 1645-1646 PMID 7992044
- Cohen J. (1994b) Fulfilling Koch's postulates. Science 266, 1647 PMID 7992045
- Cohen J. (1994c) The epidemic in Thailand. Science 266, 1647 PMID 7992046
- Cohen J. (1994d) Could drugs, rather than a virus be the cause of AIDS? Science 266, 1648-1649 PMID 7992047
- Duesberg PH. (1987) Retroviruses as carcinogens and pathogens: expectations and reality. Cancer Res 47, 1199–220 PMID 3028606
- Duesberg PH. (1988) HIV is not the cause of AIDS. Science 241, 514, 517 PMID 3399880
- Duesberg PH. (1989) HIV and AIDS: correlation but not causation. Proceedings of the National Academy of Sciences 86, 755–64 PMID 2644642
- Duesberg PH. (1992) AIDS acquired by drug consumption and other noncontagious risk factors. Pharmacol Ther. 55, 201-277 PMID 1492119
- Duesberg PH. (1996a) Inventing the AIDS virus. Regnery Publishing, Inc.
- Duesberg PH. (1996b) AIDS: Virus or Drug Induced?Springer
- Papadopulos-Eleopulos E, Turner VF, Papadimitriou J, Page B, Causer D, Alfonso H, Mhlongo S, Miller T, Maniotis A, Fiala C. (2004) A critique of the Montagnier evidence for the HIV/AIDS hypothesis. Med Hypotheses 63, 597-601 PMID 15325002
- Galéa P and Chermann JC (1998) HIV as the cause of AIDS and associated diseases Genetica 104, 133-142 PMID 10220906
- Grisson RD, Chenine AL, Yeh LY, He J, Wood C, Bhat GJ, Xu W, Kankasa C, Ruprecht RM. (2004) Infectious molecular clone of a recently transmitted pediatric human immunodeficiency virus clade C isolate from Africa: evidence of intraclade recombination. J Virol. 78, 14066-14069 PMID 15564517
- Horton R. (1995) Will Duesberg now concede defeat? Lancet 346, 656 PMID 7658817
- Hirsch VM, Johnson PR. (1994) Pathogenic diversity of simian immunodeficiency viruses. Virus Res. 32, 183-203 PMID 8067053
- Jackson JB, Kwok SY, Sninsky JJ, Hopsicker JS, Sannerud KJ, Rhame FS, Henry K, Simpson M, Balfour HH Jr. (1990) Human immunodeficiency virus type 1 detected in all seropositive symptomatic and asymptomatic individuals. J Clin Microbiol. 28, 16-19 PMID 2298875
- Jaffe HW, Darrow WW, Echenberg DF, O'Malley PM, Getchell JP, Kalyanaraman VS, Byers RH, Drennan DP, Braff EH, Curran JW, et al. (1985) The acquired immunodeficiency syndrome in a cohort of homosexual men. A six-year follow-up study. Ann Intern Med. 103, 210-214 PMID 2990275
- Joag SV, Li Z, Foresman L, Stephens EB, Zhao LJ, Adany I, Pinson DM, McClure HM, Narayan O. (1996) Chimeric simian/human immunodeficiency virus that causes progressive loss of CD4+ T cells and AIDS in pig-tailed macaques. J. Virol. 70, 3189-3197 PMID 8627799
- Koch R. (1884) Mitt Kaiser Gesundh 2, 1-88
- Koch R. (1893) J. Hyg. Inf. 14, 319-333
- Liska V, Khimani AH, Hofmann-Lehmann R, Fink AN, Vlasak J, Ruprecht RM. (1999) Viremia and AIDS in rhesus macaques after intramuscular inoculation of plasmid DNA encoding full-length SIVmac239. AIDS Res Hum Retroviruses. 15, 445-450 PMID 10195754
- Locher CP, Barnett SW, Herndier BG, Blackbourn DJ, Reyes-Teran G, Murthy KK, Brasky KM, Hubbard GB, Reinhart TA, Haase AT, Levy JA. (1998) Human immunodeficiency virus-2 infection in baboons is an animal model for human immunodeficiency virus pathogenesis in humans. Arch Pathol Lab Med. 122, 523-533 PMID 9625420
- Monti-Bragadin C, Ulrich K. (1972) Rescue of the genome of the defective murine sarcoma virus from a non-producer hamster tumor cell line, PM-1, with murine and feline leukemia viruses as helpers. Int J Cancer 9, 383-392 PMID 4339414
- O'Brien SJ, Goedert JJ. (1996) HIV causes AIDS: Koch's postulates fulfilled. Curr Opin Immunol. 8, 613-618 PMID 8902385
- O'Brien SJ (1997) The HIV-AIDS debate is over. HIV News Line 3
- O'Neil SP, novembre FJ, Hill AB, Suwyn C, Hart CE, Evans-Strickfaden T, Anderson DC, deRosayro J, Herndon JG, Saucier M, McClure HM. (2000) Progressive infection in a subset of HIV-1-positive chimpanzees. J Infect Dis. 182, 1051-1062 PMID 10979899
- MMWR weekly (1981a) Pneumocystis Pneumonia- Los Angeles June 5, 30 250-252
- MMWR weekly (1981b) Kaposi's Sarcoma and Pneumocystis Pneumonia among homosexual men - New York City and California July 4, 30 305-308
- Nkengasong JN, Maurice C, Koblavi S, Kalou M, Yavo D, Maran M, Bile C, N'guessan K, Kouadio J, Bony S, Wiktor SZ, Greenberg AE. (1999) Evaluation of HIV serial and parallel serologic testing algorithms in Abidjan, Cote d'Ivoire. AIDS 13, 109-117 PMID 10207552
- Peebles PT, Gerwin BI, Scolnick EM. (1976) Murine sarcoma virus defectiveness: serological detection of only helper virus reverse transcriptase in sarcoma virus rescued from nonmurine S + L-cells. Virology 70, 313-323 PMID 57666
- Root-Bernstein R. (1993) Rethinking AIDS: the tragic cost of premature consensus. New York: Free Press
- Samdal HH, Gutigard BG, Labay D, Wiik SI, Skaug K, Skar AG. (1996) Comparison of the sensitivity of four rapid assays for the detection of antibodies to HIV-1/HIV-2 during seroconversion. Clin Diagn Virol. 7, 55-61 PMID 9077430
- Schmidt CG. (1984) The group-fantasy origins of AIDS. J Psychohist. 12, 37-78 PMID 11611586
- Silvester C, Healey DS, Cunningham P, Dax EM. (1995) Multisite evaluation of four anti-HIV-1/HIV-2 enzyme immunoassays. Australian HIV Test Evaluation Group. J Acquir Immune Defic Syndr Hum Retrovirol. 8, 411-419 PMID 7882108
- Sinoussi F, Mendiola L, Chermann JC. (1973) Purification and partial differentiation of the particles of murine sarcoma virus (M. MSV) according to their sedimentation rates in sucrose density gradients. Spectra 4,237-243
- Tebit DM, Zekeng L, Kaptue L, Krausslich HG, Herchenroder O. (2003) Construction and characterisation of a full-length infectious molecular clone from a fast replicating, X4-tropic HIV-1 CRF02.AG primary isolate. Virology 313, 645-652 PMID 12954230
- Toplin I. (1973) Tumor Virus Purification using Zonal Rotors. Spectra 4, 225-235
- Urassa W, Godoy K, Killewo J, Kwesigabo G, Mbakileki A, Mhalu F, Biberfeld G. (1999) The accuracy of an alternative confirmatory strategy for detection of antibodies to HIV-1: experience from a regional laboratory in Kagera, Tanzania. J Clin Virol. 14, 25-29 PMID 10548127
- van den Berg H, Gerritsen EJ, van Tol MJ, Dooren LJ, Vossen JM. (1994) Ten years after acquiring an HIV-1 infection: a study in a cohort of eleven neonates infected by aliquots from a single plasma donation. Acta Paediatr. 83, 173-178 PMID 8193497
- Weiss RA, Jaffe HW. (1990) Duesberg, HIV and AIDS. Nature 345, 659-660 PMID 2163025
- Rossi Luca (1999) Sex Virus Feltrinelli-I Canguri ISBN 88-07-70107-3
- Cayley, W. E. Jr. (2004) Effectiveness of condoms in reducing heterosexual transmission of HIV. Am. Fam. Physician. 70, 1268-1269 PMID 15508535
- Clerici, M., Balotta, C., Meroni, L., Ferrario, E., Riva, C., Trabattoni, D., Ridolfo, A., Villa, M., Shearer, G.M., Moroni, M. and Galli, M. (1996) Type 1 cytokine production and low prevalence of viral isolation correlate with long-term non progression in HIV infection. AIDS Res. Hum. Retroviruses. 12, 1053-1061 PMID 8827221
- Decker, C. F. and Lazarus, A. (2000) Tuberculosis and HIV infection. How to safely treat both disorders concurrently. Postgrad Med. 108, 57-60, 65-68 PMID 10951746
- Dias, S. F., Matos, M. G., Goncalves, A. C. (2005) Preventing HIV transmission in adolescents: an analysis of the Portuguese data from the Health Behaviour School-aged Children study and focus groups. Eur. J. Public Health 15, 300-304 PMID 15941747
- Dybul M, Fauci AS, Bartlett JG, Kaplan JE, Pau AK; Panel on Clinical Practices for Treatment of HIV. (2002) Guidelines for using antiretroviral agents among HIV-infected adults and adolescents. Ann Intern Med. 137, 381-433 PMID 12617573
- Feldman, C. (2005) Pneumonia associated with HIV infection. Curr Opin Infect Dis. 18, 165-170 PMID 15735422
- Gao, F., et al. (1999) Origin of HIV-1 in the Chimpanzee Pan troglodytes troglodytes. Nature 397, 436–441 PMIID 9989410
- Gray F, Adle-Biassette H, Chrétien F, Lorin de la Grandmaison G, Force G, Keohane C. (2001) Neuropathology and neurodegeneration in human immunodeficiency virus infection. Pathogenesis of HIV-induced lesions of the brain, correlations with HIV-associated disorders and modifications according to treatments. Clin. Neuropathol. 20, 146-155 PMID 11495003
- Guerrant, R. L., Hughes, J. M., Lima, N. L., Crane, J. (1990) Diarrhea in developed and developing countries: magnitude, special settings, and etiologies. Rev Infect Dis. 12 Suppl 1, S41-50 PMID 2406855
- Guss, D. A. (1994a) The acquired immune deficiency syndrome: an overview for the emergency physician, Part 1. J. Emerg. Med. 12, 375-384 PMID 8040596
- Guss, D. A. (1994b) The acquired immune deficiency syndrome: an overview for the emergency physician, Part 2. J. Emerg. Med. 12, 491-497 PMID 7963396
- Heaton RK, Grant I, Butters N, White DA, Kirson D, Atkinson JH, McCutchan JA, Taylor MJ, Kelly MD, Ellis RJ, et al. (1995) The HNRC 500—neuropsychology of HIV infection at different disease stages. HIV Neurobehavioral Research Center. J. Int. Neuropsychol. Soc. 1, 231-251 PMID 9375218
- Holmes, C. B., Losina, E., Walensky, R. P., Yazdanpanah, Y., Freedberg, K. A. (2003) Review of human immunodeficiency virus type 1-related opportunistic infections in sub-Saharan Africa. Clin Infect Dis. 36 656-662 PMID 12594648
- Laga, M., Nzila, N., Goeman, J. (1991) The interrelationship of sexually transmitted diseases and HIV infection: implications for the control of both epidemics in Africa. AIDS 5 Suppl 1, S55-S63 PMID 1669925
- Lawn, S. D. (2004) AIDS in Africa: the impact of coinfections on the pathogenesis of HIV-1 infection. J. Infect.Dis. 48, 1-12 PMID 14667787
- Luft, B. J. and Chua, A. (2000) Central Nervous System Toxoplasmosis in HIV Pathogenesis, Diagnosis, and Therapy. Curr. Infect. Dis. Rep. 2, 358-362 PMID 11095878
- Marx, J. L. (1982) New disease baffles medical community. Science 217, 618-621 PMID 7089584
- MMWR weekly (1992) 1993 Revised classification system for HIV infection and expanded surveillance case definition for AIDS among adolescents and adults. December 18, 41 (RR17), 001
- Montessori, V., Press, N., Harris, M., Akagi, L., Montaner, J. S. (2004) Adverse effects of antiretroviral therapy for HIV infection. CMAJ 170, 229-238 PMID 14734438
- Morgan, D., Mahe, C., Mayanja, B. and Whitworth, J. A. (2002a) Progression to symptomatic disease in people infected with HIV-1 in rural Uganda: prospective cohort study. BMJ 324, 193-196 PMID 11809639
- Morgan, D., Mahe, C., Mayanja, B., Okongo, J. M., Lubega, R. and Whitworth, J. A. (2002b) HIV-1 infection in rural Africa: is there a difference in median time to AIDS and survival compared with that in industrialized countries? AIDS 16, 597-6032 PMID 11873003
- Orendi JM, Boer K, van Loon AM, Borleffs JC, van Oppen AC, Boucher CA. (1998) Vertical HIV-I-transmission. I. Risk and prevention in pregnancy. Ned. Tijdschr. Geneeskd. 142, 2720-2724 PMID 10065235
- Palella, F. J. Jr, Delaney, K. M., Moorman, A. C., Loveless, M. O., Fuhrer, J., Satten, G. A., Aschman, D. J., Holmberg, S. D. (1998) Declining morbidity and mortality among patients with advanced human immunodeficiency virus infection. HIV Outpatient Study Investigators. N. Engl. J. Med. 338 853-860 PMID 9516219
- Reeves, J. D. & Doms, R. W. (2002). "Human Immunodeficiency Virus Type 2" Journal of General Virology 83, 1253–1265 PMID 12029140
- Rothenberg, R. B., Scarlett, M., del Rio, C., Reznik, D., O'Daniels, C. (1998) Oral transmission of HIV. AIDS 12, 2095-2105 PMID 9833850
- Sadler, M. and Nelson, M. R. (1997) Progressive multifocal leukoencephalopathy in HIV. Int. J. STD AIDS 8, 351-357 PMID 9179644
- Saitoh A, Hull AD, Franklin P, Spector SA. (2005) Myelomeningocele in an infant with intrauterine exposure to efavirenz. J Perinatol. 25, 555-556 PMID 16047034
- Satishchandra P, Nalini A, Gourie-Devi M, Khanna N, Santosh V, Ravi V, Desai A, Chandramuki A, Jayakumar PN, Shankar SK. (2000) Profile of neurologic disorders associated with HIV/AIDS from Bangalore, south India (1989-96). Indian J. Med. Res. 111, 14-23 PMID
- Schneider, M. F., Gange, S. J., Williams, C. M., Anastos, K., Greenblatt, R. M., Kingsley, L., Detels, R., Munoz, A. (2005) Patterns of the hazard of death after AIDS through the evolution of antiretroviral therapy: 1984-2004. AIDS 19, 2009-2018 PMID 16260908
- Senkaali, D., Muwonge, R., Morgan, D., Yirrell, D., Whitworth, J. and Kaleebu, P. (2005) The relationship between HIV type 1 disease progression and V3 serotype in a rural Ugandan cohort. AIDS Res. Hum. Retroviruses. 20, 932-937 PMID 15585080
- Sperling RS, Shapiro DE, Coombs RW, Todd JA, Herman SA, McSherry GD, O'Sullivan MJ, Van Dyke RB, Jimenez E, Rouzioux C, Flynn PM, Sullivan JL. (1996) Maternal viral load, zidovudine treatment, and the risk of transmission of human immunodeficiency virus type 1 from mother to infant. N Engl J Med. 335, 1621–1629 PMID 8965861
- Tang, J. and Kaslow, R. A. (2003) The impact of host genetics on HIV infection and disease progression in the era of highly active antiretroviral therapy. AIDS 17, S51-S60 PMID 15080180
- Tovanabutra, S., Robison, V., Wongtrakul, J., Sennum, S., Suriyanon, V., Kingkeow, D., Kawichai, S., Tanan, P., Duerr, A., Nelson, K. E. (2002) Male viral load and heterosexual transmission of HIV-1 subtype E in northern Thailand. J. Acquir. Immune. Defic. Syndr. 29, 275-283 PMID 11873077
- UNAIDS (2005) AIDS epidemic update. December 2005.
- Wadia RS, Pujari SN, Kothari S, Udhar M, Kulkarni S, Bhagat S, Nanivadekar A. (2001) Neurological manifestations of HIV disease. J. Assoc. Physicians India. 49, 343-348 PMID 11291974
- White DA, Heaton RK, Monsch AU. (1995) Neuropsychological studies of asymptomatic human immunodeficiency virus-type-1 infected individuals. The HNRC Group. HIV Neurobehavioral Research Center. J. Int. Neuropsychol. Soc. 1, 304-315 PMID 9375225
- World Health Organisation (1990) Interim proposal for a WHO staging system for HIV infection and disease. WHO Wkly Epidem Rec 65, 221-228 PMID 1974812
- Zaidi, S. A. and Cervia, J. S. (2002) Diagnosis and management of infectious esophagitis associated with human immunodeficiency virus infection. J. Int. Assoc. Physicians AIDS Care (Chic Ill) 1, 53-62 PMID 12942677
- Zhu T, Korber BT, Nahmias AJ, Hooper E, Sharp PM, Ho DD.(1998) An African HIV-1 Sequence from 1959 and Implications for the Origin of the Epidemic. Nature 391, 594–597 PMID 9468138
- (EN) Altre fonti utilizzate per la stesura di questo articolo sono elencate nella voce AIDS di Wikipedia in inglese, sezione References[Bisogna riportare qui le fonti, non linkare a siti esterni]
Voci correlate
- Diffusione dell'HIV in Africa
- AIDS. I rapporti umani non trasmettono il virus
- Aids e cinema
- AZT
- FightAIDS@Home
- Giornata mondiale contro l'Aids
- HIV
- NAMES Project AIDS Memorial Quilt
- Mercury Phoenix Trust
- Nastro rosso
- Sieropositività
- Sindrome
- Test HIV
- Profilassi post-esposizione ad HIV
- Ryan White
- Freddie Mercury
- Rock Hudson
- Keith Haring
- Orfano da AIDS
- HLA-B
Altri progetti
 Wikiquote contiene citazioni sull'AIDS
Wikiquote contiene citazioni sull'AIDS Wikizionario contiene il lemma di dizionario «AIDS»
Wikizionario contiene il lemma di dizionario «AIDS» Wikinotizie contiene notizie di attualità su AIDS
Wikinotizie contiene notizie di attualità su AIDS Wikimedia Commons contiene immagini o altri file sull'AIDS
Wikimedia Commons contiene immagini o altri file sull'AIDS
Collegamenti esterni
- Centro Operativo AIDS (Istituto Superiore di Sanità)
- Domande e risposte relative all'infezione da HIV e all'AIDS: documento sui contenuti scientifici, promosso e finanziato dal Ministero del Lavoro, della Salute e delle Politiche Sociali con responsabilità scientifica e coordinamento dell'Istituto Superiore di Sanità.
- Template:Dmoz
Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link VdQ Template:Link AdQ