Pirimidina
| Pirimidina | |
|---|---|
 | |
| Nome IUPAC | |
| 1,3-Diazabenzene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C4H4N2 |
| Massa molecolare (u) | 80.09 |
| Numero CAS | |
| Numero EINECS | 206-026-0 |
| PubChem | 9260 |
| SMILES | C1=CN=CN=C1 |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 20–22 °C (293-295 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 226 |
| Consigli P | 210 [1] |
La pirimidina è una molecola organica eterociclica aromatica, simile al benzene e alla piridina, contenente due atomi di azoto nelle posizioni 1 e 3 dell'anello esagonale. È uno dei tre isomeri delle diazine.
Basi azotate derivate[modifica | modifica wikitesto]
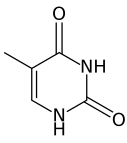
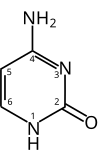
Tre basi azotate presenti negli acidi nucleici, chiamate citosina, timina ed uracile, sono derivati della pirimidina. Le molecole appartenenti a questa classe vengono chiamate pirimidine.
|

|
|
| Timina | Uracile | Citosina |
Nel DNA e nell'RNA queste basi formano legami a idrogeno con le loro purine complementari. Nel DNA la citosina interagisce con la guanina e la timina con l'adenina. Nell'RNA la base complementare di A è U (uracile) invece di T.
Questa modalità di legame idrogeno è per il classico appaiamento delle basi proposto da Watson e Crick, ma sia nel DNA che nell'RNA sono presenti altri tipi di legame idrogeno, anche se il gruppo addizionale 2'-idrossile dell'RNA espande le configurazioni attraverso le quali l'RNA può formare legami idrogeno.
Biosintesi de novo delle pirimidine[modifica | modifica wikitesto]
Diversamente dalle purine, le pirimidine vengono assemblate prima di essere legate al 5-fosforibosil-1-pirofosfato. La prima fase comincia con la formazione di carbamoil fosfato da parte della carbamoil fosfato sintetasi II. Il secondo passo è la creazione di acido carbamoil aspartico, formato dalla transcarbamoilasi aspartica (aspartato carbamoil transferasi). La successiva reazione comprende la disidratazione dell'acido catalizzata dall'enzima diidroorotasi per formare idroorotato. Il diidroorotato entra poi nei mitocondri dove viene ossidato per formare orotato. Questa è l'unica fase mitocondriale. L'enzima coinvolto è la diidrotato deidrogenasi (l'unico enzima mitocondriale). Una volta che l'orotato si è formato, esso è combinato con il 5-fosforibosil-1-pirofosfato per formare orotidina 5' monofosfato, che viene decarbossilata in una reazione catalizzata dalla orotidina monofosfato decarbossilasi per formare Uridina 5' monofosfato. L'uridina monofosfato è poi convertita in uridina difosfato, in una reazione catalizzata dal nucleotide difosfochinasi. Quest'ultima reazione può portare alla formazione di citidina 5' trifosfato.
Catabolismo delle pirimidine[modifica | modifica wikitesto]
Le pirimidine vengono degradate (catabolizzate)nel caso dell'uracile in CO2, H2O e β-alanina, la citosina viene trasformata in uracile . La timina è degradata in CO2, H2O e β-aminoisobutirrato, a sua volta degradato in altri prodotti intermedi nel ciclo dell'acido citrico. Il β-aminoisobutirrato agisce come un indicatore approssimativo del tasso di rotazione del DNA.
Note[modifica | modifica wikitesto]
- ^ scheda della pirimidina su IFA-GESTIS
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Pirimidina
Wikimedia Commons contiene immagini o altri file su Pirimidina
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) pyrimidine / pyrimidine dimer, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh85109338 · GND (DE) 4176489-4 · BNE (ES) XX530351 (data) · J9U (EN, HE) 987007551083905171 · NDL (EN, JA) 00569115 |
|---|

