Tetrafluoruro di selenio
| Tetrafluoruro di selenio | |
|---|---|
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | SeF4 |
| Massa molecolare (u) | 154,954 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 236-703-6 |
| PubChem | 123311 |
| SMILES | F[Se](F)(F)F |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,77 |
| Solubilità in acqua | reazione violenta |
| Temperatura di fusione | −13 °C (260 K) |
| Temperatura di ebollizione | 101 °C (374 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi R | 23/25-33-50/53 |
| Frasi S | 20/21-28-45 |
Il tetrafluoruro di selenio è il composto inorganico di formula SeF4. In condizioni normali è un liquido incolore fumante che reagisce violentemente con l'acqua. È un composto tossico e corrosivo. Si può usare come agente fluorurante in chimica organica (fluorurazione di alcoli, acidi carbossilici e composti carbonilici); rispetto a SF4 è più vantaggioso perché richiede condizioni più blande ed è un liquido anziché un gas.[1]
Struttura[modifica | modifica wikitesto]
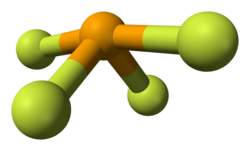
SeF4 è un composto molecolare; allo stato gassoso la molecola ha forma ad altalena, con simmetria C2v, analogamente a SF4. Questa struttura è in accordo con la teoria VSEPR, che prevede che la coppia di elettroni non condivisa occupi una posizione equatoriale in uno schema di base di bipiramide trigonale. La distanza tra l'atomo di selenio e gli atomi di fluoro assiali è di 177 pm, e l'angolo F–Se–F è di 169,2°. I due atomi di fluoro equatoriali hanno distanza di legame minore (168 pm) con un angolo F–Se–F di 100,6°. In soluzioni diluite questa struttura monomerica è la specie predominante, ma a concentrazione più elevata c'è evidenza di una debole associazione tra molecole SeF4, e attorno all'atomo di selenio si ha una coordinazione ottaedrica distorta.[2] Anche allo stato solido l'atomo di selenio ha un intorno ottaedrico distorto.[3]
Sintesi[modifica | modifica wikitesto]
SeF4 fu descritto per la prima volta nel 1907 da Paul Lebeau, che lo ottenne facendo reagire selenio e fluoro:[4]
SeF4 si può ottenere anche per fluorurazione del selenio con trifluoruro di cloro, o per reazione del tetrafluoruro di zolfo con diossido di selenio:
Reattività[modifica | modifica wikitesto]
In HF, SeF4 si comporta come una base debole, più debole di SeF4 (Kb = 2 x 10–2) :
- SeF4 + HF ⇄ SeF3+ + [HF]2– (Kb = 4 x 10–4)
Con SbF5, AsF5, NbF5, TaF5 e BF3 si formano addotti ionici contenenti cationi SeF3+.[5]
Con CsF si forma invece l'anione SeF5–, che ha struttura di piramide a base quadrata simile alle specie isoelettroniche ClF5 e BrF5.[6]
L'anione SeF62– si forma con fluoruro di esametilpiperidinio o fluoruro di 1,2-dimetilpropiltrimetilammonio; ha una struttura ottaedrica distorta, a differenza dell'analogo SeCl62– che ha struttura ottaedrica regolare.[7]
Sicurezza[modifica | modifica wikitesto]
SeF4 è un composto tossico e corrosivo, che reagisce violentemente con l'acqua. Provoca ustioni alla pelle, agli occhi, all'apparato respiratorio e a tutte le mucose.[8]
Note[modifica | modifica wikitesto]
- ^ G. A. Olah, M. Nojima, I. Kerekes, Synthetic methods and reactions. I. Selenium tetrafluoride and its pyridine complex. Convenient fluorinating agents for fluorination of ketones, aldehydes, amides, alcohols, carboxylic acids, and anhydrides, in J. Am. Chem. Soc., vol. 96, n. 3, 1974, pp. 925-927, DOI:10.1021/ja00810a052.
- ^ (DE) K. Seppelt, Die Struktur des Selentetrafluorid in Lösung, in Z. anorg. allg. Chem., vol. 416, n. 1, 1975, pp. 12-18, DOI:10.1002/zaac.19754160103.
- ^ N. N. Greenwood, A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
- ^ P. Lebeau, Action du fluor sur le sèlénium. Tétrafluorure de sèlénium, in Comptes Rendus Acad. Sci., Paris, vol. 144, 1907, pp. 1042-1044. URL consultato il 26 maggio 2011.
- ^ R. J. Gillespie, A. Whitla, Selenium tetrafluoride adducts. II. Adducts with boron trifluoride and some pentafluorides, in Can. J. Chem., vol. 48, n. 4, 1970, pp. 657-663, DOI:10.1139/v70-106.
- ^ K. O. Christe, E. C. Curtis, C. J. Schack, D. Pilipovich, Vibrational spectra and force constants of the square-pyramidal anions SF5–, SeF5–, and TeF5–, in Inorg. Chem., vol. 11, n. 7, 1972, pp. 1679-1682, DOI:10.1021/ic50113a046.
- ^ A. R. Mahjoub, X. Zhang, K. Seppelt, Reactions of the “naked” fluoride Ion: syntheses and structures of SeF62– and BrF6–, in Chem. Eur. J., vol. 1, n. 4, 1995, pp. 261-265, DOI:10.1002/chem.19950010410.
- ^ Oakwood Products, Scheda di sicurezza di SeF4 (PDF) [collegamento interrotto], su labseeker.com. URL consultato il 9 giugno 2011.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Tetrafluoruro di selenio
Wikimedia Commons contiene immagini o altri file su Tetrafluoruro di selenio


