Portale:Chimica/Composto chimico
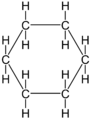
Il cicloesano è un cicloalcano, ossia un idrocarburo privo di doppi e tripli legami C-C il cui scheletro di atomi di carbonio è chiuso ad anello, per l'esattezza un anello composto da sei atomi, ciascuno dei quali lega a sé due atomi di idrogeno. A temperatura ambiente è un liquido incolore dal lieve odore tipico degli idrocarburi. È infiammabile e nocivo per inalazione e contatto con la pelle.
Benché per comodità sia rappresentata da un esagono regolare, la molecola del cicloesano non è planare, dal momento che gli atomi di carbonio hanno ibridazione sp3, tetraedrica in cui l'angolo tra due legami è di 109,5°. La molecola del cicloesano tende pertanto ad assumere una forma piegata detta a sedia, individuata da Odd Hassel, che per questa ricerca ricevette un Premio Nobel per la chimica.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
Anteprime di tutti i composti del giorno[modifica wikitesto]
1[modifica wikitesto]
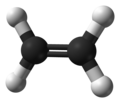
L'etilene (o etene) è il più semplice degli alcheni, la sua formula chimica è C2H4.
A temperatura e pressione ambiente si presenta come un gas incolore, dal lieve odore dolciastro. È estremamente infiammabile. Oltre ad essere un importante prodotto nell'industria chimica (è ad esempio il composto chimico da cui si ottiene il polietilene), è anche un ormone per molte specie vegetali.
Un gruppo funzionale corrispondente a un etene privato di un atomo di idrogeno si chiama comunemente vinile e i composti contenenti tale gruppo composti vinilici.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
2[modifica wikitesto]

L'acido solforico è un acido minerale forte, liquido a temperatura ambiente, oleoso, incolore e inodore; la sua formula chimica è H2SO4. Il suo numero CAS è 7664-93-9.
I suoi sali vengono chiamati solfati. Un solfato molto comune è il gesso, che è solfato di calcio diidrato.
In soluzione acquosa concentrata (>90%) è noto anche con il nome di vetriolo.
Soluzioni di anidride solforica al 30% in acido solforico sono note come oleum fumante.
Solubile in acqua e in etanolo con reazione esotermica anche violenta, in forma concentrata può causare gravi ustioni per contatto con la pelle.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
3[modifica wikitesto]

Il cloruro di sodio è il sale di sodio dell'acido cloridrico ed è il comune sale da cucina.
A temperatura ambiente si presenta come un solido cristallino incolore e con un odore e un sapore caratteristico. I suoi cristalli hanno un reticolo cubico ai cui vertici si alternano ioni sodio Na+ e ioni cloruro Cl−. In soluzione acquosa oppure fuso, conduce la corrente elettrica. Il sale è anzitutto un esaltatore di sapidità usato in tutte le tradizioni culinarie conosciute ed è ampiamente sfruttato nell'industria conserviera sia come ingrediente che come mezzo di conservazione dei cibi. Quest'ultima proprietà è dovuta all'effetto disidratante che il sale ha sui materiali con cui viene a contatto, da cui estrae l'acqua per osmosi.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
4[modifica wikitesto]

Il metano (detto anche impropriamente gas di città, essendo quest'ultimo una miscela di più gas) è un idrocarburo semplice (alcano) formato da un atomo di carbonio e 4 di idrogeno; la sua formula chimica è CH4, e si trova in natura sotto forma di gas.
La molecola ha forma tetraedrica; l'atomo di carbonio è al centro di un tetraedro regolare ai cui vertici si trovano gli atomi di idrogeno. Una particolare caratteristica dei legami tra carbonio e i 4 atomi di idrogeno è che il carbonio, nel suo stato elettronico fondamentale (non eccitato), presenterebbe solamente due elettroni di valenza, e di conseguenza avrebbe la possibilità di creare solo due legami. Tuttavia il carbonio forma 4 legami con altrettanti atomi di idrogeno. Significa che durante la formazione dei legami il carbonio, che presenta 4 elettroni nel livello orbitale con numero quantico principale pari a 2, un elettrone viene eccitato (venendogli fornita energia) e di conseguenza il carbonio presenterà un elettrone nell'orbitale 2s, uno nel 2px, uno nel 2py e uno nel 2pz (mentre prima avevamo due elettroni nel 2s, uno nel 2px, uno nel 2py e zero nel 2pz).
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
5[modifica wikitesto]

L'acqua è un composto chimico di formula molecolare H2O, in cui i due atomi di idrogeno sono legati all'atomo di ossigeno con legame covalente. In condizioni di temperatura e pressione normali si presenta come un sistema bifase - costituito da un liquido incolore e insapore (che viene chiamato "acqua" in senso stretto) e da un gas incolore (detto vapore acqueo) - ma anche come un solido (detto ghiaccio) nel caso in cui la temperatura sia uguale o inferiore alla temperatura di congelamento. Essendo l'acqua un ottimo solvente, le acque naturali contengono disciolte moltissime altre sostanze, ed è per questo motivo che con il termine "acqua" si intende comunemente sia il composto chimico puro di formula H2O, sia la miscela (liquida) formata dallo stesso, con altre sostanze disciolte al suo interno.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
6[modifica wikitesto]
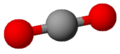
L'anidride carbonica (nota anche come biossido di carbonio o diossido di carbonio) è un ossido acido (anidride) formato da un atomo di carbonio legato a due atomi di ossigeno. È una sostanza fondamentale nei processi vitali delle piante e degli animali. È ritenuta uno dei principali gas serra presenti nell'atmosfera terrestre. Si noti che il termine anidride carbonica è obsoleto nella nomenclatura IUPAC, che riserva il termine anidride a una specifica classe di composti organici. A temperatura e pressione ambiente è un gas incolore e inodore. La sua formula chimica è CO2. Allo stato solido è comunemente chiamato "ghiaccio secco", ed ha numerose applicazioni in questa forma. Sublima ad una temperatura di -78 °C.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
7[modifica wikitesto]

L'acido acetico (o acetato in biochimica, noto anche come acido etanoico) è un composto chimico organico la cui formula chimica è CH3COOH, meglio conosciuto per conferire all'aceto il suo caratteristico sapore acre e il suo odore pungente. L'acido acetico puro, anidro (ovvero privo di acqua), chiamato acido acetico glaciale, a temperatura ambiente è un liquido incolore che attrae acqua dall'ambiente (igroscopicità) e che congela al di sotto dei 16,7 °C (62 °F) in un solido cristallino incolore. L'acido acetico è corrosivo, e i suoi vapori causano irritazione agli occhi, infiammazione delle vie respiratorie e congestione dei polmoni, ma chimicamente è un acido debole per via della sua limitata capacità di dissociarsi in soluzioni acquose.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
8[modifica wikitesto]

L'acetilene (o etino) è il più semplice degli alchini, idrocarburi con un triplo legame carbonio-carbonio. Fu scoperto nel 1836 dal chimico inglese Edmund Davy.
A temperatura e pressione standard è un gas incolore ed estremamente infiammabile. Ha una temperatura di autoaccensione di circa 20 °C. È un gas estremamente pericoloso perché può esplodere anche con inneschi minimi e per questo è normalmente diluito nell'acetone.
La maggior parte dell'acetilene (~80%) è utilizzata come intermedio di sintesi di altri composti; circa il 20% della produzione annua di acetilene è usato per saldatura e taglio dei metalli (ossiacetilene), dato che la sua combustione con l'ossigeno produce una fiamma la cui temperatura arriva a circa 3300 °C. L'acetilene è anche usato nella lavorazione dell'acciaio.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
9[modifica wikitesto]

L'ossido di etilene (o ossirano) è il più semplice composto eterociclico contenente ossigeno, e più specificatamente è il più semplice degli epossidi (eteri ciclici in cui l'ossigeno è uno degli atomi di un anello a tre termini).
A temperatura e pressione ambiente è un gas incolore dall'odore dolciastro, estremamente infiammabile, esplosivo se mescolato all'aria.
È utilizzato dall'industria chimica per la produzione di numerosi materiali.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
10[modifica wikitesto]

L'idrogenocarbonato di sodio o carbonato acido di sodio o carbonato monosodico (o bicarbonato di sodio, che è il nome più comune ma è stato deprecato dalla IUPAC) è un sale di sodio dell'acido carbonico. A differenza del carbonato, l'idrogenocarbonato mantiene uno ione idrogeno dell'acido corrispondente.
Commercialmente, è noto anche semplicemente come bicarbonato.
È tra gli additivi alimentari codificati dall'Unione europea, identificato dalla sigla E 500.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
11[modifica wikitesto]

Il perossido di idrogeno (noto anche come acqua ossigenata) è il più semplice dei perossidi. La sua formula chimica è H2O2. Fu sintetizzato per la prima volta nel 1818 da Louis Jacques Thénard. La sua molecola non è planare: i due legami O-H formano tra loro un angolo diedro di 111°.
A temperatura ambiente è un liquido incolore, viscoso e poco stabile, che può esplodere spontaneamente. Per questo non è mai utilizzato puro, ma in soluzione acquosa in percentuali mai superiori al 60%.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
12[modifica wikitesto]

L'etanolo (o alcol etilico) è un alcol a corta catena, la cui formula bruta è C2H5OH, il suo numero CAS è 64-17-5. È anche chiamato, per antonomasia, semplicemente alcol essendo alla base di tutte le bevande alcoliche. È noto anche come alcol etilico o per gli alcolici viene chiamato spirito.
A temperatura ambiente si presenta come un liquido incolore dall'odore caratteristico. È tendenzialmente volatile ed estremamente infiammabile. La fiamma che produce durante la combustione si presenta di colore blu tenue, ed è molto difficile da vedere in presenza di luce.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
13[modifica wikitesto]
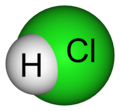
L'acido cloridrico è un idracido di formula HCl, noto commercialmente anche come acido muriatico.
È un acido minerale forte (ovvero si ionizza completamente in soluzione acquosa) monoprotico (cioè ogni sua molecola, dissociandosi, libera un solo ione idrogeno), ed è il principale costituente del succo gastrico, oltre ad essere un reagente comunemente usato nell'industria. L'acido cloridrico è uno dei liquidi più corrosivi esistenti (una sua soluzione al 37% in acqua a 20 °C ha pH inferiore a 1), quindi deve essere maneggiato con attenzione. Si presenta gassoso a temperatura ambiente, incolore, dall'odore e dall'azione irritante. Presenta un TLV-C (ACGIH) pari a 2 p.p.m..
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
14[modifica wikitesto]

L'ammoniaca è un composto dell'azoto di formula chimica NH3. Si presenta come un gas incolore, tossico, dall'odore pungente caratteristico. Molto solubile in acqua, le impartisce una netta basicità.
La forma della molecola dell'ammoniaca anidra è tetraedrica deformata; l'atomo di azoto vi compare con ibridazione sp3, occupa la posizione centrale e lega i tre atomi di idrogeno. La base è un triangolo equilatero occupato dai tre atomi di idrogeno mentre il quarto vertice del tetraedro è occupato da una coppia elettronica di non legame (lone pair), che è la principale responsabile di tutte le proprietà della molecola (formazione di legami a idrogeno, basicità secondo Lewis e secondo Bronsted-Lowry, elevata permittività elettrica e momento dipolare, elevata solubilità in acqua).
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
15[modifica wikitesto]
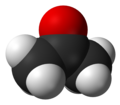
L'acetone (anche chiamato dimetilchetone, propanone e beta-chetopropano) è il chetone più semplice esistente. Il suo numero CAS è 67-64-1.
La sua formula chimica è CH3-CO-CH3; l'atomo di carbonio cui è legato l'atomo di ossigeno ha ibridazione sp2 ed è pertanto al centro di un triangolo grossomodo equilatero ai cui vertici stanno l'atomo di ossigeno e gli altri due atomi di carbonio.
L'acetone è un liquido incolore e infiammabile con un odore caratteristico (fruttato); è miscibile con acqua, etanolo e etere e trova principalmente impiego come solvente.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
16[modifica wikitesto]

Il polietene (più comunemente noto come polietilene) è il più semplice dei polimeri sintetici ed è il più comune fra le materie plastiche. Viene spesso indicato con la sigla "PE", così come ad esempio si usa "PS" per il polistirene o "PVC" per il polivinilcloruro. Ha formula chimica (-C2H4-)n dove n può arrivare fino ad alcuni milioni. Le catene possono essere di lunghezza variabile e più o meno ramificate.
Il polietilene è una resina termoplastica, si presenta come un solido trasparente (forma amorfa) o bianco (forma cristallina) con ottime proprietà isolanti e di stabilità chimica, è un materiale molto versatile ed una delle materie plastiche più economiche; gli usi più comuni sono come isolante per cavi elettrici, film per l'agricoltura, borse e buste di plastica, contenitori di vario tipo, tubazioni, strato interno di contenitori asettici per liquidi alimentari ("Tetra Brik Aseptic") e molti altri.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
17[modifica wikitesto]

Il glucosio è un monosaccaride aldeidico; è il composto organico più diffuso in natura, sia libero sia sotto forma di polimeri.
Ha formula CH2OH(CHOH)4CHO, e differisce dal galattosio per la sua configurazione.
- L'enantiomero destrogiro (D-glucosio o destrosio) è il più diffuso in natura, presente allo stato libero in numerosi frutti zuccherini; si trova anche nella maggior parte dei liquidi organici, nel fegato, nel sangue e nella milza.
- L'enantiomero levogiro (L-glucosio).
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
18[modifica wikitesto]

Il fullerene è un allotropo molecolare del carbonio scoperto il 4 settembre 1985. Le molecole di fullerene, composte interamente di carbonio, assumono una forma simile a una sfera cava, di un ellissoide o di un tubolare. Il fullerene approssimativamente sferico è denominato a volte buckyball, abbreviazione di buckminster-fullerene, con riferimento alla somiglianza con le cupole geodetiche predilette dall'architetto Richard Buckminster Fuller; il fullerene cilindrico è altresì noto come buckytube o nanotubo. Le molecole di fullerene sono generalmente stabili a temperatura e pressione ambiente, nonostante siano energeticamente sfavorite rispetto ad altri allotropi del carbonio, quali la grafite e il diamante.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
19[modifica wikitesto]

Il benzene è un composto chimico che a temperatura ambiente e pressione atmosferica si presenta sotto forma di liquido volatile incolore altamente infiammabile, dall'odore caratteristico. Dal punto di vista chimico, il benzene (talvolta indicato come Ph-H o φ-H) è un idrocarburo aromatico monociclico avente formula bruta C6H6. Il gruppo funzionale che deriva dal benzene dovuto alla perdita di un atomo di idrogeno (C6H5-) prende il nome di fenile.
Il benzene è un costituente naturale del petrolio, ma viene sintetizzato a partire da altri composti chimici presenti nel petrolio stesso.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
20[modifica wikitesto]
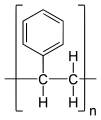
Il polistirene, o polistirolo, è il polimero dello stirene. È un polimero termoplastico, ovvero può essere fuso e rimodellato, dalla struttura lineare. A temperatura ambiente è una plastica rigida trasparente; oltre i 70 °C, al crescere della temperatura diviene sempre più plastico e scorrevole, inizia a decomporsi alla temperatura di 270 °C.
Il polistirolo espanso si presenta in forma di schiuma bianca leggerissima, spesso modellata in sferette o chips, e viene usato per l'imballaggio e l'isolamento. Chimicamente inerte verso molti agenti corrosivi, è solubile nei solventi organici clorurati (ad esempio diclorometano e cloroformio) trielina e in alcuni solventi aromatici (benzene, toluene) solvente nitro, acetone.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
21[modifica wikitesto]

Il cicloesano è un cicloalcano, ossia un idrocarburo privo di doppi e tripli legami C-C il cui scheletro di atomi di carbonio è chiuso ad anello, per l'esattezza un anello composto da sei atomi, ciascuno dei quali lega a sé due atomi di idrogeno. A temperatura ambiente è un liquido incolore dal lieve odore tipico degli idrocarburi. È infiammabile e nocivo per inalazione e contatto con la pelle.
Benché per comodità sia rappresentata da un esagono regolare, la molecola del cicloesano non è planare, dal momento che gli atomi di carbonio hanno ibridazione sp3, tetraedrica in cui l'angolo tra due legami è di 109,5°. La molecola del cicloesano tende pertanto ad assumere una forma piegata detta a sedia, individuata da Odd Hassel, che per questa ricerca ricevette un Premio Nobel per la chimica.
- Leggi tutta la voce...
- Cerca un altro composto chimico...
- Cerca un composto a partire dalla sua formula molecolare...
22[modifica wikitesto]
Portale:Chimica/Composto chimico/22
23[modifica wikitesto]
Portale:Chimica/Composto chimico/23
24[modifica wikitesto]
Portale:Chimica/Composto chimico/24
25[modifica wikitesto]
Portale:Chimica/Composto chimico/25