Canfora
| Canfora | |
|---|---|
| Nome IUPAC | |
| (1R,4R)-1,7,7-trimetilbiciclo[2.2.1]eptan-2-one | |
| Nomi alternativi | |
| D-(+)-canfora | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C10H16O |
| Massa molecolare (u) | 152,24 |
| Aspetto | solido da incolore a bianco |
| Numero CAS | |
| Numero EINECS | 200-945-0 |
| PubChem | 2537 |
| DrugBank | DB14156 |
| SMILES | CC1(C2CCC1(C(=O)C2)C)C |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,99 (20 °C) |
| Solubilità in acqua | (20 °C) insolubile |
| Temperatura di fusione | 175 °C (~448 K) |
| Temperatura di ebollizione | 210 °C (~483 K) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 66 °C (339 K) |
| Limiti di esplosione | 0,6 - 4,5 Vol% |
| Temperatura di autoignizione | 460 °C (733 K) |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 228 - 315 - 319 - 335 |
| Consigli P | 210 - 302+352 - 304+340 - 305+351+338 [1] |
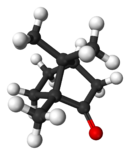
La canfora (o D-(+)-canfora), con formula chimica C10H16O, è un chetone ciclico, prodotto da ossidazione di un terpene, il pinene C10H16.
La canfora è una sostanza cerosa, bianca o trasparente con un forte odore aromatico. Si trova in parecchi vegetali, ma viene estratta principalmente dal legno della Cinnamomum camphora (Laurus camphora), un grande albero sempreverde[2], e anche della Dryobalanops aromatica (canfora del Borneo), un gigante delle foreste del Borneo.
La sostanza si può trovare anche in alcuni altri vegetali collegati della famiglia dell'alloro, in particolare nell'Ocotea usambarensis (Canfora africana). Può anche essere prodotta sinteticamente da olio di trementina. Viene usata per il suo profumo, come ingrediente in cucina (soprattutto in India), come fluido per imbalsamare, nelle cerimonie religiose e per scopi medicinali. Una delle principali fonti di canfora in Asia è l'Ocimum kilimandscharicum (Ocimum kilimandscharicum Baker ex Gurke). La canfora si trova anche in basilico, coriandolo, maggiorana, rosmarino e salvia[senza fonte].
Storia[modifica | modifica wikitesto]
La parola canfora deriva dal latino medievale camphora, dall'arabo kafur, dal sanscrito karpur.[3] Barus era il porto sulla costa occidentale dell'isola di Sumatra dove i mercanti stranieri venivano ad acquistare la canfora, per cui in malese è diventato Kapur Barus. La canfora era conosciuta nella Penisola araba già in tempi pre-islamici, come menzionato nel Corano LXXVI:5, usata come aromatizzante per bevande. Nel IX secolo, il filosofo e chimico arabo al-Kindi (noto in Europa come Alchindus), fornì la prima ricetta per la produzione di canfora nel suo Kitāb kīmīyāʾ al-ʿitr (Libro di chimica del profumo).[4] Dal XIII secolo, venne usata nelle ricette in tutto il mondo musulmano, dai piatti principali, come il tradizionale tharīd, allo stufato e ai dolci.[5]
Già nel XIX secolo si sapeva che con l'acido nitrico la canfora avrebbe potuto essere ossidata in acido canforico. Haller e Blanc pubblicarono una semisintesi di canfora da acido canforico, che, pur dimostrandone la struttura, non lo provò. La prima completa sintesi totale per l'acido canforico è stata pubblicata da Gustaf Komppa nel 1903. Egli partì da ossalato di dietile e acido 3,3-dimetilpentanoico, che reagirono per la condensazione di Claisen dando l'acido dicheto-canforico. La metilazione con ioduro di metile e una procedura complicata di riduzione produsse acido canforico. William Perkin pubblicò un'altra sintesi poco tempo dopo. Già in precedenza alcuni composti organici (come ad esempio l'urea) erano stati sintetizzati in laboratorio, ma la canfora era un prodotto naturale scarsamente disponibile e con una forte richiesta in tutto il mondo. Komppa se ne rese conto e iniziò la produzione industriale di canfora in Tainionkoski, Finlandia, nel 1907.
Molti furono i metodi ideati per la sintesi della canfora, tra i quali quello ideato dal chimico Auguste Béhal, partendo dall'essenza di trementina C10H16 e quello di Marcellin Berthelot, partendo dall'ossidazione del borneolo C10H18O o del canfene C10H16.
Produzione[modifica | modifica wikitesto]

La canfora può essere prodotta dall'α-pinene, che è abbondante negli oli delle conifere e può essere distillata dalla trementina ottenuta come prodotto della macerazione chimica[6]. Con acido acetico come solvente e con catalisi da un acido forte, l'α-pinene prontamente si riorganizza in canfene, che a sua volta subisce una trasposizione di Wagner-Meerwein a catione di isobornile, che viene catturato dall'acetato dando acetato di isobornile. L'idrolisi in isobornile seguita da deidrogenazione dà la canfora.
Estrazione della canfora naturale[modifica | modifica wikitesto]
La canfora naturale viene estratta dalle piante adulte di circa 50 anni. Gli alberi di 4 metri di circonferenza forniscono circa 300 kg di canfora cristallizzata. Per estrarre la canfora in modo non artigianale ma industriale, si sottopongono le foglie ed il legno spezzettato alla distillazione con vapore acqueo. Si ottiene una percentuale dell'1,2-1,5% di canfora e di 0,5% di olio; le percentuali variano tra estate e inverno.
La canfora grezza presenta di solito molte impurità, come acqua, ferro, olio di canfora, sabbia, legno. Acqua e olio vengono eliminati per pressione o per centrifuga; l'acqua può esser eliminata anche tramite il cloruro di calcio o calce viva. Altre impurità vengono eliminate tramite cristallizzazione o sublimazione. La canfora viene poi posta in commercio in blocchi sferici, pesanti da 1,5 a 4 kg, bianchi, cristallini, semitrasparenti ed elastici. Può essere anche sotto forma di tavolette (USA), cassette di 50–60 kg, botti di legno.
La canfora ottenuta dalla Dryobalanops aromatica (canfora del Borneo) è rara, pregiata, costosa e ha sapore ed odore molto gradevole.
Biosintesi[modifica | modifica wikitesto]
Nella biosintesi la canfora viene prodotta dal pirofosfato di geranile, tramite ciclizzazione del pirofosfato di linalolo in pirofosfato di borneolo, seguito dall'idrolisi in borneolo e ossidazione in canfora.

Usi[modifica | modifica wikitesto]
Usi moderni includono la canfora come plastificante per nitrocellulosa, come antitarma, come sostanza antimicrobica, in imbalsamazione, nei fuochi d'artificio, esplosivi, surrogati del cuoio. La canfora solida rilascia vapori che formano un rivestimento antiruggine e viene quindi posta in casse portautensili per proteggere gli strumenti dalla ruggine.[7] I cristalli di canfora vengono utilizzati anche per evitare danni alle collezioni di insetti da parte di altri piccoli insetti.
Viene anche usata in medicina. La canfora è assorbita velocemente attraverso la pelle, produce una sensazione di raffreddamento simile a quella del mentolo e svolge una leggera azione anestetica locale e antimicrobica. Ci sono gel antiprurito e gel rinfrescanti che hanno la canfora come principio attivo. La canfora è un principio attivo (assieme al mentolo) in prodotti vaporizzanti ed è efficace come sedativo della tosse. Può anche essere somministrato per via orale in piccole quantità (50 mg) per lievi sintomi di cuore e affaticamento.[8]
Nel XVIII secolo è stata utilizzata da Auenbrugger nel trattamento delle manie[9].
Alcune tradizioni popolari, inoltre, dicono che la canfora dissuada i serpenti e altri rettili a causa del suo forte odore. Allo stesso modo, si crede che la canfora sia tossica per gli insetti e quindi viene a volte usata come repellente.[10]
La canfora è ampiamente usata nelle cerimonie religiose indù. Gli indù venerano una fiamma sacra generata bruciando canfora, che costituisce una parte importante di molte cerimonie religiose. La canfora viene usata nelle celebrazioni Maha Shivaratri di Shiva, il dio indù della distruzione e della (ri)creazione. Come la pece naturale, brucia senza lasciare un residuo di ceneri, che simboleggia la coscienza. Di recente, la maggior parte dei templi nell'India del sud hanno smesso l'illuminazione con canfora nei principali Sancta sanctorum a causa di forti depositi di carbonio, tuttavia nelle aree aperte usano la canfora.
Si trova anche nelle maschere utilizzate per schiarire la pelle.
Recentemente, nanotubi di carbonio sono stati sintetizzati utilizzando con successo la canfora in un processo di deposizione chimica da vapore.[11]
Altre sostanze ricavate dagli alberi a volte sono erroneamente vendute come canfora.
Culinaria[modifica | modifica wikitesto]
Nell'Europa antica e medievale la canfora veniva utilizzata come ingrediente per i dolci. Era anche utilizzata come aromatizzante, in confezioni simili ai gelati, in Cina durante la Dinastia Tang (618-907). Veniva citata in una grande varietà di piatti, sia salati che dolci, nei libri di cucina medievale in lingua araba, come ad esempio Kitāb aṭ–ṭabīḫ scritto da Ibn Sayyār al-Warrāq nel X secolo[12] e un libro di cucina andalusa anonimo del XIII secolo[13]. Appare pure in piatti dolci e salati in un libro scritto alla fine del XV secolo per i sultani di Mandu, il Niʿmat-nama[14].
Attualmente la canfora viene utilizzata in Asia come aromatizzante, soprattutto per i dolci. È molto usata in cucina, soprattutto per i dessert, in India, dove è nota come kachha (grezza/cruda) karpuram ("canfora grezza" in tamil: பச்சைக் கற்பூரம்), e si può trovarla nei negozi di alimentari indiani dove è etichettata come "canfora commestibile".
Nel pūjā e nelle cerimonie indù, la canfora viene bruciata in un cucchiaio cerimoniale per l'esecuzione dell'aarti. Questo tipo di canfora, il tipo cristallino bianco, viene anche venduto nei negozi alimentari indiani. Tuttavia non è adatto come alimento ed è pericoloso per la salute se mangiato. Solo la canfora etichettata come "canfora commestibile" dovrebbe essere usata per cucinare.
Medicina[modifica | modifica wikitesto]
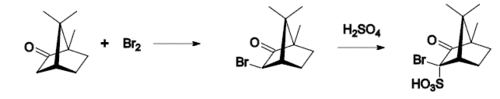
La canfora è stata usata in diversi preparati contro la tosse, come il Vicks e il Buckley, come sedativo della tosse e come analgesico locale. In passato veniva usata anche come antispasmodico, eccitante dei centri nervosi, antisettico. Quella monobromata veniva usata per curare l'asma, l'isterismo e l'eretismo genitale da blenorragia.
Tossicità[modifica | modifica wikitesto]
La canfora è pericolosa soprattutto per i bambini, le persone oltre i 55 anni e per coloro che ne assumono quantità superiori a quelle consigliate per lunghi periodi di tempo. In grandi quantità, la canfora è velenosa quando viene ingerita e può causare convulsioni, confusione, irritabilità, iperattività neuromuscolare, allucinazioni, nausea, vomito e vertigini. In casi estremi, anche l'applicazione locale di canfora può portare a epatotossicità.[15] [16] Dosi letali negli adulti sono di 50–500 mg/kg (per via orale). Generalmente 2 g provocano tossicità gravi e 4 g sono potenzialmente letali. Un sovradosaggio prolungato (0,5 ml/kg di peso corporeo) può provocare il coma o gravi danni renali.
Nel 1980 il Food and Drug Administration degli Stati Uniti pose un limite dell'11% di canfora ammissibile nei prodotti di consumo e vietò totalmente prodotti etichettati come olio canforato, olio di canfora, linimento di canfora e linimento canforato (tranne "olio essenziale di canfora bianco", che non contiene quantità significative di canfora). Dato che esistono trattamenti alternativi, l'uso medicinale della canfora è scoraggiato dalla FDA, tranne che per usi relativi alla pelle, come le polveri medicative, che contengono solo piccole quantità di canfora.
Reattività[modifica | modifica wikitesto]
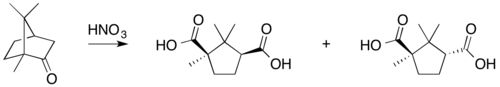
Tipiche reazioni della canfora sono
- ossidazione con acido nitrico,
- conversione a isonitrosocanfora.
La canfora può anche essere ridotta a isoborneolo usando il boroidruro di sodio.
Note[modifica | modifica wikitesto]
- ^ scheda della canfora su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ Il Cinnamomum camphora si trova in Asia (Borneo, Taiwan, Cina e Giappone) ma viene coltivato anche negli USA e nei paesi mediterranei
- ^ Online Etymology Dictionary
- ^ Al-Kindi, FSTC
- ^ Libro di cucina di anonimo andaluso del XIII secolo, su daviddfriedman.com. URL consultato il 2 maggio 2010 (archiviato dall'url originale il 23 settembre 2015).
- ^ questo tipo di macerazione corrisponde al termine inglese pulping e non all'enfleurage
- ^ Tips for Cabinet Making Shops, su cabinetshoptips.com. URL consultato il 3 maggio 2010 (archiviato dall'url originale il 4 aprile 2014).
- ^ National Agency for Medicines Archiviato il 19 febbraio 2009 in Internet Archive.
- ^ J M S Pearce, Leopold Auenbrugger: camphor-induced epilepsy - remedy for manic psychosis, in Eur. Neurol., vol. 59, 1–2, Svizzera, 2008, pp. 105–7, DOI:10.1159/000109581, PMID 17934285.
- ^ Copia archiviata (PDF), su indiacare.it. URL consultato il 3 maggio 2010 (archiviato dall'url originale il 14 giugno 2011).
- ^ Kumar M, Ando Y, Carbon Nanotubes from Camphor: An Environment-Friendly Nanotechnology, in J Phys Conf Ser., vol. 61, 2007, pp. 643–6, DOI:10.1088/1742-6596/61/1/129.
- ^ Nawal Nasrallah, Annals of the Caliphs' Kitchens: Ibn Sayyâr al-Warrâq's Tenth-century Baghdadi Cookbook, Islamic History and Civilization, 70, Leiden, Brill, 2007, ISBN 978-0-415-35059-4.
- ^ An Anonymous Andalusian cookbook of the 13th century, translated by Charles Perry, su daviddfriedman.com. URL consultato il 2 maggio 2010 (archiviato dall'url originale il 23 settembre 2015).
- ^ Norah Titley M., The Ni'matnama Manuscript of the Sultans of Mandu: The Sultan's Book of Delights, Routledge Studies in South Asia, London, UK, Routledge, 2004, ISBN 978-0-415-35059-4.
- ^ Martin D, Valdez J, Boren J, Mayersohn M, Dermal absorption of camphor, menthol, and methyl salicylate in humans, in J Clin Pharmacol, vol. 44, n. 10, ottobre 2004, pp. 1151–7, DOI:10.1177/0091270004268409, PMID 15342616.
- ^ Uc A, Bishop WP, Sanders KD, Camphor hepatotoxicity, in South Med J., vol. 93, n. 6, giugno 2000, pp. 596–8, PMID 10881777. URL consultato il 3 maggio 2010 (archiviato dall'url originale l'11 maggio 2012).
Bibliografia[modifica | modifica wikitesto]
- Grande Dizionario Enciclopedico, vol. II, pag. 855, UTET, 1934
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «canfora»
Wikizionario contiene il lemma di dizionario «canfora» Wikimedia Commons contiene immagini o altri file su canfora
Wikimedia Commons contiene immagini o altri file su canfora
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) camphor, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- la canfora, su my-personaltrainer.it.
- European Food Safety Authority, la canfora nell'alimentazione, su efsa.europa.eu.
- Gli “alberi della canfora” di Andora (Savona, Liguria) by Liguriainside.it, su liguriainside.it.
- (EN) Canfora da Natural Medicines Comprehensive Database
- (EN) INCHEM IPCS (International Programme on Chemical Safety)
- (EN) canfora su botanical.com, su botanical.com.
| Controllo di autorità | NDL (EN, JA) 00572270 |
|---|