Calce
| Calce | |
|---|---|
| Caratteristiche generali | |
| Composizione | ossido di calcio, idrossido di calcio |
Il termine calce indica una serie di materiali da costruzione, noti fin dall'antichità, ottenuti per cottura a temperatura elevata di calcare, marmo, conchiglie o altri materiali contenenti carbonato di calcio, di colore giallino.[1]
Storia[modifica | modifica wikitesto]
Già i Romani e i Fenici prima avevano imparato a usare la calce come materiale da costruzione, mescolata con la sabbia a formare la malta. Vitruvio, nella sua opera De architectura ne descrive la produzione a partire da pietre bianche, cotte in forni (le calcare) dove perdono peso (oggi sappiamo in conseguenza della liberazione di anidride carbonica). Il materiale ottenuto, la calce viva, era poi "spenta" gettandola in vasche piene d'acqua.
Inizialmente adoperata nella forma di "calce aerea" (che indurisce solo se a contatto con aria) venne successivamente mischiata con pezzi di argilla cotta (vasellame, mattoni, ecc.) oppure a pozzolana, una sabbia ricca di silice, che ne alterano le caratteristiche di resistenza e impermeabilità ma soprattutto ne consentono la presa anche in ambienti non a contatto con aria (tipicamente sott'acqua). Nascevano così le "malte idrauliche", sebbene a base di calce aerea.
In tempi moderni, gli ingegneri francesi della scuola di Ponts et Chaussées nel 1750 iniziavano a costruire le fondazioni dei ponti aggiungendo argilla alla calce e ottenendo quella stessa calce idraulica che sarà studiata dall'inglese John Smeaton. Alcune rocce calcaree (p. es. le marne) contengono al loro interno impurità argillose o silicee; da questi materiali si può ottenere la calce idraulica senza l'aggiunta di parti esterne.
Forme chimiche[modifica | modifica wikitesto]
La calce si presenta in due forme chimicamente distinte:
- La calce viva: costituita chimicamente da ossido di calcio, CaO, fortemente igroscopica;
- La calce spenta o idrata: costituita chimicamente da idrossido di calcio, Ca(OH)2.
Preparazione[modifica | modifica wikitesto]
La materia prima per la produzione della calce è il calcare, una roccia sedimentaria ricca di carbonato di calcio (CaCO3) che viene estratta da cave; tipiche sono quelle delle Dolomiti. Anche il marmo e altre rocce possono essere usate a questo scopo.
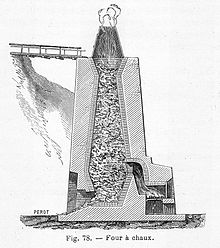
Il materiale, grossolanamente frantumato con diametro dei frammenti nell'ordine dei centimetri o anche di un paio di decimetri, è introdotto in forni o fornaci dove viene riscaldato gradualmente a 900-1100 °C[2] per poi uscire dal fondo della fornace nell'arco di una decina di ore. In questa fase avviene una reazione chimica (reazione di calcinazione) che porta alla liberazione di anidride carbonica e alla produzione dell'ossido di calcio o calce viva:
Dopo la cottura i frammenti di pietra riducono il loro peso di circa il 40% a causa degli atomi di carbonio e ossigeno perduti, e assumono una consistenza porosa. Inoltre il comune colore grigio del calcare viene perso e le pietre diventano per lo più bianche. Esse costituiscono la calce viva che può essere commercializzata come calce viva in zolle oppure ridotta in polvere e conservata in recipienti perfettamente ermetici, poiché è molto igroscopica.
Per ottenere la calce idrata, o calce spenta, il materiale deve subire la reazione di spegnimento:
associata a due effetti macroscopici evidenti: un violento rilascio di calore e la disgregazione della pietra per l'effetto espansivo della trasformazione da ossido a idrossido di calcio.
Lo spegnimento può essere condotto in due maniere differenti, per aspersione o per immersione.
Nel primo caso si ricorre a un impianto di spegnimento relativamente complesso che prevede: una prima frantumazione dell'ossido in pietre di dimensione millimetrica, il trasferimento dei frammenti su un nastro trasportatore su cui avviene il vero e proprio spegnimento, mediante spruzzatori che distribuiscono l'acqua su tutta la sezione in modo da bagnare uniformemente le pietre, che si frantumano ulteriormente per la reazione. Si usa acqua atomizzata e in pressione, favorendo la formazione di una polvere fine detta appunto calce idrata in polvere che viene suddivisa in base alla finezza. È infatti possibile commercializzare la calce idrata in due forme diverse come fiore di calce, di maggiore pregio e costo con specifiche tecniche restrittive descritte da una specifica norma UNI, o come calce da costruzione, di minor pregio e finezza.
Lo spegnimento per immersione avviene invece quando le zolle di calce viva vengono gettate in grandi vasche dal bordo alto, onde evitare incidenti poiché la reazione è altamente esotermica e la produzione di calore è tale da determinare l'ebollizione dell'acqua. In genere questo tipo di spegnimento avviene in due passaggi, con una prima vasca di spegnimento e il successivo passaggio nelle vasche di stagionatura, dentro le quali si ha la formazione della pasta detta "grassello di calce"[N 1]. Nelle vasche di stagionatura è essenziale la presenza di un film d'acqua di qualche centimetro sopra la massa plastica che garantisce che l'idrossido di calcio non reagirà con l'anidride carbonica dell'aria. Il grassello può essere utilizzato prima di quindici giorni per le malte per muratura e tre mesi per le malte per intonaci.
Un altro metodo di produzione del grassello prevede di ottenere la pasta per successiva idratazione della calce idrata in polvere ottenuta dall'impianto di spegnimento per aspersione. Questa metodologia di produzione porta a un grassello di qualità inferiore rispetto a quello ottenibile per immersione e lunga stagionatura. La sospensione bianca che "galleggia" sopra il grassello è a volte venduta come latte di calce.
Fenomeno dei calcinaroli[modifica | modifica wikitesto]
Può capitare, però, che alcuni grumi di calce viva finiscano con lo spegnersi dopo l'impiego, producendo con il loro aumento di volume rigonfiamenti e disgregamenti, spesso circolari. Questo è il fenomeno dei calcinaroli e si presenta quando si usa grassello non invecchiato o calce idrata difettosa.
Presa e indurimento delle calci aeree[modifica | modifica wikitesto]
La presa della calce in opera inizia con l'evaporazione dell'acqua e la successiva essiccazione. Ciò la rende inutilizzabile per le applicazioni a contatto con l'acqua (ponti, moli), ma la rende preferibile al cemento dove l'essiccazione avvenga rapidamente, come nell'applicazione di intonaci. Il cemento infatti non dovrebbe asciugare prima che sia terminata la fase di presa.
Una volta che la calce si è essiccata, a contatto con l'anidride carbonica presente nell'atmosfera inizia un lento processo che la trasforma in calcare (carbonatazione), il composto originario dal quale è stata prodotta. La carbonatazione parte dall'esterno e forma cristalli di CaCO3 tra i granuli di sabbia o tra i materiali che la malta deve legare. La reazione di indurimento è:
Anche se la reazione precedente è corretta dal punto di vista formale, la reazione reale è più complessa. Osservando la precedente reazione infatti, il processo sembrerebbe avvenire tra un solido Ca(OH)2 e un gas CO2, mentre in realtà la reazione avviene in fase acquosa grazie all'acqua di impasto della calce.
L'idrossido di calcio infatti si scioglie in acqua, grazie a una buona solubilità, l'anidride carbonica si scioglie anch'essa in acqua, formando una specie indicata come acido carbonico H2CO3, da cui per reazione acido base si forma un sale poco solubile, ovvero il carbonato di calcio. La forma corretta è dunque:
Resa al grassello[modifica | modifica wikitesto]
Si definisce resa al grassello di una calce il rapporto fra il volume del grassello[N 1] (nel momento in cui per evaporazione di una parte dell'acqua in eccesso inizia a fessurarsi in superficie) e il peso della calce viva che l'ha generato.
La resa al grassello viene espressa in metri cubi a tonnellata.
Classificazione[modifica | modifica wikitesto]
Una calce si dice grassa quando ha una resa al grassello ≥ 2,5, mentre si parla di calce magra per valori inferiori a 2,5 ma superiori a 1,5.
Agli effetti della normativa vigente le calci aeree si distinguono in:
- calce grassa in zolle;
- calce magra in zolle;
- calce idrata in polvere, che comprende due tipi di prodotto:
- fiore di calce;
- calce idrata da costruzione.
Impieghi[modifica | modifica wikitesto]
La calce viva è usata:
- per il pollame, al fine di aumentare il calcio presente nel guscio;
- per trattare le acque, al fine di ridurne l'acidità;
- nella depurazione, per rimuovere i fosfati e altre impurità (flocculante) e per desolforizzare i gas di scarico;
- nella fabbricazione della carta, per dissolvere le fibre di legno;
- come candeggiante e sbiancante;
- per disinfettare ambienti;
- in agricoltura, per correggere l'acidità dei terreni;
- in chimica, per purificare l'acido citrico e il glucosio, come essiccante e assorbente di anidride carbonica;
- per la stabilizzazione delle terre argillose nei sottofondi stradali e nei rilevati stradali.
La calce spenta è usata:
- come materiale da costruzione unita alla sabbia (stabilitura);
- come prodotto di finitura naturale quale marmorino, calce rasata (intonachino), pittura a calce utilizzata per la decorazione di pareti interne ed esterne;
- come rivestimento murale impermeabile utilizzato sia in interni sia in esterni (Tadelakt);
- mescolato al cemento per produrre una malta plastica adatta per gli intonaci;
- nella concia delle pelli;
- nell'industria petrolchimica, per produrre additivi per lubrificanti;
- per la produzione dello stearato di calcio;
- per la neutralizzazione e l'assorbimento di inquinanti;
- per il trattamento dell'acqua usata nell'industria alimentare;
- per correggere l'acidità dei terreni;
- in agricoltura, unita al solfato di rame, come anticrittogamico (poltiglia bordolese);
- nell'industria farmaceutica per preparare sali di calcio e magnesio;
- in odontoiatria come medicamento nei sottofondi e nell'endodonzia.
Calce idraulica[modifica | modifica wikitesto]
La calce idraulica è preparata a partire da roccia calcarea impura, che presenta un certo tenore, dal 6% al 22%, di argille o altri alluminosilicati idrati.
Il nome deriva dal fatto che, a differenza della calce normale, è in grado di fare indurimento anche non a contatto con l'aria.
Sicurezza[modifica | modifica wikitesto]
La calce, e particolarmente quella viva, presenta una forte alcalinità e causticità. Il contatto con la pelle dell'ossido anidro può provocare gravi ustioni come avviene con la soda caustica. Il contatto con poca acqua (non sufficiente ad assorbire il calore prodotto) può provocare una violenta ebollizione e la proiezione di schizzi caustici e bollenti. Per questi motivi è importante utilizzare una tuta sicuramente impermeabile, guanti di qualità e occhiali protettivi quando si maneggia la calce, sia solida sia in soluzione, sia la malta di calce.
L'ingestione di idrossido di calcio può provocare gravi sintomi, tra cui difficoltà respiratoria, emorragie gastrointestinali, ipotensione e pericolose alterazioni del pH del sangue.
Note[modifica | modifica wikitesto]
- Annotazioni
- ^ a b Il grassello di calce è una sospensione in acqua di idrossido di calcio (calce spenta). Si forma durante le operazioni di spegnimento della calce viva e si presenta come una massa plastica untuosa al tatto.
- Fonti
- ^ Calce. In: Angela Weyer et al. (a cura di), EwaGlos, European Illustrated Glossary Of Conservation Terms For Wall Paintings And Architectural Surfaces. English Definitions with translations into Bulgarian, Croatian, French, German, Hungarian, Italian, Polish, Romanian, Spanish and Turkish, Petersberg, Michael Imhof, 2015, p. 383. URL consultato il 7 marzo 2016 (archiviato dall'url originale il 25 novembre 2020).
- ^ "Calce spenta" In: Mara Nimmo (a cura di), Pittura murale. Proposta per un glossario, 2001, p. 28.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «calce»
Wikizionario contiene il lemma di dizionario «calce» Wikimedia Commons contiene immagini o altri file sulla calce
Wikimedia Commons contiene immagini o altri file sulla calce
Collegamenti esterni[modifica | modifica wikitesto]
- Calce, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- Clemente MONTEMARTINI, Riccardo OLIVERI, Francesco SCURTI e Carlo Guido FONTANA, CALCE, in Enciclopedia Italiana, Istituto dell'Enciclopedia Italiana, 1930.
- Calce², su Vocabolario Treccani, Istituto dell'Enciclopedia Italiana.
- calce (sostantivo femminile), su sapere.it, De Agostini.
| Controllo di autorità | Thesaurus BNCF 27984 · LCCN (EN) sh85077003 · J9U (EN, HE) 987007529221405171 · NDL (EN, JA) 00570622 |
|---|



