2-Ossazolidinone
| 2-Ossazolidinone | |
|---|---|
| Nome IUPAC | |
| 2-ossazolidone | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C3H5NO2 |
| Massa molecolare (u) | 87.077 g/mol |
| Aspetto | solido |
| Numero CAS | |
| Numero EINECS | 207-840-9 |
| PubChem | 73949 |
| SMILES | C1COC(=O)N1 |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 86–89 °C |
| Temperatura di ebollizione | 220 °C a 48 mmHg |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 - 317 - 319 |
| Consigli P | 280 - 305+351+338 [1] |
Il 2-ossazolidinone è un composto organico eterociclico, più precisamente un carbammato ciclico, che deriva dall'ossidazione in posizione 2 di un anello ossazolidinico. La molecola rappresenta la struttura base degli ossazolidinoni.
Ossazolidinoni[modifica | modifica wikitesto]
Gli ossazolidinoni sono una classe di composti che si caratterizza per contenere nella struttura il 2-ossazolidinone. In chimica vengono generalmente utilizzati, nel metodo di Evans, come ausiliari per la sintesi chirale. Generalmente, il cloruro acilico desiderato reagisce con l'ossazolidinone a formare un immide. I sostituenti in corrispondenza della posizione 4 e 5 dell'ossazolidinone dirigono qualsiasi reazione aldolica alla posizione in alfa al carbonile del substrato. Gli ossazolidinoni sono un gruppo di molecole che trovano impieghi farmaceutici ad esempio come antibiotici tanto che, in passato, furono utilizzati per il trattamento della tubercolosi.[2]
Storia[modifica | modifica wikitesto]

Il primo ossazolidinone mai utilizzato in clinica medica è stata la cicloserina (4-amino-1,2-ossazolidin-3-one), un farmaco di seconda linea contro la tubercolosi. Il suo utilizzo risale al 1956. A partire dagli anni novanta, quando alcuni ceppi batterici stavano diventando resistenti contro antibiotici come la vancomicina si iniziò a sviluppare tutta una serie di antimicrobici ossazolidinoni. Linezolid è stato il primo agente approvato in questa classe.

Il primo antibiotico 1,3-ossazolidinone ottenibile commercialmente è stato il linezolid, scoperto e sviluppato dalla società farmaceutica Pharmacia & Upjohn.

Nel 2002 AstraZeneca ha introdotto in commercio posizolid (AZD2563).
Usi farmaceutici[modifica | modifica wikitesto]
Antibioticoterapia[modifica | modifica wikitesto]
Gli Ossazolidinoni trovano impiego farmaceutico principalmente come antimicrobici. L'effetto antibatterico degli ossazolidinoni si esplica attraverso una inibizione della sintesi proteica, in particolare viene inibita una tappa precoce che coinvolge il legame del N-formilmetionil-tRNA al ribosoma, attraverso il legame con la subunita 50S ribosomiale.[3][4][5]
In passato alcune di queste molecole furono utilizzate per il trattamento della tubercolosi.
Attualmente alcuni dei oxazolidinoni più importanti rappresentano l'ultima generazione degli antibiotici usati contro agenti patogeni gram-positivi, tra cui superbatteri quali lo Staphylococcus aureus meticillino-resistente. Questi antibiotici in molti casi sono considerati come una scelta di ultima istanza, allorché ogni altra terapia antibiotica non ha dato esito positivo.
Esempi di antibiotici ossazolidinoni:
- Linezolid: composto utilizzabile per somministrazione per via endovenosa e con l'ulteriore vantaggio di avere un'ottima biodisponibilità orale.
- Posizolid (AZD2563): molecola che sembra dotata di un'ottima e mirata attività battericida contro tutti i più comuni batteri gram-positivi, a prescindere dalla resistenza ad altre classi di antibiotici.[6][7]
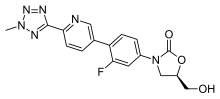
- Tedizolid: approvato per l'utilizzo nelle infezioni acute della cute.[8][9]
- Radezolid (RX-1741): questa molecola ha completato la fase 2 nei clinical trials.[10][11]
- Cicloserina: si tratta di un composto utilizzabile come seconda linea nel trattamento della tubercolosi.
Altri impieghi[modifica | modifica wikitesto]
Gli ossazolidinoni non vengono utilizzati unicamente come antimicrobici. Un derivato ossazolidinone, rivaroxaban, è stato infatti approvata dalla Food and Drug Administration (FDA) degli USA per la profilassi della tromboembolia venosa.
Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. dell'11.10.2012
- ^ A. W. Frahm, H. H. J. Hager, F. v. Bruchhausen, M. Albinus, H. Hager: Hagers Handbuch der pharmazeutischen Praxis: Folgeband 4: Stoffe A-K., Birkhäuser, 1999, ISBN 978-3-540-52688-9
- ^ Shinabarger D, Mechanism of action of the oxazolidinone antibacterial agents, in Expert Opin Investig Drugs, vol. 8, n. 8, 1999, pp. 1195–202, DOI:10.1517/13543784.8.8.1195, PMID 15992144.
- ^ Dresser LD, Rybak MJ, The pharmacologic and bacteriologic properties of oxazolidinones, a new class of synthetic antimicrobials, in Pharmacotherapy, vol. 18, n. 3, 1998, pp. 456–62, PMID 9620097. URL consultato il 3 febbraio 2015.
- ^ Diekema DI, Jones RN, Oxazolidinones: a review, in Drugs, vol. 59, n. 1, 2000, pp. 7–16, PMID 10718097.
- ^ Wookey A, Turner PJ, Greenhalgh JM, Eastwood M, Clarke J, Sefton C, AZD2563, a novel oxazolidinone: definition of antibacterial spectrum, assessment of bactericidal potential and the impact of miscellaneous factors on activity in vitro, in Clin. Microbiol. Infect., vol. 10, n. 3, 2004, pp. 247–54, PMID 15008947.
- ^ Howe RA, Wootton M, Noel AR, Bowker KE, Walsh TR, MacGowan AP, Activity of AZD2563, a novel oxazolidinone, against Staphylococcus aureus strains with reduced susceptibility to vancomycin or linezolid [collegamento interrotto], in Antimicrob. Agents Chemother., vol. 47, n. 11, 2003, pp. 3651–2, PMC 253812, PMID 14576139. URL consultato il 3 febbraio 2015.
- ^ Kisgen JJ, Mansour H, Unger NR, Childs LM, Tedizolid: a new oxazolidinone antimicrobial, in Am J Health Syst Pharm, vol. 71, n. 8, 2014, pp. 621–33, DOI:10.2146/ajhp130482, PMID 24688035.
- ^ Sahre M, Sabarinath S, Grant M, Seubert C, Deanda C, Prokocimer P, Derendorf H, Skin and soft tissue concentrations of tedizolid (formerly torezolid), a novel oxazolidinone, following a single oral dose in healthy volunteers, in Int. J. Antimicrob. Agents, vol. 40, n. 1, 2012, pp. 51–4, DOI:10.1016/j.ijantimicag.2012.03.006, PMC 3789129, PMID 22584101.
- ^ Rx 1741, su rib-x.com, Rib-X Pharmaceuticals, 2009. URL consultato il 3 febbraio 2015 (archiviato dall'url originale il 26 febbraio 2009).
- ^ Lemaire S, Kosowska-Shick K, Appelbaum PC, Verween G, Tulkens PM, Van Bambeke F, Cellular pharmacodynamics of the novel biaryloxazolidinone radezolid: studies with infected phagocytic and nonphagocytic cells, using Staphylococcus aureus, Staphylococcus epidermidis, Listeria monocytogenes, and Legionella pneumophila, in Antimicrob. Agents Chemother., vol. 54, n. 6, 2010, pp. 2549–59, DOI:10.1128/AAC.01724-09, PMC 2876393, PMID 20385852.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su 2-Ossazolidinone
Wikimedia Commons contiene immagini o altri file su 2-Ossazolidinone

