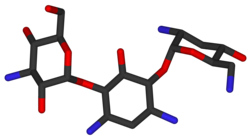
Tobramicina
| Tobramicina | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C18H37N5O9 |
| Massa molecolare (u) | 467,515 g/mol |
| Numero CAS | |
| Numero EINECS | 251-322-5 |
| Codice ATC | J01 |
| PubChem | 36294 |
| DrugBank | DB00684 |
| SMILES | C1C(C(C(C(C1N)OC2C(C(C(C(O2)CO)O)N)O)O)OC3C(CC(C(O3)CN)O)N)N |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | ---[1] |
La tobramicina è un antibiotico appartenente alla classe degli aminoglicosidi, utilizzato per trattare le infezioni batteriche associate alla fibrosi cistica, le infezioni del tratto respiratorio inferiore, del tratto urinario, degli occhi, della pelle, delle ossa e delle strutture cutanee.[2][3][4][5][6]
Gli aminoglicosidi, molti dei quali derivati direttamente da Streptomyces spp., sono antibiotici battericidi a concentrazione dipendente con un ampio spettro di attività contro organismi Gram-positivi e Gram-negativi.[2] La tobramicina inalata è particolarmente nota per il suo utilizzo nel trattamento di infezioni croniche da Pseudomonas aeruginosa nei pazienti affetti da fibrosi cistica, poiché il patogeno è notoriamente intrinsecamente resistente a molti antibiotici.[2][3][4] Tuttavia, la tobramicina può anche essere somministrata per via endovenosa e topica per trattare una varietà di infezioni causate da batteri sensibili.[5][6] Il suo impiego è limitato in alcuni casi da tossicità caratteristiche come la nefrotossicità e l'ototossicità, ma rimane una preziosa opzione di fronte alla crescente resistenza agli antibiotici di prima linea come i β-lattami e le cefalosporine.[2][7][4][6]
La tobramicina è stata approvata dalla Food and Drug Administration nel 1975 ed è attualmente disponibile in diverse forme farmaceutiche come inalazione[8], parenterale[9] e applicazione oftalmica.[10][4][5][6]
Farmacologia[modifica | modifica wikitesto]
Indicazione d'uso[modifica | modifica wikitesto]
La Food and Drug Administration ha approvato il farmaco per la somministrazione parenterale di tobramicina per il trattamento di varie reinfezioni causate da organismi suscettibili, principalmente batteri gram-negativi e Staphylococcus aureus. I batteri gram-negativi includono Pseudomonas aeruginosa, Escherichia coli e specie di Proteus, Klebsiella, Enterobacter, Serratia, Providencia e Citrobacter.[11]
Le infezioni causate da organismi sensibili alla tobramicina possono variare nella loro natura e includono setticemia, infezioni del tratto respiratorio inferiore, infezioni del sistema nervoso centrale come la meningite, infezioni intra-addominali, infezioni cutanee e del tessuto sottocutaneo, osteomielite e infezioni complicate delle vie urinarie.
La tobramicina inalata è approvata dalla Food and Drug Administration per il trattamento della fibrosi cistica nei pazienti di età superiore ai sei anni con Pseudomonas aeruginosa.[12] Le linee guida per la fibrosi cistica raccomandano l'uso cronico della tobramicina inalata nei pazienti con fibrosi cistica per migliorare la funzione polmonare, ridurre le esacerbazioni e migliorare la qualità della vita.[13]
La tobramicina per uso oftalmico è approvata dalla Food and Drug Administration per trattare infezioni oculari esterne causate da organismi suscettibili in adulti e bambini.[11][5]
L'uso off-label della tobramicina include la somministrazione intraventricolare per il trattamento delle infezioni del sistema nervoso centrale associate a catetere intraventricolare.[14] Secondo le linee guida dell'American Academy of Allergy, Asthma, and Immunology, la tobramicina può essere utilizzata per la profilassi delle infezioni batteriche del tratto respiratorio nei pazienti con malattie immunodeficitarie primarie.[15]
Farmacodinamica[modifica | modifica wikitesto]
La tobramicina è un antibiotico aminoglicosidico derivato dall'actinomicete Streptomyces tenebrarius[6] che possiede un ampio spettro di attività contro batteri Gram-negativi, inclusi Enterobacteriaceae, Escherichia coli, Klebsiella pneumoniae, Morganella morganii, Moraxella lacunata, Proteus spp., Haemophilus spp., Acinetobacter spp., Neisseria spp. e, importantemente, Pseudomonas aeruginosa. Gli aminoglicosidi in generale mantengono anche attività contro gli agenti biologici di minaccia come Yersinia pestis e Francisella tularensis. Inoltre, gli aminoglicosidi sono attivi contro alcuni batteri Gram-positivi come Staphylococcus spp., inclusi ceppi meticillino-resistenti (MRSA) e vancomicina-resistenti, Streptococcus spp. e Mycobacterium spp.[2][5]
Come gli altri aminoglicosidi, la tobramicina viene assorbita e trattenuta dalle cellule dei tubuli prossimali del rene e delle cellule cocleari nell'orecchio, comportando un rischio di nefrotossicità e ototossicità.[2][6] Esiste inoltre un rischio di blocco neuromuscolare, che può essere più accentuato nei pazienti con disturbi neuromuscolari preesistenti, come la miastenia grave o la malattia di Parkinson.[2][4][6] Gli aminoglicosidi possono attraversare la placenta, causando sordità congenita totale, irreversibile e bilaterale nei neonati nati da madri a cui è stato somministrato un aminoglicoside durante la gravidanza.[4][6] A causa del basso assorbimento sistemico delle formulazioni inalate e topiche di tobramicina, questi effetti sono più evidenti con la tobramicina iniettata rispetto ad altre formulazioni.[4][5][6] Tuttavia, tutte le formulazioni comportano un rischio di reazioni di ipersensibilità, incluse reazioni cutanee potenzialmente fatali come la sindrome di Stevens-Johnson e la necrolisi epidermica tossica.[4][5][6]
Meccanismo d'azione[modifica | modifica wikitesto]
La tobramicina è composta da un anello di 4,6-disostituito di 2-deossilstreptamina che garantisce attività contro vari batteri Gram-negativi e alcuni batteri Gram-positivi.[4][5][6] Il meccanismo d'azione della tobramicina non è stato ancora chiarito in modo univoco, e alcune informazioni sul suo meccanismo si basano sui risultati ottenuti con aminoglicosidi simili. In generale, come gli altri aminoglicosidi, la tobramicina è battericida e mostra sia un'azione battericida immediata che ritardata, attribuite a meccanismi diversi, come descritto di seguito.[2][3]
Gli aminoglicosidi sono policationici a pH fisiologico, in modo tale da legarsi facilmente alle membrane batteriche; ciò include il legame al lipopolisaccaride e ai fosfolipidi all'interno della membrana esterna dei batteri Gram-negativi e all'acido teicoico e ai fosfolipidi all'interno della membrana cellulare dei batteri Gram-positivi. Questo legame sposta i cationi bivalenti e aumenta la permeabilità della membrana, consentendo l'ingresso dell'aminoglicoside. L'ulteriore ingresso dell'aminoglicoside nel citoplasma richiede la forza protonmotrice, consentendo all'aminoglicoside di accedere al suo bersaglio intracellulare primario, il ribosoma batterico 30S. Le proteine mistradotte prodotte a seguito del legame dell'aminoglicoside al ribosoma si integrano e disturbano la membrana cellulare, consentendo un maggiore ingresso dell'aminoglicoside nella cellula. Pertanto, la tobramicina e gli altri aminoglicosidi hanno sia effetti battericidi immediati attraverso il disturbo della membrana sia effetti battericidi ritardati attraverso l'alterazione della sintesi proteica; i dati sperimentali osservati e i modelli matematici supportano questo modello a due meccanismi.[2][3]
L'inibizione della sintesi proteica è stato il primo effetto riconosciuto degli antibiotici aminoglicosidici. Studi strutturali e biologici delle cellule suggeriscono che gli aminoglicosidi si legano al 16S rRNA nell'elica 44 (h44), vicino al sito A del subunità ribosomica 30S, alterando le interazioni tra h44 e h45. Questo legame sposta anche due importanti residui, A1492 e A1493, da h44, mimando le normali variazioni conformazionali che si verificano con il corretto accoppiamento codone-anticodone nel sito A. Complessivamente, il legame dell'aminoglicoside ha diversi effetti negativi, tra cui l'inibizione dell'inizio e dell'elongazione della traduzione e il riciclaggio del ribosoma. Recenti evidenze suggeriscono che l'effetto di quest'ultimo è dovuto a un secondo sito di legame criptico situato nell'elica 69 dell'RNA ribosomiale 23S della subunità ribosomica 50S. Inoltre, stabilizzando una conformazione che imita l'accoppiamento corretto codone-anticodone, gli aminoglicosidi promuovono una traduzione errata; le proteine mistradotte possono incorporarsi nella membrana cellulare, inducendo il danneggiamento discusso sopra.[2][16]
Sebbene la mutazione diretta del 16S rRNA sia un meccanismo di resistenza raro, a causa della presenza del gene in numerose copie, la modificazione post-trascrizionale del 16S rRNA mediante metiltransferasi del 16S rRNA (16S-RMTasi) nella posizione N7 di G1405 o nella posizione N1 di A1408 è un meccanismo di resistenza comune nei batteri resistenti agli aminoglicosidi.[2] Questi mutanti supportano ulteriormente il meccanismo proposto degli aminoglicosidi. Anche la modifica diretta dell'aminoglicoside stesso tramite acetilazione, adenilazione e fosforilazione da parte di enzimi modificanti aminoglicosidi sono mutazioni di resistenza comuni.[2] Infine, a causa dell'esigenza di trasporto attivo degli aminoglicosidi attraverso le membrane batteriche, non sono attivi contro batteri obbligatamente anaerobici.[2]
Assorbimento[modifica | modifica wikitesto]
La tobramicina somministrata per via inalatoria nei pazienti affetti da fibrosi cistica ha mostrato una maggiore variabilità nell'escreato rispetto al siero. Dopo una singola dose di 112 mg, la concentrazione massima nel siero (Cmax) è stata di 1,02 ± 0,53 µg/mL, raggiunta in un'ora (Tmax), mentre la Cmax nell'escreato è stata di 1048 ± 1080 µg/g. In confronto, per una dose di 300 mg, la Cmax nel siero è stata di 1,04 ± 0,58 µg/mL, raggiunta anch'essa entro un'ora, mentre la Cmax nell'escreato è stata di 737 ± 1028 µg/g. L'esposizione sistemica (AUC0-12) è stata simile tra le due dosi, pari a 4,6 ± 2,0 µg∙h/mL per la dose di 112 mg e 4,8 ± 2,5 µg∙h/mL per la dose di 300 mg. Quando la tobramicina è stata somministrata nel corso di un ciclo di quattro settimane a 112 mg due volte al giorno, la Cmax misurata un'ora dopo la somministrazione è variata da 1,48 ± 0,69 µg/mL a 1,99 ± 0,59 µg/mL.[4]
Volume di distribuzione[modifica | modifica wikitesto]
La tobramicina inalata ha avuto un volume apparente di distribuzione nel compartimento centrale di 85,1 L per un tipico paziente affetto da fibrosi cistica.[4]
Le concentrazioni nella bile e nelle feci sono basse, indicando una minima escrezione biliare. La tobramicina è presente nel liquido cerebrospinale, e le concentrazioni dipendono dalla dose e dall'entità dell'infiammazione delle meningi. La tobramicina è distribuita nei fluidi del muco, sinoviali e peritoneali. Attraversa anche le membrane placentari. Le concentrazioni nel rene sono superiori rispetto al siero. La tobramicina inalata produce concentrazioni battericide nel tratto respiratorio inferiore nei bambini affetti da fibrosi cistica.[17]
Legame proteico[modifica | modifica wikitesto]
Il legame della tobramicina alle proteine del siero è trascurabile.[4]
Metabolismo[modifica | modifica wikitesto]
L'assorbimento della tobramicina negli epatociti è limitato e il farmaco viene scarsamente metabolizzato nel fegato.
Via di eliminazione[modifica | modifica wikitesto]
La tobramicina viene eliminata principalmente attraverso la filtrazione glomerulare. L'emivita di eliminazione della tobramicina dopo somministrazione parenterale è di 2-3 ore e varia da 50 a 70 ore nei pazienti con funzione renale compromessa.[18]
Emivita[modifica | modifica wikitesto]
La tobramicina ha un'emivita apparente nel siero di circa 3 ore dopo una singola dose inalatoria di 112 mg nei pazienti affetti da fibrosi cistica.[4]
Clearance[modifica | modifica wikitesto]
La tobramicina inalata ha un'apparente clearance nel siero di 14,5 L/h nei pazienti affetti da fibrosi cistica di età compresa tra 6 e 58 anni.[4]
Effetti Avversi[modifica | modifica wikitesto]
La struttura complessiva dell'rRNA è conservata tra diverse specie; tuttavia, gli aminoglicosidi mostrano un'affinità significativamente più elevata, circa 10 volte, per l'rRNA dei procarioti rispetto agli eucarioti. Questa maggiore affinità di legame non è sufficiente a spiegare il profilo di effetti avversi della tobramicina. Gli effetti avversi più comuni sono vertigini, mal di testa, confusione, nausea e eruzione cutanea. Le reazioni avverse gravi della tobramicina includono ototossicità, neuropatia e nefrotossicità. Sono stati segnalati casi rari di lesioni epatiche con l'uso di tobramicina.[19]
Resistenza[modifica | modifica wikitesto]
La resistenza agli aminoglicosidi si verifica, come con qualsiasi gruppo di antibiotici; tuttavia, la resistenza si verifica molto meno frequentemente rispetto ad altre classi di antibiotici. Ci sono diverse spiegazioni per questa scoperta, come il fatto che gli aminoglicosidi non vengono prescritti con la stessa frequenza di altre classi di antibiotici, come i beta-lattamici. La resistenza agli aminoglicosidi include la modifica del sito bersaglio. Tre classi di enzimi che modificano e diminuiscono l'efficacia della tobramicina includono fosfotransferasi degli aminoglicosidi (APH), nucleotidiltransferasi (ANT) e acetiltransferasi (AAC).[20]
I batteri con biofilm hanno una maggiore resistenza agli aminoglicosidi. Un altro meccanismo di resistenza agli aminoglicosidi è legato alla riduzione reversibile dell'assorbimento del farmaco nei batteri.[21] Alcuni ceppi di Pseudomonas aeruginosa hanno sviluppato resistenza agli aminoglicosidi attraverso la modifica degli enzimi e la diminuzione della permeabilità della membrana esterna per il farmaco.[22]
Interazioni Farmacologiche[modifica | modifica wikitesto]
L'uso simultaneo di altri antibiotici nefrotossici e neurotossici, in particolare altri aminoglicosidi (ad esempio, streptomicina, amikacina, kanamicina, neomicina, paromomicina e gentamicina), cefaloridina, polimixina B, viomicina, colistina, vancomicina e cisplatino, dovrebbe essere evitato.[23][24]
L'uso simultaneo di aminoglicosidi con diuretici potenti, come furosemide e acido etacrinico, dovrebbe essere evitato.[25] I diuretici dell'ansa somministrati per via endovenosa aumentano il rischio di ototossicità associata agli aminoglicosidi.[26]
L'amministrazione di BCG intravesicale dovrebbe essere evitata con la tobramicina, poiché gli antibiotici possono ridurre l'efficacia terapeutica del BCG intravesicale.[27]
Tossicità[modifica | modifica wikitesto]
Le informazioni sulla tossicità riguardanti la tobramicina non sono facilmente disponibili. I pazienti che sperimentano un sovradosaggio sono a maggior rischio di gravi effetti avversi come nefrotossicità, ototossicità, blocco neuromuscolare e insufficienza respiratoria/paralisi. Si raccomandano misure sintomatiche e di supporto; l'emodialisi può aiutare ad eliminare l'eccesso di tobramicina. L'ingestione accidentale di tobramicina è improbabile che porti a un sovradosaggio, poiché gli aminoglicosidi sono scarsamente assorbiti nel tratto gastrointestinale.[4][6]
La scarsa assorbimento gastrointestinale è evidenziata negli studi sugli animali. Quando somministrata per via intraperitoneale o sottocutanea, la dose letale DL50 per topi e ratti varia tra 367-1030 mg/kg, mentre i valori di DL50 per via orale sono superiori a 7500 mg/kg.[28]
La Food and Drug Administration ha indicato tra gli effetti avversi di tossicità: ototossicità, nefrotossicità e blocco neuromuscolare.[29]
Ototossicità[modifica | modifica wikitesto]
L'ototossicità si verifica a causa della perdita delle cellule ciliate nell'orecchio interno.[30] Il danneggiamento del nervo cranico VIII (nervo vestibolococleare) può causare disfunzioni dell'udito o dell'equilibrio. La somministrazione di tobramicina una volta al giorno è considerata utile per ridurre il rischio di citotossicità. Questo effetto avverso è spesso irreversibile.[31]
Nefrotossicità[modifica | modifica wikitesto]
A differenza dell'ototossicità, la nefrotossicità è una reazione avversa reversibile. In uno studio in doppio cieco completato presso la Johns Hopkins University School of Medicine, i ricercatori hanno osservato che l'ototossicità e la nefrotossicità indotte dagli aminoglicosidi si verificano indipendentemente l'una dall'altra.[32] Come nel caso della prevenzione dell'ototossicità, la nefrotossicità può essere evitata mediante intervalli di dosaggio più lunghi. La tobramicina può causare sia nefrotossicità diretta (dose-correlata) che reazioni di ipersensibilità. La tobramicina attiva il sistema renina-angiotensina-aldosterone e può causare vasocostrizione permanente nei reni, con conseguente stato oligurico con minima produzione di urina. I cambiamenti tossici causati dalla tobramicina sono osservabili nel tubulo prossimale. Vacuolizzazione e corpi mieloidi possono essere osservati nei lisosomi delle cellule epiteliali tubulari mediante microscopia elettronica. Anche grumi granulari, ematuria microscopica e proteinuria sono spesso presenti.[33] La stretta monitoraggio della funzione renale è essenziale per ridurre al minimo gli effetti nefrotossici.[34] Mantenere un'adeguata idratazione può anche diminuire la probabilità di eventi nefrotossici. Studi dimostrano che l'amministrazione di antiossidanti, in particolare con la deferoxamina, può alleviare gli effetti tossici osservati nei reni.[35]
Neurotossicità[modifica | modifica wikitesto]
La tobramicina causa un blocco neuromuscolare interferendo con il rilascio di acetilcolina. I pazienti con malattie che interessano la giunzione neuromuscolare, come la miastenia gravis, non dovrebbero assumere aminoglicosidi. Questo gruppo di antibiotici può scatenare o esacerbare i sintomi della miastenia gravis. Se un paziente con miastenia gravis inizia a peggiorare dopo la terapia con tobramicina, è meglio interrompere o ridurre il dosaggio.[36] Gli aminoglicosidi causano anche una sindrome miastenica da farmaco, una patologia reversibile nei pazienti che altrimenti non hanno difetti di trasmissione neuromuscolare. I sintomi della sindrome miastenica da farmaco si verificheranno poco dopo l'inizio della terapia ma cesseranno interrompendo la medicazione.[37]
Sovradosaggio[modifica | modifica wikitesto]
I pazienti in sovradosaggio di tobramicina con funzione renale normale dovrebbero essere adeguatamente idratati per preservare l'output di urina di 3-5 mL/kg/h. L'equilibrio dei fluidi e degli elettroliti, la clearance della creatinina e le concentrazioni sieriche di tobramicina dovrebbero essere monitorati attentamente fino a quando la concentrazione sierica di tobramicina scende al di sotto di 2 mcg/mL. I pazienti con un'emivita di eliminazione della tobramicina superiore a 2 ore o con funzione renale compromessa possono richiedere una terapia aggressiva, compreso il potenziale beneficio dell'emodialisi. È fondamentale notare che la tobramicina inalata può causare tossicità sistemica nei pazienti con disfunzione renale.[38]
Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. del 26.11.2012
- ^ a b c d e f g h i j k l m Alisa W. Serio, Tiffany Keepers e Logan Andrews, Aminoglycoside Revival: Review of a Historically Important Class of Antimicrobials Undergoing Rejuvenation, in EcoSal Plus, vol. 8, n. 1, 2018-11, DOI:10.1128/ecosalplus.ESP-0002-2018. URL consultato il 31 luglio 2023.
- ^ a b c d (EN) Jürgen B. Bulitta, Neang S. Ly e Cornelia B. Landersdorfer, Two Mechanisms of Killing of Pseudomonas aeruginosa by Tobramycin Assessed at Multiple Inocula via Mechanism-Based Modeling, in Antimicrobial Agents and Chemotherapy, vol. 59, n. 4, 2015-04, pp. 2315–2327, DOI:10.1128/AAC.04099-14. URL consultato il 31 luglio 2023.
- ^ a b c d e f g h i j k l m n o FDA Approved Drug Products: TOBI PODHALER (tobramycin) inhalation (PDF), su accessdata.fda.gov.
- ^ a b c d e f g h FDA Approved Drug Products: TOBREX (tobramycin) ophthalmic (PDF), su accessdata.fda.gov.
- ^ a b c d e f g h i j k l FDA Approved Drug Products: tobramycin for injection (PDF), su accessdata.fda.gov.
- ^ (EN) Yohei Doi, Jun-ichi Wachino e Yoshichika Arakawa, Aminoglycoside Resistance, in Infectious Disease Clinics of North America, vol. 30, n. 2, 2016-06, pp. 523–537, DOI:10.1016/j.idc.2016.02.011. URL consultato il 31 luglio 2023.
- ^ BRAMITOB 300 mg soluzione per nebulizzazione - Mediately Farmaci, su Mediately. URL consultato il 31 luglio 2023.
- ^ TOBRAMICINA (B.BRAUN) 1 mg/ml soluzione per infusione - Mediately Farmaci, su Mediately. URL consultato il 31 luglio 2023.
- ^ TOBRAL BB FARMA 0,3 % unguento oftalmico - Mediately Farmaci, su Mediately. URL consultato il 31 luglio 2023.
- ^ a b Gizem Reyhanoglu e Anil Kumar Reddy Reddivari, Tobramycin, StatPearls Publishing, 2023. URL consultato il 31 luglio 2023.
- ^ Jennifer K. Hagerman, Stephanie A. Knechtel e Michael E. Klepser, Tobramycin solution for inhalation in cystic fibrosis patients: a review of the literature, in Expert Opinion on Pharmacotherapy, vol. 8, n. 4, 2007-03, pp. 467–475, DOI:10.1517/14656566.8.4.467. URL consultato il 31 luglio 2023.
- ^ Peter J. Mogayzel, Edward T. Naureckas e Karen A. Robinson, Cystic fibrosis pulmonary guidelines. Chronic medications for maintenance of lung health, in American Journal of Respiratory and Critical Care Medicine, vol. 187, n. 7, 1º aprile 2013, pp. 680–689, DOI:10.1164/rccm.201207-1160oe. URL consultato il 31 luglio 2023.
- ^ Allan R. Tunkel, Rodrigo Hasbun e Adarsh Bhimraj, 2017 Infectious Diseases Society of America's Clinical Practice Guidelines for Healthcare-Associated Ventriculitis and Meningitis, in Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 64, n. 6, 15 marzo 2017, pp. e34–e65, DOI:10.1093/cid/ciw861. URL consultato il 31 luglio 2023.
- ^ Francisco A. Bonilla, David A. Khan e Zuhair K. Ballas, Practice parameter for the diagnosis and management of primary immunodeficiency, in The Journal of Allergy and Clinical Immunology, vol. 136, n. 5, 2015-11, pp. 1186–1205.e1–78, DOI:10.1016/j.jaci.2015.04.049. URL consultato il 31 luglio 2023.
- ^ (EN) B D Davis, L L Chen e P C Tai, Misread protein creates membrane channels: an essential step in the bactericidal action of aminoglycosides., in Proceedings of the National Academy of Sciences, vol. 83, n. 16, 1986-08, pp. 6164–6168, DOI:10.1073/pnas.83.16.6164. URL consultato il 31 luglio 2023.
- ^ Gizem Reyhanoglu e Anil Kumar Reddy Reddivari, Tobramycin, StatPearls Publishing, 2023. URL consultato il 31 luglio 2023.
- ^ Stefanie Hennig, Joseph F. Standing e Christine E. Staatz, Population pharmacokinetics of tobramycin in patients with and without cystic fibrosis, in Clinical Pharmacokinetics, vol. 52, n. 4, 2013-04, pp. 289–301, DOI:10.1007/s40262-013-0036-y. URL consultato il 31 luglio 2023.
- ^ Aminoglycosides, National Institute of Diabetes and Digestive and Kidney Diseases, 2012. URL consultato il 31 luglio 2023.
- ^ L. P. Kotra, J. Haddad e S. Mobashery, Aminoglycosides: perspectives on mechanisms of action and resistance and strategies to counter resistance, in Antimicrobial Agents and Chemotherapy, vol. 44, n. 12, 2000-12, pp. 3249–3256, DOI:10.1128/AAC.44.12.3249-3256.2000. URL consultato il 31 luglio 2023.
- ^ M. L. Barclay, E. J. Begg e S. T. Chambers, Adaptive resistance to tobramycin in Pseudomonas aeruginosa lung infection in cystic fibrosis, in The Journal of Antimicrobial Chemotherapy, vol. 37, n. 6, 1996-06, pp. 1155–1164, DOI:10.1093/jac/37.6.1155. URL consultato il 31 luglio 2023.
- ^ Emma Vázquez-Espinosa, Rosa María Girón e Rosa Mar Gómez-Punter, Long-term safety and efficacy of tobramycin in the management of cystic fibrosis, in Therapeutics and Clinical Risk Management, vol. 11, 2015, pp. 407–415, DOI:10.2147/TCRM.S75208. URL consultato il 31 luglio 2023.
- ^ Benjamin N. Patrick, Michael P. Rivey e Douglas R. Allington, Acute renal failure associated with vancomycin- and tobramycin-laden cement in total hip arthroplasty, in The Annals of Pharmacotherapy, vol. 40, n. 11, 2006-11, pp. 2037–2042, DOI:10.1345/aph.1H173. URL consultato il 31 luglio 2023.
- ^ Ronak A. Patel, Hayden P. Baker e Sara B. Smith, Acute Renal Failure due to a Tobramycin and Vancomycin Spacer in Revision Two-Staged Knee Arthroplasty, in Case Reports in Nephrology, vol. 2018, 2018, pp. 6579894, DOI:10.1155/2018/6579894. URL consultato il 31 luglio 2023.
- ^ Sara N. Salerno, Yuting Liao e Wesley Jackson, Association between Nephrotoxic Drug Combinations and Acute Kidney Injury in the Neonatal Intensive Care Unit, in The Journal of Pediatrics, vol. 228, 2021-01, pp. 213–219, DOI:10.1016/j.jpeds.2020.08.035. URL consultato il 31 luglio 2023.
- ^ Charlene M. T. Robertson, Juzer M. Tyebkhan e Abraham Peliowski, Ototoxic drugs and sensorineural hearing loss following severe neonatal respiratory failure, in Acta Paediatrica (Oslo, Norway: 1992), vol. 95, n. 2, 2006-02, pp. 214–223, DOI:10.1080/08035250500294098. URL consultato il 31 luglio 2023.
- ^ C. Durek, S. Rüsch-Gerdes e D. Jocham, Interference of modern antibacterials with bacillus Calmette-Guerin viability, in The Journal of Urology, vol. 162, n. 6, 1999-12, pp. 1959–1962, DOI:10.1016/S0022-5347(05)68078-0. URL consultato il 31 luglio 2023.
- ^ Cayman Chemical: tobramycin MSDS (PDF), su caymanchem.com.
- ^ Justin A. Clark e David S. Burgess, Plazomicin: a new aminoglycoside in the fight against antimicrobial resistance, in Therapeutic Advances in Infectious Disease, vol. 7, 2020, pp. 2049936120952604, DOI:10.1177/2049936120952604. URL consultato il 31 luglio 2023.
- ^ J. Prazma, D. S. Postma e J. B. Pecorak, Ototoxicity of tobramycin sulfate, in The Laryngoscope, vol. 86, n. 2, 1976-02, pp. 259–268, DOI:10.1288/00005537-197602000-00022. URL consultato il 31 luglio 2023.
- ^ P. Periti, [Tobramycin--clinical pharmacology and chemotherapy], in Journal of Chemotherapy (Florence, Italy), 8 Suppl 1, 1996-01, pp. 3–30. URL consultato il 31 luglio 2023.
- ^ C. R. Smith, J. J. Lipsky e P. S. Lietman, Relationship between aminoglycoside-induced nephrotoxicity and auditory toxicity, in Antimicrobial Agents and Chemotherapy, vol. 15, n. 6, 1979-06, pp. 780–782, DOI:10.1128/AAC.15.6.780. URL consultato il 31 luglio 2023.
- ^ A. Coca, J. Blade e A. Martinez, Tobramycin nephrotoxicity. A prospective clinical study, in Postgraduate Medical Journal, vol. 55, n. 649, 1979-11, pp. 791–796, DOI:10.1136/pgmj.55.649.791. URL consultato il 31 luglio 2023.
- ^ S. S. Pedersen, T. Jensen e D. Osterhammel, Cumulative and acute toxicity of repeated high-dose tobramycin treatment in cystic fibrosis, in Antimicrobial Agents and Chemotherapy, vol. 31, n. 4, 1987-04, pp. 594–599, DOI:10.1128/AAC.31.4.594. URL consultato il 31 luglio 2023.
- ^ M. P. Mingeot-Leclercq e P. M. Tulkens, Aminoglycosides: nephrotoxicity, in Antimicrobial Agents and Chemotherapy, vol. 43, n. 5, 1999-05, pp. 1003–1012, DOI:10.1128/AAC.43.5.1003. URL consultato il 31 luglio 2023.
- ^ Ahmed Elsais, Trine Haug Popperud e Øyvind Melien, [Drugs that may trigger or exacerbate myasthenia gravis], in Tidsskrift for Den Norske Laegeforening: Tidsskrift for Praktisk Medicin, Ny Raekke, vol. 133, n. 3, 5 febbraio 2013, pp. 296–299, DOI:10.4045/tidsskr.12.0624. URL consultato il 31 luglio 2023.
- ^ Nooreen Hussain, Faiz Hussain e Danish Haque, A diagnosis of late-onset Myasthenia gravis unmasked by topical antibiotics, in Journal of Community Hospital Internal Medicine Perspectives, vol. 8, n. 4, 2018, pp. 230–232, DOI:10.1080/20009666.2018.1487245. URL consultato il 31 luglio 2023.
- ^ (EN) Kahler Da, Schowengerdt Ko e Fricker Fj, Toxic serum trough concentrations after administration of nebulized tobramycin, in Pharmacotherapy, vol. 23, n. 4, 2003 Apr, DOI:10.1592/phco.23.4.543.32122. URL consultato il 31 luglio 2023.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Tobramicina
Wikimedia Commons contiene immagini o altri file su Tobramicina