Azoto
| Azoto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Generalità | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nome, simbolo, numero atomico | azoto, N, 7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie | non metalli | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo, periodo, blocco | 15 (VA), 2, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densità | 1,2506 kg/m³ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurazione elettronica |  | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termine spettroscopico | 4So3/2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà atomiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Peso atomico | 14,0067 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio atomico (calc.) | 65 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio covalente | 75 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio di van der Waals | 155 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurazione elettronica | [He]2s22p3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| e− per livello energetico | 2, 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stati di ossidazione | ±1, ±3, 5, 4, ±2 (acido forte) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struttura cristallina | esagonale | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stato della materia | gassoso | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto di fusione | 63,14 K (−210,01 °C)) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto di ebollizione | 77,35 K (−195,80 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | −147,14 °C a 3,39 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molare | 1,354×10−5 m³/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia di vaporizzazione | 2,7928 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calore di fusione | 360,4 J/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocità del suono | 334 m/s a 298,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Altre proprietà | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numero CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elettronegatività | 3,04 (scala di Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calore specifico | 1 040 J/(kg·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conducibilità termica | 0,02598 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di prima ionizzazione | 1 402,3 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di seconda ionizzazione | 2 856 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di terza ionizzazione | 4 578,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di quarta ionizzazione | 7 475,0 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di quinta ionizzazione | 9 444,9 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di sesta ionizzazione | 53 266,6 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di settima ionizzazione | 64 360 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopi più stabili | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| iso: isotopo NA: abbondanza in natura TD: tempo di dimezzamento DM: modalità di decadimento DE: energia di decadimento in MeV DP: prodotto del decadimento | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L'azoto (dal greco ἀ- privativa e ζωή «vita»[1]) è un elemento chimico della tavola periodica degli elementi. Il suo numero atomico è 7. Il simbolo è N, dal latino nitrogenum, passando dal francese nitrogène che fonde il greco νίτρον, nítron, «nitrato di potassio»[2] e γεν-, ghen-, «dare vita a».[3] Dal francese passò all'italiano come nitrogeno,[4] termine ormai obsoleto.
È il primo elemento del gruppo 15 del sistema periodico, facente parte del blocco p, ed è costituente fondamentale delle molecole organiche più importanti dal punto di vista biochimico (DNA, proteine, alcune vitamine), oltre che di composti inorganici estremamente diffusi come l'ammoniaca e l'acido nitrico.
L'azoto molecolare, detto anche azoto biatomico o azoto diatomico o diazoto o semplicemente azoto (formula molecolare N2), è un composto formato da due atomi di azoto. Costituisce il 78% dell'atmosfera terrestre (in frazione di volume che è anche approssimativamente la frazione molare) e allo stato puro si presenta sotto forma di gas incolore, inodore, insapore e inerte.
Storia
[modifica | modifica wikitesto]Daniel Rutherford, un allievo di Joseph Black, è considerato lo scopritore dell'azoto, nonostante esso sia stato contemporaneamente identificato da Joseph Priestley, Carl Wilhelm Scheele e Henry Cavendish.
Black, scopritore dell'"aria fissa" (anidride carbonica), aveva osservato che bruciando una sostanza "carboniosa" in un recipiente chiuso e assorbendo l'anidride carbonica sviluppatasi con potassa caustica (KOH), permaneva un residuo gassoso.
Rutherford studiò questo gas e notò che non manteneva la combustione e la respirazione, che contrariamente all'anidride carbonica non veniva assorbito da sostanze caustiche, ma non lo riconobbe come una distinta specie chimica e lo considerò come aria atmosferica saturata con flogisto. Fu Lavoisier a capire che l'aria è una miscela di un gas attivo O2, che mantiene la combustione e la respirazione, e di un gas inattivo N2.
"Azoto" deriva dal francese azotè, voce formulata dallo stesso Lavoisier, che significa "privo di vita" (dal greco ζωή, zoè, "vita", preceduto dall'alfa privativo),[5] in quanto l'azoto molecolare N2 costituisce il componente dell'aria non necessario alla respirazione degli esseri viventi.
Secondo altre fonti, il termine fu coniato nel 1787 dal chimico francese Louis-Bernard Guyton-Morveau.[1]
Fu parallelamente adottata la denominazione nitrogène (generatore di nitron), proposta nel 1790 da Jean-Antoine Chaptal in seguito alla scoperta del fatto che l'acido nitrico e i nitrati contengono azoto. In inglese si è conservata la denominazione nitrogen, in tedesco viene chiamato stickstoff.
Abbondanza e disponibilità
[modifica | modifica wikitesto]
L'azoto è il quinto elemento più abbondante nell'universo, il 19º sulla crosta terrestre (di cui costituisce lo 0,03%), il primo elemento per abbondanza nell'aria (di cui costituisce il 78,09%) ed è il quarto elemento più presente del corpo umano (di cui costituisce il 3%).
Sotto forma di molecola biatomica N2 (numero CAS ) è il costituente principale dell'atmosfera terrestre (78,08% in volume; per confronto, nell'atmosfera di Marte costituisce il 2,6% in volume).
È contenuto in depositi minerali come nitrato, soprattutto NaNO3 (salnitro del Cile, derivato del guano), ma anche KNO3, Ca(NO3)2 e Mg(NO3)2; questi sali, tutti di derivazione biologica, sono solubili in acqua, perciò i giacimenti si trovano solo in zone particolarmente aride.
È inoltre presente in tutti gli organismi viventi in numerosissime molecole quali DNA, proteine e ATP e dunque anche nei residui fossili. In particolare il carbone contiene di norma quantità significative di ammoniaca (NH3) e di N2.
Come ione ammonio, l'azoto è contenuto nei minerali rari buddingtonite e tobelite. Ancora più rari sono i nitruri osbornite, carlsbergite, roaldite, nierite e sinoite rinvenuti in meteoriti e il siderazoto di origine vulcanica (Vesuvio).
Chimica nucleare
[modifica | modifica wikitesto]La massa atomica relativa dell'azoto è 14,0067 u. Sono noti due isotopi stabili (14N 99,63% e 15N 0,37%) e numerosi isotopi radioattivi con tempo di dimezzamento brevissimo (12N, 13N, 16N, 17N, 18N, 19N, 20N, 21N, 22N, 23N e 24N).
| Nuclide | Abbondanza | Massa | Spin | Emivita | Decadimento |
|---|---|---|---|---|---|
| 10N | — | 2- | 200×10−24 s | p | |
| 11N | — | ½ | 590×10−24 s | p | |
| 11mN | — | ½ - | 6,9×10−22 s | n.m. | |
| 12N | — | 12,0186 | 1 | 0,011 s | β+ |
| 13N | — | 13,0057 | ½ - | 9,965 min | β+ |
| 14N | 99,636 | 14,0031 | 1 | stabile | — |
| 15N | 0,364 | 15,0001 | ½ - | stabile | — |
| 16N | — | 16,0061 | 2- | 7,13 s | β− |
| 17N | — | 17,0084 | ½ - | 4,173 s | β− |
| 18N | — | 18,0141 | 1- | 0,622 s | β− |
| 19N | — | 19,0170 | ½ - | 0,271 s | β− |
| 20N | — | 20,0237 | n.m. | 0,13 s | β− |
| 21N | — | 21,0270 | ½ - | 87 ms | β− |
| 22N | — | 22,0344 | n.m. | 13,9 ms | β− |
| 23N | — | 23,0405 | ½ - | >14,5 ms | β− |
| 24N | — | 24,0505 | n.m. | <52 ns | n |
| 25N | — | ½ - | <260 ns | n.m. |
Isotopi
[modifica | modifica wikitesto]I due isotopi stabili dell'azoto sono 14N e 15N. Di gran lunga il più comune è il 14N (99,634%), che è prodotto nel ciclo del carbonio-azoto nelle stelle. Dei dieci isotopi prodotti sinteticamente, il 13N ha un'emivita di dieci minuti e gli isotopi rimanenti hanno emivite nell'ordine di secondi o meno. Reazioni mediate biologicamente (ad esempio assimilazione, nitrificazione e denitrificazione) controllano fortemente la dinamica dell'azoto nel suolo. Queste reazioni danno tipicamente come risultato l'arricchimento in 15N del substrato e l'impoverimento del prodotto.
Una piccola parte (0,73%) dell'azoto molecolare nell'atmosfera della Terra è l'isotopomero 14N15N, quasi tutto il resto è 14N2.
Il radioisotopo 16N è il radionuclide dominante nel refrigerante dei reattori ad acqua pressurizzata o dei reattori ad acqua bollente durante il normale funzionamento. È prodotto dall'16O (in acqua) attraverso la reazione (n, p). Ha una breve emivita di circa 7,1 s, ma durante il suo decadimento di ritorno all'16O produce radiazioni gamma ad alta energia (da 5 a 7 MeV), per cui l'accesso alla conduttura primaria del refrigerante in un reattore ad acqua pressurizzata deve essere segregato durante il funzionamento del reattore della centrale.[6] Il 16N è uno dei principali mezzi usati per rilevare immediatamente anche le più piccole perdite dal ciclo primario del refrigerante e quello secondario del vapore.
Similmente, l'accesso a uno qualsiasi dei componenti del ciclo del vapore in una centrale con un reattore nucleare ad acqua bollente deve essere segregato durante il funzionamento. La condensa del condensatore è tipicamente trattenuta per 10 minuti per consentire il decadimento del 16N. Questo elimina il bisogno di schermare e di segregare qualsiasi conduttura o pompa dell'acqua di alimentazione.
Reazioni nucleari
[modifica | modifica wikitesto]Ernest Rutherford nel 1919 osservò la prima transmutazione realizzata in laboratorio. Fece passare le particelle alfa generate da un radionuclide naturale attraverso una camera contenente atomi di azoto e scoprì che veniva prodotta un'altra radiazione, più penetrante. Dimostrò che questa nuova radiazione consisteva di protoni di alta energia e concluse che questo era il risultato della conversione dei nuclei di azoto in nuclei di ossigeno. Rutherford ipotizzò che la cattura di una particella alfa da parte del nucleo dell'azoto produce un nucleo eccitato di fluoro-18, che a sua volta emette un protone formando nuclidi di ossigeno-17, un isotopo raro ma stabile
- α + 14N → 18F* → 17O + p
Nell'atmosfera, per effetto dei raggi cosmici, avviene la seguente reazione:
- 14N + n → 14C + p ΔE = −1,14 MeV
Questo processo è all'origine del nuclide carbonio-14.
Poiché il carbonio-14 viene largamente impiegato come tracciante, lo si produce artificialmente sfruttando la stessa reazione.
Se i neutroni hanno energia molto elevata la reazione può decorrere in modo differente dando luogo a trizio:
- 14N + n → 12C + 3H ΔE = 4,015 MeV
Impiegando neutroni termici e quindi di minor energia rispetto a quelli dei raggi cosmici si ha invece:
- 14N + n → 15N* → 15N + γ ΔE = −10,83 MeV
| Ciclo del carbonio |
|---|
| 12C + p → 13N + γ 13N → 13C + e+ + v |
I raggi γ emessi hanno una frequenza caratteristica (intorno a ΔE/h) e, poiché la maggioranza degli esplosivi di largo impiego contiene quantità importanti di azoto (tritolo 18,5%, nitroglicerina 18,5%, ciclonite o T4 37,8%, PETN 17,7%, tetryl 24,4%), questo fatto permette di sfruttare tale reazione nei rilevatori di esplosivi negli aeroporti.
I nuclidi dell'azoto giocano un ruolo importante nel ciclo del carbonio-azoto, una serie di reazioni nucleari che avviene nelle stelle della sequenza principale quando vi è una sufficiente quantità di 12C.
Nella nostra stella non vi è ancora una temperatura abbastanza elevata da produrre una sufficiente quantità di 12C perché questo ciclo sia competitivo nei confronti del ciclo protone-protone.
Separazione isotopica
[modifica | modifica wikitesto]L'arricchimento isotopico di 15N viene solitamente eseguito per scambio chimico, anche se recentemente sono stati messi a punto promettenti metodi cromatografici che sfruttano polimeri criptanti. Il sistema più efficiente e dunque più usato si basa sul seguente equilibrio bifasico:
15NO(g) + 14NO−3(aq) ⇄ 14NO(g) + 15NO−3(aq) (K = 1,055)
grazie al quale si riescono a ottenere concentrazioni di 15N superiori al 99,5%.
Altre reazioni impiegate per l'arricchimento sono:
15NH3(g) + 14NH+4(aq) ⇄ 14NH3(g) + 14NH+4(aq)
15NO(g) + 14NO2(g) ⇄ 14NO(g) + 15NO2(g)
La distillazione frazionata di NO è un altro buon metodo per l'arricchimento dell'isotopo 15N. Il prodotto finale conterrà anche una significativa concentrazione dell'isotopologo 15N18O, fonte utile del più pesante isotopo stabile dell'ossigeno.
L'acido nitrico, l'ammoniaca, i sali di ammonio, l'azoto molecolare N2, gli ossidi NO e NO2 sono disponibili in commercio con diversi gradi di arricchimento dell'isotopo 15N; da questi si possono ottenere i traccianti impiegati in numerosi ambiti di ricerca, molti dei quali sfruttano le tecniche di risonanza magnetica nucleare.
Spettroscopia di risonanza magnetica nucleare
[modifica | modifica wikitesto]Entrambi gli isotopi stabili dell'azoto (14N e 15N) hanno spin nucleare e possono dunque essere sfruttati nelle tecniche di spettroscopia NMR. La sensibilità con cui può essere rivelato 14N è di circa un millesimo rispetto a quella di 1H, ma superiore di circa 5 volte rispetto a quella di 13C. Per 15N è notevolmente inferiore sia a 1H che a 13C. 14N ha inoltre un momento di quadrupolo nucleare che comporta l'allargamento delle linee, un inconveniente che può indurre in taluni casi a preferire 15N nonostante la scarsa disponibililtà e minore sensibilità.
Gli studi NMR dei nuclidi di azoto hanno ormai acquisito notevole importanza e versatilità: l'impiego spazia dall'indagine strutturale a quella sui meccanismi di reazione, dal riconoscimento di nuove specie allo studio della natura dei legami di specie contenenti azoto.
Caratteristiche atomiche
[modifica | modifica wikitesto]| Caratteristiche atomiche | |
|---|---|
| Configurazione elettronica fondamentale | 1s22s22p3 |
| Stati | 4S, 2D, 2P |
| Energia di 1ª ionizzazione | 14,5341 eV |
| Energia di 2ª ionizzazione | 29,6013 eV |
| Energia di 3ª ionizzazione | 47,44924 eV |
| Energia di 4ª ionizzazione | 77,4735 eV |
| Energia di 5ª ionizzazione | 97,8902 eV |
| Energia di 6ª ionizzazione | 552,0718 eV |
| Energia di 7ª ionizzazione | 667,046 eV |
| Affinità elettronica | −0,07 eV |
| Elettronegatività (Pauling) | 3,04 |
| Elettronegatività (Mulliken) | 3,08 |
| Elettronegatività (Allred-Rochow) | 3,07 |
| Polarizzabilità | - |
| Raggio atomico | 0,74 Å |
| Raggio ionico di N3− | 1,71 Å |
| Raggio di van der Waals | 1,55 Å |
L'azoto è il primo elemento del 15º gruppo della tavola periodica.
L'atomo di azoto ha 5 elettroni nel guscio di valenza, lo stato elettronico fondamentale è 4S.
L'energia di 1ª ionizzazione ha un valore particolarmente elevato; contrariamente a quanto si potrebbe prevedere dall'andamento periodico, è maggiore di quello dell'ossigeno. Anche l'affinità elettronica assume un valore che devia, in questo caso in maniera molto più marcata, dalla periodicità della proprietà, presentando addirittura valore negativo.
Questi andamenti si ripresentano per tutti gli elementi del gruppo, anche se in misura più sfumata man mano che aumenta il numero atomico, e possono essere giustificati, nell'ambito del modello orbitalico, considerando che gli elettroni nello stato fondamentale dell'atomo di azoto si dispongono riempiendo per metà il guscio p. Tale disposizione, con un solo elettrone per ogni orbitale p, minimizza le repulsioni interelettroniche e rende relativamente stabile l'atomo rispetto sia alla perdita che al guadagno di un elettrone.
Per quanto riguarda l'elettronegatività e il raggio atomico, i valori rispettano bene la regolarità dell'andamento periodico.
L'azoto atomico può essere prodotto da N2, a bassa pressione, con scariche elettriche. Ha un tempo di vita relativamente lungo perché la ricombinazione ha ordine di reazione 3
- N(g) + N(g) + M(g) → N2(g) + M*(g)
M può essere sia l'azoto atomico N che l'azoto molecolare N2.
La costante di velocità a 298 K è 1,25×10−32 cm6molecole−2s−1 La ricombinazione deve essere necessariamente del 3º ordine per via dell'elevata esotermicità della reazione, è indispensabile che una terza specie chimica assorba l'energia sviluppata, altrimenti il sistema dissocerebbe nuovamente. Come è facile immaginare, l'azoto atomico è estremamente reattivo, per esempio, reagisce con:
- gli idrocarburi formando HCN, RCN e C2N2
- O2 formando NO e NO2
- H2 dando ammoniaca
- CO2 producendo NO e CO
È stata preparata la specie NC60 in cui l'atomo di azoto è incapsulato nel fullerene C60.
Allotropi
[modifica | modifica wikitesto]L'unico allotropo rilevato in natura è la molecola diatomica o biatomica N2. Di norma è chiamato semplicemente "azoto", ma le seguenti diciture sono molto più chiare: azoto molecolare, azoto biatomico o diazoto.
Dal 1890 è nota la specie chimica N−3, chiamato ione azoturo. Tende a formare composti esplosivi con metalli: gli azoturi di piombo, mercurio e bario, per esempio, vengono impiegati nelle capsule di detonazione.
Recentemente è stata riportata la sintesi della specie N+5 detta pentazenio in ambiente superacido[7]. Nonostante appaia piuttosto rischioso, il prossimo passo potrebbe essere la combinazione di N−3 e N+5 per preparare un "sale" che contenga solo azoto. Sarebbe sorprendente scoprire che una tale forma allotropica dell'azoto è stabile. È stata inoltre ipotizzata l'esistenza di cluster di atomi di azoto simili ai fullereni sulla base di calcoli quantomeccanici. Risulta però difficoltoso verificare sperimentalmente l'esistenza di questi cluster.[senza fonte]
Metodi di preparazione
[modifica | modifica wikitesto]In laboratorio N2 si può ottenere sottraendo O2 all'aria facendola passare attraverso fili di rame al calor rosso; si può anche, e questa è un'area di ricerca in forte crescita, separare N2 e O2 sfruttando membrane permeabili all'ossigeno biatomico ma non all'azoto biatomico.
Un altro metodo è la decomposizione termica di alcuni sali che contengono l'azoto, per esempio:
Se si vuole ottenere N2 a maggior grado di purezza, si sfrutta la decomposizione termica di un azoturo di un metallo alcalino o alcalino terroso:
Nell'industria viene ottenuto esclusivamente dalla distillazione frazionata dell'aria liquida. Di norma l'azoto molecolare N2 che ne risulta contiene impurezze in ppm, soprattutto Ar e O2, in misura più o meno significativa a seconda dei metodi impiegati e della qualità dell'impianto di produzione; le moderne colonne di frazionamento garantiscono purezze superiori al 99,9995%, dato che soddisfa la maggior parte delle necessità.
Tra i metodi di purificazione (tesi a ridurre il tenore di O2), resi oggi obsoleti dal miglioramento delle colonne di frazionamento, si annoveravano:
- la reazione con piccole quantità di idrogeno su catalizzatore di platino;
- il passaggio del gas su rame al calor rosso;
- il passaggio del gas attraverso soluzione riducente (p.e.contenente V2+ o Cr2+).
Caratteristiche fisiche e chimico-fisiche
[modifica | modifica wikitesto]Strutturali
[modifica | modifica wikitesto]| Caratteristiche strutturali di N2 | ||
|---|---|---|
| Gruppo puntuale | D∞h | |
| Distanza di legame (pm)
|
14N2 | 110,010 |
| 14N15N | 110,003 | |
| 15N2 | 109,998 | |
| Massa molecolare (u.a.)
|
14N2 | 28,0062 |
| 14N15N | 29,0032 | |
| 15N2 | 30,0002 | |
| Momenti d'inerzia 14N2 (g m2)
|
Ia = 0 | |
| Ib = 1,407×10−43 | ||
| Ib = 1,407×10−43 | ||
Elettroniche
[modifica | modifica wikitesto]| Caratteristiche elettroniche di N2 | |
|---|---|
| Configurazione elettronica | (σg1s)2(σu*1s)2(σg2s)2(σu*2s)2(πu2p)4(σg2p)2 |
| Stati | 1Σ+g |
| Energia di legame 14N2(kJ mol−1) | 941,7 |
| Energia di ionizzazione | 15,59 eV |
| Momento di dipolo (Debye) | 0 |
| Polarizzabilità (10−30m³) | 1,77 |
Sia la configurazione elettronica MO che le teorie elementari della valenza sono concordi nel ritenere l'ordine di legame dell'azoto molecolare (N2) uguale a 3. Ciò è coerente con gli elevati valori dell'energia di dissociazione e della costante vibrazionale.
Spettro UPS
[modifica | modifica wikitesto]
Il primo picco che si osserva nello spettro fotoelettronico UPS He I, quello a 15,59 eV, porta a N2+ (2Σ+g) strappando un elettrone dall'orbitale σg2p. Mostra una struttura vibrazionale molto modesta, vi è solo un debole picco secondario distanziato dal primo di circa 0,267 eV, quindi la costante vibrazionale di N+2(2Σ+g) è 1906,87 N m−1. È un valore inferiore a quello di N2 ma ancora elevato, sintomo del fatto che il contributo legante dell'orbitale σg2p è scarso.
Il secondo picco, che porta a N+2 (2Πu), presenta invece una struttura vibrazionale molto marcata. Si può notare che il picco più intenso della serie è quello del primo stato vibrazionale eccitato, il che significa che la distanza di legame in N+2 (2Πu) è sensibilmente superiore a quella di N2 (1Σ+g). L'espulsione di un elettrone πu2p comporta quindi un importante indebolimento del legame, come si può anche dedurre dalla separazione dei livelli vibrazionali di N+2 (2Πu) che è di circa 0,224 eV, con una costante vibrazionale che questa volta diminuisce decisamente (1351,46 N m−1).
L'ultimo picco che si può osservare in UPS è a 18,75 eV, porta a N+2 (2Σ+u), la struttura vibrazionale è simile a quella del primo picco, questa volta la separazione dei livelli vibrazionali è 0,296 eV e quindi la costante vibrazionale uguale a 2356,35 N m−1. È un valore superiore a quello di N2 (1Σ+g) e infatti l'elettrone espulso proviene da un orbitale debolmente antilegante (σu*2s).
Spettroscopiche
[modifica | modifica wikitesto]| Caratteristiche spettroscopiche di N2 | |
| Costante rotazionale 14N2 (cm−1) | 1,9987 |
| Costante della distorsione centrifuga al 1º ordine (cm−1) | 5,744×10−6 |
| Frequenza vibrazionale fondamentale 14N2 (cm−1) | 2358,07 |
| Energia di punto zero 14N2 | 0,1462 eV |
| Costante vibrazionale 14N2 (N m−1) | 2293,8 |
| Termine spettroscopico | 4So3/2 |
Il piccolo valore della costante al 1º ordine della correzione centrifuga e l'elevata costante vibrazionale sono indici di una notevole rigidità della molecola e sono coerenti con l'elevata energia di legame e con l'ordine di legame uguale a 3.
Mentre lo spettro rotazionale Raman della molecola 14N15N, di simmetria C∞v, presenta intensità concordi con quanto ci si aspetterebbe dalla distribuzione di Boltzmann, la molecola 14N2, di simmetria D∞h, mostra le tipiche alternanze (in questo caso I = 1 quindi Jdispari: Jpari = 1: 2) dovute alla statistica nucleare che possono essere interpretate solo alla luce del principio di Pauli.
Termodinamiche
[modifica | modifica wikitesto]
| Caratteristiche termodinamiche di N2 | |
| Punto di fusione (p = 1 bar) | 63,179 K |
| Entalpia di fusione (kJ mol−1) | 0,719 |
| Punto di ebollizione (p = 1 bar) | 77,244 K |
| Entalpia di vaporizzazione (kJ mol−1) | 5,586 |
| Entropia molare a 298 K (J K−1 mol−1) | 191,61 |
| Cp,m a 298 K (J K−1 mol−1) | 29,125 |
| Cv,m a 298 K (J K−1 mol−1) | 20,818 |
| Coefficiente di Joule-Thomson a 298 K (K atm−1) | 0,27 |
Stato gassoso
[modifica | modifica wikitesto]| Caratteristiche di N2 in fase gassosa | ||
| Densità (kg m−3, 1 bar, 298 K) | 1,1308 | |
| Temperatura critica | 126,3 K | |
| Pressione critica (atm) | 33,54 | |
| Volume critico (cm³ mol−1) | 90,10 | |
| Collision cross section (nm2) | 0,43 | |
| Parametro a dell'eq. di van der Waals (atm L2 mol−2) | 1,408 | |
| Parametro b dell'eq. di van der Waals (10−2L mol−1) | 3,913 | |
| Parametro ε del potenziale di Lennard-Jones (K/k) | 91,85 | |
| Parametro r0 del potenziale di Lennard-Jones (pm) | 391,9 | |
| Costante della legge di Henry a 298 K (K/torr) per H2O | 6,51×10−7 | |
| Entalpia di fisisorbimento (max osservata) (kJ mol−1) | −21 | |
| Entalpia di chemisorbimento (kJ mol−1) | Ta | −589 |
| Fe | −293 | |
Stato solido
[modifica | modifica wikitesto]Sono state osservate sei fasi solide dell'azoto, denominate α, β, γ, δ, ε e ζ, ma a pressioni inferiori a 3500 bar esistono solo le fasi alfa e beta. La temperatura di transizione tra le due fasi alla pressione di 1 bar è 36,61 K. La fase alfa, quella che esiste alla temperatura più bassa, ha un reticolo cubico a facce centrate (a =5660 Å), mentre la fase beta un reticolo esagonale (a =4036 Å e c =6630 Å). La fase gamma ha un reticolo tetragonale a corpo centrato. Le altre fasi sono stabili solo a pressioni superiori a 20000 bar.
Sopra l'elevatissima pressione di 1,5 Mbar vi è una fase semiconduttrice. Non sono ancora stati eseguiti studi strutturali accurati, ma da misure spettroscopiche si può dedurre che non siano più presenti molecole N2.
Proprietà di trasporto
[modifica | modifica wikitesto]| Proprietà di trasporto di N2 in fase gassosa (p = 1 bar, T = 298 K) | |
| Conducibilità termica (W m−1 s−1) | 0,025724 |
| Conducibilità elettrica | — |
| Viscosità (μP) | 178,05 |
| Velocità del suono (m s−1) | 351,98 |
| Proprietà di trasporto di N2 in fase liquida (p = 1 bar, T = 77,244 K, p.eb.) | |
| Conducibilità termica (W m−1 s−1) | 0,14605 |
| Conducibilità elettrica | — |
| Viscosità (μP) | 1613,7 |
| Velocità del suono (m s−1) | 852,53 |
Proprietà chimiche
[modifica | modifica wikitesto]Reattività di N2
[modifica | modifica wikitesto]La molecola N2 è incolore, inodore e insapore. Presenta un'eccezionale inerzia chimica, dovuta principalmente all'elevata energia di legame, alla scarsa polarizzabilità e all'assenza di momento dipolare.
Reazioni a temperatura ambiente
[modifica | modifica wikitesto]Le uniche reazioni note di N2 a temperatura ambiente sono le seguenti.
- L'ossidazione del litio metallico
- N2(g) + 6 Li(s) → 2 Li3N(s)
- Si tratta però di una reazione lenta.
- La coordinazione di alcuni complessi metallici
- [Ru(NH3)5(H2O)]2+(aq) + N2(g) → [Ru(NH3)5(N2)]2+(aq) + H2O
- WCl4(PMe2Ph)2 + 2 N2(g) + 2 PMe2Ph + 4 Na(Hg) → W(PMe2Ph)4(N2)2 + 4 NaCl
- MoCl5 + 4 PR3 + 2 N2(g) + 5 Na(Hg) → trans-Mo(N2)2(PR3)4 + 5 NaCl
- Nel primo caso la molecola di azoto non viene particolarmente influenzata dalla coordinazione, mentre nei complessi con gli elementi del 6º gruppo viene attivata nei confronti di forti elettrofili e forti nucleofili.
- Fissazione biologica
Reazioni a temperature elevate
[modifica | modifica wikitesto]A temperature elevate N2 mostra una reattività maggiore combinandosi direttamente con berillio, magnesio, calcio, stronzio, bario, torio, alluminio, scandio, titanio, vanadio, cromo, manganese, ittrio, zirconio, afnio, molibdeno, tungsteno, torio, uranio, plutonio e tutti i lantanoidi con formazione dei rispettivi nitruri.
Scaldando il coke all'incendescenza in atmosfera di azoto, si ha la sintesi di cianogeno, (CN)2.
La reazione che più è stata studiata per via dell'enorme interesse pratico è la sintesi dell'ammoniaca secondo il processo Haber-Bosch:
- N2(g) + 3 H2(g) ⇄ 2 NH3(g)
Si esegue a temperature comprese tra 450 e 500 °C, a pressioni comprese tra 200 e 1000 atm, in presenza di un catalizzatore costituito da ferro e tracce di Al2O3. La grande importanza di questa reazione deriva dal fatto che tutto l'azoto impiegato nell'industria chimica per la preparazione di numerosissimi composti viene dall'ammoniaca. L'impatto del processo Haber a livello sociale, economico, militare e politico nel corso del Novecento è stato notevolissimo. Ogni anno vengono convertiti in ammoniaca circa 50 milioni di tonnellate di N2.
Prima della messa a punto del processo Haber uno dei metodi utilizzati per la fissazione dell'azoto era la reazione di azoto con carburo di calcio per dare calcio cianammide:
- N2(g) + CaC2(s) → CaNCN(s)
La reazione avviene intorno ai 1000 °C.
Ma il primo metodo industriale per la fissazione dell'azoto, proposto dall'inglese William Crookes e poi migliorato dai norvegesi Birkeland ed Eyde, era basato sull'ossidazione da parte di O2:
- N2(g) + O2(g) → 2 NO(g) ΔrHº(298 K) = 90,29 kJ mol−1
Data l'elevata endotermicità della reazione, nel processo Birkeland-Eyde si operava ad elevata temperatura insufflando aria su un arco elettrico di forma circolare.
Questa reazione è responsabile ogni anno della conversione di circa 30 milioni di tonnellate di azoto in monossido di azoto e biossido di azoto; 20 milioni di tonnellate sono prodotte nelle combustioni, soprattutto nei motori a scoppio delle automobili, mentre circa 10 milioni di tonnellate a causa dei fulmini.
Questo fenomeno influisce notevolmente sulla chimica dell'atmosfera.
Nella troposfera gli ossidi di azoto catalizzano la formazione di ozono O3 secondo il seguente ciclo:
- NO2(g) + hν(λ < 400 nm) → O(g) + NO(g)
- O(g) + O2(g) + M(g) → O3(g) + M*(g)
- 2 NO(g) + O2(g) → 2 NO2(g)
Sia l'ozono che il biossido di azoto sono dannosi per gli animali attaccando la mucosa respiratoria (v. bronchite acuta irritativa).
Invece nella stratosfera gli ossidi di azoto possono distruggere lo strato di ozono necessario per l'assorbimento della radiazione UV di alta frequenza:
- NO(g) + O3(g) → NO2(g) + O2(g)
- NO2(g) + O(g) → NO(g) + O2(g)
L'apparente comportamento contraddittorio è determinato dal fatto che la concentrazione di ozono e ossigeno atomico nella stratosfera è molto superiore rispetto alla troposfera.
Piogge acide
[modifica | modifica wikitesto]Gli ossidi di azoto sono inoltre tra i maggiori responsabili dell'elevata acidità delle piogge in alcune aree particolarmente sottoposte a inquinamento atmosferico, poiché il biossido di azoto reagisce con l'acqua formando acido nitrico:
- 3 NO2(g) + H2O(g) → 2 HNO3(g) + NO(g)
Piogge troppo acide, oltre a rovinare i monumenti costruiti con rocce calcaree, possono creare non pochi problemi alle piante aumentando l'acidità dei terreni e di conseguenza la solubilità di alcuni ioni metallici, per esempio Al3+, che se assimilati indeboliscono la pianta compromettendone la crescita e in alcuni casi la sopravvivenza.
Considerazioni generali sulla chimica dell'azoto
[modifica | modifica wikitesto]L'azoto è un tipico non metallo. È uno dei pochi elementi per cui la regola dell'ottetto è valida con poche eccezioni. La sua chimica è quasi esclusivamente covalente, l'anione N3− è fortemente polarizzabile e può essere individuato come tale solo nei nitruri dei metalli alcalini e alcalino terrosi.
Stereochimica
[modifica | modifica wikitesto]| Numero di coordinazione | Geometria | Esempi |
| 0 | azoto atomico | |
| 1 | NO, N2, C2N2, CN−, RCN, NNO | |
| 2 | lineare | HNNN, NO+2 |
| angolare | NO−2, NH−2, ClNO, NO2 | |
| 3 | piramidale | NH3, N2H4, Ammine, NCl3 |
| planare | HNO3, FNO2 | |
| 4 | tetraedrica | NH+4, NF3O, NF+4 |
| 5 | bipiramide trigonale | [N(AuPPh3)5]+ |
| 6 | ottaedrica | nitruri interstiziali |
| 8 | cubica | nitruri ternari |
L'azoto forma legami con tutti gli elementi della tavola periodica ad eccezione dei gas nobili più leggeri (He, Ne e Ar). Nella tabella a fianco sono riportate le numerose stereochimiche che può adottare.
Legami a idrogeno
[modifica | modifica wikitesto]L'azoto è tra gli atomi più elettronegativi e quindi, così come l'ossigeno e il fluoro, è in grado di partecipare alla formazione di legami a idrogeno agendo sia da donatore di protoni che come accettore.
La lunghezza tipica dei legami a idrogeno N-H··N si aggira intorno ai 3,0 Å. Legami di questo tipo sono responsabili dell'elevato punto di ebollizione dell'ammoniaca se paragonato a quello degli altri idruri degli elementi del 15º gruppo della tavola periodica. Questo costituisce un esempio classico degli effetti del legame a idrogeno.
Legami a idrogeno in cui sono coinvolti atomi di azoto giocano un ruolo fondamentale nell'accoppiamento dei nucleotidi nella struttura del DNA, tenendo "incollati" i due filamenti che formano la doppia elica. Anche la struttura delle proteine è fortemente influenzata da legami a idrogeno che coinvolgono atomi di azoto.
Chimica redox in soluzione acquosa
[modifica | modifica wikitesto]Nonostante non abbiano significato fisico, i numeri di ossidazione sono spesso impiegati, soprattutto in ambito didattico, per razionalizzare la chimica degli elementi e per bilanciare le reazioni di ossidoriduzione. L'azoto in questo senso è uno degli elementi che presenta la maggior varietà, adottando tutti i valori da −3 a +5. Uno strumento efficace per visualizzare le stabilità termodinamiche relative dei diversi stati di ossidazione in soluzione acquosa può essere fornita da un diagramma di Frost:
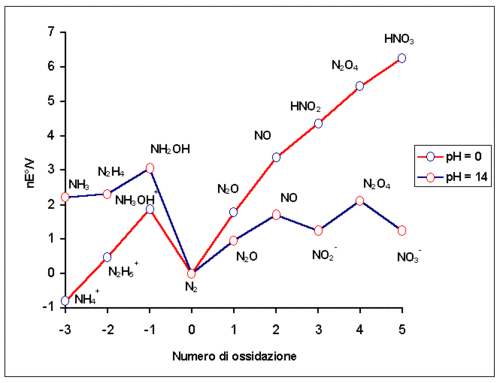
Specie chimiche che hanno elevata stabilità termodinamica rispetto a numerose reazioni (che dunque spesso possono favorire le reazioni che le vedono come prodotti) vengono talvolta chiamate pozzi termodinamici. Fra queste si possono annoverare CO2, H2O, NaCl e appunto N2. Questa caratteristica dell'azoto è l'aspetto più evidente del diagramma.
È però necessario osservare che la formazione di N2 è cineticamente sfavorita, e quasi sempre la riduzione di nitrati e nitriti si ferma a NO2 o NO, talvolta anche procedere fino a NH+4.
Si può notare che la chimica redox dei composti dell'azoto è significativamente influenzata dal pH, in particolare nitrati e nitriti, che a pH bassi sono forti ossidanti, perdono quasi totalmente il loro potere ossidante in ambiente alcalino.
Viene di seguito riportata una tabella che raccoglie i potenziali standard per alcune semireazioni in cui compaiono specie chimiche contenenti azoto.
| Semireazione di riduzione | Eº (V) |
| H2N2O2 + 2 H+ + 2 e− → N2 + 2 H2O | +2,65 |
| HN3 + 3 H+ + 2 e− → NH+4 + N2 | +1,96 |
| N2O + 2 H+ + 2 e− → N2 + H2O | +1,77 |
| NO+ + e− → NO | +1,46 |
| 2 NH3OH+ + H+ + 2 e− → 2 N2H+5 + 2 H2O | +1,42 |
| NH3OH+ + 2 H+ + 2 e− → NH+4 + H2O | +1,35 |
| HNO2 + 4 H+ + 4 e− → N2O + 3 H2O | +1,29 |
| N2H+5 + 3 H+ + 2 e− → 2 NH+4 | +1,275 |
| N2O4 + 2 H+ + 2 e− → 2 HNO2 | +1,065 |
| N2O4 + 4 H+ + 2 e− → 2 NO + 2 H2O | +1,035 |
| HNO2 + H+ + e− → NO + H2O | +0,983 |
| NO−3 + 4 H+ + 3 e− → NO + 2 H2O | +0,957 |
| NO−3 + 3 H+ + 2 e− → HNO2 + H2O | +0,94 |
| 2 HNO2 + 4 H+ + 4 e− → H2N2O2 + 2 H2O | +0,86 |
| 2 NO−3 + 4 H+ + 2 e− → N2O4 + 2 H2O | +0,803 |
| 2 NO + 2 H+ + 2 e− → H2N2O2 | +0,712 |
| HN3 + 11 H+ + 8 e− → 3 NH+4 | +0,695 |
| H2N2O2 + 6 H+ + 4 e− → 2 NH3OH+ | +0,387 |
| N2 + 5 H+ + 4 e− → N2H+5 | -0,23 |
| 3/2 N2 + H+ + e− → HN3 | -3,09 |
Composti dell'azoto
[modifica | modifica wikitesto]
Meritano una menzione particolare i composti più importanti.
- Ammoniaca (NH3)
- Idrazina (H2N-NH2)
- Idrossilammina (H2N-OH)
- Ossido di diazoto (N2O)
- Ossido di azoto (NO)
- Diossido di azoto (NO2)
- Tetrossido di diazoto (N2O4)
- Pentossido di diazoto (N2O5)
- Acido nitrico (HNO3)
- Acido nitroso (HNO2)
- Acido cianidrico (HCN)
- Nitrati
- Nitriti
- Cianuri
- Urea
- Amminoacidi
Impieghi
[modifica | modifica wikitesto]La maggior parte dell'azoto prodotto è destinato alla sintesi dell'ammoniaca, con cui verranno poi preparati fertilizzanti, polimeri, esplosivi, coloranti e altri prodotti.
Grandi quantità sono anche destinate alle applicazioni criogeniche e per la creazione di atmosfere inerti.
Applicazioni criogeniche dell'azoto liquido
[modifica | modifica wikitesto]
L'azoto liquido, o meglio N2 liquido, avendo il punto di ebollizione a −195,82 °C e un costo di produzione ragionevole, è molto utilizzato per il raffreddamento di apparecchiature scientifiche, la crioconservazione di campioni biologici e vari altri processi nei quali è necessario ottenere o conservare temperature estremamente basse.
Applicazioni per atmosfere inerti
[modifica | modifica wikitesto]L'azoto molecolare N2 è particolarmente indicato per la creazione di atmosfere inerti in diversi ambiti industriali e tecnologici in virtù della sua scarsa reattività, dell'abbondanza e del basso costo. Viene dunque preferito all'argon Ar, gas che offre in assoluto le prestazioni migliori, in quasi tutte le applicazioni a temperatura ambiente, talvolta anche alle alte temperature.
Industria chimica e petrolchimica
[modifica | modifica wikitesto]In diverse reazioni chimiche, condotte sia nell'industria sia nei laboratori, è richiesta un'atmosfera priva di O2 affinché si giunga ai prodotti desiderati. Grandi quantità di azoto sotto forma di azoto molecolare (N2) vengono riservate per questo scopo.
N2 viene anche impiegato per le bonifiche e le polmonazioni di reattori e serbatoi, sempre per evitare che i composti contenuti possano reagire, anche in maniera esplosiva, con O2 contenuto dell'aria.
Nella lavorazione delle materie plastiche si usa l'azoto per la produzione di polimeri espansi e nello stampaggio ad iniezione assistito da gas.
Metallurgia
[modifica | modifica wikitesto]In numerosi processi metallurgici è indispensabile un'atmosfera priva di ossigeno per evitare la formazione di ossidi, l'azoto non è indicato come materiale inerte per tutti i trattamenti, poiché ad alta temperatura reagisce con alcuni metalli, in alcuni trattamenti termico-metallurgici l'interazione è voluta:
- Nella ricottura (annealing, in inglese) di acciai, rame, alluminio e altri metalli e leghe; in alcuni processi è necessaria una diluizione con argon (decisamente migliore) per mantenere l'inerzia dell'azoto.
- Nella sinterizzazione di acciaio e alluminio.
- Come costituente delle miscele nella carbocementazione in fase gassosa degli acciai.
- Nella protezione durante la brasatura, il taglio e la saldatura; i metalli più reattivi nei confronti dell'azoto, per esempio titanio e zirconio, necessitano dell'argon come gas protettivo.
- Nella tempra di acciai in forni sottovuoto.
- Come elemento di apporto nella nitrurazione ad alta temperatura degli acciai, dove la formazione di nitruri conferisce durezza e resistenza alla usura al metallo negli strati superficiali, conservando per contro resilienza agli strati profondi.
Industria alimentare
[modifica | modifica wikitesto]L'azoto è largamente impiegato, puro o in miscela, nella conservazione in atmosfera protettiva di prodotti alimentari industriali. Miscele particolarmente ricche di azoto sono usate nella protezione di alimenti che contengono quantità significative di grassi insaturi: in questi casi l'O2 viene eliminato per evitare l'irrancidimento.
L'azoto molecolare N2 viene di norma impiegato anche nell'imbottigliamento dei vini, per evitare che il vino venga a contatto con ossigeno molecolare O2.
Industria elettronica
[modifica | modifica wikitesto]Nella produzione di componenti elettronici come transistor, diodi e circuiti integrati si usa l'azoto sia come gas vettore dei gas di processo, sia per la creazione di atmosfere inerti durante i trattamenti termici.
Condizionamento
L'azoto viene utilizzato negli impianti frigoriferi e condizionatori per la prova di tenuta di tubazioni e saldature sotto pressione, prima di effettuare la carica di gas refrigerante con il quale funzioneranno gli impianti. Durante le operazioni di riparazione viene inoltre utilizzato per pulire la parte interna dei tubi dalle impurità e i residui che si vengono a creare durante le saldature sul rame.[8]
Altre applicazioni
[modifica | modifica wikitesto]L'azoto molecolare si usa per gonfiare gli pneumatici delle automobili, per spurgare l'interno dei binocoli (sostituendo l'ossigeno per evitare l'appannamento delle lenti) o nell'estrazione di petrolio e gas naturale. Costituisce il mezzo attivo del laser ad azoto[9] e viene anche utilizzato per il "lavaggio" (flussaggio) di serbatoi e delle tubazioni nelle industrie (il flusso di N2 rimuove l'ossigeno con gli eventuali gas o fluidi combustibili o reattivi contenuti). L'azoto viene inoltre usato in Alabama al fine di causare ipossia nei condannati a morte, costretti a respirarlo attraverso una apposita maschera. La prima esecuzione con l'azoto avvenne il 22 gennaio 2024 nel carcere di Atmore nei confronti di Kenneth Eugene Smith, morto tra gli spasmi dopo 22 minuti di inalazione forzata del gas inerte.[10]
Precauzioni
[modifica | modifica wikitesto]Ad alte pressioni parziali, raggiungibili con camere iperbariche o durante le immersioni subacquee, l'azoto si comporta come gas narcotico ed è la causa principale della malattia da decompressione. Particolare attenzione va posta nell'utilizzo di tale gas nella forma liquida. Le ustioni dovute al freddo non sono immediatamente avvertibili. I recipienti contenenti azoto liquido a contatto con l'aria tendono a rilasciare il liquido e contemporaneamente a condensare umidità, O2 e acetilene al loro interno, formando in tal modo atmosfere ipossiche (con scarsità di O2) che in ambiente poco ventilato possono risultare fatali.
In caso di flussaggio (lavaggio gassoso) con azoto di serbatoi o di altri vani accessibili occorre ricordare che le atmosfere inerti sono incompatibili con la sopravvivenza umana. Dato che l'azoto è inodore, l'anossia (anche totale) può non essere avvertita: il soggetto non prova alcuna difficoltà respiratoria, l'anossia si manifesta con l'improvvisa perdita dei sensi e la morte in breve tempo. Deve essere quindi impedita la possibilità fisica che le persone abbiano accesso ai vani, e prima di ammetterne la presenza deve essere verificata la rimozione completa dell'atmosfera inerte.
Note
[modifica | modifica wikitesto]- ^ a b http://www.treccani.it/vocabolario/azoto/
- ^ Online Etymology Dictionary, su etymonline.com.
- ^ Online Etymology Dictionary, su etymonline.com.
- ^ http://www.treccani.it/vocabolario/nitrogeno
- ^ Dizionario etimologico online, su etimo.it.
- ^ Karl Heinz Neeb, The Radiochemistry of Nuclear Power Plants with Light Water Reactors, Berlino-New York, Walter de Gruyter, 1997, ISBN 3-11-013242-7.
- ^ Attivazione dell'azoto, su chimdocet.it. URL consultato il 9 luglio 2020 (archiviato dall'url originale il 15 agosto 2021).
- ^ (EN) Yu Chang Zhen, Why Nitrogen is Preferred to Use for Flush & Leak Test AC?, su aircondlounge, 19 luglio 2021. URL consultato il 15 marzo 2022.
- ^ (EN) IUPAC Gold Book, "nitrogen laser", su goldbook.iupac.org.
- ^ Giovanni Esperti, La prima condanna a morte con l'azoto puro, su Wired Italia, 20 settembre 2023. URL consultato il 15 luglio 2024.
Bibliografia
[modifica | modifica wikitesto]- Francesco Borgese, Gli elementi della tavola periodica. Rinvenimento, proprietà, usi. Prontuario chimico, fisico, geologico, Roma, CISU, 1993, ISBN 88-7975-077-1.
- R. Barbucci, A. Sabatini, P. Dapporto, Tavola periodica e proprietà degli elementi, Firenze, Edizioni V. Morelli, 1998 (archiviato dall'url originale il 22 ottobre 2010).
- F. A. Cotton G. Wilkinson, Chimica Inorganica, Casa Editrice Ambrosiana, 3ª Edizione, 1984
- N. N. Greenwood A. Earnshaw, Chemistry of the Elements, Butterworth Heinemann, 2ª Edizione, 1997
- D. F. Shriver P. W. Atkins, Inorganic Chemistry, Oxford University Press, 3ª Edizione, 1999
- L. Malatesta, Compendio di Chimica Inorganica, Casa Editrice Ambrosiana, 4ª Edizione, 1999
- L. Berti M. Calatozzolo R. di Bartolo, L'industria dell'azoto, Casa Editrice G.D'Anna, 1994
- A. J. Ihde, The Development of Modern Chemistry, Dover Publications, 2ª Edizione, 1984
- C. E. Wayne R. P. Wayne, Photochemistry, Oxford Chemistry Primers, 1999
- P. W. Atkins, Physical Chemistry, Oxford University Press, 6ª Edizione, 1998
Voci correlate
[modifica | modifica wikitesto]- Azotemia
- Azoto liquido
- Azoto ureico
- Bilancio dell'azoto
- Ciclo dell'azoto
- Ciclo del carbonio-azoto
- Economia ad azoto liquido
- Narcosi da azoto
Altri progetti
[modifica | modifica wikitesto] Wikiquote contiene citazioni di o su azoto
Wikiquote contiene citazioni di o su azoto Wikizionario contiene il lemma di dizionario «azoto»
Wikizionario contiene il lemma di dizionario «azoto» Wikimedia Commons contiene immagini o altri file su azoto
Wikimedia Commons contiene immagini o altri file su azoto
Collegamenti esterni
[modifica | modifica wikitesto]- azoto, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- (EN) R. Thomas Sanderson, nitrogen, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Database del NIST, su webbook.nist.gov.
- Polimerica, su polimerica.it.
| Controllo di autorità | Thesaurus BNCF 14013 · LCCN (EN) sh85092062 · GND (DE) 4125639-6 · BNE (ES) XX525774 (data) · BNF (FR) cb11975683p (data) · J9U (EN, HE) 987007531393105171 · NDL (EN, JA) 00573098 |
|---|



