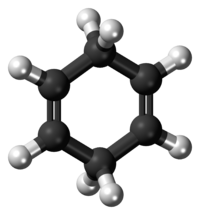
1,4-cicloesadiene
| 1,4-cicloesadiene | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | |
| Cicloesa-1,4-diene | |
| Nomi alternativi | |
| 1,4-diidrobenzene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H8 |
| Massa molecolare (u) | 80,13 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 211-043-1 |
| PubChem | 12343 |
| SMILES | C1C=CCC=C1 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,847[1] |
| Indice di rifrazione | 1,473 |
| Solubilità in acqua | poco solubile[1] |
| Coefficiente di ripartizione 1-ottanolo/acqua | 2,30 |
| Temperatura di fusione | –49 °C[1] |
| Temperatura di ebollizione | 88-90 °C[1] |
| Tensione di vapore (Pa) a 25 °C K | 77,4 mmHg |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | ≈68[2] |
| S0m(J·K−1mol−1) | 189,37[2] |
| C0p,m(J·K−1mol−1) | ≈144[2] |
| ΔcombH0 (kJ·mol−1) | ≈–3572[2] |
| Indicazioni di sicurezza | |
| Punto di fiamma | –6 °C[1] |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 225 - 340 - 350 - 204 [1] |
| Consigli P | 210 - 280 - 301+310 - 303+361+353 - 405 - 501 [1] |
Il 1,4-cicloesadiene è un diene ciclico con due doppi legami isolati (non coniugati), di formula bruta C6H8, o anche 1,4-ciclo-C6H8. Con i doppi legami coniugati è ben noto anche l'isomero 1,3-cicloesadiene (1,3-ciclo-C6H8). A temperatura ambiente è un liquido incolore, volatile e infiammabile, poco solubile in acqua[1], ma solubile negli idrocarburi, negli eteri e nella maggior parte dei solventi organici.[3] Il 1,4-cicloesadiene non ha applicazioni industriali. Viene utilizzato come donatore di una coppia di atomi di idrogeno, trasformandosi in benzene, in reazioni di idrogenazione catalitica,[4] impiegata anche per rimuovere alcuni gruppi funzionali.[5][6]
Un suo derivato naturale è il γ-terpinene, contenuto nell'olio essenziale di coriandolo.[7]
Proprietà e struttura molecolare[modifica | modifica wikitesto]
L'1,4-cicloesadiene è un composto endotermico (ΔHƒ° =66,1 kJ/mol[8]), ma è cineticamente piuttosto stabile se tenuto a bassa a temperatura per prevenire la polimerizzazione[9] e protetto dal contatto con l'ossigeno dell'aria, con il quale tende lentamente ad ossidarsi. Nella molecola i doppi legami sono isolati e, come tali, dovrebbero interagire solo debolmente; tuttavia, il potenziale di ionizzazione della molecola è di 8,82 eV e la sua affinità protonica ammonta a 837 kJ/mol;[10] confrontando con i corrispondenti valori per l'etene (10,51 eV; 680,5 kJ/mol[11]), si può notare come l'1,4-cicloesadiene sia alquanto più facile da ionizzare e protonare.
La sua struttura molecolare ha suscitato interesse teorico riguardo all'accoppiamento preferenziale di orbitali π: se questo avvenga attraverso i legami oppure direttamente attraverso lo spazio, con il relativo ordinamento energetico risultante.[12]
La molecola è stata indagata a più riprese[13] con la diffrazione elettronica in fase gassosa, con calcoli quantomeccanici ed anche, allo stato solido, con la diffrattometria a raggi X a bassa temperatura, oltre ad indagini spettroscopiche IR, Raman[14] e di RMN,[15] tutte e tre queste ultime concordi nell'assegnare la conformazione planare come la più probabile. Non è però del tutto chiaro se lo scheletro della molecola sia esattamente planare, ma in ogni caso sembra molto vicino a tale condizione. Assumendo planarità, come per lo più è stato fatto,[16] la simmetria della molecola sarebbe D2h, il che comporta momento dipolare nullo.
Un'indagine di diffrazione elettronica ha fornito lunghezze ed angoli di legame di seguito riportati:[17]
- r(C=C) = 133,4 pm; r(C–C) = 149,6 pm; r(Csp2–H) = 110,3 pm; r(Csp3–H) = 111,4 pm;
- ∠(C=C–C) = 123,4°; ∠(C–C–C) = 113,3°.
Sono anche riportate le distanze tra atomi Csp2 opposti nell'anello (283,0 pm), come pure quelle di atomi Csp3 opposti (298,4 pm); queste distanze sono comunque minori del doppio del raggio di van der Waals del carbonio, che è nell'intervallo 330-340 pm.[18] Gli autori propendono per lo scheletro planare ma non escludono una lieve deformazione verso una conformazione a sedia.[17]
Un'altra indagine di diffrazione elettronica riporta come preferita una conformazione a barca, con un angolo diedro di 159,3°.[19]
Un'analisi diffrattometrica ai raggi X eseguita su un monocristallo di 1,4-cicloesadiene a -120° C ha stabilito che, almeno per molecole all'interno del reticolo cristallino, lo scheletro è planare e ha fornito i seguenti parametri strutturali:[20]
- r(C=C) = 131,8 pm; r(C–C) = 148,6 pm;
- ∠(C=C–C) = 123,5°; ∠(C–C–C) = 113,1°.
Un'indagine strutturale teorica, basata su calcoli quantomeccanici conclude che lo scheletro della molecola è planare e dà i seguenti parametri strutturali:[21]
- r(C=C) = 131,7 pm; r(C–C) = 150,9 pm;
- ∠(C=C–C) = 123,8°; ∠(C–C–C) = 112,4°.
Infine, una indagine di spettroscopia di quantità di moto elettronica sul norbornadiene e sull'1,4-cicloesadiene è risultata, per quest'ultimo, in accordo alla conformazione planare dello scheletro e incompatibile con una conformazione a barca (simmetria molecolare C2v).[22]
Complessi metallici[modifica | modifica wikitesto]
Come fanno in generale le olefine, l'1,4-cicloesadiene e il suo isomero si complessano facilmente con centri metallici in bassi stati di ossidazione. Per reazione con il ferro pentacarbonile si ha l'espulsione di due carbonili (regola dei 18 elettroni) e la formazione del complesso olefinico ma con isomerizzazione a dare la diolefina coniugata (se non lo era), per cui entrambi gli isomeri danno luogo allo stesso complesso:
- 1,4-ciclo-C6H8 + Fe(CO)5 → (1,3-ciclo-C6H8)Fe(CO)3 + 2 CO
e una reazione analoga avviene anche con il suo analogo perfluorurato, l'octafluoro-1,4-cicloesadiene.[23] Con lo ione Ag+ si forma un complesso, ma senza isomerizzazione:[24]
- 1,4-ciclo-C6H8 + AgBF4 → (1,4-ciclo-C6H8)AgBF4
Sintesi[modifica | modifica wikitesto]
Il 1,4-cicloesadiene può essere preparato a partire da benzene tramite una riduzione di Birch.[25] Per questa reazione il benzene in ammoniaca liquida è trattato con sodio e un alcool come donatore di protoni:

Il 1,4-cicloesadiene può essere ottenuto anche per deidrobromurazione di 1,4-dibromocicloesano, tuttavia in questo modo il prodotto principale è l'isomero 1,3-cicloesadiene.[26]
Tossicità/indicazioni di sicurezza[modifica | modifica wikitesto]
Il 1,4-cicloesadiene è disponibile in commercio, in genere stabilizzato con butilidrossitoluene. Per rallentarne la decomposizione va tenuto sotto azoto in frigorifero.[6] È un liquido facilmente infiammabile; vanno evitate fonti di calore, fiamme e scintille. È tossico per ingestione e inalazione. Viene considerato cancerogeno e mutageno, nonché pericoloso per gli organismi acquatici.[1]
Note[modifica | modifica wikitesto]
- ^ a b c d e f g h i Alfa Aesar 2014
- ^ a b c d US National Institute of Standards and Technology
- ^ (EN) John C. Walton e Fernando Portela-Cubillo, 1,4-Cyclohexadiene, John Wiley & Sons, Ltd, 17 settembre 2007, DOI:10.1002/047084289x.rn00806, ISBN 978-0-471-93623-7. URL consultato il 31 maggio 2023.
- ^ (EN) John F. Quinn, Dana A. Razzano e Kathryn C. Golden, 1,4-Cyclohexadiene with Pd/C as a rapid, safe transfer hydrogenation system with microwave heating, in Tetrahedron Letters, vol. 49, n. 42, 13 ottobre 2008, pp. 6137–6140, DOI:10.1016/j.tetlet.2008.08.023. URL consultato il 31 maggio 2023.
- ^ Felix et al. 1978
- ^ a b J. C. Walton e Portela-Cubillo 2007
- ^ Valtcho D. Zheljazkov, Tess Astatkie e Vicki Schlegel, Hydrodistillation Extraction Time Effect on Essential Oil Yield, Composition, and Bioactivity of Coriander Oil, in Journal of Oleo Science, vol. 63, n. 9, 2014, pp. 857–865, DOI:10.5650/jos.ess14014. URL consultato il 31 maggio 2023.
- ^ (EN) 1,4-Cyclohexadiene, su webbook.nist.gov. URL consultato il 30 maggio 2023.
- ^ I. L. Finar, ORGANIC CHEMISTRY The fundamental principles, Fourth Edition, Longmans, 1963, p. 483.
- ^ (EN) 1,4-Cyclohexadiene, su webbook.nist.gov. URL consultato il 31 maggio 2023.
- ^ (EN) Ethylene, su webbook.nist.gov. URL consultato il 31 maggio 2023.
- ^ Eric V. Anslyn e Dennis A. Dougherty, Modern Physical Organic Chemistry, University Science Books, 2006, pp. 854-855, ISBN 978-1-891389-31-3.
- ^ (EN) Peter W. Rabideau, The conformational analysis of 1,4-cyclohexadienes: 1,4-dihydrobenzenes, 1,4-dihydronaphthalenes, and 9,10-dihydroanthracenes, in Accounts of Chemical Research, vol. 11, n. 4, 1º aprile 1978, pp. 141–147, DOI:10.1021/ar50124a003. URL consultato il 31 maggio 2023.
- ^ (EN) Howard D. Stidham, Vibrational spectra of 1,4-cyclohexadiene and 1,4-cyclohexadiene-d8, in Spectrochimica Acta, vol. 21, n. 1, 1º gennaio 1965, pp. 23–32, DOI:10.1016/0371-1951(65)80102-3. URL consultato il 31 maggio 2023.
- ^ (EN) Edgar W. Garbisch e Michael G. Griffith, The conformation of 1,4-cyclohexadiene from steroisomeric allylic-allylic proton couplings, in Journal of the American Chemical Society, vol. 90, n. 13, 1968-06, pp. 3590–3592, DOI:10.1021/ja01015a068. URL consultato il 31 maggio 2023.
- ^ CCCBDB Experimental Data page 1, su cccbdb.nist.gov. URL consultato il 31 maggio 2023.
- ^ a b (EN) G. Dallinga e (Miss)L. H. Toneman, Electron diffraction by gases: The molecular structure of 1,4-cyclohexadiene, in Journal of Molecular Structure, vol. 1, n. 2, 1º dicembre 1967, pp. 117–125, DOI:10.1016/0022-2860(67)85001-4. URL consultato il 30 maggio 2023.
- ^ J. E. Huheey, E. A. Keiter e R. L. Keiter, Chimica Inorganica, Principi, Strutture, Reattività, 2ª ed., Piccin, 1999, p. 292, ISBN 88-299-1470-3.
- ^ (EN) Heinz Oberhammer e Simon H. Bauer, Structures and conformations of the cyclohexadienes, in Journal of the American Chemical Society, vol. 91, n. 1, 1969-01, pp. 10–16, DOI:10.1021/ja01029a002. URL consultato il 31 maggio 2023.
- ^ (EN) George A. Jeffrey, Juergen. Buschmann e Christian W. Lehmann, The structure of 1,4-cyclohexadiene at 153 K, in Journal of the American Chemical Society, vol. 110, n. 21, 1988-10, pp. 7218–7219, DOI:10.1021/ja00229a049. URL consultato il 31 maggio 2023.
- ^ (EN) Svein Saebo e James E. Boggs, Structure and conformations of cyclohexene,1,4-cyclohexadiene, and 1,3-cyclohexadiene, in Journal of Molecular Structure, vol. 73, n. 1, 1º aprile 1981, pp. 137–144, DOI:10.1016/0022-2860(81)85056-9. URL consultato il 31 maggio 2023.
- ^ (EN) Masahiko Takahashi, Ryuji Ogino e Yasuo Udagawa, An electron momentum spectroscopy study of π orbitals of norbornadiene and 1,4-cyclohexadiene: evidence for through-space and through-bond interactions, in Chemical Physics Letters, vol. 288, n. 5, 29 maggio 1998, pp. 714–718, DOI:10.1016/S0009-2614(98)00363-7. URL consultato il 31 maggio 2023.
- ^ (EN) H. W. Quinn e J. H. Tsai, Olefin Complexes of the Transition Metals, vol. 12, Academic Press, 1º gennaio 1970, pp. 263–264, DOI:10.1016/s0065-2792(08)60050-3. URL consultato il 31 maggio 2023.
- ^ (EN) H. W. Quinn e J. H. Tsai, Olefin Complexes of the Transition Metals, vol. 12, Academic Press, 1º gennaio 1970, p. 340, DOI:10.1016/s0065-2792(08)60050-3. URL consultato il 31 maggio 2023.
- ^ Alder e Münz 1959
- ^ Markownikoff 1898
Bibliografia[modifica | modifica wikitesto]
- (DE) K. Alder e F. Münz, Diensynthese und substituierende Addition beim Divinyl-methan-typus Addition von Maleinsäure-anhydrid an Pentadien-1,4 und an 1,4-Dihydro-benzol, in Justus Liebigs Annalen der Chemie, vol. 565, n. 1, 1949, pp. 126–135, DOI:10.1002/jlac.19495650113.
- Alfa Aesar, Scheda di dati di sicurezza del 1,4-cicloesadiene (PDF), su alfa.com, 2014. URL consultato il 26 settembre 2015 (archiviato dall'url originale il 29 settembre 2015).
- (EN) A. M. Felix, E. P. Heimer, T. J. Lambros, C. Tzougraki e J. Meienhofer, Rapid removal of protecting groups from peptides by catalytic transfer hydrogenation with 1,4-cyclohexadiene, in J. Org. Chem., vol. 43, n. 21, 1978, pp. 4194–4196, DOI:10.1021/jo00415a045.
- (DE) W. Markownikoff, Derivate der Naphten- oder Cyclohexanreihe, in Justus Liebigs Annalen der Chemie, vol. 302, n. 1-2, 1898, pp. 1-42, DOI:10.1002/jlac.18983020102.
- US National Institute of Standards and Technology, 1,3-Cyclohexadiene, in NIST Chemistry WebBook, 2011. URL consultato il 25 settembre 2015.
- (EN) J. C. Walton e F. Portela-Cubillo, 1,4-Cyclohexadiene, in e-EROS Encyclopedia of Reagents for Organic Synthesis, 2007, DOI:10.1002/047084289X.rn00806.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su 1,4-cicloesadiene
Wikimedia Commons contiene immagini o altri file su 1,4-cicloesadiene