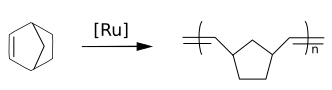Norbornene
| Norbornene | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| Biciclo[2.2.1]ept-2-ene | |
| Nomi alternativi | |
| 2-norbornene, norbornilene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C7H10 |
| Massa molecolare (u) | 94,15 |
| Aspetto | solido bianco |
| Numero CAS | |
| Numero EINECS | 207-866-0 |
| PubChem | 10352 |
| SMILES | C1CC2CC1C=C2 |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | 0,13 g/L a 20 °C |
| Coefficiente di ripartizione 1-ottanolo/acqua | 3,24 |
| Temperatura di fusione | 44–46 °C (317–319 K) |
| Temperatura di ebollizione | 95–96 °C (368–369 K) |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 11300 oral rat |
| Indicazioni di sicurezza | |
| Punto di fiamma | –8 °C (265 K) |
| Simboli di rischio chimico | |
  
| |
| Frasi H | 228 - 319 - 411 |
| Consigli P | 210 - 273 - 305+351+338 [1] |
Il norbornene è un composto organico di formula C7H10. In condizioni normali è un solido bianco di odore acre. È un alchene biciclico; lo scheletro può pensarsi ottenuto da quello del cicloesano, con l'aggiunta di un ponte metilenico (-CH2-) tra le posizioni 1 e 4 e un doppio legame in posizione 2. Questo conferisce una significativa tensione all'anello e comporta una notevole reattività in aggiunta a quella degli alcheni.
Il composto può essere sintetizzato con una reazione di Diels-Alder tra ciclopentadiene ed etilene.[2][3] Molecole correlate sono il norbornadiene che contiene due doppi legami (in 2 e 5), e il norbornano che è l'idrocarburo saturo da cui il norbornene formalmente deriva.
Il norbornene dà con l'acqua una reazione di idratazione catalizzata da acidi per formare norborneolo. Questa reazione e il catione 2-norbornilico implicato è di interesse scientifico per gli studi su carbocationi non classici.
Polinorborneni[modifica | modifica wikitesto]
I norborneni sono monomeri importanti per la polimerizzazione ROMP (Ring Opening Metathesis Polymerization = polimerizzazione per metatesi ad apertura d'anello), per esempio con il catalizzatore di Grubbs.
I polinorborneni sono polimeri con elevata temperatura di transizione vetrosa e alta trasparenza ottica. Oltre alla polimerizzazione ROMP, i monomeri del norbornene possono dare anche polimerizzazione per addizione vinilica.
Usi[modifica | modifica wikitesto]
Il norbornene non è usato in grandi quantità, come l'etilene e altri composti principali della chimica industriale. Viene usato per produrre intermedi di farmaci, pesticidi, fragranze artificiali e in generale in sintesi organiche. In combinazione con etilene si forma un copolimero nel ciclo-olefinico.
Sicurezza[modifica | modifica wikitesto]
Il norbornene è un solido infiammabile, irritante per gli occhi. È anche pericoloso per l'ambiente, in quanto tossico per gli organismi, compresi quelli acquatici. Non ci sono dati che indichino proprietà cancerogene.[4]
Note[modifica | modifica wikitesto]
- ^ Scheda del norbornene su IFA GESTIS, su gestis-en.itrust.de. URL consultato il 7 maggio 2021 (archiviato dall'url originale il 16 ottobre 2019).
- ^ Binger et. al.
- ^ Oda et. al.
- ^ Alfa Aesar.
Bibliografia[modifica | modifica wikitesto]
- Alfa Aesar, Scheda di sicurezza del norbornene (PDF), su alfa.com. URL consultato il 14-9-2011.
- P. Binger, P. Wedemann, U. H. Brinker, Cyclopropene: A New Simple Synthesis and its Diels-Alder Reaction with Cyclopentadiene, in Org. Synth., Coll. Vol. 10, 2004, p. 321. URL consultato il 14-9-2011.
- M. Oda, T. Kawase, T. Okada, T. Enomoto, 2-Cyclohexene-1,4-dione, in Org. Synth., Coll. Vol. 9, 1998, p. 186. URL consultato il 14-9-2011.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su norbornene
Wikimedia Commons contiene immagini o altri file su norbornene
| Controllo di autorità | LCCN (EN) sh2020006730 · J9U (EN, HE) 987012575354205171 |
|---|