Risonanza magnetica funzionale
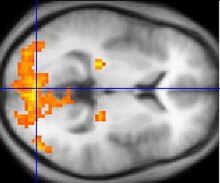
La risonanza magnetica funzionale, abbreviata RMF o fMRI (Functional Magnetic Resonance Imaging), è una tecnica di imaging biomedico che consiste nell'uso dell'imaging a risonanza magnetica per valutare la funzionalità di un organo o un apparato, in maniera complementare all'imaging morfologico.
Sebbene risonanza magnetica funzionale sia una terminologia generica, ovvero applicabile a qualsiasi tecnica di imaging a risonanza magnetica che dia informazioni aggiuntive rispetto alla semplice morfologia (ad esempio imaging metabolico, quantificazione del flusso sanguigno, imaging dei movimenti cardiaci etc.), essa è spesso usata come sinonimo di risonanza magnetica funzionale neuronale, una delle tecniche di neuroimaging funzionale di sviluppo più recente.
Questa tecnica è in grado di visualizzare la risposta emodinamica (cambiamenti nel contenuto di ossigeno del parenchima e dei capillari) correlata all'attività neuronale del cervello o del midollo spinale, nell'uomo o in altri animali.
Introduzione[modifica | modifica wikitesto]
Da più di cento anni, è noto che le variazioni del flusso sanguigno e dell'ossigenazione sanguigna nel cervello (emodinamica) sono strettamente correlate all'attività neurale. Charles Scott Sherrington e Charles S. Roy vengono frequentemente citati come i primi ad aver postulato, nel 1890, che il cervello possiede ‘meccanismi intrinseci attraverso i quali il suo supporto vascolare può variare localmente in corrispondenza di variazioni locali dell’attività funzionale’ (Kullmann, 2014. Brain. Editorial 137:307). Ma la prima tra le evidenze sperimentali è stata invece fornita a fine Ottocento dal fisiologo italiano Angelo Mosso, inventore della prima tecnica di neuroimaging funzionale della storia, conosciuta come ‘bilancia della circolazione umana’ e capace di misurare in modo non invasivo la ridistribuzione del sangue durante l’attività emotiva e intellettuale.[1]Il manoscritto che descrive i primi esprimenti fatti con la ‘bilancia della circolazione umana’ è stato riscoperto da Stefano Sandrone e colleghi nel 2013.[2].
Quando le cellule nervose sono attive, consumano l'ossigeno trasportato dall'emoglobina degli eritrociti che attraversano i capillari sanguigni locali. Effetto di questo consumo di ossigeno è un aumento del flusso sanguigno nelle regioni ove si verifica maggiore attività neurale, che avviene con un ritardo da 1 a 5 secondi circa. Tale risposta emodinamica raggiunge un picco in 4-5 secondi, prima di tornare a diminuire fino al livello iniziale (in genere scende anche sotto di esso): si hanno così, oltre che variazioni del flusso sanguigno cerebrale, anche modificazioni localizzate del volume sanguigno cerebrale e della concentrazione relativa di ossiemoglobina (emoglobina ossigenata) e deossiemoglobina (emoglobina non ossigenata).
L'emoglobina è diamagnetica quando ossigenata, ma paramagnetica quando non ossigenata e il segnale dato dal sangue nella risonanza magnetica nucleare (RMN) varia in funzione del livello di ossigenazione. Questi differenti segnali possono essere rilevati usando un'appropriata sequenza di impulsi RMN, ad esempio il contrasto Blood Oxygenation Level Dependent (BOLD). Maggiori intensità del segnale BOLD derivano da una riduzione della concentrazione di emoglobina non ossigenata, dal momento che la suscettività magnetica del sangue risulta avere un valore più vicino a quello dei tessuti.
Mediante analisi con scanner per imaging a risonanza magnetica, usando parametri sensibili alla variazione della suscettività magnetica, è possibile stimare le variazioni del contrasto BOLD, che possono risultare di segno positivo o negativo in funzione delle variazioni relative del flusso sanguigno cerebrale e del consumo d'ossigeno. Incrementi del flusso sanguigno cerebrale, in proporzione superiori all'aumento del consumo d'ossigeno, porteranno ad un maggiore segnale BOLD; viceversa, diminuzioni nel flusso, di maggiore entità rispetto alle variazioni del consumo d'ossigeno, causeranno minore intensità del segnale BOLD.
La scoperta dei principi chiave della risonanza magnetica funzionale e del segnale BOLD è accreditata a Seiji Ogawa e Kenneth Kwong.
BOLD e attività neurale[modifica | modifica wikitesto]
La corretta relazione tra segnali neurali e BOLD è ancora oggetto di ricerca, ma, in generale, le modifiche del segnale BOLD sono correlate alle variazioni del flusso sanguigno. Numerosi studi, svolti negli ultimi decenni, hanno identificato un accoppiamento tra il flusso sanguigno e il tasso metabolico; ovvero l'apporto di sangue è strettamente regolato nello spazio e nel tempo in funzione dell'apporto delle sostanze nutrienti necessarie al metabolismo del cervello. Ad ogni modo, i neuroscienziati stanno ricercando una relazione più diretta tra l'apporto di sangue e gli input/output neurali che possono essere collegati sia all'attività elettrica osservabile che ai modelli circuitali della funzione cerebrale.
Le osservazioni sulle correnti elettriche indicherebbero che i potenziali di campo locale, indici dell'attività elettrica integrata, hanno una maggiore correlazione con il flusso sanguigno rispetto ai potenziali d'azione che sono più direttamente in relazione con le comunicazioni neurali. Tuttavia, nessuna misura della sola attività elettrica ha fornito un'adeguata correlazione con il metabolismo e l'apporto di sangue in ampie e dinamiche gamme sperimentali. Presumibilmente, ciò riflette la complessa natura dei processi metabolici, di cui fa parte anche l'attività elettrica. Alcune recenti ricerche hanno suggerito che l'aumento nel flusso sanguigno cerebrale, che segue l'attività neurale, non sarebbe correlato alla richiesta metabolica della regione cerebrale, ma sarebbe piuttosto guidato dalla presenza di neurotrasmettitori, in particolare l'acido glutammico.
Risultati di recenti ricerche suggeriscono che un lieve calo iniziale precedente al segnale BOLD positivo avrebbe dimensione più localizzata e sarebbe in relazione con le diminuzioni locali della concentrazione d'ossigeno nei tessuti (forse riflettendo l'aumentato metabolismo locale durante l'attivazione dei neuroni). Con l'analisi di questo segnale BOLD negativo e maggiormente localizzato, è stato possibile l'imaging delle colonne di dominanza oculare nella corteccia visiva primaria con una risoluzione di circa 0,5 mm. Tuttavia, il segnale BOLD negativo iniziale è debole e può essere rilevato sono con l'uso di scanner potenti, con campi magnetici di almeno 3 tesla. Il segnale è anche molto meno intenso rispetto al normale segnale BOLD positivo, cosa che rende difficile l'estrazione di esso dal rumore di fondo. Inoltre, questa piccola variazione avviene in circa 1-2 secondi dall'inizio dello stimolo e potrebbe non essere rilevata quando i segnali sono registrati con lunghi tempi di ripetizione. Se il tempo di ripetizione è sufficientemente basso, l'osservazione del segnale negativo può essere falsata dall'aumentata velocità della risposta del flusso sanguigno cerebrale, causata dall'eventuale consumo di sostanze vasoattive (come la caffeina).
Il segnale BOLD è generato dal complessivo afflusso sanguigno cerebrale da parte delle grandi arterie e vene, piccole arteriole e venule e da parte dei capillari. I risultati sperimentali indicano che il segnale BOLD può essere stimato dai vasi più piccoli, quindi più vicini ai neuroni attivi, usando campi magnetici più intensi. Per esempio, mentre circa il 70% del segnale BOLD deriva dai vasi maggiori in uno scanner da 1,5 tesla, circa il 70% deriva dai vasi minori in uno scanner da 4 tesla. Inoltre, l'entità del segnale BOLD varia circa in proporzione al quadrato dell'intensità del campo magnetico. Vi è stato quindi uno aumento dell'attenzione nei confronti di scanner a campo più intenso, sia per migliorare la localizzazione delle misure che per aumentare il segnale rilevabile. Negli ultimi anni sono stati resi operativi scanner da 7 tesla e sono in sviluppo scanner sperimentali da 8 e da 9 tesla.
Tecnica[modifica | modifica wikitesto]
Il segnale BOLD è misurato mediante rapida acquisizione volumetrica di immagini con contrasto a pesata T2 o T2*. Tali immagini possono essere acquisite con discreta risoluzione spaziale e temporale: esse sono acquisite con periodo che va da 1 a 4 secondi e ciascun voxel rappresenta un cubo di tessuto di circa 2-4 mm per lato. Recenti sviluppi tecnologici, come l'uso di intensi campi magnetici e ricezione a radiofrequenza multicanale, hanno reso possibile una risoluzione spaziale sulla scala del millimetro. Le risposte agli stimoli, distanti l'una dall'altra circa uno o due secondi, sono distinguibili mediante un metodo noto come risonanza magnetica funzionale event-related, mentre il tempo totale di svolgimento di una risposta BOLD ad un breve stimolo dura circa 15 secondi, a causa dell'intenso segnale positivo.
Discipline coinvolte[modifica | modifica wikitesto]
I principi su cui si basa la FMRI coinvolgono varie discipline scientifiche; l'uso efficace nella ricerca e lo studio di questa tecnica richiedono buone conoscenze relative ai seguenti campi:
- fisica: i ricercatori dovrebbero avere una comprensione ragionevole dei principi fisici coinvolti nel funzionamento dei dispositivi.
- neuroanatomia e neurofisiologia: i risultati forniti dai segnali RMF possono essere collocati correttamente nel loro contesto solo con la conoscenza di queste due discipline. Negli studi più recenti, l'obiettivo è quello di spiegare i fenomeni della cognizione umana in termini fisici (anatomici e fisiologici).
- elettrofisiologia: familiarità con il comportamento dei neuroni a livello elettrofisiologico può contribuire a progettare studi di utilità su questa tecnica.
- psicologia: molti studi sulla RMF sono alla base dei paradigmi sperimentali della psicologia cognitiva e della psicofisica, essendo possibile una valutazione quantitativa degli effetti analizzati.
- statistica: la corretta applicazione della statistica è essenziale per una corretta interpretazione delle osservazioni, evitando i falsi positivi.
- Psichiatria: sono stati pubblicati numerosissimi studi che documentano l'alterata attivazione di determinate aree cerebrali in numerose malattie di rilevanza psichiatrica.
Valenza della RMF[modifica | modifica wikitesto]
Fin dalla sua introduzione, la RMF è stata fortemente criticata sia come tecnica di ricerca, sia per l'interpretazione dei suoi risultati.
Critiche alla tecnica della RMF[modifica | modifica wikitesto]
- Il segnale BOLD è solo una misura indiretta dell'attività neurale ed è quindi suscettibile ad influenza da parte di fenomeni fisiologici non neurali.
- Aree differenti del cervello potrebbero avere diverse risposte emodinamiche, che non sarebbero rappresentate accuratamente dal modello generale lineare, spesso usato per filtrare i segnali temporali della RMF.
- La RMF è stata spesso usata per individuare dove avvengano le attivazioni neurali nel cervello e ciò ha portato al nascere di critiche che l'accusano di essere quasi una nuova forma di frenologia. La maggior parte degli scienziati preferisce modelli che spieghino come funzionino i meccanismi psicologici. In risposta a questa critica, è sostenuto che è di vitale importanza il dove sia situata una determinata funzione cognitiva. La neuropsicologia, la manipolazione invasiva delle funzioni del cervello e il neuroimaging funzionale permettono di analizzare differenti aspetti del ruolo di ciascuna regione cerebrale. L'analogia con la frenologia è quindi errata e fuorviante: la frenologia non ha fondamento scientifico (o comunque minimo), mentre la RMF permette di stabilire importanti ipotesi e di verificarle mediante il metodo scientifico.
- La RMF è spesso usata per visualizzare l'attivazione localizzata in regioni specifiche, senza rappresentare adeguatamente la natura distribuita del funzionamento delle reti neurali biologiche. Alcune recenti tecniche di statistica multivariata studiano questo problema caratterizzando le interazioni tra le regioni attivate, analizzate con tradizionali tecniche univariate. Queste tecniche potrebbero rivelarsi utili in futuro.
- Nonostante sia una tecnica non invasiva, la RMF fornisce una risoluzione spaziale abbastanza buona. Tuttavia, la risposta temporale relativa all'afflusso sanguigno, su cui si basa la RMF, è piuttosto lieve in relazione ai segnali elettrici veicolo delle comunicazioni neuronali. Alcuni gruppi di ricerca stanno quindi lavorando su questo problema, combinando la RMF con dati forniti da altri tipi di esami, come l'elettroencefalografia (EEG) o magnetoencefalografia (MEG). L'EEG ha una risoluzione temporale molto maggiore, ma una risoluzione spaziale piuttosto ridotta, mentre la MEG ha una risoluzione temporale al pari della EEG e risoluzione spaziale simile alla RMF. Ciò ha portato alcuni a considerare la MEG un esame più valevole rispetto alla RMF.
- Molti modelli teorici utilizzati per descrivere i segnali RMF sono poco precisi, tanto da non essere falsificabili (la falsificabilità è un principio fondamentale del metodo scientifico). Di conseguenza, secondo alcuni, la RMF non avrebbe basi scientifiche sufficientemente solide. Contro questa critica viene sostenuto che gli studi condotti con la RMF, se ben strutturati, possono fornire prove in grado di falsificare una teoria precedente. Inoltre, con l'uso di ben definiti modelli matematici e computazionali dei processi neurali, la RMF può verificare o confutare le predizioni di tali teorie.
Critiche generiche[modifica | modifica wikitesto]
Come per ogni altra tecnica, la valenza della RMF è fortemente influenzata dalla progettazione dell'esperimento che ne coinvolge l'uso. Molti ricercatori hanno usato la RMF invano poiché non avevano adeguate conoscenze di tutti gli aspetti coinvolti nella tecnica, o perché hanno ricevuto insegnamenti in discipline caratterizzate da meno rigore rispetto ai rami della psicologia e delle neuroscienze qui coinvolti. L'uso inefficace della tecnica è un problema, ma non dovuto alle caratteristiche della tecnica in sé.
Vantaggi della fMRI[modifica | modifica wikitesto]
- Può registrare segnali cerebrali (umani o animali) in modo non invasivo senza utilizzo di radiazioni ionizzanti sfruttate in altri metodi come TC o PET.
- Può registrare dati con risoluzione spaziale da 3 a 6 millimetri, ma con risoluzione temporale scarsa (nell'ordine dei secondi), se comparata con altre tecniche come l'EEG. La bassa risoluzione temporale è però dovuta al fenomeno rilevato, non alla tecnica in sé: l'EEG misura l'attività elettrica dei neuroni, mentre la RMF misura l'attività sanguigna, che ha tempi di risposta più lunghi. Per la misurazione di altri fenomeni, invece, gli scanner a RMN utilizzati per la RMF possono operare ad alta risoluzione temporale.
Utilizzo commerciale[modifica | modifica wikitesto]
Almeno due aziende si sono attrezzate per l'uso della RMF come macchina della verità[3]. I segnali ottenuti dallo scanner RMF sono visualizzati su uno schermo, dove vengono evidenziate le regioni cerebrali attive. A seconda delle regioni più attive, si ritiene sia possibile determinare se un soggetto stia dicendo la verità o meno. Questo utilizzo è nato piuttosto recentemente e i suoi sostenitori sperano possa sostituire le precedenti tecniche di rivelazione, come il poligrafo, tuttavia vi sono dubbi sulla scientificità di questi metodi.
Esecuzione dell'esame[modifica | modifica wikitesto]

I soggetti che partecipano ad un esame di RMF devono semplicemente stendersi sul lettino dello scanner. Sono solitamente usati dei cuscinetti morbidi per impedire che piccoli movimenti possano interferire con la misurazione. Alcuni laboratori adoperano uno strumento fatto per essere morso dal paziente in modo che la testa rimanga ferma, ma non è pratica molto diffusa dato che causa spesso disagio. È possibile correggere l'effetto di piccolissimi movimenti nella fase di post-elaborazione dei dati, ma oltre i tre millimetri di spostamento la misura è irrimediabilmente invalidata. Il problema del movimento emerge con tutti i pazienti, ma specialmente con soggetti che non sono fisicamente o emotivamente preparati ad esami, anche brevi, di questo tipo (ad esempio persone affette da malattia di Alzheimer, schizofrenia o bambini piccoli). In questo genere di soggetti, possono essere usate varie tecniche di reinforcement per attenuare gli artefatti, ma in generale le soluzioni consistono nel progettare un paradigma compatibile con questi pazienti.
Un esame RMF ha una durata generalmente compresa tra 15 minuti e due ore, dipendentemente dall'obiettivo dello studio. I soggetti possono essere sottoposti a vari test come visione di video, ascolto di suoni, percezione di odori, esecuzione di operazioni cognitive come memorizzare o immaginare qualcosa, premere alcuni pulsanti o altri tipi di compiti. I ricercatori devono fornire dettagliate istruzioni e descrizioni dello schema dell'esperimento a ciascun soggetto, che deve fornire di conseguenza il consenso informato per la procedura.
La sicurezza è un importante fattore in tutti gli esperimenti coinvolgenti la RMF. I soggetti devono assicurarsi di essere nelle condizioni di compiere un esame che coinvolga la RMN. A causa della tecnica usata (RMN), è infatti presente un campo magnetico molto intenso in prossimità dello scanner (1,5 T o più). I pazienti devono prima essere esaminati attentamente per individuare qualsiasi tipo di oggetto ferromagnetico (orologi, occhiali, pacemaker, placche ossee, viti ossee etc.) che renderebbe pericoloso anche solo l'avvicinamento allo scanner. Se gli oggetti di questo tipo non sono rimovibili, come avviene per i dispositivi medici, non è possibile effettuare l'esame.
Tecniche simili[modifica | modifica wikitesto]
Oltre alla fMRI vi sono altre tecniche complementari per lo studio dell'attività cerebrale mediante la risonanza magnetica nucleare.
MRI con contrasto[modifica | modifica wikitesto]
L'iniezione di un mezzo di contrasto, come ossido di ferro coperto da zucchero o amido (per renderlo non individuabile da parte del sistema immunitario), causa un'interferenza locale nel campo magnetico, misurabile con lo scanner per imaging a risonanza magnetica (MRI). I segnali associati a questo tipo di mezzi di contrasto sono proporzionali al volume sanguigno cerebrale. Sebbene questo metodo semi-invasivo presenti uno svantaggio considerevole nello studio della funzione cerebrale in soggetti normali, permette una sensibilità di misurazione molto più elevata rispetto alla misura del segnale BOLD, cosa che potrebbe permettere l'eseguibilità di esami simili ad una popolazione più numerosa. Sono oggetto di ricerca altri metodi per rilevare il volume sanguigno che non richiedano iniezioni, tuttavia si pensa che non si possa raggiungere con altre tecniche la sensibilità fornita dall'iniezione di un mezzo di contrasto.
Imaging spettroscopico a risonanza magnetica[modifica | modifica wikitesto]
L'imaging spettroscopico a risonanza magnetica è un altro esame basato sulla RMN per valutare le funzioni del cervello. Mentre la semplice spettroscopia a risonanza magnetica (MRS) non prevede nessuna risoluzione spaziale, considerando la totalità del campione presente nello scanner, l'imaging spettroscopico consiste nella valutazione delle specie chimiche presenti in piccole regioni (dell'ordine di 1 cm³). La valutazione spettroscopica è possibile in quanto i protoni degli atomi di idrogeno possiedono proprietà risonanti differenti in funzione dell'ambiente chimico in cui si trovano, ovvero la molecola alla quale sono legati (acqua o proteine ad esempio). Il risultato dell'imaging spettroscopico può essere letto o come una serie di immagini, ognuna rappresentante una diversa specie chimica, oppure come una serie di spettri, ognuno associato ad una specifica locazione spaziale.
Il grafico dello spettro è composto da una serie di picchi, ognuno dei quali corrisponde ad una diversa molecola contenente idrogeno. L'area sottostante al picco di ciascuna risonanza fornisce una misura quantitativa della concentrazione del composto. Il picco maggiore è dato dall'acqua, ma sono distinguibili anche picchi per colina, creatina, n-acetilaspartato (NAA) e acido lattico. Il NAA è sostanzialmente inattivo nei neuroni, fungendo da precursore per il glutammato e da deposito per i gruppi acetile, usati nella sintesi degli acidi grassi; la sua concentrazione è però un'approssimazione ragionevole dello stato di integrità e funzionalità dei neuroni. Malattie cerebrali (schizofrenia, ictus, alcuni tipi di tumore, sclerosi multipla) possono essere caratterizzate da alterazioni locali nei livelli di NAA comparati con soggetti sani. La creatina è usata come valore di controllo relativo, dal momento che i suoi livelli rimangono pressoché costanti. I livelli di colina e lattato sono invece usati per valutare tumori cerebrali.
Imaging con tensore di diffusione[modifica | modifica wikitesto]
L'imaging con tensore di diffusione (DTI, diffusion tensor imaging) consiste nell'utilizzo della risonanza magnetica per la misura della connettitività anatomica tra le aree. Tecnicamente, non è propriamente una tecnica di imaging funzionale poiché non misura dinamicamente le variazioni della funzione cerebrale; le rilevazioni di connettività sono quindi complementari alle immagini funzionali della corteccia cerebrale, fornite dal segnale BOLD nella RMF. I fasci di sostanza bianca trasportano l'informazione funzionale tra le diverse aree cerebrali e la diffusione molecolare dell'acqua è ostacolata in corrispondenza degli assi di tali fasci. La misura della diffusione dell'acqua può quindi rivelare informazioni sulla posizione e la morfologia dei grandi canali di sostanza bianca. Malattie che alterano la normale organizzazione o integrità della sostanza bianca cerebrale (come la sclerosi multipla) hanno un impatto di tipo quantitativo sugli esami di tipo DTI.
Arterial spin labeling[modifica | modifica wikitesto]
La tecnica dell'arterial spin labeling (ASL) consiste nel marcare magneticamente l'afflusso prossimale di sangue affluente ad una determinata area di tessuto: in questo caso, il segnale rilevato nel tessuto è proporzionale al flusso sanguigno, si ha cioè una misura di perfusione. Questa tecnica fornisce una quantità maggiore di informazioni fisiologiche quantitative rispetto al segnale BOLD e ha la stessa sensibilità nel rilevare le variazioni localizzate dell'attività indotte dallo svolgimento di azioni da parte del soggetto; tuttavia è ancora in fase sperimentale a causa della bassa stabilità e della bassa risoluzione spaziale ottenibile.
PET di perfusione cerebrale[modifica | modifica wikitesto]
La tomografia ad emissione di positroni (PET) può essere usata per ottenere informazioni sul metabolismo cerebrale e specificamente sulla perfusione delle varie aree cerebrali. Come già visto per l'arterial spin labeling, la perfusione può essere correlata con l'attivazione funzionale. Nonostante sia stato recentemente provato[4] che le tecniche di misura di perfusione basate su MRI e PET danno risultati statisticamente equivalenti, la PET è attualmente lo standard di riferimento, in quanto maggiormente validata. Rispetto alla risonanza magnetica, la PET ha un rapporto segnale/rumore molto più alto, in quanto il segnale ricevuto proviene esclusivamente dal tracciante radioattivo e non dai tessuti circostanti, a scapito però di una più bassa risoluzione spaziale (5x5 mm²) e temporale (15s)[5]. La PET è inoltre molto più costosa e dannosa per il paziente in quanto richiede la preparazione del tracciante radioattivo. In generale, la PET può essere considerata meno efficace rispetto alla fMRI per studi di carattere funzionale[6]
Analisi dei dati della fMRI[modifica | modifica wikitesto]
L'obiettivo ultimo dell'analisi dei dati forniti dalla RMF è di rilevare i collegamenti tra l'attivazione del cervello e i compiti che il soggetto esegue durante la scansione. Il segnale BOLD conseguente all'attivazione è però relativamente debole, quindi altre sorgenti di rumore nei dati acquisiti devono essere controllate attentamente. Ciò significa che, prima che l'analisi statistica sull'attivazione possa iniziare, deve essere eseguita una serie di fasi di elaborazione delle immagini acquisite
In una normale scansione RMF, il volume tridimensionale della testa del soggetto è scansionato ogni uno o due secondi con una sequenza di impulsi echo-planar imaging (EPI), producendo per ciascuna sessione una quantità di immagini compresa tra qualche centinaio e qualche migliaio. Per la natura della tecnica usata, le immagini sono acquisite in un k-spazio e devono essere riconvertite in uno spazio normale per essere utilizzabili. A causa di limitazioni tecniche, i campioni non sono acquisiti su una griglia, quindi le imperfezioni dello scanner (come variazioni termiche e rumore di picco) introducono ulteriori distorsioni. Piccoli movimenti del soggetto, il suo battito cardiaco e la sua respirazione possono anch'essi influire sulle immagini.
La situazione più comune vede i ricercatori utilizzare una sequenza di impulsi indicata dal produttore dello scanner, ad esempio una sequenza EPI bustrofedica. Il software della piattaforma dello scanner esegue esso stesso la ricostruzione delle immagini dal k-spazio. Durante questa fase viene persa parte dell'informazione, in particolare la fase complessa del segnale ricostruito. Alcuni tipi di artefatti, come il rumore di picco, diventano più difficili da rimuovere dopo la ricostruzione, ma si ritiene siano relativamente poco influenti. Per sequenze di impulsi non indicate dal produttore, ad esempio EPI a spirale, la ricostruzione deve essere eseguita da software su una piattaforma separata.
Dopo la ricostruzione, l'output della sessione di scansione consiste in una serie di immagini tridimensionali del cervello. Le più comuni correzioni eseguite su tali immagini sono la correzione dei movimenti e la correzione degli effetti fisiologici. Possono essere eseguite ulteriori correzioni e filtraggi spaziali e/o temporali. Se si ritiene che il compito eseguito dal soggetto produca impulsi di attivazione troppo brevi rispetto al tempo di risposta BOLD (nell'ordine dei 6 secondi), può essere eseguito un filtraggio temporale per tentare di escludere la risposta BOLD e ripristinare il pattern temporale di attivazione.
A questo punto i dati forniscono una serie temporale di campioni per ogni voxel del volume scansionato. Sono poi usati vari metodi per collegare la serie di voxel al compito eseguito dal soggetto, allo scopo di produrre mappe di attivazione dipendente da esso.
Software per il neuroimaging[modifica | modifica wikitesto]
- MRIcro, su sph.sc.edu.
- MRIcron, su cabiatl.com.
- Mappatura statistica parametrica SPM
- Analysis of Functional NeuroImages (AFNI)
- BrainVoyager
- Cambridge Brain Analysis (CamBA)
- FreeSurfer
- FMRIB Software Library
- 3D Slicer
- ImageJ
- Voxel based-morphometry
Note[modifica | modifica wikitesto]
- ^ Sandrone, Angelo Mosso, in Journal of Neurology, vol. 259, 2012, pp. 2513–2514, DOI:10.1007/s00415-012-6632-1, PMID 23010944.
- ^ Sandrone, Weighing brain activity with the balance: Angelo Mosso's original manuscripts come to light, in Brain, vol. 137, 2014, pp. 621–633, DOI:10.1093/brain/awt091, PMID 23687118.
- ^ No Lie MRI, Inc Archiviato il 28 agosto 2019 in Internet Archive. e Cephos Corporation.
- ^ Feng C-M, Narayana S, Lancaster JL, Jerabeck PA, Arnow TL, Zhu F, Tan LH, Fox PT, Gao J-H, CBF changes during brain activation: fMRI vs. PET (PDF), in NeuroImage, vol. 22, 2004, pp. 443-446 (archiviato dall'url originale il 24 agosto 2005).
- ^ (EN) Presentazione, dal Mathematical Biosciences Institute della Ohio State University Archiviato il 7 settembre 2006 in Internet Archive.
- ^ (EN) Articolo del blog specialistico BrainyBehavior che paragona PET e fMRI
Bibliografia[modifica | modifica wikitesto]
- (EN) Scott A. Huettel, Allen W. Song, Gregory McCarthy. Functional Magnetic Resonance Imaging. Sinauer Associates, 2004. ISBN 0-87893-288-7
- (EN) C. Weiller et al. Clinical potential of brain mapping using MRI. Journal of Magnetic Resonance Imaging. 2004, 23 (6): 840–850.
- (EN) A. L. Baert, K. Sartor, J. E. Youker. Functional MRI. Springer-Verlag Berlin Heidelberg, 2000. ISBN 3-540-67215-X
Voci correlate[modifica | modifica wikitesto]
- Echo-planar imaging
- FMRIB Software Library
- Imaging biomedico
- Imaging a risonanza magnetica
- Mappatura statistica parametrica (SPM)
- Morfometria basata sui voxel (VBM)
- Neuroimaging funzionale
- Risonanza magnetica nucleare
- Spettroscopia di risonanza magnetica nucleare
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su risonanza magnetica funzionale
Wikimedia Commons contiene immagini o altri file su risonanza magnetica funzionale
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) An introduction to functional MRI (PDF), su sph.sc.edu.
- (EN, ES) Radiologyinfo.org - Functional MR Imaging (fMRI) - Brain, su radiologyinfo.org.
- (EN) About Functional MRI: informazioni sulla RMF.
- (EN) Introduction to FMRI: introduzione alla RMF.
- Centri di ricerca
- (EN) Martinos Centre for Biomedical Imaging: Centro Martinos per l'imaging biomedico, Mass General Hospital, Università di Harvard.
- (EN) fMRI Data Center: Centro dati sulla RMF, College di Dartmouth.
- (EN) Wellcome Trust Centre for Neuroimaging: Centro Wellcome per il neuroimaging, istituto di neurologia, Università College di Londra.
- (EN) Oxford Centre for Functional Magnetic Resonance Imaging of the Brain: Centro di Oxford per la risonanza magnetica funzionale del cervello, Università di Oxford.
- (EN) Sir Peter Mansfield Magnetic Resonance Centre: Centro Sir Peter Mansfield per la risonanza magnetica, Università di Nottingham.
- (EN) The Brain Mapping Unit (BMU): Unità di mappatura del cervello, dipartimento di psichiatria, Università di Cambridge.
- (EN) Functional MRI Research Center: Centro di ricerca sulla RMF, Columbia University.
- (EN) York Neuroimaging Center: Centro di neuroimaging di York, Università di York.
- il link a fmri.it[collegamento interrotto]: alcuni gruppi italiani che fanno neuroimaging.
| Controllo di autorità | GND (DE) 7618675-1 |
|---|