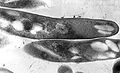
Mycobacterium tuberculosis
| Mycobacterium tuberculosis | |
|---|---|
 | |
| Classificazione scientifica | |
| Dominio | Prokaryota |
| Regno | Bacteria |
| Phylum | Actinobacteria |
| Ordine | Actinomycetales |
| Sottordine | Corynebacterineae |
| Famiglia | Mycobacteriacee |
| Genere | Mycobacterium |
| Specie | M. tuberculosis |
| Nomenclatura binomiale | |
| Mycobacterium tuberculosis Zopf, 1883 | |
| Nomi comuni | |
|
bacillo di Koch | |
Il Mycobacterium tuberculosis (chiamato anche bacillo di Koch) appartenente alla famiglia delle Mycobacteriacee, famiglia di batteri gram-variabili. È il bacillo responsabile della tubercolosi nell'uomo. Sono bacilli immobili, non sporigeni, aerobi obbligati, delle dimensioni di 0,2-0,6 x 1-10 µm, caratterizzati dalla lenta crescita, da una parete ricca di acidi micolici e da un DNA con elevato contenuto di guanina e citosina (60-70%). Il nome deriva da Robert Koch che lo scoprì nel 1882.

Struttura della parete[modifica | modifica wikitesto]
La parete cellulare del bacillo di Koch è peculiare sotto molti punti di vista. È composta da
- Lipidi
- 60% del peso secco della parete cellulare (30% del peso secco del corpo batterico), soprattutto acidi micolici e cere (A, B, C, D).
- Proteine
- Costituiscono il 15% della parete cellulare. Hanno una potente attività antigenica, con attivazione della Immunità cellulo-mediata. Estratte con metodi opportuni vengono definite PPD o derivato proteico purificato, principale responsabile della reazione di ipersensibilità di IV tipo.
La struttura è a strati; dall'interno verso l'esterno sono presenti peptidoglicano, arabinogalattano e glicolipidi di superficie dove si ancorano gli acidi micolici. Gruppi di lipo-arabinomannani ancorati direttamente alla membrana attraversano per intero tutta la parete. Tale complessità giustifica la resistenza ai fattori ambientali (essiccamento), l'alcool-acido resistenza (vedi più avanti), l'elevato tempo di replicazione (12-24 ore), le caratteristiche di crescita in vitro (colonie visibili solo dopo 40 giorni), la particolare antigenicità (dovuta alla componente proteica della parete), la resistenza a molti antibiotici e la tendenza del batterio all'aggregazione (dovuta al dimicoliltrealosio o fattore cordale).
I glicolipidi di Mycobacterium sono detti anche micosidi; gli acidi micolici sono lipidi a 60 - 90 atomi di carbonio uniti a carboidrati tramite legami covalenti.
Il fattore cordale è responsabile della crescita in forma di catene parallele, è tossico se inoculato nel topo ed è implicato nella virulenza dei micobatteri (inibizione della fagocitosi mediata dai macrofagi con sopravvivenza endovescicolare).
La cera D sembra invece essere uno degli elementi responsabile della reazione di ipersensibilità di IV tipo.
Patogenesi[modifica | modifica wikitesto]
Dopo inalazione di aerosol infetti o ingestione di acqua e cibo contaminati o l'inoculazione di farmaci bioderivati infetti si ha la fagocitosi dei batteri da parte dei macrofagi alveolari. Il blocco della fusione lisosoma-fagosoma garantito dal fattore cordale, porta alla sopravvivenza del batterio all'interno dei macrofagi con attivazione di una risposta immune cellulo-mediata (linfociti T CD4+ e linfociti T CD8+). In particolare l'attivazione dei T CD4+ porta alla produzione di anticorpi (non proteggenti a causa della localizzazione intracellulare del bacillo) e alla produzione di IFN e IL-2 con attivazione dei macrofagi. I macrofagi attivati possono a questo punto fagocitare e uccidere i micobatteri. L'attivazione dei linfociti T CD8+ porta alla lisi delle cellule fagocitiche contenenti micobatteri in replicazione. Il risultato complessivo è la promozione di un'infiammazione cronica con formazione di granulomi contenenti necrosi caseosa (materiale formato da bacilli, cellule epitelioidi e macrofagi morti). Intorno alla necrosi caseosa si localizzano macrofagi con nuclei a ferro di cavallo (cellula di Langhans), stretti a formare uno strato epitelioide (simile a un epitelio); ancora più esternamente, sono presenti linfociti T e plasmacellule. Il granuloma così composto è contornato da uno strato capsulare formato da fibroblasti e tessuto connettivo, formatosi come esito dell'evento infiammatorio-compressivo.
Sulle cause della necrosi caseosa si è molto discusso; sembra infatti che siano coinvolti diversi fattori. In primo luogo, si dà grande importanza alla reazione di ipersensibilità di IV tipo mediata dalla componente proteica del batterio dissolta nei tessuti, con produzione di interferone e conseguente citossicità. Sembrano essere coinvolte anche alcune particolari endotossine contenute nello stesso bacillo, in grado di mediare citolesività diretta. È spesso considerato evento eziologico l'obliterazione compressiva della rete vascolare mediata dai processi infiammatori cronici; Florey ha fatto rilevare che la compressione con conseguente trombosi è invece un fenomeno tardivo, che si instaura solo dopo la genesi della necrosi caseosa[1].
Le lesioni primarie si localizzano soprattutto nel lobo polmonare medio destro e nel lobo superiore sinistro. A questo punto si può avere disseminazione secondaria polmonare (apici), pleurica, tracheo-bronchiale, digestiva, miliare (reni), nervosa e ossea. L'invasione può avvenire per continuità, ingestione dell'espettorato o per via ematica.
L'evoluzione dei granulomi dopo svuotamento con creazione di un tragitto fistoloso, esita verso la formazioni di caverne (e possibile tisi) che si tappezzano di epitelio brochiale (fenomeno detto detersione); le caverne possono essere sovrainfettate da funghi del genere Aspergillus. I granulomi possono andare incontro a fibrosi e cicatrizzazione con possibile calcificazione o ossificazione.
Epidemiologia[modifica | modifica wikitesto]
Il serbatoio naturale è l'uomo con tubercolosi conclamata. La trasmissione avviene per inalazione di aerosol infetti. I soggetti a rischio sono soprattutto tossicodipendenti, senzatetto, alcolizzati, carcerati e pazienti con AIDS.
Profilo clinico[modifica | modifica wikitesto]
La tubercolosi (TBC) primaria nell'immunocompetente è per lo più asintomatica o paucisintomatica (febbre, abbondante sudorazione notturna, tosse stizzosa e malessere). La TBC primaria in persone a rischio ha una localizzazione polmonare progressiva primaria con febbre, tosse, espettorazione, emottisi e dispnea. La TBC secondaria (post primaria) è caratterizzata da tosse cronica, espettorazione francamente purulenta, emottisi, febbre, dispnea, dolore toracico e anoressia. La TBC extrapolmonare può colpire vari organi e apparati come linfonodi (25%), pleura (20%), tratto genito-urinario (15%), ossa (10%-la localizzazione osteoarticolare più frequente è la colonna vertebrale), meningi (5%). La TBC miliare è caratterizzata da piccole lesioni a forma di seme di miglio, che si diffondono rapidamente dai polmoni ai visceri (soprattutto reni).
Profilo diagnostico[modifica | modifica wikitesto]

La diagnosi di M. tubercolosis si avvale dell'esame microscopico, dell'esame colturale, di esami biochimici e di esami immunomolecolari.
Esame microscopico[modifica | modifica wikitesto]
Lo strato esterno della membrana è funzionalmente simile alla membrana esterna dei Gram-negativi; tuttavia la colorazione di Gram non è idonea alla sua identificazione[2]. Si utilizzano, infatti, colorazioni in grado di evidenziarne la caratteristica acido-alcol resistenza. La colorazione di Ziehl-Neelsen (carbolfucsina a caldo) avviene dopo raccolta su un vetrino porta oggetto di un campione idoneo (come espettorato fluidificato con N-acetilcisteina). Successivamente, il campione deve essere lasciato essiccare per alcuni minuti; passato questo tempo, si procede con la colorazione mediante carbolfucsina di Ziehl, colorante in grado di penetrare all'interno della parete dei micobatteri dopo opportuno riscaldamento (vetrino sopra al becco Bunsen fino ai primi vapori). Successivamente all'esposizione al becco Bunsen si procede con il lavaggio del vetrino mediante alcool e acido solforico; questa tappa consente di decolorare i batteri che non possiedono la struttura tipica dei micobatteri. Successivamente, il vetrino può essere colorato con un colorante di contrasto come il blu di metilene. La presenza di micobatteri è documentata dalla presenza di bacilli fucsia in campo blu. Tale metodica non è esente da problematiche riguardanti la specificità; la colorazione di Ziehl-Neelsen identifica, infatti, non tanto i micobatteri, quanto bacilli acido-alcool resistente (BAAR), che possono non essere patogeni o semplici contaminanti del campione. La valutazione di un esame microscopico dopo colorazione di Ziehl-Neelsen deve essere fatta in base alla presenza di BAAR in un campo microscopico a 1.000 ingrandimenti[3], secondo lo schema seguente.
| BAAR per campi | Referto |
| 0 BAAR su 300 campi | Negativo per BAAR. |
| 1-2 BAAR su 300 campi | Dubbio: ripetizione dell'esame. |
| 1-9 BAAR su 100 campi | Positivo +--- |
| 1-9 BAAR su 10 campi | Positivo ++-- |
| 1-9 BAAR su 1 campo | Positivo +++- |
| Più di 9 BAAR su 1 campo | Positivo ++++ |
La sensibilità dell'esame microscopico condotto con la colorazione di Ziehl-Neelsen è condizionata dalla carica microbica, dal tipo di campione biologico, da eventuali errori tecnici nella procedura e dalla bravura dell'operatore. In definitiva si stima[4] che la colorazione di Ziehl-Neelsen riesca a identificare BAAR solo se presenti con una soglia minima di 10.000 – 100.000 batteri per ml di campione. La specificità è condizionata dal fatto che le diverse specie di Nocardia, di Rhodococcus possono dare falsi positivi per BAAR. Analogamente, Legionella micdadei e cisti di Cryptosporidium e di Cyclospora possono colorarsi con la colorazione di Ziehl-Neelsen. Si deve anche considerare che alcuni particolari ceppi di micobatteri possono variare la capacità di colorarsi come BAAR. Inoltre, l'esame microscopico non fornisce alcuna informazione riguardo alla vitalità dei micobatteri osservati; in pazienti in terapia è possibile il reperto di esame microscopico positivo ed esame colturale negativo (vedi esame colturale). Altre possibili colorazioni sono la colorazione di Kinyoun (carbolfucsina a freddo), la colorazione con auramina o altri coloranti associati a fluorescenza.
Esame colturale[modifica | modifica wikitesto]
Rispetto all'esame microscopico, l'esame colturale ha un'elevatissima sensibilità (è in grado di dare positività in campioni biologici contenenti 10 – 100 BAAR per ml) e la massima specificità. L'esame colturale deve essere preceduto da raccolta di campione appropriato (urina, feci, sangue, espettorato fluidificato) e trattato con idrossido di sodio al 10% al fine di eliminare eventuali batteri contaminanti (soprattutto possibili micobatteri a rapida crescita non patogeni in grado di dare falsi positivi). M. tubercolosis è in grado di resistere al pH elevato e di procedere indenne alle successive fasi della coltura. Si possono utilizzare sia terreni solidi sia terreni liquidi. I terreni solidi possono essere a base di uovo, come il terreno di Lowenstein-Jensen e il terreno di Petragnani o sintetici (agarizzati), come il terreno di Middlebrook 7H10 -7H11. Il terreno di Lowenstein-Jensen è un terreno in provetta che si solidifica dopo riscaldamento; in particolare, la solidificazione avviene dopo che il terreno è stato posto in posizione leggermente inclinata, in modo che la superficie esposta all'aria risulti a becco di clarino (ulteriore nome del terreno). La solidificazione avviene grazie alle proteine dell'uovo che si coagulano al calore; ulteriori componenti di questo terreno sono il verde malachite, l'asparagina, il glicerolo, il magnesio, il potassio e la fecola di patate. L'utilizzo di terreni solidi comporta la crescita lenta e/o difficile (2-3 settimane); tuttavia, la rilevazione manuale delle colonie consente di rilevare colture miste, di analizzare la morfologia delle colonie e la determinazione della carica batterica. Si assume infatti che vi sia una relazione diretta tra il numero delle colonie e la sensibilità del rilievo[5], secondo lo schema seguente.
| Numero colonie | Referto |
| 0 colonie | Negativo |
| <50 colonie | Dubbio; si devono eseguire altri test biochimici |
| 50-100 colonie | Positivo +--- |
| 100-200 colonie | Positivo ++-- |
| 200-500 colonie | Positivo +++- |
| > 500 (patina) | Positivo ++++ |
I terreni liquidi, come il sistema MGIT, consentono una crescita più rapida e una rilevazione automatizzata operata da sistemi di incubazione computerizzati. Necessitano, tuttavia di sub-colture su solidi, data l'impossibilità di quantificare la carica batterica. In particolare, nel terreno liquido Middlebrook 7H9 è presente un fondo di silicone contenente un composto fluorescente (un complesso metallico di rutenio), sensibile alla riduzione della tensione di ossigeno (consumato dagli eventuali micobatteri presenti), che funge da sistema rivelatore.
Sistema Bactec[modifica | modifica wikitesto]
Il sistema Bactec per M. tubercolosis è spesso utilizzato per rilevare l'eventuale batteriemia e disseminazione. All'interno di un flacone sigillato è presente un terreno di coltura liquido contenente acido palmitico marcato con 14C. L'utilizzo di tale sostanza da parte dei micobatteri comporta la produzione di 14CO2 che si accumula all'interno del flacone stesso. Il gas presente nel flacone sigillato viene analizzato automaticamente dallo strumento e la quantità di 14CO2 viene rilevata da un rilevatore di radioattività, quantificata ed espressa come indice di crescita.
Test di identificazione molecolare[modifica | modifica wikitesto]
Il test AccuProbe ha come bersaglio la subunità 16S dell'rRNA. Il test INNO-LiPA ha come bersaglio la regione spaziatrice presente tra il gene 16S e il gene 23S dell'rRNA. Queste due metodiche, dotate entrambe di elevata specificità e sensibilità sono in grado di distinguere tra
- Mycobacterium tuberculosis complex
- Mycobacterium kansasii
- Mycobacterium gordonae
- Mycobacterium avium complex

Test di Mantoux[modifica | modifica wikitesto]
Consiste nell'inoculazione intradermica di 5 unità di derivato proteico purificato o PPD (equivalente a 0,1 mg). La intradermoreazione (conseguente alla risposta dei linfociti sensibilizzati) deve essere valutata dopo 48 ore. Una lesione con un diametro maggiore di 10 mm deve essere considerata, nell'individuo sano, positiva. Nell'individuo non immunocompetente, si assume come positiva una lesione maggiore di 5 mm di diametro. Il test di Mantoux, benché ancora valido come misura di controllo, risulta spesso positivo non solo nella tubercolosi attiva, ma anche dopo esposizione a micobatteri ambientali innocui, dopo esposizione asintomatica recente a M. tuberculosis, nelle infezioni latenti e nei soggetti vaccinati.
QuantiFERON o TB-Test[modifica | modifica wikitesto]
Il test, che è stato introdotto nel 2005 nella routine diagnostica[6], consiste nel cimentare, per 16-24 ore, il sangue intero del soggetto indagato con particolari antigeni tubercolari come ESAT-6, CFP-10 o lo stesso derivato proteico purificato. Successivamente, dopo il tempo necessario alla processazione degli antigeni, si valuta mediante ELISA la presenza di interferone, che testimonia l'attività dei linfociti T sensibilizzati al M. tubercolosis.
Terapia, prevenzione e controllo[modifica | modifica wikitesto]
La terapia per M. tubercolosis si compone di una serie di farmaci specifici come isoniazide, rifampicina, pirazinamide ed etambutolo per 9 mesi, 2 volte a settimana. Il trattamento con rifampicina può durare anche per un anno. Il vaccino a germi vivi e attenuati è detto vaccino BCG (Mycobacterium bovis attenuato su patata glicerinata e biliata, detto anche Bacillo di Calmette-Guérin) ed è consigliato nelle zone dove la tubercolosi è endemica. La vaccinazione deve essere controllata mediante il test di Mantoux.
Galleria d'immagini[modifica | modifica wikitesto]
-
Tubercolosi polmonare in RX torace. Le frecce indicano il granuloma.
-
Immagine da microscopio elettronico a scansione di M. tubercolosis.
-
Immagine da microscopio elettronico a trasmissione di M. tubercolosis.
-
Bacilli di Koch in espettorato, colorati in rosso.
Note[modifica | modifica wikitesto]
- ^ M. Umberto Dianzani, Istituzioni di patologia generale, Torino, UTET, 2006, ISBN 978-88-02-06211-2.
- ^ Antonelli, Clementi, Pozzi, Rossolini, Microbiologia Medica, Rozzano (MI), Ambrosiana, 2008.
- ^ Kent and Kubuka, 1985, CDC
- ^ Patrick R. Murray, Microbiologia medica, Roma, EMSI, 2008, ISBN 978-88-86669-56-6.
- ^ ATS. Diagnosic Standards and Classification of Tuberculosis in Adults and Children, Am J Respir Crit Care Med 161:1376-1395, 2000
- ^ Michele La Placa, Principi di Microbiologia Medica, Bologna, Esculapio, 2012.
Bibliografia[modifica | modifica wikitesto]
- Jawetz, Melnick, & Adelberg's, 2008, Medical Microbiology. Ventiquattresima Ed.
- Patrick R.Murray, 2008, Microbiologia Medica. Quinda Ed.
- Molina Romanzi, 2006, Microbiologia Clinica. Prima Ed.
- La Placa, 2005, Principi di Microbiologia Medica. Decima Ed.
- Bistoni, Nicoletti, Nicolosi, 2002, Microbiologia e microbiologia clinica. Prima Ed.
- Harrison, Principi di Medicina Interna (16ª edizione), New York - Milano, McGraw-Hill, 2006, ISBN 88-386-2459-3.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Mycobacterium tuberculosis
Wikimedia Commons contiene immagini o altri file su Mycobacterium tuberculosis Wikispecies contiene informazioni su Mycobacterium tuberculosis
Wikispecies contiene informazioni su Mycobacterium tuberculosis
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) Mycobacterium tuberculosis, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN) Sito della CDC sulla tubercolosi, su cdc.gov.
- (EN) Interessantissimo sito di microbiologia che include anche dimostrazioni interattive delle metodiche diagnostiche, su microbiologybytes.com. URL consultato il 30 novembre 2008 (archiviato dall'url originale il 19 dicembre 2008).
| Controllo di autorità | Thesaurus BNCF 10665 · LCCN (EN) sh85089186 · GND (DE) 4186384-7 · BNE (ES) XX548558 (data) · J9U (EN, HE) 987007555873405171 · NDL (EN, JA) 00565485 |
|---|