Diabete mellito di tipo 1
| Diabete mellito di tipo 1 | |
|---|---|
 | |
| Specialità | diabetologia |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 250.01 |
| ICD-10 | E10 |
| OMIM | 222100 |
| MeSH | D003922 |
| MedlinePlus | 000305 |
| eMedicine | 117739 |
| Sinonimi | |
| DM1 | |
Il diabete mellito di tipo 1 è una forma di diabete, che si configura come malattia autoimmune,[2] caratterizzata dalla distruzione delle cellule β pancreatiche (dalle CD4+ e CD8+ cellule T e infiltrazione dei macrofagi nelle isole pancreatiche),[3] e che comporta solitamente associazione all'insulino-deficienza[4][5].
Storia[modifica | modifica wikitesto]
La prima classificazione, per quanto riguarda i due tipi principali di diabete (il tipo 1 e il tipo 2), è stata proposta da Avicenna intorno all'anno 1000.[6]
Epidemiologia[modifica | modifica wikitesto]
Si manifesta maggiormente in Scandinavia (specie in Finlandia), in Sardegna[7][8] e in diversi stati del nord degli USA,[9] mentre in paesi come il Giappone o il sud dell'Europa l'incidenza è minore.[10]
Per quanto riguarda l'età, in circa la metà dei casi esordisce in età inferiore ai 20 anni (proprio per questo in passato veniva chiamato "diabete giovanile") e più frequentemente nel corso della pubertà.
L'incidenza a livello mondiale è stata calcolata del 3%.[11]
Eziologia[modifica | modifica wikitesto]
Le cause sono un insieme di fattori che riguardano la genetica, l'ambiente e l'immunologia: a una predisposizione genetica di base si unisce uno stimolo immunologico che, col passare del tempo, porta alla distruzione delle cellule beta; quando la percentuale di cellule beta perse arriva all'80%, ci si ritrova di fronte al diabete mellito di forma 1.[12]
L'insorgenza ha variazione stagionale e può seguire, tra l'altro, il morbillo, l'epatite o infezioni da Coxsackie virus. Si teorizza che tali infezioni realizzino una risposta autoimmunitaria con la comparsa di linfociti T citotossici, che completino la distruzione delle cellule β del pancreas, producenti insulina.
Fattori autoimmunitari[modifica | modifica wikitesto]
Durante il processo di distruzione delle cellule beta, le altre forme cellulari (alfa, PP e altre simili) non vengono intaccate; il processo infiammatorio termina quando ha completato la distruzione cellulare.[13]
Fattori ambientali[modifica | modifica wikitesto]
Si sospetta che i fattori ambientali possano sviluppare forme di diabete, ma non esistono prove certe al riguardo. Virus e composti della nitrosourea sono i possibili responsabili. Una recente ipotesi prende in considerazione fenomeni di mimetismo con antigeni del Mycobacterium avium sottospecie paratuberculosis[14][15][16], già chiamato in causa per la patogenesi della malattia di Crohn[17][18][19]. Infezioni croniche subcliniche di tale micobatterio, contratto durante l'infanzia, comporterebbero, in individui suscettibili[20][21][22], interazioni crociate di stampo autoimmunitario, come rilevato in alcuni studi[23][24][25].
In relazione alle infezioni da Coxackie, il sierotipo B4 è stato correlato all'insorgenza di diabete insulino-dipendente. La ragione va ricercata nell'omologia di sequenza con l'antigene self GAD65, un'isoforma della glutammico decarbossilasi espressa dalle cellule β del pancreas, che condurrebbe a una cross-reattività con esito di autoimmunità contro le insule stesse.[26]
Fattori genetici[modifica | modifica wikitesto]
Sembra che, come altre malattie autoimmuni, sia correlata a particolari combinazioni di alleli HLA.
Alcuni studi hanno evidenziato un ruolo del timo, con la produzione d'insulina da parte della ghiandola, negli eventi che fisiologicamente portano alla tolleranza immunologica da parte delle cellule T verso le cellule beta pancreatiche. L'insorgenza di autoimmunità verso queste cellule, quindi, deriverebbe da un difettoso funzionamento di tale processo.[27]. La presenza di HLA nel cromosoma 6 fu il primo locus a essere sospettato di una correlazione col diabete di tipo 1[28], mentre i B8 o B15 aumentano di circa tre volte il rischio di sviluppare diabete I e le combinazioni di antigeni DR4-DQ8 e DR3-DQ2 si manifestano nel 90% delle persone affette dal diabete.[29] Tuttavia, lo stato omozigote per un allele non fa aumentare ulteriormente il rischio.
È stata dimostrata l'importanza delle posizioni 45 e 57 della catena DQb nella suscettibilità al diabete I.
L'eziologia genica è però ancora incerta: l'indice di concordanza per i gemelli monozigoti con meno di 40 anni è inferiore al 50%. Inoltre, non c'è prevalenza nella trasmissione verticale.
Sintomatologia[modifica | modifica wikitesto]
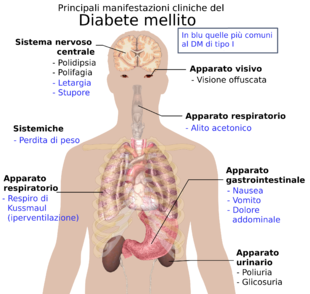
I sintomi si sviluppano tipicamente in un breve periodo di tempo.[30]
Fra i sintomi e segni clinici si riscontrano poliuria, polidipsia (secondaria alla poliuria), polifagia paradossa (il paziente mangia molto, ma dimagrisce) e perdita di peso; spesso il sintomo di esordio è costituito dalla chetoacidosi diabetica.
Ulteriori sintomi possono includere visione offuscata, sensazione di stanchezza e scarsa guarigione.
Spesso si ha una interruzione dei sintomi subito dopo la fase di esordio. Questa fase, nota come luna di miele, dura per alcuni mesi, dopodiché i sintomi si presentano nuovamente e permangono stabilmente, dando luogo, definitivamente, allo stato di diabete. La spiegazione di questo fenomeno è da ricercarsi nell'iperproduzione compensatoria di insulina da parte delle cellule β.
Complicanze[modifica | modifica wikitesto]
Si riscontrano inoltre, come complicanze temibili della malattia:
Quest'ultima complicanza può evidenziarsi nella forma normale e in quella proliferativa, anche se in misura minore rispetto al passato.[31]
Diagnosi[modifica | modifica wikitesto]
Il diabete mellito è caratterizzato da iperglicemia ricorrente o persistente e viene diagnosticato dimostrando uno dei seguenti segni:[32]
- Livello glicemico a digiuno pari o superiore a 7,0 mmol / l (126 mg / dl).
- Glucosio plasmatico pari o superiore a 11,1 mmol / l (200 mg / dl) due ore dopo un carico glicemico orale di 75 g come in un test di tolleranza al glucosio.
- Sintomi di iperglicemia e glicemia casuale pari o superiore a 11,1 mmol / l (200 mg / dl).
- Emoglobina glicata (emoglobina A1C) uguale o superiore a 48 mmol / mol (≥ 6,5 DCCT%). (Questo criterio è stato raccomandato dall'American Diabetes Association nel 2010, sebbene debba ancora essere adottato dall'OMS.)[33]
| Condizione | Glicemia a 2 ore | Glicemia a digiuno | Glicata | |
|---|---|---|---|---|
| Unità | mmol/l(mg/dl) | mmol/l(mg/dl) | DCCT % | mmol/mol |
| Normale | <7.8 (<140) | <6.1 (<110) | <6.0 | <42 |
| Glicemia a digiuno alterata | <7.8 (<140) | ≥6.1(≥110) & <7.0(<126) | 6.0-6.4 | 42-46 |
| Tolleranza al glucosio alterata | ≥7.8 (≥140) | <7.0 (<126) | 6.0-6.4 | 42-46 |
| Diabete mellito | ≥11.1 (≥200) | ≥7.0 (≥126) | ≥6.5 | ≥48 |
Circa un quarto delle persone con nuovo diabete di tipo 1 ha sviluppato un certo grado di chetoacidosi diabetica (un tipo di acidosi metabolica causata da alte concentrazioni di corpi chetonici, formata dalla rottura degli acidi grassi e dalla deaminazione degli amminoacidi) per il momento il diabete è riconosciuto. La diagnosi di altri tipi di diabete viene solitamente effettuata in altri modi. Questi includono lo screening sanitario ordinario, l'individuazione dell'iperglicemia durante altre indagini mediche e sintomi secondari come cambiamenti della vista o stanchezza inspiegabile. Il diabete viene spesso rilevato quando una persona soffre di un problema che può essere causato dal diabete, come infarto, ictus, neuropatia, scarsa guarigione della ferita o ulcera del piede, alcuni problemi agli occhi, alcune infezioni fungine o il rilascio di un bambino con macrosomia o ipoglicemia (basso livello di zucchero nel sangue).[32]
Un risultato positivo, in assenza di iperglicemia inequivocabile, dovrebbe essere confermato da una ripetizione di uno dei metodi sopra elencati in un giorno diverso. La maggior parte dei medici preferisce misurare il livello glicemico a digiuno a causa della facilità di misurazione e del notevole impegno nel tempo del test formale di tolleranza al glucosio, che richiede due ore per completare e non offre alcun vantaggio prognostico rispetto al test del digiuno.[34]
Autoanticorpi
È stato dimostrato che la comparsa di autoanticorpi correlati al diabete è in grado di predire la comparsa del diabete di tipo 1 prima che si verifichi un'iperglicemia, i principali sono autoanticorpi anti-insulina, autoanticorpi insulinici, autoanticorpi diretti all'isoforma 65-kDa di decarbossilasi dell'acido glutammico (GAD), autoanticorpi diretti contro la molecola IA-2 correlata alla fosfatasi e autoanticorpi trasportatori di zinco (ZnT8).[35]
Per definizione, la diagnosi di diabete di tipo 1 può essere fatta prima all'apparizione di sintomi e / o segni clinici, ma l'emergenza di autoanticorpi può essere definita "diabete autoimmune latente". Non tutti con autoanticorpi progrediscono verso il diabete di tipo 1, ma il rischio aumenta con il numero di tipi di anticorpi, con tre o quattro tipi di anticorpi che danno il rischio di progredire verso il diabete di tipo 1 del 60-100%.[35] L'intervallo di tempo tra l'emergenza di autoanticorpi e il diabete clinicamente diagnosticabile può essere di alcuni mesi nei neonati e nei bambini piccoli, ma in alcune persone possono essere necessari anni - in alcuni casi più di 10 anni.[35] Gli autoanticorpi delle cellule delle isole sono rilevati mediante immunofluorescenza convenzionale, mentre il resto viene misurato con specifici test di radiobinding.[35]
Prevenzione[modifica | modifica wikitesto]
Nel corso dei tempi molti sono stati i tentativi di prevenzione del diabete mellito di tipo 1, ma non si sono mai avuti risultati degni di nota e si registrano fallimenti, come quello degli studi condotti dal Diabetes Prevention Trial-type 1 sulla somministrazione di insulina alle persone con elevati fattori di rischio del diabete.[36]
Terapia[modifica | modifica wikitesto]
La terapia si avvale di esercizio fisico, dieta a basso contenuto calorico, monitorando soprattutto l'apporto di glucosio, somministrazione di insulina, trapianto di pancreas o trapianto di cellule beta pancreatiche. L'insulina utilizzata per il trattamento può essere somministrata per via sottocutanea o con infusore, avviando il rilascio di insulina prima dei pasti.
Il trattamento con insulina predispone all'ipoglicemia, nella cui eventualità è necessario apporto di zuccheri. In caso di crisi ipoglicemica severa, il trattamento è invece con somministrazione di glucagone.
Comorbilità psicologica[modifica | modifica wikitesto]
Alcune ricerche dimostrano come le difficoltà incontrate dalle persone affette da una malattia cronica come il diabete mellito di tipo 1 si ripercuotano sul piano psicologico ed emotivo del paziente, ostacolando talvolta la gestione stessa della malattia. Quando la persona malata è sopraffatta dalle responsabilità, dai controlli periodici e dalle restrizioni (perlopiù alimentari), che la malattia stessa comporta, la probabilità che si sviluppino contemporaneamente alla malattia cronica anche disturbi psicologici come la depressione e l’ansia, aumenta. La presenza di comorbilità comporta, inoltre, un ulteriore peggioramento della cura di sé in generale, e del controllo dell’andamento glicemico in particolare[37]. A questo quadro clinico potrebbero associarsi disturbi dell’appetito e anedonia[38]. Tra gli studi effettuati su campioni di pazienti con diabete mellito emergono:
- Depressive symptoms and glycemic control in adolescents with type 1 diabetes: mediational role oof blood glucose monitoring. SI tratta di uno studio condotto su 144 Adolescenti e loro caregiver dal quale è emerso che quasi un quarto dei partecipanti presenta sintomi depressivi significativi quali tristezza, indecisione, scarsa autoefficacia e anedonia[39].
- Studio longitudinale su 92 giovani pazienti dal quale è emerso che più del 45% del campione ha sviluppato nel corso della sua vita disturbi psichiatrici (perlopiù depressione).
- Search for Diabetes in Youth. Studio multicentrico di giovani diabetici tra i 10 e i 20 anni i cui risultati hanno riportato una percentuale pari al 14% di pazienti lievemente depressi mentre quasi il 9% è affetta depressione moderata/grave[40].
- Studio effettuato su due campioni, uno formato da 24 giovani con diabete di tipo 1 e disturbo depressivo maggiore (MDD) e l'altro formato da 30 soggetti depressi sotto controllo psichiatrico. È emerso che le caratteristiche del MDD in soggetti diabetici e psichiatrici sembrano essere simili in molti aspetti sebbene si registri nei giovani diabetici una maggiore probabilità di sintomi depressivi protratti nel tempo e di ricadute (soprattutto per le donne diabetiche)[41].
- Studi sugli effetti psicologici dell'ipoglicemia hanno riscontrato che la paura di non saper gestire glicemie con valori particolarmente bassi e la paura che tale condizione possa ripetersi in futuro stimolano l'aumento di livelli di stress e ansia[42].
- Studi su un campione di adulti affetti da diabete mellito di tipo 1 hanno rilevato un'associazione tra sintomi ansiosi e monitoraggio della glicemia meno frequente e valore della emoglobina glicata non ottimale[43].
- Studio su un campione di adolescenti con diabete mellito di tipo 1 che ha indicato un'associazione tra ansia di stato e scarso monitoraggio e controllo glicemico[44] la quale, inoltre, risulta essere maggiore rispetto a quella riscontrata con i sintomi depressivi; si ipotizza che tale situazione sia dovuta alla forte somiglianza tra i sintomi dell'ansia (aumento della frequenza cardiaca, sudorazione, vertigini, dolore addominale) e i sintomi legati al diabete che induce il paziente ad una difficoltà nel prendere decisioni terapeutiche.
Gli studi citati, mostrano come la comorbilità possa comportare problemi e disagi ben più gravi rispetto alla presenza esclusiva di sintomi depressivi o ansiosi e per questo motivo la sfera emotiva del paziente diabetico dovrebbe essere essa stessa parte integrante del trattamento terapeutico poiché tanto la situazione medica quanto quella psicologica e sociale condizionano la capacità del paziente di adottare correttamente tutti i mezzi a disposizione per curarsi.
Note[modifica | modifica wikitesto]
- ^ Diabetes Blue Circle Symbol, su diabetesbluecircle.org, International Diabetes Federation, 17 marzo 2006 (archiviato dall'url originale il 5 agosto 2007).
- ^ McDevitt HO, Unanue ER., Autoimmune diabetes mellitus--much progress, but many challenges, in Adv Immunol.., vol. 100, 2008, pp. 1-12.
- ^ Foulis AK, McGill M, Farquharson MA. Insulitis in type 1 (insulin-dependent) diabetes mellitus in man — macrophages, lymphocytes, and interferon-gamma containing cells. J Pathol 1991;165:97-103
- ^ Carlo M. Rotella, Edoardo Mannucci, Barbara Cresci, Il diabete mellito. Criteri diagnostici e terapia: un aggiornamento. Pag 29, SEE Editrice Firenze, 1999, ISBN 978-88-8465-009-2.
- ^ "Diabetes Fact sheet N°312". WHO. November 2016, su who.int.
- ^ G. Restori, Il diabete mellito. Fisiopatologia, clinica e terapia. Pag 2, Piccin, 1991, ISBN 978-88-299-0915-5.
- ^ Diabete: Sardegna come Finlandia, record del tipo 1, su portalediabete.org. URL consultato il 5 giugno 2012 (archiviato dall'url originale il 4 marzo 2016).
- ^ Progetto Diabete: il portale italiano sul diabete
- ^ Kathleen M. Gillespie, Type 1 diabetes: pathogenesis and prevention, in CMAJ, vol. 175, 1973, pp. 165–170.
- ^ G. Restori, Il diabete mellito. Fisiopatologia, clinica e terapia. Pag 6, Piccin, 1991, ISBN 978-88-299-0915-5.
- ^ EURODIAB ACE Study Group. Variation and trends in incidence of childhood diabetes in Europe. Lancet 2000;355:873-6.
- ^ Jameson J. Larry, Harrison: Endocrinologia clinica Pag 315, Casarile (Milano), McGraw-Hill, 2007, ISBN 978-88-386-3921-0.
- ^ Jameson J. Larry, Harrison: Endocrinologia clinica Pag 316, Casarile (Milano), McGraw-Hill, 2007, ISBN 978-88-386-3921-0.
- ^ Rosu V, Ahmed N, Paccagnini D 2009 Specific immunoassays confirm association of Mycobacterium avium subsp. paratuberculosis with type-1 but not type-2 diabetes mellitus PLoS ONE 4(2):e4386.
- ^ Sechi La, Rosy V, Pacifico A 2008 Humoral immune responses of type-1 diabetes pateints to Mycobacterium avium subspecies paratuberculosis lend support to the infectious trigger hypothesis Clin Vaccine Immunol 15:320-326.
- ^ Sechi LA, Salza S, Pacifico A 2008 Mycobacterium avium subspecies paratuberculosis bacteremia in type-1 diabetes mellitus: an infectious trigger? Clin Infect Dis 46:148-149.
- ^ Rowe MT, Grant IR. 2006 Mycobacterium avium ssp. paratuberculosis and its potential survival tactics Lett Appl Microbiol Apr;42(4):305-11.
- ^ Naser SA, Ghobrial G, Romero C, Valentine JF 2004 Culture of Mycobacterium avium subspecies paratuberculosis from the blood of patients with Crohn's disease Lancet Sep 18-24;364(9439):1039-44
- ^ Sechi LA, Scanu AM, Molicotti P, Cannas S, Mura M, Dettori G, Fadda G, Zanetti S 2005 Detection and Isolation of Mycobacterium avium subspecies paratuberculosis from intestinal mucosal biopsies of patients with and without Crohn's disease in Sardinia Am J Gastroenterol Jul;100(7):1529-36
- ^ Davies JM 1997 Molecular mimicry: can epitope mimicry induce autoimmune disease? Immunol Cell Biol Apr;75(2):113-26.
- ^ Daneman D 2006 Type 1 diabetes Lancet 367:847-858
- ^ Knip M, Veijola R, Virtanen Sm 2005 Environmental triggers and determinants of type-1 diabetes Diabetes 54:125-136.
- ^ van Halteren AG, Roep BO, Gregori S, Cooke A, van Eden W, Kraal G, Wauben MH 2002 Cross-reactive mycobacterial and self hsp60 epitope recognition in I-A(g7) expressing NOD, NOD-asp and Biozzi AB/H mice J Autoimmun Mar;18(2):139-47.
- ^ Polymeros D, Bogdanos DP, Day R, Arioli D, Vergani D, Forbes A 2006 Does cross-reactivity between mycobacterium avium paratuberculosis and human intestinal antigens characterize Crohn's disease? Gastroenterology Jul;131(1):85-96
- ^ Dow CT 2006 Paratuberculosis and Type I diabetes: is this the trigger? Med Hypotheses 67(4):782-5.
- ^ Analysis of antibody responses against coxsackie... [J Med Virol. 1999] - PubMed - NCBI
- ^ (EN) Fan Y., Rudert WA, Grupillo M, He J, Sisino G, Trucco M., Thymus-specific deletion of insulin induces autoimmune diabetes., in EMBO J., vol. 18, n. 28, 16, pp. 2812-24, PMID 19680229.
- ^ Cudworth AG, Woodrow JC, HLA system and diabetes mellitus, Diabetes 1975;24:345-9.
- ^ Devendra D, Eisenbarth GS, Immunologic endocrine disorders, J Allergy Clin Immunol 2003;111:S624-36
- ^ Symptoms & Causes of Diabetes What are the symptoms of diabetes?, su niddk.nih.gov.
- ^ Klein R, Knudtson MD, Lee KE, Gangnon R, Klein BE., The Wisconsin Epidemiologic Study of Diabetic Retinopathy: XXII the twenty-five-year progression of retinopathy in persons with type 1 diabetes., in Ophthalmology., vol. 115, novembre 2008.
- ^ a b World Health Organisation Department of Noncommunicable Disease Surveillance (1999). "Definition, Diagnosis and Classification of Diabetes Mellitus and its Complications".
- ^ ""Diabetes Care" January 2010". American Diabetes Association. Archived from the original on 13 January 2010. Retrieved 29 January 2010., su care.diabetesjournals.org.
- ^ Saydah SH, Miret M, Sung J, Varas C, Gause D, Brancati FL (August 2001). "Postchallenge hyperglycemia and mortality in a national sample of U.S. adults". Diabetes Care. 24 (8): 1397–402.
- ^ a b c d Knip M, Veijola R, Virtanen SM, Hyöty H, Vaarala O, Akerblom HK (2005). "Environmental Triggers and Determinants of Type 1 Diabetes". Diabetes. 54: S125–S13.
- ^ Barker JM, McFann KK, Orban T., Effect of oral insulin on insulin autoantibody levels in the Diabetes Prevention Trial Type 1 oral insulin study., in Diabetologia.., vol. 50, agosto 2007, pp. 1603-1606.
- ^ Skinner TC, Psychological barriers, in European Journal of Endocrinology, vol. 151, 2 pp. T13-T17.
- ^ Mc Grady M., Laffel L., Drotar D., Repaske D., Hood KK, Depressive symptoms and glycemic control in adolescents with type 1 diabetes: mediatonal role of blood glucose monitoring, in Diabetes Care, 32, pp. 804-806.
- ^ M. McGrady, L.Laffel, D.Drotar, D.Repaske, K.K Hood, Depressive symptoms and glycemic control in adolescents with type 1 diabetes: mediational role of blood glucose monitoring, in Diabetes Care, 32 pp. 804-806.
- ^ J.M Lawrence et al., Prevalence and correlates of depressed mood among yputh with diabetes: The Search for Diabetes in Youth Study, in Pediatrics, 117 pp.1348-1358.
- ^ M. Kovacs, D. Goldstone, D. Obrosky et al., Psychiatric disprders in youth with IDDM: rates and risk factors, in Diabetes Care, 20 pp.36-44.
- ^ L.A. Gonder-Frederick, C.D. Fischer, L.M: Ritterband et al., Predictors of fear of hypoclycemia in adolescents with type 1 diabetes and thei parents, in Pediatric Diabetes, 7 pp.215-222.
- ^ E.D. Mollema et al., Insulin-treated diabetes patients with fear of self-injecting or fear of self-testing: psychological comorbidity and general well-being, in J Psychosom Res, vol. 51, 5 pp.665-672.
- ^ M. Herzer, K.K Hood, Anxity symptoms in adolescens with type 1 diabetes: associationwith blood glucose monitoring and glycemic control, in Journal of Pediatric Psychology, 35 pp. 415-425.
Bibliografia[modifica | modifica wikitesto]
- Carlo M. Rotella, Edoardo Mannucci, Barbara Cresci, Il diabete mellito. Criteri diagnostici e terapia: un aggiornamento, SEE Editrice Firenze, 1999, ISBN 978-88-8465-009-2.
- G. Restori, Il diabete mellito. Fisiopatologia, clinica e terapia: fisiopatologia, clinica e terapia, Piccin, 1991, ISBN 978-88-299-0915-5.
- Jameson J. Larry, Harrison: Endocrinologia clinica, Casarile (Milano), McGraw-Hill, 2007, ISBN 978-88-386-3921-0.
- Research Laboratories Merck, The Merck Manual quinta edizione, Milano, Springer-Verlag, 2008, ISBN 978-88-470-0707-9.
- NICE. The National Institute for Health and Care Excellence. Type 1 diabetes in adults: diagnosis and management
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su diabete mellito di tipo 1
Wikimedia Commons contiene immagini o altri file su diabete mellito di tipo 1
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) insulin-dependent diabetes mellitus, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 23663 |
|---|