2C-B
| 2C-B | |
|---|---|
 | |
 | |
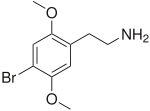
| Nome IUPAC | |
| 2-(4-bromo-2,5-dimetossi-fenil)etanamina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C10H14BrNO2 |
| Massa molecolare (u) | 260.13 g/mol |
| Numero CAS | |
| Numero EINECS | 636-275-4 |
| PubChem | 98527 |
| DrugBank | DB01537 |
| SMILES | COC1=CC(=C(C=C1CCN)OC)Br |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | Sconosciuto |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi R | 26/27/28 |
| Frasi S | 22‐36/37/39‐45 |
La 2C-B è una sostanza psicoattiva appartenente alla famiglia delle feniletilammine 2C, con effetti di tipo prevalentemente psichedelico o entactogeno (a seconda dei dosaggi). Negli anni '80 venne commercializzata come farmaco afrodisiaco ed utilizzata in ambito psichiatrico come adiuvante di alcune forme di psicoterapia. La 2C-B si ritrova sotto forma di compresse o, più raramente, di polvere (di colore bianco/giallognolo).[1] Il suo nome (a volte scritto tucibi, tusibi o tusi) viene anche usato per chiamare un mix di sostanze stupefacenti venduto in forma di polvere rosa (chiamata erroneamente Pink Cocaine), che però spesso non contiene alcuna traccia di 2C-B.[2] Questo mix, originalmente venduto dai cartelli messicani e poi esportato altrove, risulta molto pericoloso in quanto l'utente finale non conosce la composizione esatta del mix, che può variare di molto e contenere MDMA, Ketamina, Benzodiazepine, Catinoni, Anfetamine, Oppiodi, LSD, Mescalina e altro, a cui viene aggiunto un colorante rosa.[3]
Venne descritta per la prima volta nel libro PiHKAL (Phenethylamines I Have Known And Loved) dello studioso Alexander Shulgin, che la sintetizzò nel 1974.[4]
Attualmente è quasi ovunque una sostanza controllata e vietata a causa dei suoi effetti psicoattivi. In Italia, la molecola 2C-B risulta inclusa nella Tabella I del D.P.R. 309/90 e s.m.i. delle Sostanze Stupefacenti e Psicotrope.
Storia[modifica | modifica wikitesto]
La 2C-B fu sintetizzata a partire dalla 2,5-dimetossibenzaldeide dal chimico statunitense Alexander Shulgin nel 1974. Inizialmente venne utilizzata nelle comunità psichiatriche come adiuvante della psicoterapia perché a bassi dosaggi non presenta effetti psichedelici ma incrementa la capacità di autoanalisi emotiva, l'introspezione e permette di instaurare un migliore rapporto paziente-terapeuta. È considerata uno dei migliori farmaci per questo scopo, per via della sua breve durata e la relativa assenza di effetti collaterali (attualmente l'MDMA è in sperimentazione per gli stessi scopi, specie come adiuvante della terapia psicologica nel trattamento del disturbo post traumatico da stress). Diventando in breve popolare tra le comunità mediche, lasciò l'ambito clinico diventando presto una popolare sostanza ricreativa utilizzata come sostituto MDMA o come psichedelico (a dosi più alte di quelle terapeutiche). Si è recentemente rilevato che alcune pasticche vendute come MDMA erano in realtà adulterate con 2C-B (in media 5 mg) per mimarne o potenziarne gli effetti.[1]
La 2C-B venne anche commercializzata come afrodisiaco sotto il nome di "Erox", fabbricato dalla casa farmaceutica tedesca Drittewelle negli anni '70 e '80.[5] Per diversi anni, fu venduta nei Paesi Bassi sotto forma di pasticche predosate, fino a quando non venne aggiunta nella I Lista della cosiddetta Opium Law, diventando di fatto illegale. Non avendo mai causato incidenti, divennero in breve popolari i suoi analoghi come la 2C-I, la 2C-T-2 e la 2C-T-7, che in quel momento non erano illegali nei Paesi Bassi. In breve però anche queste nuove sostanze vennero presto aggiunte alle liste delle sostanze controllate, dopo un breve periodo di vendite. Dal 2 luglio 1995 sono considerati del tutto illegali.
Da qualche decennio viene utilizzata da alcune tribù sciamaniche del Sudafrica in sostituzione delle tradizionali erbe magiche, che per diverse cause scarseggiano e sono difficili da reperire, nel corso dei riti religiosi.
Viene utilizzata nella scena rave, comunemente confusa ed eventualmente venduta, come ecstasy (MDMA), data la sua similarità di effetti, talvolta più distorsivi e prolungati, specie ai dosaggi più elevati (alcune pastiglie vendute come ecstasy si è scoperto in realtà contenere 2C).[6][7][8]
Farmacologia[modifica | modifica wikitesto]
Meccanismo d'azione[modifica | modifica wikitesto]
Il meccanismo d'azione di questa sostanza non è ancora stato del tutto delucidato. A differenza di molti altri allucinogeni, non è un potente agonista del recettore 5HT2A, su cui sembra agire in realtà come un agonista parziale a bassa efficacia.[9] Ciò suggerisce che gli effetti possano essere dovuti dall'attivazione della pathway metabolica della fosfolipasi D accoppiata a tale recettore o mediati dall'altro target su cui agisce che è il recettore serotoninergico 5HT2C. Inoltre ricerche su ratti suggeriscono che incrementa i livelli di dopamina nel cervello.[10][11][12]
Metabolismo[modifica | modifica wikitesto]
Il metabolismo di tale composto appare avvenire essenzialmente per deamminazione ossidativa per azione degli enzimi MAO-A e MAO-B, seguita da metabolismi minori di demetilazione. Il metabolismo tra diverse specie sembra essere simile, tuttavia sono state osservate, negli umani, differenze individuali nella tossicità epatica del composto.[13]
La coingestione di inibitori delle MAO può causare un aumento della tossicità, dei livelli plasmatici e dell'emivita del composto per inibizione dei suoi metabolismi degradativi.[14]
Tossicità[modifica | modifica wikitesto]
Nel settembre 1998, il Journal of Analytical Toxicology riporta che esistono pochissimi dati riguardo alla farmacologia, al metabolismo e alla tossicità della 2C-B. In generale la tossicità e meccanismo d'azione delle feniletilammine è molto eterogeneo e poco studiato, pur essendo delle diffuse sostanze d'abuso. Un case-report descrive il caso di uno psicologo che assunse accidentalmente 100 mg della sostanza senza riportare danni. Sono descritti in letteratura diversi casi di morte o ricovero dovuti a reazioni avverse a seguito dell'assunzione di feniletilammine della classe 2C, anche se spesso è stata rilevata co-assunzione di altre sostanze, non è stato possibile identificare con certezza la sostanza assunta o è stato rilevato un dosaggio eccessivo.[15][16]
Interazioni[modifica | modifica wikitesto]
La coassunzione con alcol genera effetti simili a quelli di un'ubriacatura. Gli inibitori delle MAO-B come la selegilina sembrano aumentare esponenzialmente gli effetti della sostanza, probabilmente per inibizione delle vie metaboliche degradative, per cui deve essere evitata la coassunzione di tali farmaci come gli inibitori delle MAO (utilizzato come antidepressivi), gli inibitori delle MAO-B (utilizzati nella terapia del Parkinson).
Effetti[modifica | modifica wikitesto]
La dose comune per uso ricreativo di tipo psichedelico si aggira tra i 15 e i 25 mg, dove genera effetti essenzialmente nel campo visivo che vengono descritti come più facilmente gestibili di quelli generati da altri psichedelici;[17] dosaggi minori mancano in genere di questa componente apparendo accomunabili ad una bassa dose di MDMA senza però condividerne gli sgradevoli effetti di hangover.[18] Gli effetti della 2C-B includono:[19][20]
- L'insorgenza, o "coming-up": quando viene assunta per via orale, la 2C-B ha un effetto molto più ritardato rispetto a quando inalata; se sniffata, in questo caso gli effetti saranno repentini ma di una durata più breve, se assunta per via orale gli effetti saranno tendenzialmente più miti ma di una durata maggiore. In questo caso, gli effetti si riscontrano in genere dopo 30-90 minuti; mentre per inalazione si ottengono quasi immediatamente e permangono per 3-6 ore. La 2C-B è considerata una tra le più dolorose sostanze da inalare in quanto provoca un fortissimo bruciore al naso di una durata di circa 5 minuti. L'insorgenza degli effetti di solito non è schiacciante per la maggior parte dei soggetti, ma l'intensità dell'esperienza può provocare nausea e/o spaventi specie a dosi elevate.
- Dalle esperienze raccolte dagli utilizzatori, risulta che le allucinazioni (che si verificano a dosi elevate, oltre i 15 mg) sono molto meno intense di quelle prodotte dall'LSD e sono descritte come “clichéd in stile anni ’70" con un andamento non costante, tendendo cioè a diminuire temporaneamente per poi ripresentarsi, anche con intensità maggiore. Sono stati tuttavia segnalati due casi dove la 2C-B sarebbe risultata molto più potente dell'LSD ma ciò sarebbe stato dovuto all'elevatissimo dosaggio assunto dai soggetti.
- In genere sono accompagnate da una diminuzione dell'acuità visiva e delle capacità di concentrazione, anche se particolari attività che coinvolgono la sfera estetica ed emotiva, come l'ascolto di musica o la visione di un film, possono essere più coinvolgenti ed emotivamente intense. In tali situazioni può verificarsi sinestesia.
- Gli effetti entactogeni ed empatici, di autoanalisi emotiva, afrodisiaci sono invece prevalenti a basse dosi (5 e 10 mg) e risentono fortemente della dose assunta, con variazione evidente degli effetti percepiti anche con differenze di dose assunta di soli 2 mg.
In alcuni esperimenti condotti su animali, la somministrazione di basse dosi del composto è risultata simile a bassi dosaggi di amfetamine (quindi stimolanti), rispetto alle quali però sembra agire con un meccanismo d'azione diverso.[21]
I seguenti effetti sono presenti nei soggetti che hanno assunto forti dosi di 2C-B:
- Visioni ad occhi aperti (OEVs), distorsioni della realtà simili a cartoni animati; attorno agli oggetti appaiono aloni rossi e verdi. Le visioni ad occhi chiusi (CEVs) sono molto comuni. Perdita di coordinazione dei movimenti, dell'equilibrio e difficoltà nel distinguere le percezioni.
- Alterazione dell'abilità di comunicazione, di concentrarsi e restare vigili.
- Alcuni soggetti descrivono l'esperienza come terribile. Alcuni hanno descritto sensazioni di freddo o gelo mentre altri hanno riferito di sentirsi come avvolti in confortevoli coperte.
Gli effetti indesiderati possono includere diarrea, nausea, tremori e spasmi muscolari, mal di testa e bad trip specie a dosaggi molto alti accompagnati da ansia e panico; dosi maggiori di 30/40 mg generano forti allucinazioni che inducono tachicardia, ipertensione e ipertermia;[22] alcuni soggetti riportano lieve irritabilità dopo l'uso. Questi effetti sono tuttavia generalmente lievi ed il 2C-B è meglio tollerato di altri stupefacenti come l'ecstasy, di cui non possiede i pesanti effetti di down. Se combinato con l'alcol dà effetti simili a quelli di una sbornia.
Note[modifica | modifica wikitesto]
- ^ a b (EN) M.D. Cole, C. Lea e N. Oxley, 4-Bromo-2,5-dimethoxyphenethylamine (2C-B): a review of the public domain literature, in Science and Justice, vol. 42, n. 4, 1º ottobre 2002, DOI:10.1016/S1355-0306(02)71832-7. URL consultato il 1º agosto 2017.
- ^ (EN) What Is Pink Cocaine? | What To Know About 2C-B, su Ohio Recovery Center. URL consultato il 5 luglio 2023.
- ^ Max Daly, Giacomo Stefanini, Cos'è la “cocaina rosa” colombiana che si sta diffondendo in Europa, su Vice, 10 gennaio 2023. URL consultato il 7 gennaio 2024.
- ^ Erowid Online Books : "PIHKAL" - #20 2C-B, su erowid.org. URL consultato il 10 settembre 2021.
- ^ Erowid Chemicals Vaults : Images : 2cb pack (JPG), su erowid.org. URL consultato il 10 settembre 2021.
- ^ Joseph J. Palamar, Monica J. Barratt e Jason A. Ferris, Correlates of new psychoactive substance use among a self-selected sample of nightclub attendees in the United States, in The American Journal on Addictions, vol. 25, n. 5, 1º agosto 2016, pp. 400-407, DOI:10.1111/ajad.12403. URL consultato il 7 maggio 2017.
- ^ Sara Odoardi, Francesco Saverio Romolo e Sabina Strano-Rossi, A snapshot on NPS in Italy: Distribution of drugs in seized materials analysed in an Italian forensic laboratory in the period 2013-2015, in Forensic Science International, vol. 265, 1º agosto 2016, pp. 116-120, DOI:10.1016/j.forsciint.2016.01.037. URL consultato il 7 maggio 2017.
- ^ (EN) James Nolan, This Is What 2-CB Does to You, su vice.com, 5 marzo 2019. URL consultato il 10 settembre 2021.
- ^ Esther Papaseit, Magí Farré e Clara Pérez-Mañá, Acute Pharmacological Effects of 2C-B in Humans: An Observational Study, in Frontiers in Pharmacology, vol. 0, 2018, DOI:10.3389/fphar.2018.00206. URL consultato il 9 settembre 2021.
- ^ (EN) Claudio A Villalobos, Paulina Bull e Patricio Sáez, 4-Bromo-2,5-dimethoxyphenethylamine (2C-B) and structurally related phenylethylamines are potent 5-HT2A receptor antagonists in Xenopus laevis oocytes, in British Journal of Pharmacology, vol. 141, n. 7, 1º aprile 2004, pp. 1167-1174, DOI:10.1038/sj.bjp.0705722/abstract. URL consultato il 7 maggio 2017.
- ^ Pablo R. Moya, Kelly A. Berg e Manuel A. Gutiérrez-Hernandez, Functional selectivity of hallucinogenic phenethylamine and phenylisopropylamine derivatives at human 5-hydroxytryptamine (5-HT)2A and 5-HT2C receptors, in The Journal of Pharmacology and Experimental Therapeutics, vol. 321, n. 3, 1º giugno 2007, pp. 1054-1061, DOI:10.1124/jpet.106.117507. URL consultato il 7 maggio 2017.
- ^ Thomas S. Ray, Psychedelics and the Human Receptorome, in PLOS ONE, vol. 5, n. 2, 2 febbraio 2010, pp. e9019, DOI:10.1371/journal.pone.0009019. URL consultato il 7 maggio 2017.
- ^ Helena Carmo, Jan G. Hengstler e Douwe de Boer, Metabolic pathways of 4-bromo-2,5-dimethoxyphenethylamine (2C-B): analysis of phase I metabolism with hepatocytes of six species including human, in Toxicology, vol. 206, n. 1, 5 gennaio 2005, pp. 75-89, DOI:10.1016/j.tox.2004.07.004. URL consultato il 7 maggio 2017.
- ^ Be Vang Dean, Samuel J. Stellpflug e Aaron M. Burnett, 2C or Not 2C: Phenethylamine Designer Drug Review, in Journal of Medical Toxicology, vol. 9, n. 2, 7 maggio 2017, pp. 172-178, DOI:10.1007/s13181-013-0295-x, PMC 3657019. URL consultato il 7 maggio 2017.
- ^ Fernando Caudevilla-Gálligo, Jordi Riba e Mireia Ventura, 4-Bromo-2,5-dimethoxyphenethylamine (2C-B): presence in the recreational drug market in Spain, pattern of use and subjective effects, in Journal of Psychopharmacology (Oxford, England), vol. 26, n. 7, 1º luglio 2012, pp. 1026-1035, DOI:10.1177/0269881111431752. URL consultato il 7 maggio 2017.
- ^ (EN) Cerebral Vasculopathy After 4-Bromo-2,5-Dimethoxyphenethylam... : The Neurologist, in LWW, DOI:10.1097/NRL.0b013e3181a3cb53. URL consultato il 7 maggio 2017.
- ^ Pablo Mallaroni, Natasha Mason e Johannes Reckweg, Assessment of the acute effects of 2C-B vs psilocybin on subjective experience, mood and cognitio, 2023. URL consultato il 4 marzo 2023.
- ^ Débora González, Marta Torrens e Magí Farré, Acute Effects of the Novel Psychoactive Drug 2C-B on Emotions, in BioMed Research International, vol. 2015, 1º gennaio 2015, p. 643878, DOI:10.1155/2015/643878. URL consultato il 7 maggio 2017.
- ^ 2C-B, in PsychonautWiki. URL consultato il 7 maggio 2017.
- ^ Erowid 2C-B Vault: Basics, su erowid.org. URL consultato il 1º agosto 2017.
- ^ Helena Carmo, Jan G. Hengstler, Douwe de Boer, Michael Ringel, Fernando Remião, Félix Carvalho, Eduarda Fernandes, Lesseps A. dos Reys, Franz Oesch e Maria de Lourdes Bastos, Metabolic pathways of 4-bromo-2,5-dimethoxyphenethylamine (2C-B): analysis of phase I metabolism with hepatocytes of six species including human, in Toxicology, vol. 206, n. 1, 5 gennaio 2005, pp. 75-89, DOI:10.1016/j.tox.2004.07.004, ISSN 0300-483X.
- ^ Metabolic pathways of 4-bromo-2,5-dimethoxyphenethylamine (2C-B): analysis of phase I metabolism with hepatocytes of six species including human. [collegamento interrotto], su ncbi.nlm.nih.gov. URL consultato il 28 maggio 2008.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su 2C-B
Wikimedia Commons contiene immagini o altri file su 2C-B
Collegamenti esterni[modifica | modifica wikitesto]
- Il 2C-B in PiHKAL, su erowid.org.
- Erowid 2C-B vault — include i rapporti di chi ha fatto uso di 2C-B, scientifici e governativi
- Dosaggi del 2C-B, su erowid.org.
- Marquis testing with 2C-B and 2C-I, comparative reactions with pictures from the whole process and results, su drogoteca.blogspot.com.
- Storia del 2C-B, su tacethno.com.
- 2C-B - Psyconautwiki.org
