Paracetamolo: differenze tra le versioni
m fix parametri in template cita using AWB |
m fix parametri in template cita using AWB |
||
| Riga 82: | Riga 82: | ||
== Antidoti == |
== Antidoti == |
||
In casi di [[avvelenamento]] si utilizza come antidoto l'[[acetilcisteina]] in dosi elevate (140 mg/kg come dose di carico seguita da 70 mg/kg ogni 4 ore).<ref>{{en}} {{cita pubblicazione |
In casi di [[avvelenamento]] si utilizza come antidoto l'[[acetilcisteina]] in dosi elevate (140 mg/kg come dose di carico seguita da 70 mg/kg ogni 4 ore).<ref>{{en}} {{cita pubblicazione |cognome=Kanter |nome=Michele Zell |anno=2006 |titolo=Comparison of oral and i.v. acetylcysteine in the treatment of acetaminophen poisoning |rivista=Am J Health Syst Pharm |volume=63 |numero=19 |pagine=1821-1827 |pmid=16990628 |url=http://www.ajhp.org/cgi/content/full/63/19/1821 |accesso=31 ottobre 2007 }}</ref> [[Glutatione]] ridotto in [[fleboclisi|endovena]]. |
||
== Gravidanza e allattamento == |
== Gravidanza e allattamento == |
||
Studi clinici effettuati sull’uomo non hanno evidenziato [[teratogenesi|effetti teratogeni]] o fetotossici. Secondo un piccolo numero di studi l’impiego del paracetamolo in gravidanza potrebbe essere associato ad un rischio ridotto di aborto e nascita pre-termine. |
Studi clinici effettuati sull’uomo non hanno evidenziato [[teratogenesi|effetti teratogeni]] o fetotossici. Secondo un piccolo numero di studi l’impiego del paracetamolo in gravidanza potrebbe essere associato ad un rischio ridotto di aborto e nascita pre-termine. |
||
La [[Food and Drug Administration]] (FDA) ha inserito il paracetamolo in classe B per l’uso dei farmaci in gravidanza. La classe B comprende i farmaci i cui studi riproduttivi sugli animali non hanno mostrato un rischio per il feto e per i quali non esistono studi controllati sull'uomo oppure farmaci i cui studi sugli animali hanno mostrato un effetto dannoso (oltre a un decremento della fertilità) che non è stato confermato con studi controllati in donne nel I trimestre e per i quali non c'è evidenza di danno nelle fasi avanzate della gravidanza.<ref>{{Cita web | autore= Onyeka Otugo |coautori= Olabode Ogundare, Christopher Vaughan, Emmanuel Fadiran, Leyla Sahin | titolo = Consistency of Pregnancy Labeling Across Different Therapeutic Classes | url = http://www.fda.gov/downloads/ScienceResearch/SpecialTopics/WomensHealthResearch/UCM308982.pdf | editore= Food and Drug Administration - Office of Women’s Health | data= 1979 | accesso = 27 giugno 2013 }}</ref><ref name="pmid8852521">{{Cita pubblicazione | cognome = Sannerstedt | nome = R. | coautori = P. Lundborg; BR. Danielsson; I. Kihlström; G. Alván; B. Prame; E. Ridley | titolo = Drugs during pregnancy: an issue of risk classification and information to prescribers. | rivista = Drug Saf | volume = 14 | numero = 2 | pagine = 69-77 | mese=febbraio| anno = 1996 | |
La [[Food and Drug Administration]] (FDA) ha inserito il paracetamolo in classe B per l’uso dei farmaci in gravidanza. La classe B comprende i farmaci i cui studi riproduttivi sugli animali non hanno mostrato un rischio per il feto e per i quali non esistono studi controllati sull'uomo oppure farmaci i cui studi sugli animali hanno mostrato un effetto dannoso (oltre a un decremento della fertilità) che non è stato confermato con studi controllati in donne nel I trimestre e per i quali non c'è evidenza di danno nelle fasi avanzate della gravidanza.<ref>{{Cita web | autore= Onyeka Otugo |coautori= Olabode Ogundare, Christopher Vaughan, Emmanuel Fadiran, Leyla Sahin | titolo = Consistency of Pregnancy Labeling Across Different Therapeutic Classes | url = http://www.fda.gov/downloads/ScienceResearch/SpecialTopics/WomensHealthResearch/UCM308982.pdf | editore= Food and Drug Administration - Office of Women’s Health | data= 1979 | accesso = 27 giugno 2013 }}</ref><ref name="pmid8852521">{{Cita pubblicazione | cognome = Sannerstedt | nome = R. | coautori = P. Lundborg; BR. Danielsson; I. Kihlström; G. Alván; B. Prame; E. Ridley | titolo = Drugs during pregnancy: an issue of risk classification and information to prescribers. | rivista = Drug Saf | volume = 14 | numero = 2 | pagine = 69-77 | mese=febbraio| anno = 1996 | pmid = 8852521 }}</ref> |
||
Paracetamolo è escreto nel latte materno in quantità clinicamente non rilevanti. Sulla base dei dati di letteratura medica disponibili, l’uso del paracetamolo nelle donne che [[allattamento al seno|allattano al seno]] non è controindicato. |
Paracetamolo è escreto nel latte materno in quantità clinicamente non rilevanti. Sulla base dei dati di letteratura medica disponibili, l’uso del paracetamolo nelle donne che [[allattamento al seno|allattano al seno]] non è controindicato. |
||
Versione delle 11:43, 24 mar 2014
| Paracetamolo | |
|---|---|
 | |
 | |
| Nome IUPAC | |
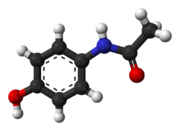
| N-(4-idrossifenil)acetammide | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C8H9NO2 |
| Massa molecolare (u) | 151,17 g/mol |
| Numero CAS | |
| Numero EINECS | 203-157-5 |
| Codice ATC | N02 |
| PubChem | 1983 |
| DrugBank | DBAPRD00252 |
| SMILES | CC(=O)NC1=CC=C(C=C1)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,263 |
| Solubilità in acqua | 14 gr/100 ml |
| Temperatura di fusione | 169 °C |
| Dati farmacologici | |
| Modalità di somministrazione | orale, rettale |
| Dati farmacocinetici | |
| Metabolismo | epatico |
| Emivita | 1-4 ore |
| Escrezione | renale |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 - 315 - 319 - 335 |
| Consigli P | 261 - 305+351+338 [1] |
Il paracetamolo (o acetaminofene) (N-acetil-para-amminofenolo)[2] è un farmaco ad azione analgesica largamente utilizzato sia da solo, sia in associazione ad altre sostanze, ad esempio nei comuni preparati da banco per le forme virali da raffreddamento, o nei farmaci destinati al trattamento del dolore acuto e cronico.
A causa della diffusione come farmaco generico, i nomi "paracetamolo" e "acetaminofene" sono ben conosciuti in altri paesi, soprattutto di cultura anglosassone. In Italia, al contrario, il nome della sostanza è poco conosciuto, mentre sono ben noti i nomi commerciali dei farmaci che lo contengono (Tachipirina, Efferalgan, ecc.).
Storia
Il paracetamolo fu sintetizzato per la prima volta nel 1878 da Harmon Northrop Morse per riduzione di p-nitrofenolo con stagno in acido acetico glaciale, secondo la seguente reazione
- 2 HO-C6H4-NO2 + 2 CH3COOH + 3 Sn → 2 C8H9NO2 + 3 SnO2
dove l'azione riducente di metallo e acido converte il p-nitrofenolo a p-amminofenolo, che viene immediatamente acetilato. Si iniziò a utilizzarlo per fini medici solo a partire dagli anni cinquanta del XX secolo.
Inizialmente si usavano acetanilide e fenacetina, derivati dell'anilina, come antipiretici di elezione, ma essi avevano forti conseguenze tossiche sul paziente. In realtà, molti anni dopo si scoprì che i benefici effetti prodotti dall'assunzione di acetanilide o di fenacetina erano determinati dal fatto che l'organismo trasformava entrambe queste molecole in paracetamolo. Era quindi il paracetamolo la sostanza che realmente determinava l'analgesia e il calo della temperatura. Quando una sostanza farmacologicamente attiva si origina, come nel caso del paracetamolo, in seguito all'assunzione di un altro prodotto (l’acetanilide o la fenacetina), questo prodotto viene indicato come precursore, mentre la sostanza che si forma viene detta metabolita attivo. Il paracetamolo era dunque il metabolita attivo sia dell’acetanilide, sia della fenacetina.
Rispetto ai suoi precursori, oggi non più usati in farmacologia, il paracetamolo presentava due vantaggi importanti: 1) non è tossico; 2) è più facile da sintetizzare.
Rispetto ai FANS, inoltre, non presenta gastrolesività e nefrotossicità.
Dal 1949 il paracetamolo ha iniziato ad essere usato come farmaco. Oggi è l'unico analgesico derivato dall'anilina che si continua ad usare in clinica.
Somministrazione e biodisponibilità
Il paracetamolo può essere somministrato attraverso diverse vie e presenta una elevata biodisponibilità, che non subisce importanti cambiamenti, eccezion fatta per i casi di epatopatia cronica. A livello del fegato, infatti, la molecola viene trasformata in un metabolita che si è rivelato tossico per il tessuto epatico. Alle dosi comunemente impiegate, tuttavia, i rischi di epatotossicità sono nulli, tanto che l'utilizzo di paracetamolo non è controindicato in età pediatrica, né in gravidanza.
L'effetto analgesico compare prontamente (circa 11 minuti) dopo la somministrazione orale e l'emivita del farmaco è di 1-4 ore.
La dose massima raccomandata (Farmacopea Statunitense) è di 4 grammi al giorno e la singola dose non deve superare il grammo, mentre la Farmacopea Ufficiale Italiana raccomanda l'assunzione di non più di 3 grammi al giorno. Pur con le dovute cautele di riduzione della dose nei soggetti che presentano una compromissione della funzionalità epatica, il paracetamolo è considerato un trattamento di prima linea nella terapia farmacologica del dolore ed è posizionato al primo gradino nella scala OMS del trattamento del dolore cronico.
Meccanismo d'azione
Il paracetamolo non è da considerarsi un farmaco antinfiammatorio non steroideo (FANS). Non ha infatti attività antiaggregante e la sua attività antinfiammatoria è molto debole. Si pensa (Graham GG, Scott KF 2005) che l'azione antinfiammatoria sia attribuibile ad una inibizione debole della via di sintesi delle prostaglandine. In vivo – cioè quando la concentrazione di acido arachidonico è bassa (<5 μmol/L) – la produzione di prostaglandine è determinata in maggior parte dalla COX-2 e in minor parte dalla COX-1. In condizioni fisiologiche e a dosi terapeutiche di paracetamolo, la sua debole azione inibitoria sulla COX-2 – che catalizza la biosintesi predominante a bassa velocità – diventa quindi significativa e produce gli effetti di blanda riduzione dell’infiammazione osservati in vivo.
Al di fuori dell'inibizione della COX-2, sembra che esista una terza isoforma di ciclo-ossigenasi espressa a livello cerebrale (COX-3) che potrebbe essere il bersaglio preferenziale del paracetamolo e di altri antipiretici. L'inibizione di questo enzima, che è stato dimostrato essere una variante molecolare della COX-1, potrebbe dar conto di una parte degli effetti analgesici e antifebbrili centrali mediati dal paracetamolo nell'uomo, dato che nel ratto non sembrano essere importanti.
Effetti tossicologici
Un rischio correlato con il suo utilizzo è rappresentato dalla sua presenza in diversi medicinali, sia come unica sostanza che in associazione, e ciò conduce spesso al sovradosaggio. Dosi superiori a quattro grammi di sostanza al giorno (riferito ad un adulto del peso di 80 kg o più) sono considerate pericolose per la salute, con una tossicità che si rivolge verso il fegato con effetti potenzialmente fatali. Una dose di 10 - 15 grammi è letale, in quanto porta ad un'epatite fulminante (in relazione alla suscettibilità del singolo soggetto anche quantità inferiori del 50% possono essere fatali). Per questo motivo, il dosaggio giornaliero massimo raccomandato negli alcolisti non deve superare i 2,5 grammi al giorno.[3]
Tossicità epatica
Il paracetamolo viene metabolizzato dalle cellule della zona 3 dell'acino epatico. In queste cellule c'è una concentrazione elevata di citocromo P450, il quale trasforma il paracetamolo in N-acetilbenzochinoneimmina, un composto molto reattivo e tossico, che colpisce soprattutto le proteine epatiche. La tossicità della N-acetilbenzochinoneimmina è strettamente correlata alla presenza sull'anello aromatico di due doppi legami: uno con l'azoto e l'altro con l'ossigeno.
Anche le cellule della zona 1 dell'acino epatico potrebbero coniugare il paracetamolo con glutatione (GSH) e formare un glutatione-coniugato, facilmente eliminabile, ma, poiché la concentrazione di glutatione nelle cellule della zona 1 è bassa, agisce principalmente il citocromo P450 della zona 3. In generale la tossicità di questa sostanza è legata al limitato potere detossificante del GSH; in caso di ingestione eccessiva, il paracetamolo porta necrosi delle cellule epatiche in 3-5 giorni.
Tossicità renale
Nel caso di avvelenamento da sovradosaggio, il paracetamolo è potenzialmente tossico per il rene. Attualmente, tuttavia, è il farmaco meno nefrotossico tra quelli utilizzabili per il dolore e i traumi ed è per tale motivo notoriamente considerato di prima scelta nelle persone affette da insufficienza renale che non possono fare uso dei classici FANS.
Antidoti
In casi di avvelenamento si utilizza come antidoto l'acetilcisteina in dosi elevate (140 mg/kg come dose di carico seguita da 70 mg/kg ogni 4 ore).[4] Glutatione ridotto in endovena.
Gravidanza e allattamento
Studi clinici effettuati sull’uomo non hanno evidenziato effetti teratogeni o fetotossici. Secondo un piccolo numero di studi l’impiego del paracetamolo in gravidanza potrebbe essere associato ad un rischio ridotto di aborto e nascita pre-termine. La Food and Drug Administration (FDA) ha inserito il paracetamolo in classe B per l’uso dei farmaci in gravidanza. La classe B comprende i farmaci i cui studi riproduttivi sugli animali non hanno mostrato un rischio per il feto e per i quali non esistono studi controllati sull'uomo oppure farmaci i cui studi sugli animali hanno mostrato un effetto dannoso (oltre a un decremento della fertilità) che non è stato confermato con studi controllati in donne nel I trimestre e per i quali non c'è evidenza di danno nelle fasi avanzate della gravidanza.[5][6]
Paracetamolo è escreto nel latte materno in quantità clinicamente non rilevanti. Sulla base dei dati di letteratura medica disponibili, l’uso del paracetamolo nelle donne che allattano al seno non è controindicato.
Avvertenze
- Febbre
- Le linee guida del NICE (National Institute for Clinical Excellence) relative all’uso degli antipiretici nei pazienti pediatrici raccomandano di non somministrare questi farmaci con il solo scopo di abbassare la febbre in assenza di altri sintomi. Gli antipiretici, incluso il paracetamolo, non riducono il rischio di convulsioni febbrili; devono essere somministrati solo se la febbre supera i 38,5 °C e/o se si associa ad altri sintomi quali affaticamento, malessere, cefalea, dolore.[7]
- Cefalea da abuso/cefalea da rimbalzo
- La somministrazione di quantità eccessive di paracetamolo per il trattamento sintomatico della cefalea può, in pazienti predisposti, provocare cefalea da abuso (MOH, medication-overuse headache), nota anche come cefalea da rimbalzo. Sembra che la cefalea da abuso sia limitata a pazienti con distubi cefalgici preesistenti, in particolare quelli con emicrania o cefalea di tipo tensivo. La MOH può presentarsi con le stesse caratteristiche di quella di cui soffre il paziente (peggioramento della cefalea preesistente) oppure con caratteristiche diverse; è tipicamente a localizzazione bilaterale con dolore gravativo o costrittivo. La MOH risponde alla sospensione del farmaco coinvolto: la cefalea si risolve completamente o torna alle caratteristiche originarie entro due mesi dalla sospensione del farmaco. Il meccanismo alla base della MOH non è noto: è stata ipotizzata la possibilità di una predisposizione genetica perché, la cefalea da abuso si è sviluppata in pazienti emicranici dopo trattamento con analgesici per malattie dolorose diverse dalla cefalea stessa. È possibile anche che la somministrazione prolungata dell’analgesico induca delle modificazioni per quanto riguarda espressione, sensibilizzazione e attivazione dei recettori nervosi coinvolti. Nei pazienti pediatrici l’abuso di paracetamolo (farmaco di scelta nel trattamento delle crisi emicraniche di lieve e moderata intensità nei bambini con età inferiore ai 12 anni) può portare a cronicizzazione della cefalea. Si raccomanda pertanto di limitarne l’uso alla fase acuta mantenendo la posologia nel range di dosaggio raccomandato.[7]
- Tossicità epatica
- La minima dose singola tossica negli adulti sani è compresa fra 7,5 e 10 grammi ed è pari o maggiore a 150 mg/kg nei bambini. Il paracetamolo può indurre tossicità epatica soprattutto quando somministrato a dosi elevate o quando l’intervallo di tempo fra una dose e la successive è inferiore a quello raccomandato (4-6 ore). I sintomi di epatotossicità comprendono nausea, vomito, sedazione, sudorazione, dolore addominale, incremento delle transaminasi e della concentrazione sierica di bilirubina, aumento del tempo di protrombinemia a più di 20 secondi. Seguono insufficienza epatica, encefalopatia, coma e morte. L’insufficienza epatica può presentarsi complicata da acidosi, edema cerebrale, ipotensione, emorragia, ipoglicemia, infezione ed insufficienza renale.
- Il rischio di epatopatia può aumentare in pazienti in terapia con farmaci che inducono il metabolismo ossidativo del paracetamolo; in caso di digiuno o di diete a basso contenuto proteico [8]; in caso di carenza di vitamina E, nei primi giorni di sospensione dell’assunzione di alcool negli alcolisti cronici.[9]
- Insufficienza epatica
- Il paracetamolo deve essere somministrato con cautela in caso di pazienti con insufficienza funzionale epatica lieve o moderata per il rischio di tossicità. Nei pazienti con insufficienza epatica grave il paracetamolo non è raccomandato.[7]
- Alcolismo
- L’interazione fra alcool e paracetamolo è complessa. Potrebbe verificarsi una maggior vulnerabilità agli effetti tossici sul fegato del paracetamolo soprattutto quando il farmaco è somministrato nei primi giorni di non assunzione di alcool negli alcolisti cronici. Potrebbe quindi essere opportuno non interrompere l’assunzione di alcool, negli alcolisti cronici, durante il trattamento con paracetamolo.[10] Sebbene il consumo cronico di alcool non comporti necessariamente un aumento dell’epatotossicità iatrogena quando il paracetamolo è somministrato alle dosi terapeutiche raccomandate,[11] il rischio potenziale potrebbe aumentare per la presenza di fattori predisponenti aggiuntivi come una preesistente disfunzione epatica e/o una deplezione delle riserve di glutatione (attraverso il quale è eliminato il metabolita epatotossico del paracetamolo, n-acetil-p-benzochinoneimina).[7]
- Denutrizione cronica
- I pazienti affetti da denutrizione cronica presentano un rischio più elevato di danno epatico anche con dosi terapeutiche di paracetamolo per insufficiente capacità metabolica del fegato.[7]
- Pazienti nefropatici/disidratati
- Nei pazienti pediatrici con disidratazione o insufficienza renale, il paracetamolo rappresenta il farmaco di scelta rispetto all'ibuprofene.[12]
- Nefropatia cronica
- Nei pazienti con nefropatia cronica non è necessario ridurre il dosaggio di paracetamolo (perché sia diagnosticata nefropatia cronica in stadio iniziale deve essere presente da 3 mesi o più danno renale confermato da anomalie patologiche o marker di danno renale. Negli stadi successive della patologia, è sufficiente per la diagnosi una riduzione della velocità di filtrazione glomerulare stimata, e-GFR, per 3 mesi o più).[13]
- Deficit di G6PD
- La somministrazione di paracetamolo alle dosi terapeutiche non induce emolisi nei pazienti affetti da favismo (carenza dell’enzima glucosio-6-fosfato deidrogenasi, G6PD). Il G6PD è un enzima necessario per la stabilità ematica e una eventuale sua carenza può esporre gli eritrociti a danno ossidativo ed emolisi (anemia emolitica). La relazione causa-effetto fra paracetamolo e anemia emolitica non è stata confermata e gli episodi di anemia emolitica riportati in associazione a paracetamolo sono da attribuire molto probabilmente a sovradosaggio.[14][15][16][17]
- Colestiramina
- Si raccomanda di assumere la colestiramina almeno un’ora dopo la somministrazione del paracetamolo. La colestiramina infatti può ridurre l’assorbimento del paracetamolo somministrato per via orale.[7]
- Cloramfenicolo
- Ridurre le dosi di cloramfenicolo quando associato a paracetamolo.[7]
- Warfarin
- Nei pazienti in trattamento con anticoagulanti orali (warfarin), la somministrazione di dosi di paracetamolo uguali o superiori a 2 g/die per più giorni richiede un controllo dell'indice INR più frequente rispetto ai tempi previsti (a causa dell’interazione farmacologica l’indice INR potrebbe infatti aumentare, con conseguente incremento del rischio emorragico).[7]
- Aspartame
- La presenza di aspartame fra gli eccipienti rappresenta una controindicazione alla somministrazione della specialità medicinale a pazienti affetti da fenilchetonuria.[7]
- Saccarosio
- Somministrare con cautela a pazienti diabetici le formulazioni in sciroppo a base di paracetamolo perché possono contenere saccarosio.[7]
- Sodio metabisolfito
- Alcune formulazioni farmaceutiche possono annoverare fra gli eccipienti sodio metabisolfito. Questa sostanza può scatenare in soggetti sensibili e nei pazienti asmatici reazioni allergiche, inclusa grave broncocostrizione.[7]
Note
- ^ Sigma Aldrich; rev. del 14.09.2012
- ^ (EN) Database ChemIndustry.com
- ^ raccomandazione della Food and Drug Administration
- ^ (EN) Michele Zell Kanter, Comparison of oral and i.v. acetylcysteine in the treatment of acetaminophen poisoning, in Am J Health Syst Pharm, vol. 63, n. 19, 2006, pp. 1821-1827, PMID 16990628. URL consultato il 31 ottobre 2007.
- ^ Onyeka Otugo, Olabode Ogundare, Christopher Vaughan, Emmanuel Fadiran, Leyla Sahin, Consistency of Pregnancy Labeling Across Different Therapeutic Classes (PDF), su fda.gov, Food and Drug Administration - Office of Women’s Health, 1979. URL consultato il 27 giugno 2013.
- ^ R. Sannerstedt, P. Lundborg; BR. Danielsson; I. Kihlström; G. Alván; B. Prame; E. Ridley, Drugs during pregnancy: an issue of risk classification and information to prescribers., in Drug Saf, vol. 14, n. 2, febbraio 1996, pp. 69-77, PMID 8852521.
- ^ a b c d e f g h i j k Pharmamedix: Paracetamolo
- ^ Whitcomb D.C. et al., JAMA, 1994, 272, 1845
- ^ Gomez-Moreno G. et al., Med. Oral. Patol. Oral. Cir. Bucal., 2008, 13 (4), E235
- ^ Gomez-Moreno G. et al., Med. Oral. Patol. Oral. Cir. Bucal., 2008, 13 (4), E235
- ^ Prescott L.F. et al., Eur. J. Clin. Pharmacol., 1989, 36, 291
- ^ John C.M. et al., Arch. Dis. Child., 2007, 92, 524
- ^ Dtb, Drug and Therapeutics Bullettin, 2006, vol 44 (12), 89
- ^ Beutler E., NEJM, 1991, 24, 1743
- ^ Bartsocas C.S., Acta Haematol., 1982, 67, 228
- ^ Pootrakul P. et al., Acta Haematol., 1983, 69, 358
- ^ Cottava F. et al., Pediatria medica e chirurgica, 1990, 12, 631
Bibliografia
- Botting R. Paracetamol-inhibitable COX-2. J Physiol Pharmacol. 2000 Dec; 51(4 Pt 1):609-18.
- Graham GG, Scott KF. Mechanism of action of paracetamol. Am J Ther. 2005 Jan-Feb; 12(1):46-55. Review. PMID: 15662292 [PubMed - indexed for MEDLINE]
- Chandrasekharan NV et al. COX-3, a cyclooxygenase-1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: cloning, structure, and expression. Proc Natl Acad Sci U S A. 2002 Oct 15; 99(21):13926-31. Epub 2002 Sep 19.
- Schwab JM, Schluesener HJ, Laufer S. COX-3: just another COX or the solitary elusive target of paracetamol? Lancet. 2003 Mar 22; 361(9362):981-82.
- Botting R, Ayoub SS. COX-3 and the mechanism of action of paracetamol/acetaminophen. Prostaglandins Leukot Essent Fatty Acids. 2005 Feb; 72(2):85-87.
- Mallet C et al. Endocannabinoid and serotonergic systems are needed for acetaminophen-induced analgesia. Pain 2008 Sep 30; 139(1):190-200. PMID: 18485596 [PubMed - indexed for MEDLINE]
Altri progetti
 Wikiquote contiene citazioni di o su paracetamolo
Wikiquote contiene citazioni di o su paracetamolo Wikimedia Commons contiene immagini o altri file su paracetamolo
Wikimedia Commons contiene immagini o altri file su paracetamolo
Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link AdQ Template:Link AdQ