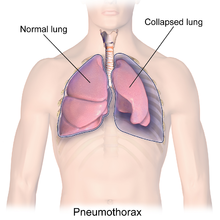
Pneumotorace
| Pneumotorace o PNX | |
|---|---|
 | |
| Specialità | medicina d'emergenza-urgenza, pneumologia e chirurgia toracica |
| Classificazione e risorse esterne (EN) | |
| ICD-10 | J93 |
| OMIM | 173600 e 173600 |
| MeSH | D011030 |
| MedlinePlus | 000087 |
| eMedicine | 424547, 360796, 808162, 827551 e 1003552 |
Lo[1] pneumotorace (abbreviato anche in PNX) è una patologia ad esordio improvviso che consiste nell'accumulo di aria nel cavo pleurico; può essere spontaneo, post-traumatico o secondario a patologie.
Quando la parete della gabbia toracica è integra, sulle superfici esterne dei polmoni si esercita una pressione inferiore a quella atmosferica: questa differenza di pressione contrasta la tendenza alla retroazione elastica del polmone facendo sì che l'organo resti insufflato e disteso e possa così svolgere la sua funzione fisiologica.
Lo pneumotorace, cioè la penetrazione di gas nella cavità pleurica, provoca, indipendentemente dalla causa che l'ha determinata, una riduzione o la scomparsa della pressione negativa ivi presente. Questo non permette l'espansione del polmone, cosicché questo collabisce in misura direttamente proporzionale alla quantità di gas penetrata nella cavità pleurica.
Storia[modifica | modifica wikitesto]

Una prima descrizione dello pneumotorace traumatico secondario dovuto a fratture costali compare in Chirurgia Imperial del chirurgo turco Şerafeddin Sabuncuoğlu (1385-1468), che raccomanda anche un metodo di semplice aspirazione.[2]
Lo pneumotorace è stato descritto nel 1803 da Jean Marc Gaspard Itard, allievo di René Laennec, che ha fornito una descrizione dettagliata del quadro clinico.[3] Mentre Itard e Laennec riconobbero che alcuni casi non erano dovuti alla tubercolosi (allora la causa più comune), il concetto di pneumotorace spontaneo primario è stato introdotto dal medico danese Hans Kjærgaard nel 1932.[4][5] Nel 1941, i chirurghi Tyson e Crandall introdussero l'abrasione pleurica per il trattamento dello pneumotorace.[4][6]
Prima dell'avvento dei farmaci anti-tubercolari, pneumotorace iatrogeni sono stati intenzionalmente causati a persone con tubercolosi, nel tentativo di chiudere un lobo o l'intero polmone, intorno ad una lesione da cavitazione. Questo è stato conosciuto come "il riposo del polmone". Fu introdotto dal chirurgo italiano Carlo Forlanini nel 1888 e propagandato dal chirurgo statunitense John Benjamin Murphy nel XX secolo (dopo aver scoperto la stessa procedura in modo indipendente). Murphy usò l'allora recente scoperta dei raggi X per creare pneumotoraci di diametro appropriato.[7]
Epidemiologia[modifica | modifica wikitesto]
L'incidenza dello pneumotorace primario spontaneo risulta essere da 3 a 6 volte superiore nei maschi rispetto alle femmine. Il Fishman[8][9] riporta da 7,4 a 1,2 casi per 100 000 anni-persona, rispettivamente per i maschi e per le femmine. Un'altezza significativamente superiore alla media è anche associata ad un aumento di rischio di incorrere nella condizione. Negli individui superiori ai 1,9 metri l'incidenza è di 200 casi per 100 000 anni-persona. Si ritiene che anche gli individui magri abbiano un aumento di rischio.[8]
Il rischio di contrarre uno pneumotorace spontaneo è elevato tra i fumatori di sesso maschile e femminile rispettivamente per fattori da circa 22 e 9, in confronto con i non fumatori dello stesso sesso.[10] Le persone che fumano sviluppano uno pneumotorace con maggior intensità. È stato dimostrato che il rischio legato al fumo abbia un andamento più che lineare: gli uomini che fumano 10 sigarette al giorno hanno approssimativo un rischio aumentato di 20 volte rispetto ai non fumatori, mentre coloro che consumano 20 sigarette al giorno mostrano un aumento di rischio di circa 100 volte.[8]
Nello pneumotorace spontaneo secondario, l'incidenza è di 6,3 e 2,0 casi per 100 000 anni-persona rispettivamente per i maschi e per le femmine[8][9], con un rischio basso di recidiva in base alla presenza e alla gravità di una malattia polmonare sottostante. Una volta che un secondo episodio si verifica, vi è un'elevata probabilità di successivi ulteriori episodi.[11] L'incidenza nei bambini non è stata ben studiata,[12] ma è stimata tra i 5 e i 10 casi per 100.000 anni-persona.[8]
La morte da pneumotorace è molto rara (se non si verifica uno pneumotorace iperteso). Statistiche britanniche mostrano un tasso annuo di mortalità di 1,26 e 0,62 morti per milione di anni-persona rispettivamente negli uomini e nelle donne.[4] Un aumento significativo del rischio di morte si nota nei pazienti anziani e in quelli con pneumotorace secondario.[11]
Eziologia[modifica | modifica wikitesto]
Pneumotorace spontaneo primario[modifica | modifica wikitesto]
Lo pneumotorace spontaneo o semplice è ad eziologia sconosciuta e si verifica spesso in assenza di malattie polmonari. Viene frequentemente riscontrato in soggetti di sesso maschile, con meno di 40 anni, alti, magri, spesso fumatori. È causato dalla rottura spontanea di piccole bolle subpleuriche ("blebs"), localizzate agli apici polmonari. Interessa spesso il polmone destro e ha un'alta probabilità di recidivare (50%).
Pneumotorace spontaneo secondario[modifica | modifica wikitesto]
Lo pneumotorace secondario spontaneo si verifica nel contesto di una varietà di malattie polmonari. La più comune è la broncopneumopatia cronica ostruttiva, che rappresenta circa il 70% dei casi.[13] Malattie polmonari note che possono aumentare significativamente il rischio di incorrere nello pneumotorace sono:
| Tipo | Cause |
|---|---|
| Malattie delle vie aeree[14] | Broncopneumopatia cronica ostruttiva (soprattutto quando sono presenti enfisema e bolle polmonari), asma, fibrosi cistica |
| Infezione dei polmoni[14] | Pneumocistosi (PCP), tubercolosi, polmonite |
| Malattia interstiziale del polmone[14] | Sarcoidosi, fibrosi polmonare idiopatica, istiocitosi a cellule di Langerhans, linfangioleiomiomatosi (LAM) |
| Malattie del tessuto connettivo[14] | artrite reumatoide, spondilite anchilosante, polimiosite e dermatomiosite, sclerosi sistemica, sindrome di Marfan e sindrome di Ehlers-Danlos |
| Neoplasie[14] | Tumore del polmone, sarcoma che interessa il polmone |
| Varie[15] | Pneumotorace catameniale (associato con il ciclo mestruale e relativo all'endometriosi) |
Nei bambini, altre cause sono il morbillo, l'echinococcosi, l'inalazione di un corpo estraneo e alcune malformazioni congenite (Malformazione adenomatoide cistica e l'enfisema lobare congenito).[12]
L'11,5% degli individui con uno pneumotorace spontaneo avevano un membro della famiglia che a sua volta aveva in precedenza avuto questa condizione. Le condizioni ereditarie come la sindrome di Marfan, l'omocistinuria, la sindrome di Ehlers-Danlos, l'alfa 1-antitripsina (che porta a enfisema) e la sindrome di Birt-Hogg-Dubé sono state collegate con pneumotorace familiare.[16] In generale, queste condizioni causano altri segni e sintomi e, lo pneumotorace non è di solito il primo evento a manifestarsi.[16] La sindrome di Birt-Hogg-Dubé è causata da mutazioni nel gene FLCN (che si trova sul cromosoma 17 p11.2), che codifica per una proteina chiamata follicolina.[12][16] Mutazioni del gene FLCN e lesioni polmonari sono state identificate anche nei casi familiari di pneumotorace in cui altre caratteristiche della sindrome di Birt-Hogg-Dubé sono assenti.[12] Oltre alle correlazioni genetiche appena descritte, l'aplotipo HLA A2B40 è anch'essa una predisposizione genetica per lo pneumotorace spontaneo.[17][18]
Pneumotorace traumatico[modifica | modifica wikitesto]
Uno pneumotorace traumatico può derivare da trauma contusivo o da una ferita penetrante nella parete toracica.[15] L'evento più comune è una frattura costale in cui il moncone osseo penetra la pleura danneggiando il tessuto polmonare.[13] Questo tipo di pneumotorace può essere riscontrato anche nelle vittime di esplosioni.[19]
Alcune procedure mediche che riguardano il torace, come l'inserimento di un catetere venoso centrale o il prelievo bioptico del tessuto polmonare, possono portare ad uno pneumotorace. La somministrazione di ventilazione a pressione positiva, sia meccanica che non invasiva, può provocare un barotrauma che porta ad uno pneumotorace.[15]
Fisiopatologia[modifica | modifica wikitesto]

La cavità toracica è lo spazio all'interno della gabbia toracica che contiene i polmoni, il cuore e un certo numero di vasi sanguigni. Su ogni lato della cavità, la membrana pleurica copre la superficie del polmone (pleura viscerale) e riveste l'interno della parete toracica (pleura parietale). Normalmente, i due strati sono separati solo da una piccola quantità di liquido sieroso lubrificante. I polmoni sono completamente gonfiati all'interno della cavità per via della loro pressione interna, superiore alla pressione della cavità pleurica. Nonostante la bassa pressione nella cavità pleurica, l'aria non entra perché non vi sono connessioni fisiche e la pressione del gas nel sangue è troppo bassa per poter essere forzata ad andare nello spazio pleurico.[15] Pertanto, uno pneumotorace può svilupparsi solo se l'aria può entrare attraverso un danno alla parete toracica o al polmone stesso.[15]
Difetti della parete del torace sono solitamente evidenti, come nel caso di ferite da taglio. In uno pneumotorace secondario spontaneo, la vulnerabilità del tessuto polmonare è causato da una varietà di processi patologici, in particolare la rottura di bolle di grandi dimensioni e contenenti aria, nei casi di enfisema grave. Le aree di necrosi (morte del tessuto) possono causare episodi di pneumotorace, sebbene l'esatto meccanismo non sia chiaro.[14] Per molti anni, lo pneumotorace spontaneo primario è stato ritenuto essere causato da "vesciche" o "blebs" (piccole lesioni piene d'aria appena sotto la superficie pleurica, "blebs subpleuriche"), che si presumeva fossero più comuni negli individui ritenuti maggiormente a rischio, cioè i maschi alti. Diversi studi basati sull'evidenza, suggeriscono che questa ipotesi non possa essere sufficiente a spiegare tutti gli episodi di pneumotorace spontaneo primario, come ad esempio il fatto che lo pneumotorace possa ripresentarsi anche dopo il trattamento chirurgico delle vesciche e che le vesciche si verificano nel 15% delle persone sane. È stato pertanto suggerito che lo pneumotrace spontaneo primario possa essere causato da zone di interruzione (porosità) nello strato pleurico, che possono facilmente rompersi.[14][15] inoltre, il fumo può causare infiammazione e ostruzione delle piccole vie aeree, si riscontra pertanto un marcato aumento del rischio di pneumotorace spontaneo nei fumatori.[4] Quando l'aria si forma nella cavità pleurica, essa viene gradualmente riassorbita spontaneamente.[4]
Il pneumotorace iperteso è una condizione pericolosa per la vita del soggetto che risulta da un lento deterioramento e peggioramento di un normale pneumotorace per effetto di un meccanismo a valvola che si può venire a creare in corrispondenza della rottura del parenchima polmonare o della parete toracica che ha causato lo pneumotorace e che consente il passaggio di aria solo verso il cavo pleurico e non viceversa. Per questo motivo si può verificare l'aumento della pressione contenuta nello spazio pleurico che, oltre al collasso del polmone colpito, provoca lo spostamento del mediastino e degli organi in esso contenuti verso il lato opposto fino a generare l'insufficienza respiratoria e/o sintomi cardiovascolari, legati principalmente al ridotto ritorno venoso che possono causare la morte del paziente.[20]
Segni e sintomi[modifica | modifica wikitesto]
Caratteristiche cliniche[modifica | modifica wikitesto]
Lo pneumotorace primario spontaneo (PSP) tende a verificarsi in persone giovani senza problemi polmonari e di solito provoca segni e sintomi limitati. Il dolore toracico e lieve dispnea sono solitamente le caratteristiche predominanti.[14][15] Metà dei pazienti con pneumotorace spontaneo primario non sono consapevoli del potenziale pericolo nella loro condizione e attendono diversi giorni prima di consultare un medico.[4] Il PSP si verifica più comunemente durante i cambiamenti di pressione atmosferica e durante l'esposizione a musica ad alto volume, ciò spiega perché molti episodi di pneumotorace accadono in gruppo.[15] È raro che PSP possa causare un pneumotorace iperteso.[14]
Lo pneumotorace secondario spontaneo (SSP), per definizione, si verifica in soggetti con significative malattie polmonari sottostanti. I segni e sintomi nell'SSP tendono ad essere più gravi rispetto a PSP: infatti il polmone inalterato non è generalmente in grado di sostituire la perdita del polmone colpito. Solitamente si verifica ipossiemia (riduzione dei livelli di ossigeno nel sangue) che può essere rilevata come cianosi (colorazione blu delle labbra e della pelle). L'ipercapnia (accumulo di anidride carbonica nel sangue) viene talvolta riscontrata, questa può causare confusione e, in casi molto gravi, portare al coma. L'insorgenza improvvisa di dispnea in una persona con broncopneumopatia cronica ostruttiva, con la fibrosi cistica o altre malattie polmonari gravi, dovrebbe indurre a compiere indagini per individuare la possibilità di uno pneumotorace.[4][14]
Lo pneumotorace traumatico si verifica più comunemente quando la parete toracica viene trafitta, come da una coltellata o una ferita da arma da fuoco. La ferita permette all'aria di entrare nello spazio pleurico o perché qualche altra lesione meccanica al polmone compromette l'integrità delle strutture coinvolte. Lo pneumotorace traumatico si verifica in più della metà di tutti i casi di trauma toracico con fratture costali. Lo pneumotorace può essere occulto (non evidente) in metà di questi casi ma può ingrandirsi, soprattutto se la ventilazione meccanica si rende necessaria.[15]
All'esame fisico i rumori respiratori udibili (utilizzando uno stetoscopio) possono essere ridotti nel lato colpito, in parte perché l'aria nello spazio pleurico smorza la trasmissione del suono. È importante sottolineare che il volume dello pneumotorace può mostrare una limitata correlazione con l'intensità dei sintomi riscontrati dalla vittima,[4] e ci possono essere segni evidenti fisici quando lo pneumotorace è relativamente piccolo.[15]
Pneumotorace iperteso[modifica | modifica wikitesto]
Sebbene esistano numerose definizioni, uno pneumotorace iperteso è generalmente considerato essere presente quando uno pneumotorace porta ad una significativa compromissione della respirazione o della circolazione del sangue.[20] I risultati più comuni riscontrati nelle persone con pneumotorace iperteso sono dolore al petto e difficoltà respiratoria, spesso con un aumento della frequenza cardiaca (tachicardia) e con la respirazione rapida (tachipnea).[20] Si tratta di un'emergenza medica che può richiedere un trattamento immediato, senza ulteriori indagini.[4][20]
Pneumotorace iperteso può verificarsi in ventilazione meccanica, nel qual caso può essere difficile da individuare, difatti la persona colpita risulta essere sedata. Deviazione della trachea su un lato e la presenza di aumento della pressione venosa giugulare (vene del collo dilatate) non sono affidabili come segni clinici.[20]
Diagnosi[modifica | modifica wikitesto]
I sintomi di uno pneumotorace possono esser vaghi, soprattutto nei pazienti con un lieve pneumotorace spontaneo primitivo e quindi una conferma della diagnosi, tramite tecniche di imaging medico, si rende solitamente necessaria.[4] Al contrario, uno pneumotorace iperteso rappresenta un'emergenza medica e può essere necessario trattarlo prima degli approfondimenti diagnostici, soprattutto se vi è una grave ipossia, una pressione sanguigna molto bassa, o uno stato di coscienza alterato. Nello pneumotorace iperteso, i raggi X a volte sono necessari se vi sono dubbi circa la posizione anatomica dello pneumotorace.[13][20]
La radiografia del torace[modifica | modifica wikitesto]

Tradizionalmente una radiografia del torace, in una proiezione postero-anteriore, è l'indagine diagnostica più appropriata.[4][15] Se la radiografia non mostra uno pneumotorace ma c'è un forte sospetto, un'ulteriore radiografia del torace in proiezione laterale può essere necessaria.[4][12] Non è insolito che il mediastino (la struttura posta tra i polmoni e che contiene il cuore, i grandi vasi sanguigni e le vie aeree) sia spostato verso il polmone sano a causa delle differenze di pressione. In uno pneumotorace iperteso, la diagnosi è principalmente determinata grazie all'osservazione dei sintomi, quali ipossia e shock.[15]
La dimensione dello pneumotorace (ossia il volume di aria nello spazio pleurico) può essere determinato con un ragionevole grado di precisione misurando la distanza tra la parete toracica e quella del polmone. Questo è rilevante per il trattamento, in quanto pneumotoraci di diversa dimensione vanno gestiti in modo diverso. L'utilizzo della tomografia computerizzata permette una misura più accurata delle dimensioni, ma il suo uso di routine in questo contesto non è raccomandato.[21]
Non tutti i pneumotoraci sono uniformi. Piccole quantità di fluido possono essere viste sulla radiografia del torace (idropneumotorace), questo liquido può essere sangue (emopneumotorace).[15] In alcuni casi, l'unica significativa anomalia visibile in radiografia è il "segno del solco profondo", in cui viene visto ingrandito lo spazio tra la parete toracica e il diaframma per la presenza anomala di fluido.[20]
La tomografia computerizzata[modifica | modifica wikitesto]

La tomografia computerizzata (TC) può essere utile in particolari situazioni. In alcune malattie polmonari, in particolare nell'enfisema, è possibile, per via della presenza di aree anormali del polmone come bolle (grandi sacche piene d'aria), avere lo stesso aspetto di uno pneumotorace sulla radiografia, e quindi è necessario distinguere le due patologie prima di iniziare un trattamento.[4] In trauma, in cui potrebbe non essere possibile eseguire una radiografia in piedi, e quindi perdere di sensibilità, la TC può essere una valida soluzione.[13]
Un ulteriore utilizzo della TC è l'identificazione di lesioni polmonari sottostanti. In un presunto pneumotorace primario, può aiutare ad identificare lesioni cistiche e nello pneumotorace secondario può aiutare ad identificare la maggior parte delle cause sopra elencate.[4][12]
Ecografia[modifica | modifica wikitesto]
L'ecografia viene comunemente utilizzata nella valutazione di persone che hanno subito traumi fisici, per esempio con il protocollo eco FAST.[23] L'utilizzo dell'ecografia può risultare più sensibile rispetto alla radiografia del torace nell'identificazione di uno pneumotorace dopo un trauma chiuso.[24] Questa tecnica può anche fornire una diagnosi rapida in altre situazioni di emergenza e consentire la quantificazione della dimensione dello pneumotorace.[25]
Trattamento[modifica | modifica wikitesto]
Il trattamento dello pneumotorace dipende da una serie di fattori, e può variare da una decompressione precoce all'inserimento di un tubo toracico. La strategia di gestione dipende dalla gravità dei sintomi, dalla presenza di una malattia polmonare di base, dalla dimensione stimata dello pneumotorace visibile nella radiografia, e in alcuni casi, sulle preferenze del paziente.[4]
Nello pneumotorace traumatico, solitamente viene inserito un tubo toracico. Se la ventilazione meccanica si rende necessaria, il rischio di pneumotorace iperteso aumenta di molto e l'inserimento di un tubo toracico diviene obbligatorio.[15][26] Ogni ferita aperta del torace deve essere coperta con una chiusura ermetica, in quanto comporta un elevato rischio di condurre ad uno pneumotorace iperteso. Possibilmente si può utilizzare una chiusura particolare, detta "medicazione Asherman", un dispositivo appositamente progettato che aderisce alla parete toracica e, attraverso una valvola, permette all'aria di uscire ma non di entrare nel petto.[27]
Lo pneumotorace iperteso solitamente è trattato con una decompressione urgente mediante ago. Questo potrebbe rendersi necessario prima del trasporto in ospedale.[20][27] L'ago viene lasciato in sede fino a quando un tubo toracico viene inserito.[20][27] Se lo pneumotorace iperteso porta ad un arresto cardiaco, l'inserimento di un ago di decompressione viene eseguito come parte delle procedure di rianimazione, in quanto può ripristinare la gittata cardiaca.[28]
Trattamento conservativo[modifica | modifica wikitesto]
Piccoli pneumotoraci spontanei non sempre richiedono un trattamento, in quanto è improbabile che possano provocare insufficienza respiratoria o pneumotorace iperteso e generalmente si risolvono da soli. Questo approccio è il più appropriato se la dimensione stimata dello pneumotorace è piccola (definita come <50% del volume dell'emitorace), non vi è mancanza di respiro e non vi è presenza di alcuna malattia polmonare.[12][21] La strategia conservativa può essere appropriata per trattare uno pneumotorace spontaneo se i sintomi appaiono limitati.[4] Il ricovero in ospedale spesso non si rende necessario, purché vengano date chiare istruzioni nel caso di peggioramento dei sintomi. Ulteriori indagini possono essere eseguite in regime ambulatoriale, ripetendo l'indagine radiografica per confermare il miglioramento e valutare la prevenzione di recidive.[4] I tassi di riassorbimento sono compresi tra l'1,25% e il 2,2% del volume della cavità al giorno. Ciò significa che anche uno pneumotorace completo dovrebbe risolversi spontaneamente in un periodo di circa 6 settimane.[4]
Pneumotoraci secondari sono trattati in modo conservativo solo se la dimensione è molto piccola (1 cm o meno di cavità) e vi sono limitati sintomi. il ricovero in ospedale è generalmente raccomandato. La somministrazione di ossigeno a velocità di flusso elevata può accelerare il riassorbimento.[4][29]
Aspirazione[modifica | modifica wikitesto]
In un importante pneumotorace spontaneo primario (> 50%), alcune linee guida professionali consigliano di ridurne la dimensione mediante l'aspirazione, ottenendo un risultato sovrapponibile a quello dell'inserimento di un tubo toracico. Questo prevede la somministrazione di anestetico locale e l'inserimento di un ago collegato ad un rubinetto a tre vie. Negli adulti possono essere rimossi fino a 2,5 litri di aria. Se alla valutazione radiografica appare una significativa riduzione delle dimensioni dello pneumotorace, il resto del trattamento può essere conservativo. Questo approccio è stato dimostrato essere efficace nel 50% dei casi.[4][12][14] Ciò, inoltre, riduce significativamente il numero di persone che necessitano il ricovero, senza, peraltro, aumentare il rischio di complicanze.[30]
L'aspirazione è una strategia che può essere considerata anche nello pneumotorace secondario di medie dimensioni (1–2 cm d'aria) senza particolari sintomi respiratori, con la differenza che un periodo di osservazione in ospedale si rende necessaria anche dopo una procedura di successo.[4]
Drenaggio toracico[modifica | modifica wikitesto]

Un drenaggio toracico è il trattamento iniziale definitivo di uno pneumotorace. Il tubo di drenaggio viene tipicamente inserito in una zona sotto l'ascella chiamato "triangolo sicuro", dove danni agli organi interni possono essere evitati. Questa zona è delimitata da una linea orizzontale al livello del capezzolo e dai due muscoli della parete toracica (gran dorsale e grande pettorale). Un anestetico locale viene applicato durante la procedura. Due tipi di tubo possono essere utilizzati. Nello pneumotorace spontaneo, tubi di piccolo diametro (minore di 14 Fr, 4,7 mm di diametro) possono essere inseriti con la tecnica di Seldinger.[4] Nello pneumotorace traumatico sono utilizzati tubi più grandi (28 Fr, 9,3 millimetri).[27]
Il drenaggio toracico si rende inoltre necessario nei casi in cui l'aspirazione con ago non abbia avuto successo e nei pazienti che presentano pneumotorace iperteso. Essi vengono collegati ad un sistema di valvola unidirezionale che permette all'aria di fuoriuscire ma non di rientrare. Questo può includere una bottiglia di acqua che funziona come un sigillo d'acqua o una valvola di Heimlich. Essi non sono normalmente collegati a un circuito di pressione negativa, in quanto ciò comporterebbe una rapida riespansione del polmone e un conseguente rischio di edema polmonare. Il tubo viene rimosso soltanto quando l'aria è completamente fuoriuscita e quando la radiografia conferma la riespansione del polmone.[4][12][21]
Se dopo 2-4 giorni vi è ancora evidenza di una perdita d'aria, sono disponibili varie opzioni. Ad esempio, può essere tentata un'aspirazione a pressione negativa (a basse pressioni che vanno da -10 a -20 cmH2O), si pensa che ciò possa accelerare la guarigione. In caso contrario, la chirurgia può rendersi indispensabile.[4]
Il drenaggio toracico può essere utilizzato come intervento di elezione nei pazienti che presentano AIDS, che sviluppano solitamente lo pneumotorace come conseguenza della polmonite da Pneumocystis jirovecii, in quanto questa condizione è associata a perdite d'aria prolungate. Lo pneumotorace bilaterale è relativamente comune nelle persone con la polmonite da Pneumocystis e la chirurgia è spesso richiesta.[4]
Pleurodesi e chirurgia[modifica | modifica wikitesto]
La pleurodesi è una procedura che elimina in modo permanente lo spazio pleurico attaccando il polmone alla parete toracica. Sebbene invasiva, una tecnica prevede toracotomia (apertura chirurgica del torace) con identificazione di qualsiasi fonte di perdite d'aria, seguita da pleurectomia (strippaggio del rivestimento pleurico) dello strato esterno pleurico e abrasione pleurica (raschiamento della pleura) dello strato interno. Durante il processo di guarigione, il polmone aderisce alla parete toracica, di fatto invadendo lo spazio pleurico. I tassi di recidiva sono circa l'1%.[4][14]
Un approccio meno invasivo è la toracoscopia, di solito sotto forma di una procedura chiamata videotoracoscopia. I risultati di questa metodica sono soddisfacenti e producono solo piccole cicatrici della pelle.[4][14] Rispetto alla toracotomia, la videotoracoscopia necessita di un breve ricovero in ospedale, meno necessità di un controllo del dolore post-operatorio ed un ridotto rischio di problemi polmonari a seguito dell'intervento.[4] La tecnica consiste nell'asportazione della bolla o dell'area distrofica del polmone associata alla pleurodesi meccanica (irritazione della pleura parietale, che attiva una reazione infiammatoria che induce l'adesione del polmone alla parete toracica). La pleurodesi generalmente eseguita è quella meccanica, ma in alcuni casi (pazienti anziani) può essere effettuata quella chimica: ciò comporta l'insufflazione di talco .[4][14]
Se un tubo toracico è già stato messo in sede, vari agenti possono essere instillati attraverso esso al fine di ottenere pleurodesi chimica, in particolare talco o tetraciclina. I risultati della pleurodesi chimica tendono ad essere peggiori rispetto all'approccio chirurgico,[4][14], alcuni autori ritengono che la pleurodesi per mezzo del talco dia poche conseguenze negative a lungo termine nei pazienti più giovani.[14]
Prevenzione[modifica | modifica wikitesto]
Una procedura di prevenzione (toracotomia o toracoscopia con pleurodesi) può essere raccomandata dopo un episodio di pneumotorace, con l'intenzione di prevenire le recidive. Le prove sul trattamento più efficace sono ancora dibattute e vi sono differenze tra i trattamenti disponibili in Europa e negli Stati Uniti.[11] Non tutti gli episodi di pneumotorace richiedono tali interventi. La decisione dipende in gran parte dalla stima del rischio di recidiva. Queste procedure sono spesso raccomandate dopo il verificarsi di uno pneumotorace secondario.[11] L'intervento chirurgico può essere necessario se il paziente ha sperimentato pneumotorace su entrambi gli emitoraci ("bilaterale"), episodi in sequenza che coinvolgono entrambe le parti o se un episodio è stato associato alla gravidanza.[4]
Note[modifica | modifica wikitesto]
- ^ Parere della Redazione Consulenza Linguistica dell'Accademia della Crusca circa l'articolo precedente il gruppo /pn/.
- ^ Kaya SO, Karatepe M, Tok T, Onem G, Dursunoglu N, Goksin, I, Were pneumothorax and its management known in 15th-century anatolia?, in Texas Heart Institute Journal, vol. 36, n. 2, settembre 2009, pp. 152-153, PMID 19436812.
- ^ (FR) Laennec RTH, Traité de l'auscultation médiate et des maladies des poumons et du coeur - part II, Paris, 1819.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae MacDuff A, Arnold A, Harvey J, BTS Pleural Disease Guideline Group, Management of spontaneous pneumothorax: British Thoracic Society pleural disease guideline 2010, in Thorax, vol. 65, n. 8, dicembre 2010, pp. ii18–ii31, DOI:10.1136/thx.2010.136986, PMID 20696690.
- ^ Kjærgard H, Spontaneous pneumothorax in the apparently healthy, in Acta Medica Scandinavica, 43 Suppl, 1932, pp. 1–159, DOI:10.1111/j.0954-6820.1932.tb05982.x.
- ^ Tyson MD, Crandall WB, The surgical treatment of recurrent idiopathic spontaneous pneumothorax, in Journal of Thoracic Surgery, vol. 10, 1941, pp. 566–70.
- ^ Herzog H, History of tuberculosis (PDF), in Respiration, vol. 65, n. 1, 1998, pp. 5–15, DOI:10.1159/000029220, PMID 9523361.
- ^ a b c d e Levine DJ, Sako EY, Peters J, Fishman's Pulmonary Diseases and Disorders, 4th, McGraw-Hill, 2008, pp. 1519, ISBN 0-07-145739-9.
- ^ a b Light RW, Pleural diseases, 5th, Lippincott Williams & Wilkins, 2007, pp. 306, ISBN 0-7817-6957-4.
- ^ Bense L, Eklund G, Wiman LG, Smoking and the increased risk of contracting spontaneous pneumothorax, in Chest, vol. 92, n. 6, 1987, pp. 1009–12, DOI:10.1378/chest.92.6.1009, PMID 3677805.
- ^ a b c d Baumann MH, Noppen M, Pneumothorax, in Respirology, vol. 9, n. 2, giugno 2004, pp. 157–64, DOI:10.1111/j.1440-1843.2004.00577.x, PMID 15182264.
- ^ a b c d e f g h i Robinson PD, Cooper P, Ranganathan SC, Evidence-based management of paediatric primary spontaneous pneumothorax, in Paediatric Respiratory Reviews, vol. 10, n. 3, settembre 2009, pp. 110–7, DOI:10.1016/j.prrv.2008.12.003, PMID 19651381.
- ^ a b c d Marx J, Rosen's emergency medicine: concepts and clinical practice 7th edition, Philadelphia, PA, Mosby/Elsevier, 2010, pp. 393–396, ISBN 978-0-323-05472-0.
- ^ a b c d e f g h i j k l m n o p Tschopp JM, Rami-Porta R, Noppen M, Astoul P, Management of spontaneous pneumothorax: state of the art, in European Respiratory Journal, vol. 28, n. 3, settembre 2006, pp. 637–50, DOI:10.1183/09031936.06.00014206, PMID 16946095.
- ^ a b c d e f g h i j k l m n Noppen M, De Keukeleire T, Pneumothorax, in Respiration, vol. 76, n. 2, 2008, pp. 121–7, DOI:10.1159/000135932, PMID 18708734.
- ^ a b c Chiu HT, Garcia CK, Familial spontaneous pneumothorax, in Current Opinion in Pulmonary Medicine, vol. 12, n. 4, luglio 2006, pp. 268–72, DOI:10.1097/01.mcp.0000230630.73139.f0, PMID 16825879.
- ^ Levine DJ, Sako EY, Peters J, Fishman's Pulmonary Diseases and Disorders, 4th, McGraw-Hill, 2008, pp. 1520, ISBN 0-07-145739-9.
- ^ Light RW, Pleural diseases, 5th, Lippincott Williams & Wilkins, 2007, pp. 307, ISBN 0-7817-6957-4.
- ^ Wolf SJ, Bebarta VS, Bonnett CJ, et al, Blast injuries, in Lancet, vol. 374, n. 9687, agosto 2009, pp. 405–15, DOI:10.1016/S0140-6736(09)60257-9, PMID 19631372.
- ^ a b c d e f g h i Leigh-Smith S, Harris T, Tension pneumothorax—time for a re-think?, in Emergency Medicine Journal, vol. 22, n. 1, gennaio 2005, p. 8–16.
- ^ a b c Baumann MH, Strange C, Heffner JE, et al, Management of spontaneous pneumothorax: an American College of Chest Physicians Delphi consensus statement, in Chest, vol. 119, n. 2, febbraio 2001, pp. 590–602, DOI:10.1378/chest.119.2.590, PMID 11171742. URL consultato il 5 aprile 2012 (archiviato dall'url originale il 16 marzo 2020).
- ^ UOTW #6 – Ultrasound of the Week, su Ultrasound of the Week, 24 giugno 2014. URL consultato il 27 maggio 2017 (archiviato dall'url originale l'8 settembre 2017).
- ^ Scalea T, Rodriguez A, Chiu W, et al, Focused Assessment with Sonography for Trauma (FAST): results from an international consensus conference, in Journal of Trauma, vol. 46, n. 3, 1999, pp. 466–72, DOI:10.1097/00005373-199903000-00022, PMID 10088853.
- ^ Wilkerson RG, Stone MB, Sensitivity of bedside ultrasound and supine anteroposterior chest radiographs for the identification of pneumothorax after blunt trauma, in Academic Emergency Medicine, vol. 17, n. 1, gennaio 2010, pp. 11–17, DOI:10.1111/j.1553-2712.2009.00628.x, PMID 20078434.
- ^ Volpicelli G, Sonographic diagnosis of pneumothorax, in Intensive Care Medicine, vol. 37, n. 2, febbraio 2011, pp. 224–32, DOI:10.1007/s00134-010-2079-y, PMID 21103861.
- ^ Keel M, Meier C, Chest injuries - what is new?, in Current Opinion in Critical Care, vol. 13, n. 6, dicembre 2007, pp. 674–9, DOI:10.1097/MCC.0b013e3282f1fe71, PMID 17975389.
- ^ a b c d Lee C, Revell M, Porter K, Steyn R, The prehospital management of chest injuries: a consensus statement. Faculty of Pre‐hospital Care, Royal College of Surgeons of Edinburgh, in Emergency Medicine Journal, vol. 24, n. 3, marzo 2007, pp. 220–4, DOI:10.1136/emj.2006.043687, PMC 2660039, PMID 17351237.
- ^ Neumar RW, Otto CW, Link MS, et al, Part 8: adult advanced cardiovascular life support: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care, in Circulation, vol. 122, 18 Suppl 3, novembre 2010, pp. S729–67, DOI:10.1161/CIRCULATIONAHA.110.970988, PMID 20956224.
- ^ Light RW, Pleural diseases, 5th, Lippincott Williams & Wilkins, 2007, pp. 310, ISBN 0-7817-6957-4.
- ^ Wakai A, O'Sullivan RG, McCabe G, Simple aspiration versus intercostal tube drainage for primary spontaneous pneumothorax in adults, in Cochrane Database of Systematic Reviews, n. 1, 2007, pp. CD004479, DOI:10.1002/14651858.CD004479.pub2, PMID 17253510. URL consultato il 27 ottobre 2012 (archiviato dall'url originale il 16 aprile 2020).
Bibliografia[modifica | modifica wikitesto]
- (EN) American (AAOS), Advanced Assessment and Treatment of Trauma, Jones & Bartlett Learning, 2009, ISBN 978-0-7637-5131-9.
- (EN) Richard W. Light, Pleural Diseases, Lippincott Williams & Wilkins, 2007, ISBN 978-0-7817-6957-0.
- A. D'Agata, L. Voltolini, Alberto Oliaro, Pneumotorace, Minerva Medica, 2005, ISBN 978-88-7711-508-9.
- Gaetano Crepaldi, Aldo Baritussio, Trattato di medicina interna, PICCIN, 2002, ISBN 978-88-299-1642-9.
- Claudio Terzano (a cura di), Malattie dell'apparato respiratorio, Springer, 2006, ISBN 978-88-470-0466-5.
- Angelo Casalini, Pneumologia interventistica, Springer, 2007, ISBN 978-88-470-0555-6.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su pneumotorace
Wikimedia Commons contiene immagini o altri file su pneumotorace
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) pneumothorax, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Occhioclinico.it. URL consultato il 6 giugno 2007 (archiviato dall'url originale il 21 febbraio 2007).
- Università degli Studi di Napoli Seconda, su unina2.it. URL consultato il 6 giugno 2007 (archiviato dall'url originale il 7 marzo 2007).
| Controllo di autorità | Thesaurus BNCF 45767 · LCCN (EN) sh85103632 · GND (DE) 4250684-0 · BNF (FR) cb122588766 (data) · J9U (EN, HE) 987007558093505171 · NDL (EN, JA) 00565798 |
|---|