Sindrome di Goodpasture
| Sindrome di Goodpasture | |
|---|---|
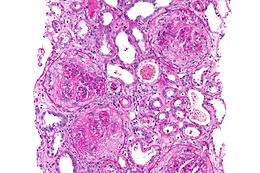 | |
| Malattia rara | |
| Cod. esenz. SSN | RG0060 |
| Specialità | nefrologia, pneumologia e immunologia |
| Classificazione e risorse esterne (EN) | |
| OMIM | 233450 |
| MeSH | D019867 |
| MedlinePlus | 000142 |
| eMedicine | 1001872 e 240556 |
| Eponimi | |
| Ernest William Goodpasture | |
La sindrome di Goodpasture è una malattia autoimmune a eziologia idiopatica caratterizzata da una glomerulonefrite e da emorragie interstiziali polmonari a rapida evoluzione. Le lesioni, rinvenute nel 90% della popolazione affetta, sono provocate da auto-anticorpi forse diretti contro la catena alpha-3 del collagene IV della membrana basale dei glomeruli renali e degli alveoli polmonari. Rientra nell'elenco delle malattie rare definito dall'Istituto Superiore di Sanità (codice RG0060).
Tale malattia è stata descritta per la prima volta dal patologo statunitense Ernest William Goodpasture dell'Università Vanderbilt nel 1919 e da cui ha preso in seguito il suo nome attuale[1][2].
Epidemiologia[modifica | modifica wikitesto]
La sindrome di Goodpasture è rara e colpisce circa lo 0,5÷1,8 per milione di persone all'anno in Europa e in Asia.[3] Si riscontra più frequentemente nei maschi rispetto alle femmine ed è anche meno comune nei neri rispetto ai bianchi. Si presenta, tuttavia, con maggior probabilità in persone Maori della Nuova Zelanda.[3] Le fasce di età di picco per l'insorgenza della malattia sono tra i 20 e i 30 e tra i 60 e i 70 anni.[3]
Segni e sintomi[modifica | modifica wikitesto]
Gli anticorpi anti-membrana basale glomerulare (MBG) attaccano principalmente reni e polmoni, dando, tuttavia, sintomi generici quali malessere generalizzato, perdita di peso, stanchezza, febbre, brividi e dolori articolari.[4] Dal 60% all'80% di coloro che hanno la condizione, presentano sia un coinvolgimento polmonare che renale; tra il 20 e il 40% ha solo un coinvolgimento renale e meno del 10% solo polmonare.[4] I sintomi polmonari di solito si presentano prima di quelli renali e solitamente includono: tosse con sangue, dolore toracico (in meno del 50% dei casi nel complesso), tosse e mancanza di respiro.[5] Solitamente i sintomi renali includono sangue nelle urine, proteine nelle urine, inspiegabile gonfiore degli arti o del viso, elevate quantità di urea nel sangue e la pressione alta.[4]
Aspetto fisiopatologico[modifica | modifica wikitesto]
Il polmone presenta diffuse emorragie alveolari con aree rosse più consistenti per la presenza di sangue e microscopicamente si nota necrosi, ispessimento delle pareti e presenza di emosiderina. La presenza di immunocomplessi è il punto fermo per la diagnosi. Clinicamente può manifestarsi con emoftoe.
Nel rene si possono evidenziare in immunofluorescenza i depositi di immunocomplessi nella membrana basale dell'endotelio glomerulare.[senza fonte]
Terapia[modifica | modifica wikitesto]
Il principale cardine del trattamento della sindrome consiste nella plasmaferesi, un procedimento in cui il sangue del paziente viene passato attraverso una centrifuga e i vari elementi separati in base al peso.[6] Il plasma, la parte fluida del sangue e che contiene gli anticorpi anti-MGB che attaccano i polmoni e i reni causando la malattia, viene filtrato reimmettendo nel paziente le altre parti del sangue, ovvero i globuli rossi, globuli bianchi e piastrine.[6] Inoltre, la maggior parte degli individui affetti dalla malattia devono essere trattati con immunosoppressori (farmaci che deprimono il funzionamento del sistema immunitario), e in particolare con la ciclofosfamide, il prednisone e il rituximab, al fine di impedire la formazione di nuovi anticorpi anti-MGB per evitare ulteriori danni a reni e polmoni.[6] Altri immunosoppressori meno forti e dunque con meno effetti collaterali, come l'azatioprina, possono essere utilizzati per mantenere la remissione.[6]
Se la malattia ha colpito pesantemente il rene, è necessario ricorrere al trapianto.
Prognosi[modifica | modifica wikitesto]
Senza trattamento la prognosi sarà infausta praticamente per ogni paziente, in quanto andrà in corso al decesso o per l'insufficienza renale o per l'emorragie polmonari.[3] Con il trattamento, il tasso di sopravvivenza a 5 anni risulta maggiore dell'80% e meno del 30% degli individui affetti necessitano di emodialisi a lungo termine.[3] Allo stesso modo, il tempo medio di sopravvivenza è di circa 5,93 anni, come appare in uno studio effettuato sulle popolazioni dell'Australia e della Nuova Zelanda.[3]
Note[modifica | modifica wikitesto]
- ^ Goodpasture EW, The significance of certain pulmonary lesions in relation to the etiology of influenza, in Am J Med Sci, vol. 158, n. 6, 1919, pp. 863–870, DOI:10.1097/00000441-191911000-00012.
- ^ Salama AD, Levy JB, Lightstone L, Pusey CD, Goodpasture's disease, in Lancet, vol. 358, n. 9285, settembre 2001, pp. 917–920, DOI:10.1016/S0140-6736(01)06077-9, PMID 11567730.
- ^ a b c d e f Kathuria, P; Sanghera, P; Stevenson, FT; Sharma, S; Lederer, E; Lohr, JW; Talavera, F; Verrelli, M, Goodpasture Syndrome, su Batuman, C (a cura di), Medscape Reference, WebMD, 21 maggio 2013. URL consultato il 14 marzo 2014.
- ^ a b c Kathuria, P; Sanghera, P; Stevenson, FT; Sharma, S; Lederer, E; Lohr, JW; Talavera, F; Verrelli, M, Goodpasture Syndrome Clinical Presentation, su Batuman, C (a cura di), Medscape Reference, WebMD, 21 maggio 2013. URL consultato il 14 marzo 2014.
- ^ Schwarz, MI, Goodpasture Syndrome: Diffuse Alveolar Hemorrhage and Pulmonary-Renal Syndrome, su Merck Manual Professional, novembre 2013. URL consultato il 14 marzo 2014.
- ^ a b c d Kathuria, P; Sanghera, P; Stevenson, FT; Sharma, S; Lederer, E; Lohr, JW; Talavera, F; Verrelli, M, Goodpasture Syndrome Treatment & Management, su Batuman, C (a cura di), Medscape Reference, WebMD, 21 maggio 2013. URL consultato il 14 marzo 2014.
Bibliografia[modifica | modifica wikitesto]
- Robbins: Basic Pathology ISBN 1-4160-2973-7
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file sulla sindrome di Goodpasture
Wikimedia Commons contiene immagini o altri file sulla sindrome di Goodpasture
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) Goodpasture syndrome, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.