Broncopneumopatia cronica ostruttiva: differenze tra le versioni
m Bot: Collegamento alla voce di qualità en:Chronic obstructive pulmonary disease; modifiche estetiche |
→Eziologia: amplio con testo fontato tradotto da en.wiki |
||
| Riga 41: | Riga 41: | ||
== Eziologia == |
== Eziologia == |
||
=== Fattori di rischio === |
|||
L'origine della malattia è un'infiammazione di carattere cronico che perdura da anni e interessa le vie respiratorie nell'individuo. Essa comporta una graduale perdita delle funzioni dei polmoni con una disfunzione non completamente reversibile anche se trattata,<ref name="American">{{cita pubblicazione | quotes =no | autore =American Thoracic Society and European Respiratory Society. | autorelink = | anno = 2004| mese = | titolo = Standards for the diagnosis and treatment. | rivista =COPD Guidelines | volume = | pagine =| doi = |}}</ref> |
L'origine della malattia è un'infiammazione di carattere cronico che perdura da anni e interessa le vie respiratorie nell'individuo. Essa comporta una graduale perdita delle funzioni dei polmoni con una disfunzione non completamente reversibile anche se trattata,<ref name="American">{{cita pubblicazione | quotes =no | autore =American Thoracic Society and European Respiratory Society. | autorelink = | anno = 2004| mese = | titolo = Standards for the diagnosis and treatment. | rivista =COPD Guidelines | volume = | pagine =| doi = |}}</ref> |
||
La causa principale della BPCO è il [[tabagismo|fumo di tabacco]], mentre l'esposizione professionale e l'inquinamento da incendi possono essere cause significative per alcuni paesi.<ref name=GOLD2013Chp1/> In genere, queste esposizioni devono avvenire diversi decenni prima che i sintomi si sviluppino.<ref name=GOLD2013Chp1/> Il corredo [[genetica|genetico]] di una persona può influire sul rischio.<ref name=GOLD2013Chp1/> |
|||
* Il fumo di sigaretta è il maggiore fattore di rischio e di mortalità per lo sviluppo dell'[[enfisema]] e della [[bronchite cronica]], che sono comprese nella definizione di broncopneumopatia cronica ostruttiva. L'intensità del fumo di sigaretta, espresso in pacchetti all'anno (''pack years''), correla con un abbassamento del [[FEV1|FEV<sub>1</sub>]] (''Forced Expiratory Volume in the 1st second'') cioè il volume di aria espirata nel primo secondo durante un'espirazione massima forzata, indicatore del grado di pervietà delle vie aeree. Malgrado ciò, solo il 15% della variabilità del FEV<sub>1</sub> è spiegata dal fumo di sigaretta. Il sesso maschile, in cui la percentuale di fumatori è maggiore, è più colpito da questa patologia, ma dal momento che il sesso femminile fa registrare una crescita netta del numero di fumatori, stanno aumentando i casi anche tra le donne.<ref name="Sundblad">{{cita pubblicazione | quotes =no | autore =Sundblad BM, Larsson K, Nathell L. | autorelink = | anno = 2008| mese=maggio| titolo =IHigh rate of smoking abstinence in COPD patients: Smoking cessation by hospitalization| rivista =Nicotine Tob Res.| volume = 10| pagine =883-890.| doi = |}}</ref>. Si sospetta un contributo anche da parte del fumo passivo. |
|||
{{senza fonte| |
|||
===Fumo=== |
|||
* L'iperattività bronchiale (broncocostrizione) in risposta a diversi stimoli esterni, per esempio istamina, è un fattore di rischio per la BPCO oltre che per l'asma. |
|||
* L'esposizione occupazionale a sostanze contenenti cadmio, polveri di carbone, silicio e oro favoriscono l'ostruzione bronchiale cronica e una riduzione di FEV1 e si sospettano essere un fattore di rischio per questa patologia, anche se nel complesso pesano certamente meno del fumo di sigaretta. |
|||
{{doppia immagine verticale|right|Female Smoking by Country.png|Male Smoking by Country.png|250|Percentuale di donne fumatrici di tabacco tra la fine del XX secolo e l'inizio del XX.|Percentuale di uomini fumatori di tabacco tra la fine del XX secolo e l'inizio del XX. Notare che la scala utilizzata tra donne e uomini è differente.<ref name="isbn92-4-159628-7">{{cite book | author = World Health Organization | title = WHO Report on the Global Tobacco Epidemic 2008: The MPOWER Package | edition = | language = | publisher = World Health Organization | location = Geneva | year = 2008 | isbn = 92-4-159628-7 | url = http://www.who.int/tobacco/mpower/mpower_report_full_2008.pdf |pages=268–309}}</ref>}} |
|||
* Le infezioni respiratorie sono potenziali fattori di rischio per la BPCO, ma il loro contributo non è stato confermato. Di certo, sono un rischio per la sua riacutizzazione. L'inquinamento ambientale delle aree urbane è un potenziale fattore di rischio in quanto coloro che abitano in aree fortemente urbanizzate hanno una maggiore predisposizione allo sviluppo di BPCO rispetto a coloro che abitano in aree rurali a causa, si pensa, dell'inquinamento dell'aria e all'esposizione a una varietà di fumi. La correlazione tra BPCO e inquinamento atmosferico non è però confermata. |
|||
* Il deficit di α1-antitripsina (una glicoproteina che inibisce un ampio numero di proteasi. A livello polmonare inibisce la elastasi neutrofila, una proteasi che causa danni agli alveoli polmonari. Una insufficienza di alfa-1-antitripsina funzionante fa sì che si abbia una mancanza del suo ruolo difensivo e predispone allo sviluppo di enfisema polmonare) è un fattore di rischio genetico per la BPCO. |
|||
Il principale [[fattore di rischio]] a livello mondiale per la BPCO, è il fumo di tabacco.<ref name=GOLD2013Chp1/> Circa il 20% di coloro che fumano svilupperà questa condizione,<ref name=Ward2012>{{cite book|last=Ward|first=Helen|title=Oxford Handbook of Epidemiology for Clinicians|year=2012|publisher=Oxford University Press|isbn=978-0-19-165478-7|pages=289–290|url=http://books.google.ca/books?id=dHLjLwru-l8C&pg=RA1-PT194#v=onepage&q&f=false}}</ref> mentre tra coloro che hanno fumato permanentemente circa la meta soffrirà di BPCO.<ref name=La2009>{{cite journal|last=Laniado-Laborín|first=R|title=Smoking and chronic obstructive pulmonary disease (COPD). Parallel epidemics of the 21st century|journal=International journal of environmental research and public health|date=January 2009|volume=6|issue=1|pages=209–24|pmid=19440278|doi=10.3390/ijerph6010209|pmc=2672326}}</ref> Negli Stati Uniti e nel Regno Regno, tra coloro che convivono con tale condizioni, tra l'80% e il 95% sono fumatori lo sono stati.<ref name=Ward2012/><ref name=Ren2013>{{cite book|last=Rennard|first=Stephen|title=Clinical management of chronic obstructive pulmonary disease|year=2013|publisher=Informa Healthcare|location=New York|isbn=978-0-8493-7588-0|page=23|url=http://books.google.ca/books?id=DiTThQJkc0UC&pg=PA23|edition=2nd}}</ref><ref name=Rich2010>{{cite book|author=Anita Sharma ; with a contribution by David Pitchforth ; forewords by Gail Richards|title=COPD in primary care|year=2010|publisher=Radcliffe Pub.|location=Oxford|isbn=978-1-84619-316-3|page=9|url=http://books.google.com/books?id=CrXFqhezbeMC&pg=PA9|coauthors=Barclay, Joyce}}</ref> La probabilità di sviluppare la BPCO aumenta con il numero di sigarette fumate.<ref>{{cite book|last=Goldman|first=Lee|title=Goldman's Cecil medicine|publisher=Elsevier/Saunders|location=Philadelphia|isbn=978-1-4377-1604-7|page=537|url=http://books.google.ca/books?id=Qd-vvNh0ee0C&pg=PA537|edition=24th|year=2012}}</ref> Inoltre, le donne risultano essere più suscettibili agli effetti nocivi del fumo rispetto agli uomini.<ref name=Rich2010/> Nei non fumatori, il fumo passivo è causa di circa il 20% dei casi.<ref>{{cite book|last=Goldman|first=Lee|title=Goldman's Cecil medicine|publisher=Elsevier/Saunders|location=Philadelphia|isbn=978-1-4377-1604-7|page=537|url=http://books.google.ca/books?id=Qd-vvNh0ee0C&pg=PA537|edition=24th|year=2012}}</ref> Anche fumare la [[marijuana]], il [[sigaro]] e la [[pipa]] può aumentare il rischio.<ref name=GOLD2013Chp1/> Le donne che fumano durante la [[gravidanza]] possono causare un aumento del rischio di BPCO nel loro bambino.<ref name=GOLD2013Chp1/> |
|||
Inoltre è da diverso tempo sospettata una predisposizione genetica alla malattia, questo spiegherebbe l'insorgere in date persone a differenza delle altre con pari fattori di rischio, infatti, in queste, si registra una carenza di α1-antitripsina}} |
|||
===Inquinamento atmosferico=== |
|||
Fuochi di cottura in luoghi scarsamente ventilati, spesso alimentati a carbone o a [[biomassa|biomasse]] come legno e sterco animale, portano all'inquinamento dell'aria e sono una delle cause più comuni della BPCO nei [[paesi in via di sviluppo]].<ref name=Ken2007>{{cite journal |author=Kennedy SM, Chambers R, Du W, Dimich-Ward H|title=Environmental and occupational exposures: do they affect chronic obstructive pulmonary disease differently in women and men?|journal=Proceedings of the American Thoracic Society|volume=4 |issue=8 |pages=692–4 |year=2007 |month=December|pmid=18073405 |url=http://pats.atsjournals.org/cgi/content/full/4/8/692 |doi=10.1513/pats.200707-094SD}}</ref> Questi fuochi sono il metodo di cottura e riscaldamento utilizzato da quasi 3 miliardi di persone e i loro effetti negativi sulla salute si ripercuotono maggiormente tra le donne a causa di una maggiore esposizione.<ref name=GOLD2013Chp1/><ref name=Ken2007/> Essi sono utilizzati come principale fonte di energia nel 80% delle case in [[India]], in [[Cina]] e in [[Africa sub-sahariana]].<ref name=Piro2012/> |
|||
Le persone che vivono nelle grandi città presentano un più alto tasso di BPCO rispetto alle persone che vivono nelle zone rurali.<ref>{{cite journal|author=Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM |title=Global burden of COPD: systematic review and meta-analysis |journal=Eur. Respir. J. |volume=28 |issue=3 |pages=523–32 |year=2006 |month=September|pmid=16611654|doi=10.1183/09031936.06.00124605 }}</ref> Mentre l'[[inquinamento atmosferico]] urbano è un fattore che contribuisce alle riacutizzazioni, il suo ruolo globale come causa della BPCO non è chiaro.<ref name=GOLD2013Chp1/> Zone con cattiva qualità dell'aria in genere presentano tassi più alti di BPCO tra i propri residenti.<ref name=Piro2012/> L'effetto complessivo, in comparazione con il fumo, si ritiene che sia inferiore.<ref name=GOLD2013Chp1/> |
|||
===Esposizioni professionali=== |
|||
L'esposizione intensa e prolungata alle polveri, agli agenti chimici e ai fumi, aumenta il rischio di BPCO sia nei fumatori che nei non.<ref name=Dev2006/> Le esposizioni sul posto di lavoro sono ritenute essere la causa del 10-20% dei casi.<ref>{{cite book|last=Laine|first=Christine|title=In the Clinic: Practical Information about Common Health Problems|year=2009|publisher=ACP Press|isbn=978-1-934465-64-6|page=226|url=http://books.google.ca/books?id=bvg9he4FOB0C&pg=PA226}}</ref> Negli Stati Uniti si ritiene che queste cause possoano essere correlate a più del 30% dei casi tra coloro che non hanno mai fumato e, probabilmente, rappresentano un rischio maggiore nei paesi sprovvisti di sufficienti regole in materia.<ref name=GOLD2013Chp1/> |
|||
Un certo numero di industrie e attività sono responsabili, tra cui gli elevati livelli di polvere delle [[miniere di carbone]], le miniere d'oro e l'[[industria tessile]] del cotone, le attività che comportano l'esposizione a [[cadmio]] e [[isocianati]] e ai fumi di [[saldatura]].<ref name=Dev2006>{{cite journal |doi=10.1136/bmj.332.7550.1142 |title=Definition, epidemiology and risk factors |year=2006 |last1=Devereux |first1=Graham |journal=BMJ |volume=332 |issue=7550 |pages=1142–4 |pmid=16690673 |pmc=1459603}}</ref> Anche l'attività agricola comporta dei rischi.<ref name=Piro2012/> Per alcune professioni i rischi sono stati stimati equivalenti a quelli di fumare da mezzo a due pacchetti di sigarette al giorno.<ref name=Barn2009/> L'esposizione alla polvere di [[silicio]] può anche portare alla BPCO, con il rischio correlato a quello per la [[silicosi]].<ref>{{cite journal |doi=10.1515/REVEH.2007.22.4.255 |title=Chronic Obstructive Pulmonary Disease and Occupational Exposure to Silica |year=2007 |last1=Rushton |first1=Lesley |journal=Reviews on Environmental Health |volume=22 |issue=4 |pmid=18351226 |pages=255–72}}</ref> Gli effetti negativi dell'esposizione polvere e dell'esposizione al fumo di sigaretta sembrano essere additivi o forse più che additivi.<ref name=Barn2009>{{cite book |editor1-first=Peter J. |editor1-last=Barnes |editor2-first=Jeffrey M. |editor2-last=Drazen |editor3-first=Stephen I. |editor3-last=Rennard |editor4-first=Neil C. |editor4-last=Thomson |year=2009 |chapter=Relationship between cigarette smoking and occupational exposures |chapterurl=http://books.google.ca/books?id=HY9PiQL3kQMC&pg=PA464 |title=Asthma and COPD: Basic Mechanisms and Clinical Management |publisher=Academic |location=Amsterdam |isbn=978-0-12-374001-4 |page=464}}</ref> |
|||
===Genetica=== |
|||
La [[genetica]] gioca un ruolo importante nello sviluppo della BPCO.<ref name=GOLD2013Chp1/> Infatti la condizione risulta essere più comune tra i parenti delle persone con BPCO che fumano, rispetto ai fumatori senza familiarità.<ref name=GOLD2013Chp1/> Attualmente, l'unico fattore di rischio ereditario conosciuto è legato al [[deficit da alfa 1-antitripsina]] (AAT).<ref name=Foreman2012>{{cite journal | author = Foreman MG, Campos M, Celedón JC | title = Genes and chronic obstructive pulmonary disease | journal = Med. Clin. North Am. | volume = 96 | issue = 4 | pages = 699–711 | year = 2012 | month = July | pmid = 22793939 | pmc = 3399759 | doi = 10.1016/j.mcna.2012.02.006 }}</ref> Questo rischio è particolarmente elevato è associato anche al tabagismo.<ref name=Foreman2012/> Il deficit è responsabile di circa tra l'1% e il 5% dei casi<ref name=Foreman2012/><ref name=Foreman2012/><ref name=Brode2012>{{cite journal | author = Brode SK, Ling SC, Chapman KR | title = Alpha-1 antitrypsin deficiency: a commonly overlooked cause of lung disease | journal = CMAJ | volume = 184 | issue = 12 | pages = 1365–71 | year = 2012 | month = September | pmid = 22761482 | pmc = 3447047 | doi = 10.1503/cmaj.111749 }}</ref> e la condizione è presente in circa 3-4 individui su 10.000.<ref name=Harr2012/> Altri fattori genetici sono oggetto di indagine<ref name=Foreman2012/>, e si ritiene che molti di essi possano essere correlabili alla malattia.<ref name=Piro2012>{{cite journal | author = Pirozzi C, Scholand MB | title = Smoking cessation and environmental hygiene | journal = Med. Clin. North Am. | volume = 96 | issue = 4 | pages = 849–67 | year = 2012 | month = July | pmid = 22793948 | doi = 10.1016/j.mcna.2012.04.014 }}</ref> |
|||
===Altro=== |
|||
=== Associazione con altre malattie === |
|||
Un certo numero di altri fattori sono meno strettamente legati alla BPCO. Un rischio maggiore appare in coloro che versano in una situazione di povertà, anche se non è chiaro se ciò sia dovuto alla povertà stessa o ad altri fattori di rischio associati alla insufficiente condizione economica, come l'inquinamento dell'aria e la [[malnutrizione]].<ref name=GOLD2013Chp1/> Non vi è evidenza sperimentale che gli individui affetti da [[asma]] e [[iperreattività bronchiale]] siano più a rischio di BPCO.<ref name=GOLD2013Chp1/> Fattori correlati alla nascita, come un basso peso, possono anche svolgere un ruolo, come alcune [[malattia infettiva|malattie infettive]] come l'[[HIV]]/[[AIDS]] e la [[tubercolosi]].<ref name=GOLD2013Chp1/> Infezioni respiratorie come la [[polmonite]] non sembrano aumentare il rischio di BPCO, almeno negli adulti.<ref name=Harr2012/> |
|||
L'entità [[nosologia|nosologica]] BPCO è definita come un insieme variabile di [[enfisema polmonare]] e [[bronchite cronica]] |
|||
===Riacutizzazioni=== |
|||
* [[Enfisema polmonare]], distensione permanente delle porzioni [[distale|distali]] al [[bronchiolo]] terminale in seguito alla distruzione delle pareti in assenza di [[fibrosi]] |
|||
* [[Bronchite cronica]], presenza di [[tosse cronica]] produttiva non attribuibile ad altre cause per almeno tre mesi consecutivi per almeno due anni successivi. |
|||
Una riacutizzazione (un improvviso peggioramento dei sintomi)<ref name=GOLD2013Chp5>{{cite book |last=Vestbo |first=Jørgen |title=Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease|year=2013|publisher=Global Initiative for Chronic Obstructive Lung Disease |chapter=Management of Exacerbations |pages=39–45 |chapterurl=http://www.goldcopd.org/uploads/users/files/GOLD_Report_2013_Feb20.pdf#56}}</ref> si verifica comunemente in seguito ad infezioni, all'esposizione a inquinanti ambientali o per mezzo di altri fattori quali l'uso improprio di [[farmaco|farmaci]].<ref name=Dhar2012>{{cite book|last=Dhar|first=Raja|title=Textbook of pulmonary and critical care medicine|year=2011|publisher=Jaypee Brothers Medical Publishers|location=New Delhi|isbn=978-93-5025-073-0|page=1056|url=http://books.google.ca/books?id=rAT1bdnDakAC&pg=PA1056}}</ref> Le infezioni sembrano essere la causa del 50%-75% dei casi<ref name=Dhar2012/><ref>{{cite book|last=Palange|first=Paolo|title=ERS Handbook of Respiratory Medicine|year=2013|publisher=European Respiratory Society|isbn=978-1-84984-041-5|page=194|url=http://books.google.ca/books?id=48gaALnXhcQC&pg=PA194}}</ref>, con i [[batteri]] responsabili nel 25% delle riacutizzazioni, i [[virus (biologia)|virus]] nel 25% ed entrambi sempre nel 25%.<ref>{{cite book|last=Lötvall|first=Jan|title=Advances in combination therapy for asthma and COPD|year=2011|publisher=John Wiley & Sons|location=Chichester, West Sussex|isbn=978-1-119-97846-6|page=251|url=http://books.google.ca/books?id=oPDU4xQLVWEC&pg=PT265}}</ref> |
|||
La BPCO spesso si associa a [[scompenso cardiaco]] (definito in questo caso cuore polmonare cronico) e naturalmente ad altre patologie tipiche dell'età avanzata (es. [[ipertensione]], [[diabete]], ecc.) |
|||
Gli inquinanti ambientali comprendono sia una scarsa qualità dell'aria sia esterna che interna.<ref name=Dhar2012/> L'esposizione al fumo, sia attivo che passivo, aumenta il rischio.<ref name=Piro2012/> Anche le temperature più fredde possono svolgere un ruolo, con le riacutizzazioni che si verificano più comunemente in inverno.<ref name=Barnes2009>{{cite book|last=Barnes|first=Peter|title=Asthma and COPD : basic mechanisms and clinical management|year=2009|publisher=Academic|location=Amsterdam|isbn=978-0-12-374001-4|page=837|url=http://books.google.ca/books?id=HY9PiQL3kQMC&pg=PA837|edition=2nd}}</ref> Quelli che soffrono di una condizione di base più grave hanno riacutizzazioni più frequenti. Nei casi lievi, si stimano 1,8 riacutizzazioni all'anno, da 2 a 3 nei casi moderati e 3,4 nelle situazioni più gravi.<ref>{{cite book|last=Hanania|first=Nicola|title=COPD a Guide to Diagnosis and Clinical Management|publisher=Springer Science+Business Media, LLC|location=Totowa, NJ|isbn=978-1-59745-357-8|page=197|url=http://books.google.ca/books?id=wMzWnIdRD1MC&pg=PA197|edition=1st|date=2010-12-09}}</ref> coloro che sperimentano molteplici riacutizzazioni, hanno un tasso più veloce di deterioramento della loro funzione polmonare.<ref name=Beasley2012>{{cite journal|last=Beasley|first=V|coauthors=Joshi, PV; Singanayagam, A; Molyneaux, PL; Johnston, SL; Mallia, P|title=Lung microbiology and exacerbations in COPD|journal=International journal of chronic obstructive pulmonary disease|year=2012|volume=7|pages=555–69|pmid=22969296|doi=10.2147/COPD.S28286|pmc=3437812}}</ref> L'[[embolia polmonare]] ([[Coagulo|coaguli]] di [[sangue]] nei polmoni) può peggiorare i sintomi nei pazienti con BPCO preesistente.<ref name=Harr2012/> |
|||
Il paziente affetto da BPCO può presentare infine una serie di problemi sistemici (es [[calo ponderale]], [[atrofia muscolare]], ecc.) che in parte sono da attribuirsi allo stato infiammatorio generalizzato del soggetto. |
|||
== Sintomatologia == |
== Sintomatologia == |
||
Versione delle 23:52, 26 gen 2014
| Broncopneumopatia cronica ostruttiva | |
|---|---|
 | |
| Specialità | pneumologia |
| Eziologia | fumare e polvere |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 490 - 492, 494 - 496 |
| ICD-10 | -/J40 J40 - -/J44 J44 , -/J47 J47 |
| OMIM | 606963 |
| MeSH | D029424 |
| MedlinePlus | 000091 |
| eMedicine | 807143 e 297664 |
| Sinonimi | |
| BPCO COPD COLD Pneumopatia cronica ostruttiva. | |
La broncopneumopatia cronica ostruttiva è un'affezione cronica polmonare caratterizzata da una ostruzione bronchiale, con limitazione del flusso aereo per niente o solo parzialmente reversibile, lentamente progressiva, causata da un'infiammazione cronica delle vie aeree e del parenchima polmonare. Considerata la quarta causa di morte in Europa e negli USA (almeno 65.000 morti all'anno,[1]) studi recenti hanno evidenziato un aumento della mortalità a livello mondiale[2][3].
Storia
Il termine è stato introdotto negli anni sessanta.
Epidemiologia

nessun dato
meno di 110
110-220
220-330
330-440
440-550
550-660
660-770
770-880
880-990
990-1100
1100-1350
più di 1350
L'incidenza totale risulta del 6-8%[5], colpisce principalmente maschi adulti, ma si è notato negli ultimi anni un aumento considerevole anche nelle donne. Essendo il fumo di sigaretta il principale fattore di rischio, si è calcolato che il 15-20% dei fumatori abituali contragga tale malattia, tuttavia alcuni di essi non mostrano mai i sintomi della malattia.[6] Inoltre vi è correlazione anche per quanto riguarda l'inquinamento atmosferico, questo a causa dei gas di scarico ambientali, in particolare il PM10 chiamato anche particolato fine, ma si presuppone che sia soltanto una forma di causa aggiuntiva.
Il numero di fumatrici fino al 1960 era considerato bassissimo, ma tale rapporto cambiò rapidamente negli anni successivi, fino alla fine del 1990 quando si stimò che più di una donna su cinque fumava regolarmente.[7] La malattia alla fine del secolo scorso ebbe una crescita esponenziale, la sua presenza nella sola Inghilterra, in sette anni, è aumentata del 25% negli uomini e del 69% nelle donne.[8]
In realtà vi sono prove che i dati sarebbero più alti di quelli indicati, questo perché durante varie autopsie si sono trovati segni di enfisema.
Eziologia
L'origine della malattia è un'infiammazione di carattere cronico che perdura da anni e interessa le vie respiratorie nell'individuo. Essa comporta una graduale perdita delle funzioni dei polmoni con una disfunzione non completamente reversibile anche se trattata,[9]
La causa principale della BPCO è il fumo di tabacco, mentre l'esposizione professionale e l'inquinamento da incendi possono essere cause significative per alcuni paesi.[10] In genere, queste esposizioni devono avvenire diversi decenni prima che i sintomi si sviluppino.[10] Il corredo genetico di una persona può influire sul rischio.[10]
Fumo
Il principale fattore di rischio a livello mondiale per la BPCO, è il fumo di tabacco.[10] Circa il 20% di coloro che fumano svilupperà questa condizione,[12] mentre tra coloro che hanno fumato permanentemente circa la meta soffrirà di BPCO.[13] Negli Stati Uniti e nel Regno Regno, tra coloro che convivono con tale condizioni, tra l'80% e il 95% sono fumatori lo sono stati.[12][14][15] La probabilità di sviluppare la BPCO aumenta con il numero di sigarette fumate.[16] Inoltre, le donne risultano essere più suscettibili agli effetti nocivi del fumo rispetto agli uomini.[15] Nei non fumatori, il fumo passivo è causa di circa il 20% dei casi.[17] Anche fumare la marijuana, il sigaro e la pipa può aumentare il rischio.[10] Le donne che fumano durante la gravidanza possono causare un aumento del rischio di BPCO nel loro bambino.[10]
Inquinamento atmosferico
Fuochi di cottura in luoghi scarsamente ventilati, spesso alimentati a carbone o a biomasse come legno e sterco animale, portano all'inquinamento dell'aria e sono una delle cause più comuni della BPCO nei paesi in via di sviluppo.[18] Questi fuochi sono il metodo di cottura e riscaldamento utilizzato da quasi 3 miliardi di persone e i loro effetti negativi sulla salute si ripercuotono maggiormente tra le donne a causa di una maggiore esposizione.[10][18] Essi sono utilizzati come principale fonte di energia nel 80% delle case in India, in Cina e in Africa sub-sahariana.[19]
Le persone che vivono nelle grandi città presentano un più alto tasso di BPCO rispetto alle persone che vivono nelle zone rurali.[20] Mentre l'inquinamento atmosferico urbano è un fattore che contribuisce alle riacutizzazioni, il suo ruolo globale come causa della BPCO non è chiaro.[10] Zone con cattiva qualità dell'aria in genere presentano tassi più alti di BPCO tra i propri residenti.[19] L'effetto complessivo, in comparazione con il fumo, si ritiene che sia inferiore.[10]
Esposizioni professionali
L'esposizione intensa e prolungata alle polveri, agli agenti chimici e ai fumi, aumenta il rischio di BPCO sia nei fumatori che nei non.[21] Le esposizioni sul posto di lavoro sono ritenute essere la causa del 10-20% dei casi.[22] Negli Stati Uniti si ritiene che queste cause possoano essere correlate a più del 30% dei casi tra coloro che non hanno mai fumato e, probabilmente, rappresentano un rischio maggiore nei paesi sprovvisti di sufficienti regole in materia.[10]
Un certo numero di industrie e attività sono responsabili, tra cui gli elevati livelli di polvere delle miniere di carbone, le miniere d'oro e l'industria tessile del cotone, le attività che comportano l'esposizione a cadmio e isocianati e ai fumi di saldatura.[21] Anche l'attività agricola comporta dei rischi.[19] Per alcune professioni i rischi sono stati stimati equivalenti a quelli di fumare da mezzo a due pacchetti di sigarette al giorno.[23] L'esposizione alla polvere di silicio può anche portare alla BPCO, con il rischio correlato a quello per la silicosi.[24] Gli effetti negativi dell'esposizione polvere e dell'esposizione al fumo di sigaretta sembrano essere additivi o forse più che additivi.[23]
Genetica
La genetica gioca un ruolo importante nello sviluppo della BPCO.[10] Infatti la condizione risulta essere più comune tra i parenti delle persone con BPCO che fumano, rispetto ai fumatori senza familiarità.[10] Attualmente, l'unico fattore di rischio ereditario conosciuto è legato al deficit da alfa 1-antitripsina (AAT).[25] Questo rischio è particolarmente elevato è associato anche al tabagismo.[25] Il deficit è responsabile di circa tra l'1% e il 5% dei casi[25][25][26] e la condizione è presente in circa 3-4 individui su 10.000.[27] Altri fattori genetici sono oggetto di indagine[25], e si ritiene che molti di essi possano essere correlabili alla malattia.[19]
Altro
Un certo numero di altri fattori sono meno strettamente legati alla BPCO. Un rischio maggiore appare in coloro che versano in una situazione di povertà, anche se non è chiaro se ciò sia dovuto alla povertà stessa o ad altri fattori di rischio associati alla insufficiente condizione economica, come l'inquinamento dell'aria e la malnutrizione.[10] Non vi è evidenza sperimentale che gli individui affetti da asma e iperreattività bronchiale siano più a rischio di BPCO.[10] Fattori correlati alla nascita, come un basso peso, possono anche svolgere un ruolo, come alcune malattie infettive come l'HIV/AIDS e la tubercolosi.[10] Infezioni respiratorie come la polmonite non sembrano aumentare il rischio di BPCO, almeno negli adulti.[27]
Riacutizzazioni
Una riacutizzazione (un improvviso peggioramento dei sintomi)[28] si verifica comunemente in seguito ad infezioni, all'esposizione a inquinanti ambientali o per mezzo di altri fattori quali l'uso improprio di farmaci.[29] Le infezioni sembrano essere la causa del 50%-75% dei casi[29][30], con i batteri responsabili nel 25% delle riacutizzazioni, i virus nel 25% ed entrambi sempre nel 25%.[31]
Gli inquinanti ambientali comprendono sia una scarsa qualità dell'aria sia esterna che interna.[29] L'esposizione al fumo, sia attivo che passivo, aumenta il rischio.[19] Anche le temperature più fredde possono svolgere un ruolo, con le riacutizzazioni che si verificano più comunemente in inverno.[32] Quelli che soffrono di una condizione di base più grave hanno riacutizzazioni più frequenti. Nei casi lievi, si stimano 1,8 riacutizzazioni all'anno, da 2 a 3 nei casi moderati e 3,4 nelle situazioni più gravi.[33] coloro che sperimentano molteplici riacutizzazioni, hanno un tasso più veloce di deterioramento della loro funzione polmonare.[34] L'embolia polmonare (coaguli di sangue nei polmoni) può peggiorare i sintomi nei pazienti con BPCO preesistente.[27]
Sintomatologia
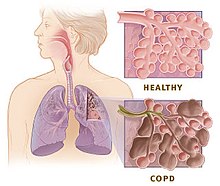
I sintomi compaiono dopo anni di consumo abituale di sigarette: studi sui fumatori hanno riscontrato che nelle persone che hanno fumato almeno 20 sigarette al giorno per 20 anni si manifesta una forma di tosse spesso produttiva a carattere compulsivo intorno alla quarta decade di vita.[35] Altri sintomi, oltre alla tosse, sono:
- Dispnea progressiva causata dall'alterazione della capacità dell'apparato respiratorio;
- Ipercapnia;[36]
- Ipossiemia
- Cianosi
- Poliglobulia
- Torace a botte
- Perdita di peso
- Nei casi molto gravi sono presenti il segno di Hoover e il respiro paradosso
Esistono due tipologie di malato di BPCO, indicati con una terminologia anglosassone:
- Pink puffer - magri, scavati, espirazione prolungata a labbra socchiuse (auto-peep), assumono spesso la posizione del cocchiere (seduto con appoggio di gomiti o mani) per migliorare la respirazione accessoria e diaframmatica. Poco catarro, leggera ipossia, enfisema e dispnea molto severa.
- Blue bloater - Cianosi a riposo o da minimi sforzi, edemi agli arti inferiori e rantoli e ronchi alle basi polmonari. In un quadro maggiormente evolutivo che porta a insufficienza respiratoria cronica e scompenso cardiaco destro.
La maggior parte dei pazienti tuttavia presenta un quadro intermedio molto variabile con prevalenza di taluni aspetti su altri.
Diagnosi
La diagnosi deve tener conto dei fattori di rischio ed essere accompagnata da un esame spirometrico (in condizione di stabilità clinica) che registri una riduzione del flusso aereo. I valori di FEV1 risulteranno inferiori all'80% dei valori ottimali di riferimento. La misurazione viene ripetuta a distanza di 40 minuti dopo la somministrazione di 400 µg di β2 agonista, un broncodilatatore.
- Se non migliorano i risultati, ma solo la sintomatologia, è possibile la diagnosi di BPCO: indice di Tiffeneau (FEV1/FVC) ridotto.
- L'incremento del FEV1 sia di 200 ml che del 12% rispetto al valore pre-broncodilatatore è considerato un indice prognostico favorevole.
- Se il valore di FEV1 torna nella norma si esclude diagnosi di BPCO, è verosimile una diagnosi di asma.
Altri esami utili alla diagnosi e all'indice prognostico di mortalità sono:
- Saturazione emoglobinica arteriosa - se inferiore al 94% è utile eseguire:
- Emogasanalisi
- Test 6 Minutes Walking
- Calcolo dell'indice di massa corporea (BMI)
- Calcolo del grado di dispnea
Stadiazione
Una volta diagnosticata la malattia è necessario studiarla per sapere quali provvedimenti terapeutici eseguire:
| Stadio | severità | VEMS/CVF | VEMS |
|---|---|---|---|
| I | lieve | <0,7 | > 80% del valore atteso |
| II | moderata | <0,7 | tra il 50% e l'80% dell'atteso |
| III | grave | <0,7 | tra il 30% e l'50% dell'atteso |
| IV | molto grave | <0,7 | minore del 30% dell'atteso o del 50% se presente insufficienza respiratoria o cuore polmonare cronico |
Diagnosi differenziale
Diverse sono le malattie che hanno un'insorgenza simile per cui devono essere differenziate tramite esami specifici, per una corretta diagnosi:[37]
- Scompenso cardiaco
- Embolia polmonare
- Pneumotorace
- Polmonite, la versione più leggera della Broncopneumopatia
Risulta utile allo scopo una radiografia toracica.
Riacutizzazioni
Le riacutizzazioni si hanno quando il paziente presenta un rapido peggioramento dei sintomi da ostruzione respiratoria. Le cause più comuni sono dovute all'inquinamento atmosferico oppure a infezioni. Nel 75% sono attribuibili a batteri come l'hemophilus influenzae (40%), lo pneumococco(10%), la moraxella catarrhalis(15%) e altri batteri come S. Auerus, P. Aeruginosa, Gram -,M. Pneumoniae e Chlamidia (10% in totale). Il 25% sono causate da virus (virus influenzale, parainfluenzale,RSV, Rhinovirus, Coronavirus)Dato che queste 2 cause sono più presenti nei mesi invernali anche le riacutizzazioni hanno un picco di incidenza in questo periodo e sono più gravi e frequenti in chi è già colonizzato da batteri o ha un livello di ostruzione severo. La mortalità supera il 10% e spesso è necessaria l'ospedalizzazione.
Terapia
Il primo intervento è agire sui fattori di rischio: ridurre l'esposizione ad inquinanti domestici e/o esterni, smettere di fumare, che porta (in una percentuale variabile nei casi e negli studi) ad un arresto nella sua progressione a distanza di 1-3 anni.[38]
I provvedimenti più prettamente medici attualmente disponibili includono:
- beta 2 agonisti short acting al bisogno o long acting in terapia cronica
- corticosteroidi
- vaccini anti influenza e pneumococco
- teofillina
- immunomodulatori
- antiossidanti
- mucolitici
Altre terapie includono:
- Fisioterapia respiratoria
- Interventi chirurgici in casi altamente selezionati che comprendono:
- Riduzione del volume polmonare - riduce l'iperinflazione polmonare
- Bollectomia - rimozione di una bolla enfisematosa
- Trapianto polmonare
Tutte queste risorse vanno utilizzate a seconda dello stadio della malattia. In particolare:
| stadio | terapia più usata |
|---|---|
| I | riduzione dei fattori di rischio, vaccini, broncodilatatori short acting al bisogno |
| II | come stadio 1 + broncodilatori long acting in cronico e riabilitazione respiratoria |
| III | come stadio 2 + corticosteroidi inalatori (in caso di ripetute riacutizzazioni) |
| IV | aggiungere l'ossigeno in cronico se insufficienza respiratoria* |
(*l'insufficienza respiratoria si ha quando la PaO2 scende sotto i 55 mmHg oppure se è compresa fra 55 e 60 mmHg e il paziente ha almeno una delle caratteristiche sotto:)
- cuore polmonare
- poliglobulia
- pressione arteriosa polmonare >25 mmHg
- SatO2 media nel sonno <88%
Si è visto che l'ossigenoterapia migliora qualità di vita e sopravvivenza nei pazienti molto gravi e ne riduce complicanze e ospedalizzazione, la ventilazione meccanica non invasiva a pressione positiva invece è utile nei pazienti ipercapnici con BPCO stabile per migliorare la qualità di vita, ma non la sopravvivenza.
Terapia delle riacutizzazioni
Le esacerbazioni possono essere trattate sia a domicilio che in ospedale. I criteri che portano a optare per l'ospedalizzazione sono:
- aumento molto marcato dei sintomi
- esordio in pazienti già gravi
- comparsa di nuovi reperti obiettivi
- non responders o impossibilità a valutare
- importanti patologie concomitanti
- aritmie di nuova insorgenza
- età avanzata
- obnulamento del sensorio
- non autosufficienza o mancanza di supporto a domicilio
La terapia prevede di seguire una serie di provvedimenti ben precisa. Si inizia con la stimolazione di broncodilatatori (beta 2 short acting e anche anticolinergici e aminofillina). Se la VEMS va sotto il 50% del predetto aggiungere 30–40 mg di prednisone per via orale oppure butesonide inalatorio.
Inoltre se si sospetta un'eziologia batterica è opportuno impostare un'adeguata terapia antibiotica e in ogni caso prevenire il rischio trombotico (tramite la somministrazione di eparina a basso peso molecolare). Utile anche la riabilitazione.
In ospedale è opportuno eseguire un'emogasanalisi (da ripetere dopo 30 minuti) e somministrare ossigeno mantenendo la sua saturazione arteriosa fra il 90 e il 96% (non aumentarla troppo perché c'è il rischio che il paziente vada in carbonarcosi per blocco della respirazione a livello centrale causato dall'eccesso di ossigeno. Infatti in questi pazienti che hanno un accumulo cronico di CO2 i meccanismi di controllo della respirazione da parte di quest'ultima vengono meno)
Un approccio più aggressivo è inoltre richiesto nel caso il paziente sia in insufficienza respiratoria acuta: dispnea, tachipnea, respiro paradosso (l'addome si gonfia in espirazione. È un segno di affaticamento dei muscoli respiratori) associati a una SatO2 < 90% o a un rapporto PaO2/FiO2<300.
Di norma, la ventilazione meccanica non invasiva si usa quando osservo i segni elencati sotto anche dopo aver adottato i presidi terapeutici descritti sopra:
- segni di fatica respiratoria presenti
- frequenza respiratoria > 25 atti/min
- acidosi respiratoria (pH <7,36 e PaCO2>45 mmHg)
La modalità di NINV più usata è la C-PAP con pressione di supporto (PEEP) che ha come vantaggi:
- migliora ancora di più gli scambi gassosi
- riduce la mortalità, la durata della degenza e la necessità di intubare il paziente
- favorisce lo svezzamento dal ventilatore
- presenta rischio infettivo minore rispetto all'intubazione
- abbatte i costi sanitari (non è necessaria una terapia intensiva, basta una semintensiva)
Nel fare ciò è opportuno tenere il paziente inclinato di 30°, e monitorare sia i segni vitali sia L'EGA; impostando una PEEP partendo da 4-5 cmH20 fino a 8-12 se necessario. Le maschere più utilizzate all'inizio sono il "pallone" e la facciale; per lo svezzamento si usa di solito quella nasale. Perché la terapia vada a buon fine il paziente deve abituarsi a seguire i tempi del ventilatore. La NINV non si può fare se:
- paziente in arresto respiratorio
- instabilità emodinamica
- paziente in coma o non collaborante
- ostruzione delle vie aeree da secrezioni
- recente trauma o chirurgia facciale
- Multi organ Failure
- fallimento della tecnica
Unica eccezione è il paziente in coma leggero da ipercapnia (in questo caso la C-PAP può produrre miglioramenti già dopo mezzora). Lo svezzamento si fa riducendo di 2 cmH2O la PEEP e intervallando la NINV con periodi di respirazione spontanea; se la frequenza respiratoria scende sotto i 24 atti/min, la cardiaca sotto i 110 battiti/min, il pH è >7,36 e la SatO2 è >90% si può interrompere definitivamente la ventilazione.
Prognosi
A 10 anni dall'insorgenza della broncopneumopatia cronica ostruttiva la sopravvivenza è del 40%.[6]
Note
- ^ Joseph C. Segen, Concise Dictionary of Modern Medicine pag 98, New York, McGraw-Hill, 2006, ISBN 978-88-386-3917-3.
- ^ Celli BR., Update on the Management of COPD., in Chest., vol. 133, giugno 2008, pp. 1451-1462.
- ^ Halpin D., Mortality in COPD: inevitable or preventable? Insights from the cardiovascular arena., in COPD., vol. 5, giugno 2008, pp. 187-200.
- ^ WHO Disease and injury country estimates, in World Health Organization, 2009. URL consultato l'11 novembre 2009.
- ^ Manca il riferimento : sulla popolazione, sul numero dei malati cronici ... su cosa ?
- ^ a b Giovanni Bonsignore, Bellia Vincenzo, Malattie dell’apparato respiratorio terza edizione pag 241-242, Milano, McGraw-Hill, 2006, ISBN 978-88-386-2390-5.
- ^ Public Health Service. Office of the Surgeon General. Centers for Disease Control and Prevention, Women and Smoking A Report of the Surgeon General, in National Center for Chronic Disease Prevention and Health Promotion, 2001.
- ^ Soriano JB, Maier WC, Egger P,, Recent trends in physician diagnosed COPD in women and men in the UK., in Thorax, vol. 55, 2000, pp. 789–794..
- ^ American Thoracic Society and European Respiratory Society., Standards for the diagnosis and treatment., in COPD Guidelines, 2004.
- ^ a b c d e f g h i j k l m n o Errore nelle note: Errore nell'uso del marcatore
<ref>: non è stato indicato alcun testo per il marcatoreGOLD2013Chp1 - ^ World Health Organization, WHO Report on the Global Tobacco Epidemic 2008: The MPOWER Package (PDF), Geneva, World Health Organization, 2008, pp. 268–309, ISBN 92-4-159628-7.
- ^ a b Helen Ward, Oxford Handbook of Epidemiology for Clinicians, Oxford University Press, 2012, pp. 289–290, ISBN 978-0-19-165478-7.
- ^ R Laniado-Laborín, Smoking and chronic obstructive pulmonary disease (COPD). Parallel epidemics of the 21st century, in International journal of environmental research and public health, vol. 6, n. 1, January 2009, pp. 209–24, DOI:10.3390/ijerph6010209.
- ^ Stephen Rennard, Clinical management of chronic obstructive pulmonary disease, 2nd, New York, Informa Healthcare, 2013, p. 23, ISBN 978-0-8493-7588-0.
- ^ a b Anita Sharma ; with a contribution by David Pitchforth ; forewords by Gail Richards, Barclay, Joyce, COPD in primary care, Oxford, Radcliffe Pub., 2010, p. 9, ISBN 978-1-84619-316-3.
- ^ Lee Goldman, Goldman's Cecil medicine, 24th, Philadelphia, Elsevier/Saunders, 2012, p. 537, ISBN 978-1-4377-1604-7.
- ^ Lee Goldman, Goldman's Cecil medicine, 24th, Philadelphia, Elsevier/Saunders, 2012, p. 537, ISBN 978-1-4377-1604-7.
- ^ a b Kennedy SM, Chambers R, Du W, Dimich-Ward H, Environmental and occupational exposures: do they affect chronic obstructive pulmonary disease differently in women and men?, in Proceedings of the American Thoracic Society, vol. 4, n. 8, December 2007, pp. 692–4, DOI:10.1513/pats.200707-094SD.
- ^ a b c d e Pirozzi C, Scholand MB, Smoking cessation and environmental hygiene, in Med. Clin. North Am., vol. 96, n. 4, July 2012, pp. 849–67, DOI:10.1016/j.mcna.2012.04.014.
- ^ Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM, Global burden of COPD: systematic review and meta-analysis, in Eur. Respir. J., vol. 28, n. 3, September 2006, pp. 523–32, DOI:10.1183/09031936.06.00124605.
- ^ a b Definition, epidemiology and risk factors, in BMJ, vol. 332, n. 7550, 2006, pp. 1142–4, DOI:10.1136/bmj.332.7550.1142.
- ^ Christine Laine, In the Clinic: Practical Information about Common Health Problems, ACP Press, 2009, p. 226, ISBN 978-1-934465-64-6.
- ^ a b Relationship between cigarette smoking and occupational exposures, in Asthma and COPD: Basic Mechanisms and Clinical Management, Amsterdam, Academic, 2009, p. 464, ISBN 978-0-12-374001-4.
- ^ Chronic Obstructive Pulmonary Disease and Occupational Exposure to Silica, in Reviews on Environmental Health, vol. 22, n. 4, 2007, pp. 255–72, DOI:10.1515/REVEH.2007.22.4.255.
- ^ a b c d e Foreman MG, Campos M, Celedón JC, Genes and chronic obstructive pulmonary disease, in Med. Clin. North Am., vol. 96, n. 4, July 2012, pp. 699–711, DOI:10.1016/j.mcna.2012.02.006.
- ^ Brode SK, Ling SC, Chapman KR, Alpha-1 antitrypsin deficiency: a commonly overlooked cause of lung disease, in CMAJ, vol. 184, n. 12, September 2012, pp. 1365–71, DOI:10.1503/cmaj.111749.
- ^ a b c Errore nelle note: Errore nell'uso del marcatore
<ref>: non è stato indicato alcun testo per il marcatoreHarr2012 - ^ Jørgen Vestbo, Management of Exacerbations (PDF), in Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease, Global Initiative for Chronic Obstructive Lung Disease, 2013, pp. 39–45.
- ^ a b c Raja Dhar, Textbook of pulmonary and critical care medicine, New Delhi, Jaypee Brothers Medical Publishers, 2011, p. 1056, ISBN 978-93-5025-073-0.
- ^ Paolo Palange, ERS Handbook of Respiratory Medicine, European Respiratory Society, 2013, p. 194, ISBN 978-1-84984-041-5.
- ^ Jan Lötvall, Advances in combination therapy for asthma and COPD, Chichester, West Sussex, John Wiley & Sons, 2011, p. 251, ISBN 978-1-119-97846-6.
- ^ Peter Barnes, Asthma and COPD : basic mechanisms and clinical management, 2nd, Amsterdam, Academic, 2009, p. 837, ISBN 978-0-12-374001-4.
- ^ Nicola Hanania, COPD a Guide to Diagnosis and Clinical Management, 1st, Totowa, NJ, Springer Science+Business Media, LLC, 9 dicembre 2010, p. 197, ISBN 978-1-59745-357-8.
- ^ V Beasley, Joshi, PV; Singanayagam, A; Molyneaux, PL; Johnston, SL; Mallia, P, Lung microbiology and exacerbations in COPD, in International journal of chronic obstructive pulmonary disease, vol. 7, 2012, pp. 555–69, DOI:10.2147/COPD.S28286.
- ^ Research Laboratories Merck, The Merck Manual quinta edizione pag 419-420, Milano, Springer-Verlag, 2008, ISBN 978-88-470-0707-9.
- ^ Begin P, Grassino A, Inspiratory muscle dysfunction and chronic hypercapnia in chronic obstructive pulmonary disease, in Am Rev Respir Dis, vol. 143, 1991, pp. 905–912.
- ^ Keith Stone, Humphries L.Roger, Guida pratica alla diagnosi e alla terapia in medicina d’urgenza 1ª edizione pag 39, Milano, McGraw-Hill, 2005, ISBN 88-386-3908-6.
- ^ Errore nelle note: Errore nell'uso del marcatore
<ref>: non è stato indicato alcun testo per il marcatoreSundblad
Bibliografia
- Giovanni Bonsignore, Bellia Vincenzo, Malattie dell’apparato respiratorio terza edizione, Milano, McGraw-Hill, 2006, ISBN 978-88-386-2390-5.
- Keith Stone, Humphries L.Roger, Guida pratica alla diagnosi e alla terapia in medicina d’urgenza 1ª edizione, Milano, McGraw-Hill, 2005, ISBN 88-386-3908-6.
- Research Laboratories Merck, The Merck Manual quinta edizione, Milano, Springer-Verlag, 2008, ISBN 978-88-470-0707-9.
- (EN) Linee Guida GOLD per la BPCO
Altri progetti
 Wikimedia Commons contiene immagini o altri file su broncopneumopatia cronica ostruttiva
Wikimedia Commons contiene immagini o altri file su broncopneumopatia cronica ostruttiva

