Triossido di xeno
| Triossido di xeno | |
|---|---|
 | |
 | |
| Nomi alternativi | |
| ossido di xeno(VI) | |
| Caratteristiche generali | |
| Formula bruta o molecolare | XeO3 |
| Massa molecolare (u) | 179,288 |
| Aspetto | solido cristallino incolore |
| Numero CAS | |
| SMILES | O=[Xe](=O)=O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 4,55 |
| Solubilità in acqua | solubile (reagisce) |
| Temperatura di fusione | 25 °C (298 K) decomposizione violenta |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | 402 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| Frasi H | -- |
| Consigli P | -- |
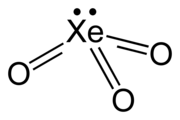
Il triossido di xeno è il composto chimico di formula XeO3, dove lo xeno ha numero di ossidazione +6. È un solido incolore, igroscopico, fortissimo ossidante e pericoloso esplosivo. È solubile in acqua con la produzione di acido xenico.
Struttura[modifica | modifica wikitesto]
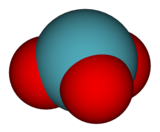
La molecola XeO3 ha struttura piramidale, in accordo con la teoria VSEPR, dato che è presente una coppia di elettroni non condivisi. Per evaporazione di soluzioni di XeO3 si ottengono cristalli incolori, di struttura ortorombica con a = 6,163, b = 8,115, c = 5,234 Å e 4 molecole per cella elementare. La densità del cristallo è 4,55 g/mL.[1]
struttura cristallina di XeO3 |
impaccamento del cristallo |
geometria di coordinazione dello Xe
|
Sintesi[modifica | modifica wikitesto]
XeO3 si forma per idrolisi di soluzioni di XeF4 o XeF6:
6XeF4 + 12H2O → 2XeO3 + 4Xe + 24HF + 3O2
XeF6 + 3H2O → XeO3 + 6HF
Il solido XeO3 si ottiene per evaporazione a secchezza da queste soluzioni dopo aver allontanato HF. XeO3 solido è un esplosivo pericoloso e può facilmente detonare.
Reattività[modifica | modifica wikitesto]
XeO3 è un ossidante molto forte, anche se spesso cineticamente lento.
XeO3 + 6H+ + 6e- → Xe + 3H2O (E° = 2,10 V)
XeO3 solido è stabile per giorni in aria secca, ma è fortemente igroscopico. Soluzioni di XeO3 in acqua sono stabili se si evita la presenza di sostanze ossidabili e l'esposizione alla luce.
Soluzioni di XeO3 in ambiente acido o neutro ossidano quantitativamente acidi carbossilici formando diossido di carbonio e acqua.[2]
In soluzione basica si formano xenati. L'anione HXeO4- è la specie prevalente in queste soluzioni:[3]
XeO3 + OH- → HXeO4-
Queste soluzioni alcaline non sono stabili e disproporzionano formando perxenati (dove lo xeno ha numero di ossidazione +8), xeno e ossigeno:[4]
2HXeO4- + 2OH- → XeO64- + Xe + O2 + 2H2O
XeO3 reagisce con fluoruri come KF, RbF e CsF per dare fluoroxenati del tipo MXeO3F.[5]
XeO3 reagisce con l'acqua formando acido xenico:
XeO3 + H2O → H2XeO4
Indicazioni di sicurezza[modifica | modifica wikitesto]
XeO3 non ha utilizzi industriali, ed è un composto da trattare con grande cautela. Alcuni campioni di XeO3 sono detonati spontaneamente a temperatura ambiente. Cristalli secchi reagiscono esplosivamente con la cellulosa.[1][6]
Note[modifica | modifica wikitesto]
- ^ a b D. H. Templeton, A. Zalkin, J. D. Forrester e S. M. Williamson, Crystal and molecular structure of xenon trioxide, in J. Am. Chem. Soc., vol. 85, n. 6, 1963, p. 817, DOI:10.1021/ja00889a037.
- ^ B. Jaselskis e R. H. Krueger, Titrimetric determination of some organic acids by xenon trioxide oxidation, in Talanta, vol. 13, n. 7, 1966, pp. 945–949, DOI:10.1016/0039-9140(66)80192-3.
- ^ J. L. Peterson, H. H. Claassen e E. H. Appelman, Vibrational spectra and structures of xenate(VI) and perxenate(VIII) ions in aqueous solution, in Inorg. Chem., vol. 9, n. 3, 1970, pp. 619–621, DOI:10.1021/ic50085a037.
- ^ W. Henderson, Main group chemistry, Royal Society of Chemistry, 2000, pp. 152–153, ISBN 0-85404-617-8.
- ^ E. Wiberg, N. Wiberg e A. F. Holleman, Inorganic chemistry, Academic Press, 2001, p. 399, ISBN 0-12-352651-5.
- ^ N. Bartlett e P. R. Rao, Xenon hydroxide: an experimental hazard, in Science, vol. 139, n. 3554, 1963, p. 506, DOI:10.1126/science.139.3554.506.
Bibliografia[modifica | modifica wikitesto]
- N. N. Greenwood, A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
- J. G. Malm, H. Selig, J. Jortner e S. A. Rice, The chemistry of xenon, in Chem. Rev., vol. 65, n. 2, 1965, pp. 199-236, DOI:10.1021/cr60234a003.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su triossido di xeno
Wikimedia Commons contiene immagini o altri file su triossido di xeno



