Diossido di plutonio
| Diossido di plutonio | |
|---|---|
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | PuO2 |
| Massa molecolare (u) | 276,06 |
| Aspetto | solido cristallino giallo marrone |
| Numero CAS | |
| Numero EINECS | 235-037-3 |
| PubChem | 9795444 |
| SMILES | [Pu+4].[O-2].[O-2] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 11,5 |
| Solubilità in acqua | insolubile |
| Temperatura di fusione | 2400 °C (2673,15 K) |
| Temperatura di ebollizione | 2800 °C (3073,15 K) |
| Indicazioni di sicurezza | |
Il diossido di plutonio è un composto chimico con formula PuO2. Si tratta di un solido a elevato punto di fusione che rappresenta uno dei principali composti del plutonio. La sua colorazione può variare dal giallo al verde oliva, in relazione alla dimensione delle particelle, alla temperatura e al metodo di produzione.[1]
Struttura[modifica | modifica wikitesto]
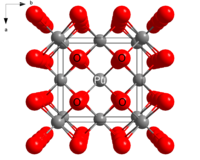
PuO2 cristallizza nel sistema cristallino caratteristico della fluorite, con centri di Pu4+ in un sistema cubico a facce centrate e ioni ossido che occupano le lacune tetraedriche.[2] Il diossido di plutonio viene utilizzato come combustibile nucleare grazie al fatto che le lacune ottaedriche consentono di ospitare i prodotti di fissione senza che si abbia la rottura della struttura del materiale.
Sintesi[modifica | modifica wikitesto]
Il plutonio metallico si ossida spontaneamente a PuO2 in presenza di ossigeno. Il diossido di plutonio viene principalmente prodotto attraverso la calcinazione dell'ossalato di plutonio(IV), Pu(C2O4)2·6H2O, a 300 °C. L'ossalato di plutonio è ottenuto durante il riprocessamento del combustibile nucleare.
Applicazioni[modifica | modifica wikitesto]

Il diossido di plutonio viene utilizzato nel MOX quale combustibile per reattori nucleari. Il diossido di plutonio-238 è utilizzato come fonte di energia per le sonde spaziali come la New Horizons. L'isotopo decade emettendo particelle α generando calore in seguito alla conversione dell'energia cinetica in energia termica: la potenza specifica del plutonio-238 è di circa 567 W/kg, che vale circa 390 W/kg sotto forma di diossido di plutonio — l'isotopo di plutonio-238 non è mai puro, raggiungendo generalmente una concentrazione dal 75 all'80%, con un contenuto spesso dal 15 al 20% di plutonio-239 e diversi altri attinidi.
Questa tecnologia presenta molti vantaggi per l'esplorazione spaziale, ma continua a suscitare i timori dell'opinione pubblica rispetto ai rischi di contaminazione radioattiva in caso di incidente durante il lancio o in caso di caduta del velivolo nell'atmosfera terrestre.
Sicurezza[modifica | modifica wikitesto]
Il diossido di plutonio è altamente tossico per gli esseri umani, specialmente attraverso l'inalazione.[3] Come tutti i composti del plutonio, è soggetto al controllo inerente al Trattato di non proliferazione nucleare. A causa del decadimento alfa del plutonio, PuO2, come tutti gli altri composti formati da questo elemento, risulta caldo al tatto.
Note[modifica | modifica wikitesto]
- ^ Nitric acid processing, Los Alamos Laboratory. URL consultato il 12 maggio 2011 (archiviato dall'url originale il 27 maggio 2010).
- ^ Greenwood, Norman N.; Earnshaw, A. (1984), Chemistry of the Elements, Oxford: Pergamon, p. 1471, ISBN 0-08-022057-6
- ^ Toxicological Profile For Plutonium (PDF), su atsdr.cdc.gov, U.S. Department of Health and Human Services, 27 settembre 2007. URL consultato il 12 maggio 2011.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Diossido di plutonio
Wikimedia Commons contiene immagini o altri file su Diossido di plutonio