Rabbia
| Rabbia | |
|---|---|
| Specialità | infettivologia e veterinaria |
| Eziologia | virus della rabbia |
| Classificazione e risorse esterne (EN) | |
| MeSH | D011818 |
| MedlinePlus | 001334 |
| eMedicine | 220967 |
| Eponimi | |
| rage cane | |
La rabbia è una malattia virale causata da alcuni virus del genere Lyssavirus. È una zoonosi, diffusa ed endemica in alcune famiglie di mammiferi, tra cui spiccano canidi e pipistrelli, la cui trasmissione avviene per introduzione nell'ospite di liquido salivare tramite ferite da morsi di animali, e che può essere trasmessa anche all'uomo. La malattia causa l'infiammazione acuta del cervello e del sistema nervoso centrale negli esseri umani e in altri animali. Negli esseri umani, se non vaccinati, il decorso della malattia è mortale, praticamente nella totalità dei casi.[1]
Generalità
[modifica | modifica wikitesto]Tipicamente la malattia si presenta a seguito del morso di un animale, come ad esempio un pipistrello, che può essere una ferita piccola e passare inosservata. Negli esseri umani, I primi sintomi si manifestano a distanza di tempo, all'inizio sono generici e possono includere febbre e prurito nel sito di esposizione.[2] Questi sintomi sono seguiti, nel tempo, dalla comparsa di una sintomatologia chiaramente neurologica, presentando uno o più dei seguenti segni: movimenti violenti, emozioni incontrollate, idrofobia, incapacità di muovere parti del corpo, confusione e perdita di coscienza.[2] La malattia distrugge gradualmente le funzionalità del sistema nervoso centrale. Una volta che i sintomi compaiono, quasi sempre la malattia si conclude nel decesso.[2] Il periodo di tempo tra il momento in cui la malattia viene contratta e l'inizio dei sintomi varia solitamente da uno a tre mesi; tuttavia, questo periodo di tempo può andare anche da meno di una settimana a più di un anno.[2] Il tempo dipende dalla distanza che il virus deve percorrere per raggiungere il sistema nervoso centrale.[3]
L'agente eziologico della rabbia sono alcuni virus del genere Lyssavirus, tra cui il virus della rabbia e il virus denominato Lyssavirus del pipistrello australiano.[4] La rabbia si trasmette quando un animale infetto graffia o morde un altro animale o un uomo.[2] La saliva di un animale infetto può anche trasmettere la rabbia se essa viene a contatto con la bocca, il naso o gli occhi.[2] Complessivamente i cani sono gli animali più comunemente coinvolti.[2] Più del 99% dei casi di rabbia è causato dai morsi di cani nei paesi dove più frequentemente hanno la malattia.[5] Nelle Americhe, i morsi di pipistrello sono la fonte più comune delle infezioni di rabbia negli esseri umani e meno del 5% dei casi provengono da cani.[2][5] I roditori sono raramente infettati dalla rabbia.[5] Il virus della rabbia raggiunge il cervello seguendo i nervi periferici. La malattia può essere diagnosticata solo dopo l'inizio dei sintomi.[2]
Il controllo degli animali e i programmi di vaccinazione hanno ridotto il rischio dello sviluppo della rabbia nei cani in un certo numero di regioni del mondo.[2] L'immunizzazione è consigliata nelle persone ad alto rischio prima di essere esposte. I gruppi ad alto rischio comprendono le persone che lavorano con i pipistrelli o che trascorrono periodi prolungati in aree del mondo dove la rabbia è endemica.[2] Nelle persone che sono state esposte alla rabbia, il vaccino antirabbico e, talvolta, le immunoglobuline sono efficaci nel prevenire l'esordio della malattia se la persona riceve questo trattamento prima dell'inizio dei sintomi.[2] L'immediato lavaggio di morsi e graffi per 15 minuti con acqua e sapone, iodopovidone o detergente, può ridurre il numero di particelle virali e quindi può essere un metodo in qualche modo efficace per prevenire la trasmissione.[2][6] Solo poche persone sono sopravvissute a un'infezione da rabbia dopo aver mostrato i sintomi e ciò grazie all'adozione di un trattamento noto come protocollo di Milwaukee.[7]
La rabbia provoca da circa 26 000 a 55 000 decessi nel mondo ogni anno.[2][8] Oltre il 95% di queste morti avviene in Asia e Africa.[2] La rabbia è presente in più di 150 paesi e in tutti i continenti, escluso l'Antartide.[2] Più di 3 miliardi di persone vivono in regioni del mondo in cui si verifica.[2] Un certo numero di paesi, tra cui l'Australia, il Canada, il Giappone, gli Stati Uniti e i paesi dell'Europa occidentale, non presentano casi tra i cani.[9][10] Anche molte piccole nazioni insulari sono prive della malattia.[11]
Epidemiologia
[modifica | modifica wikitesto]
Si stima che, nel 2010, circa 26 000 persone siano morte di rabbia, in calo rispetto ai 54 000 decessi avvenuti nel 1990.[8] La maggior parte dei decessi si è verificata in Asia e in Africa.[12]
Il virus della rabbia sopravvive in diffusi e vari serbatoi della fauna rurale. È presente nelle popolazioni animali di quasi tutti i paesi del mondo ad eccezione dell'Australia e della Nuova Zelanda.[13] Il lyssavirus del pipistrello australiano, scoperto nel 1996, è simile alla rabbia e si crede che sia prevalente nelle popolazioni indigene di pipistrelli.
Circa 20.000 persone ogni anno muoiono di rabbia in India, più di un terzo del totale a livello mondiale.[14] L'India ha il più alto tasso di casi di rabbia umana nel mondo, principalmente a causa dei cani randagi,[15] il cui numero è notevolmente aumentato in seguito a una legge del 2001 che vieta l'uccisione dei cani.[14] Un controllo efficace e il trattamento della rabbia in India è anche ostacolato da una forma di isteria di massa nota come "sindrome del cucciolo singolo". Le vittime del morso dei cani (sia maschi che femmine) si convincono che vi siano cuccioli in crescita al loro interno e spesso cercano l'aiuto di guaritori, piuttosto che dai servizi medici convenzionali. Nei casi in cui il morso fosse stato di un cane rabbioso, questa decisione può rivelarsi fatale. Il dottor Nitai Kishore Marik, ex ufficiale medico di West Midnapur, afferma: «Ho visto decine di casi di rabbia che hanno raggiunto i nostri ospedali molto tardi a causa dell'intervento di guaritori. Non siamo riusciti a salvare molte vite umane».[16]
Nel 2007, il Vietnam possedeva il secondo più alto tasso, seguito dalla Thailandia. In questi paesi, il virus si trasmette principalmente attraverso i canidi (cani selvatici e altre specie canine selvatiche).[17]
Un'altra fonte della rabbia in Asia è la continua crescita della presenza degli animali domestici. Nel 2006 la Cina ha introdotto severi controlli sulla popolazione dei cani a Pechino.[18]
In Asia e in alcune parti delle Americhe e dell'Africa, i cani rimangono comunque l'ospite principale.
Negli Stati Uniti, la rabbia è comune tra gli animali selvatici. Pipistrelli, procioni, puzzole e volpi rappresentano quasi tutti i casi segnalati (98% nel 2009). Pipistrelli rabbiosi si trovano in tutti i 48 stati contigui. Altri serbatoi naturali sono più limitati geograficamente; per esempio, la variante del virus della rabbia si trova solo in una fascia relativamente stretta lungo la costa orientale. Grazie a un'elevata consapevolezza pubblica del virus, ai tentativi di vaccinazione degli animali domestici e alla decurtazione delle popolazioni selvatiche e la disponibilità di profilassi post-esposizione, gli episodi di rabbia negli esseri umani sono molto rari. Un totale di 49 casi di malattia sono stati segnalati nel paese tra il 1995 e il 2011; di questi, 11 si ritengano essere stati contagiati all'estero. Quasi tutti i casi a livello nazionale acquisiti sono stati attribuiti ai morsi di pipistrello, che possono passare inosservati da parte della vittima e quindi non essere trattati tempestivamente.[19][20] Il numero di morti umane dovute a rabbia, negli Stati Uniti, è sceso da un valore superiore a 100 dei primi anni del XX secolo ad uno o due casi all'anno grazie alla diffusa vaccinazione dei cani e dei gatti domestici e allo sviluppo di vaccini umani e trattamenti di immunoglobuline.
Etimologia
[modifica | modifica wikitesto]Il termine deriva dal latino rabies, "follia".[21] Questo, a sua volta, può essere correlato a rabhas in sanscrito, "fare violenza".
Il nome del genere Lyssavirus, che include i virus responsabili di questa patologia, deriva dalla parola greca lyssa, da lud, "violento".[22]
Storia
[modifica | modifica wikitesto]La rabbia è conosciuta fin da circa il 2000 a.C.[23] La prima testimonianza scritta della condizione si trova nelle "Leggi di Eshnunna", scritte in Mesopotamia intorno al 1930 a.C., che impongono al proprietario di un cane che mostra i sintomi di prendere misure preventive contro i morsi, erano state stipulate delle punizioni per le persone proprietarie di un “kalbum segum” (un cane rabbioso).[24]
Omero descrisse Ettore come un uomo con un irrefrenabile coraggio marziale dovuto a qualcosa che va oltre alla stessa rabbia come emozione, ma più di tutti il personaggio di Lyssa (“lycos” - “lupo”) descritto come crudo, terrificante, violento e “animalescamente” distruttivo nei confronti degli altri.[25]
Il virus della rabbia compare pure nel “Sushruta Samhita” una guida medica indiana databile 400 a.C.: esso identifica correttamente molti aspetti della malattia: il morso da parte di un animale causa all'uomo la perdita delle sue facoltà umane.[26]
Nei primi due secoli dopo Cristo l'antica tradizione medica greco-romana iniziò a cercare di capire questa malattia: il primo fu Aulo Cornelio Celso, che nel suo “De medicina” collegò il sintomo dell'idrofobia alla malattia della rabbia.[27] Dopo circa 100 anni emerse la scuola dei “metodisti”, un gruppo di menti scientifiche i quali non solo migliorarono la comprensione della rabbia, ma quella di molte altre malattie. Il fondatore della scuola, Temisone, e un suo discepolo erano famosi per esser sopravvissuti all'attacco e al morso di un cane rabbioso. Il primo vero metodista che parlò di rabbia fu Sorano il quale riconobbe che il contatto con l'animale poteva essere l'unico motivo dell'idrofobia. Descrisse inoltre alcuni sintomi come il polso irregolare, la febbre, l'incontinenza, il tremore e l'involontaria eiaculazione.[28]

Nei tempi antichi era praticato il fissaggio del frenulo linguale, una membrana mucosa, che veniva tagliata e rimossa, in quanto si pensava che fosse all'origine della malattia. Questa pratica è cessata con la scoperta della vera causa della rabbia.[29]
Nel medioevo il concetto della trasmissione di una malattia da parte degli animali era ancora oscuro. Le uniche due malattie di cui avevano ipotizzato il contagio tramite un animale erano la rabbia (dai cani) e il carbonchio (dal bestiame). La trasmissione di queste malattie da animale a uomo si è velocizzata a causa dell'aumento dell'urbanizzazione e dell'agricoltura e nel XV secolo un terzo fattore ha portato le persone a contatto con le più gravi malattie della storia: i viaggi nell'oceano.[30]
Durante il medioevo, i primi veri cambiamenti riguardo alla comprensione della rabbia si hanno grazie al mondo islamico. I tre principali esponenti della medicina islamica furono: Al Razi, Avicenna e Ibn Zuhr. Il primo ebbe personali esperienze di contatto con malati di rabbia: "c'erano con noi in ospedale una sorta di uomo che abbaiava la notte e poi morì. Un altro non beveva acqua, ma quando dell'acqua gli veniva portata, non ne aveva paura, ma diceva: "puzza, e lo stomaco di gatti e cani è là dentro”. Poi un altro paziente quando vedeva l'acqua rabbrividiva e tremava finché non gli era portata via". Egli preferiva trattare il morso cauterizzandolo e scarnificandolo. Ibn Zuhr successivamente scrisse un trattato chiamato Sui mali furiosi, ma i veri progressi ci furono con Avicenna, il quale nel suo quarto libro scrisse che secondo lui il caldo e il freddo aiutavano a fomentare la malattia nei cani. Inoltre egli attribuì la causa del contagio della malattia al consumo di acqua e carne infetta.
Successivamente durante i giorni dell'Inquisizione, verso la fine del XV secolo, una misteriosa confraternita di curatori girava di città in città, offrendo protezione contro la rabbia. Si facevano chiamare i “Saludadores”, dotati di poteri donati direttamente dai santi. I Saludadores potevano annullare quel morso nocivo spesso attraverso la loro saliva o il loro respiro. L'inquisizione cominciò a considerarli eretici e l'ordine fu quello di distruggere questa confraternita; alcuni membri furono catturati e sotto tortura confessarono che si trattava di un'enorme frode.[31]

La rabbia sembra abbia aver avuto origine nel Vecchio Mondo, la prima diffusione tra gli animali nel Nuovo Mondo si verificò a Boston nel 1768.[32] Iniziando da lì, nel corso degli anni si spostò in diversi altri Stati, nonché alle Antille francesi, fino a diventare comune in tutto il Nord America.
Nel XIX secolo, la rabbia era considerata un flagello per la sua prevalenza. In Francia e in Belgio, dove si venerava Sant'Uberto, la "chiave di Sant'Uberto" veniva riscaldata e applicata per cauterizzare la ferita. Inoltre, la credenza popolare faceva sì che i cani venissero marchiati con la chiave nella speranza di proteggerli dalla rabbia. La paura della malattia per la sua estrema letalità, l'improvvisa emergenza e l'assenza di qualsiasi trattamento efficace, portò a stigmatizzare in particolare i lupi come estremamente pericolosi[33][34]. Non era raro che una persona morsa da un cane, ma che era solo sospettato di essere rabbioso, si suicidasse o fosse uccisa da altri.[22] Ciò permise a Louis Pasteur, a partire dalla sua scoperta del primo vaccino antirabbico nel 1885, ampie opportunità di provare trattamenti post-esposizione.[35]
Nei tempi moderni, la paura della rabbia non è diminuita e la malattia e i suoi sintomi (soprattutto il delirio) hanno ispirato numerose storie di zombie o a tema simile, spesso raccontando di un virus della rabbia reso più potente e che trasforma gli esseri umani, con rabbia omicida o malattia inguaribile, determinando un devastante pandemia diffusa.[36]
Il 28 settembre è la "giornata mondiale della rabbia", che promuove l'informazione, la prevenzione e l'eliminazione della malattia.[37]
Antiche terapie per curare la rabbia
[modifica | modifica wikitesto]Nel Sushruta Samhita viene spiegato come trattare una ferita dovuta ad un cane rabico: cauterizzare la ferita con burro che poi il paziente era costretto a bere, inoltre un impasto di sesamo doveva essere applicato nella ferita mentre il paziente veniva nutrito con una torta di riso, radici e foglie.
Durante l'epoca Greco-Romana, Celso ipotizzò vari rimedi per il trattamento del morso: oltre alla cauterizzazione, l'applicazione di sale e cetriolini in salamoia nella ferita. Bisognava inoltre mandare il paziente in un bagno turco in maniera tale da farlo sudare fino al limite della sopportazione per permettere alla ferita di espellere il veleno della rabbia. Dopo di ciò il dottore doveva applicare del vino sul morso. La cura più calzante probabilmente la offrì Celso: bisogna buttare il paziente in acqua e se egli non può nuotare affonderà e berrà acqua, mentre se può nuotare deve essere spinto sott'acqua finché non ne berrà un po'. Così la paura e la sete verranno sconfitte contemporaneamente.
Successivamente Plinio il giovane fu il primo ad ipotizzare l'utilizzo dell'animale per curare l'uomo: inserire nella ferita le ceneri dei peli della coda del cane che ha inflitto la ferita; la stessa testa dell'animale a volte veniva ridotta in cenere e applicata sulla ferita. Lo stesso Plinio ipotizzò una cura per l'idrofobia: bisogna mettere il paziente in zone speciali con aria "buona", massaggiare gli arti e coprirlo con vestiti puliti e caldi nei punti affetti da spasmi.[38]
Eziologia
[modifica | modifica wikitesto]
La rabbia è causata da una serie di Lyssavirus, della famiglia dei Rhabdoviridae, ordine Mononegavirales, tra cui il virus della rabbia e l'Australian bat lyssavirus.[4]
Tutte le specie a sangue caldo, compresi gli esseri umani, possono essere infettati con il virus della rabbia e svilupparne i sintomi. La maggior parte degli animali possono essere infettati dal virus e possono trasmettere la malattia agli esseri umani. La trasmissione tra esseri umani è estremamente rara; alcuni casi sono stati registrati in seguito a trapianti d'organi.[39]
Pipistrelli infetti,[40][41] scimmie, procioni, volpi, puzzole, bovini, lupi, coyote, cani, manguste (normalmente manguste gialle)[42] e gatti presentano il maggior rischio per l'uomo. La rabbia può diffondersi anche attraverso l'esposizione con bestiame, animali domestici, marmotte, donnole, orsi e altri carnivori selvatici infetti. Piccoli roditori, come scoiattoli, criceti, ratti e topi, e lagomorfi come conigli e lepri, non sono quasi mai stati trovati infettati con la rabbia e non sono noti per poterla trasmettere agli esseri umani.[43] Morsi di topi, ratti o scoiattoli raramente richiedono la profilassi per la rabbia, poiché questi roditori sono tipicamente uccisi da un incontro con un animale infetto più grande e quindi non sono portatori.[44] La didelphis virginiana è resistente ma non immune dalla rabbia.[45]
Nel 1884 si è provato ad infettare artificialmente gli uccelli con la rabbia; tuttavia, i volatili infetti si sono dimostrati in gran parte, se non del tutto, asintomatici e sono guariti.[46] Sono state scoperte alcune specie di uccelli che hanno sviluppato anticorpi contro la rabbia, un segno di infezione, dopo essere stati nutriti con mammiferi infetti.[47][48]
Il virus si è anche adattato a crescere nelle cellule dei vertebrati a "sangue freddo" (pecilotermia).[49][50]
Il virus della rabbia appartiene al genere Lyssavirus: essi hanno una simmetria elicoidale, con una lunghezza di circa 180 nm e una sezione trasversale di circa 75 nm.[51] Questi virus sono avvolti e possiedono un singolo filamento di genoma a RNA con senso negativo. L'informazione genetica è contenuta in un complesso di ribonucleoproteina in cui l'RNA è strettamente vincolato alla nucleoproteina virale. Il genoma del virus RNA codifica cinque geni il cui ordine è altamente conservato: nucleoproteina (N), fosfoproteina (P), proteina di matrice (M), glicoproteina (G) e la polimerasi RNA virale (L).[52]
Il virus è normalmente presente nei nervi e nella saliva di un animale rabbioso e sintomatico.[53][54] La via di infezione è di solito, ma non sempre, attraverso un morso. In molti casi, l'animale infetto è eccezionalmente aggressivo e può attaccare senza che vi sia provocazione e presentando un comportamento altrimenti insolito:[55] questo è un esempio di patogeno virale in grado di modificare il comportamento dell'ospite per facilitare la trasmissione ad altri ospiti.
Una volta all'interno di una cellula muscolare o nervosa, il virus inizia a replicarsi. Le punte trimeriche sull'esterno della membrana del virus interagiscono con un recettore specifico della cellula, il più probabile è il recettore dell'acetilcolina, l'acetile. Un processo noto come pinocitosi permette l'ingresso del virus nella cellula mediante un endosoma. Il virus utilizza il necessario ambiente acido dell'endosoma, contemporaneamente si fonde alla membrana, rilasciando le sue cinque proteine e l'RNA singolo filamento nel citoplasma.[56]
La proteina L poi trascrive cinque filoni di mRNA e un filamento positivo di RNA dall'originale filamento negativo RNA utilizzando i nucleotidi liberi nel citoplasma. Questi cinque filoni di mRNA vengono poi tradotti nelle loro proteine corrispondenti (proteine P, L, N, G e M) nei ribosomi liberi nel citoplasma. Alcune proteine richiedono modificazioni post-traslatorie. Per esempio, la proteina G viaggia attraverso il reticolo endoplasmatico rugoso, dove subisce un'ulteriore piegatura, e viene quindi trasportata all'apparato del Golgi, in cui viene aggiunto un gruppo di zucchero (glicosilazione).[56]
Qualora vi siano abbastanza proteine, la polimerasi virale inizierà a sintetizzare nuovi filamenti negativi di RNA dal modello del filamento di RNA positivo. Questi filamenti negativi formeranno i complessi con le proteine N, P, L e M e poi raggiungere la membrana interna della cellula, in cui una proteina G è parte integrante della membrana. La proteina G poi arrotola attorno al complesso di proteine NPLM prendendo alcuni frammenti della membrana della cellula ospite, che costituirà la nuova sacca esterna della particella virale. I virus poi fuoriescono dalla cellula.[56]
Patogenesi
[modifica | modifica wikitesto]
Dopo una tipica infezione da morso, il virus entra nel sistema nervoso periferico e dal punto di ingresso viaggia lungo i nervi afferenti verso il sistema nervoso centrale.[57] Solitamente, il virus prima infetta le cellule muscolari vicino al sito di infezione, dove è in grado di replicarsi senza essere rilevato dal sistema immunitario dell'ospite (in questo stadio la vaccinazione può ancora conferire immunità cellulo-mediata per prevenire l'esordio dei sintomi). Una volta che il virus si è replicato a sufficienza inizia a legarsi ai recettori dell’acetilcolina (p75NR) a livello della giunzione neuromuscolare.[58] Il virus poi viaggia attraverso l'assone della cellula nervosa. Raggiunto il corpo cellulare, arriva rapidamente al sistema nervoso centrale, replicandosi nei motoneuroni.[3]
Quando il virus raggiunge il cervello, provoca rapidamente l'encefalite, la fase prodromica, ed è l'inizio dei sintomi. Una volta che il paziente diventa sintomatico, il trattamento è quasi mai efficace e la mortalità è superiore al 99%.
La rabbia può anche infiammare il midollo spinale, producendo mielite trasversa.[59][60]
Dopo che il cervello è infetto, il virus viaggia verso il sistema nervoso periferico e autonomo, eventualmente migrando alle ghiandole salivari, in cui è pronto per essere trasmesso all'ospite successivo.
Anatomia patologica
[modifica | modifica wikitesto]Della rabbia sono tipiche delle inclusioni intracitoplasmatiche eosinofile, dette corpi di Negri, la cui presenza assicura una diagnosi di rabbia al 100%, tuttavia si trovano solo in circa l'80% dei casi.[51]
Clinica
[modifica | modifica wikitesto]Segni e sintomi
[modifica | modifica wikitesto]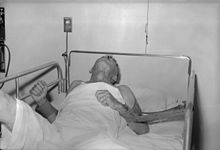
Negli esseri umani, il periodo tra l'infezione e la presenza dei primi sintomi (di tipo simil-influenzale) è tipicamente variabile tra le 2 e le 12 settimane. Tuttavia, sono stati documentati periodi di incubazione di quattro giorni e fino a sei anni, a seconda della posizione e della gravità della ferita contaminata, nonché della quantità di virus introdotto.
Segni e sintomi possono consistere in una lieve o parziale paralisi, ansia, insonnia, confusione, agitazione, comportamento anormale, paranoia, terrore e allucinazioni, fino al delirio.[3][61] La persona può sviluppare idrofobia.
Solitamente si susseguono tre fasi:
- Fase prodromica: dopo il morso si possono rilevare sintomi aspecifici, quali febbre, cefalea, mialgia. L'unico sintomo specifico, che si presenta nel 60% dei casi, è una parestesia nella sede del morso.
- Fase di latenza o "rabbia furiosa": caratterizzata dall'idrofobia, un laringospasmo doloroso in seguito al tentativo di far bere il paziente (negli animali tale sintomo si verifica perlopiù nei gatti).[62] L'idrofobia è comunemente associata con la rabbia furiosa che colpisce l'80% delle persone infette. Il restante 20% può sperimentare una forma di paralisi caratteristica della rabbia che è caratterizzata da debolezza muscolare, perdita di sensibilità e paralisi. Questa forma solitamente non causa idrofobia.[63]
- Fase terminale: il virus ha colonizzato i tessuti del sistema nervoso centrale e si hanno sintomi neurologici. La sintomatologia prevalente (75% dei casi) è di tipo furioso (forma furiosa), con aggressività, irascibilità, perdita di senso dell'orientamento, allucinazioni, iperestesia, meningismo, lacrimazione, aumento della salivazione, priapismo, eiaculazione spontanea, Babinsky positivo, paralisi delle corde vocali e idrofobia. Nel restante 25% dei casi si ha una sintomatologia di tipo paralitico (forma paralitica).
Idrofobia
[modifica | modifica wikitesto]"Idrofobia" ("paura dell'acqua") è il nome storico usato per la rabbia.[64] Con esso ci si riferisce ad un insieme di sintomi presenti nelle fasi successive di una infezione, in cui la persona ha difficoltà e dolore a deglutire liquidi, mostra panico quando deve bere e non riesce a placare la sua sete. Anche altri mammiferi infettati con il virus della rabbia possono mostrare questa condizione.[63]
La produzione di saliva risulta notevolmente aumentata (scialorrea) e il tentativo di bere o addirittura solo l'intenzione o il suggerimento di bere, può provocare spasmi atrocemente dolorosi dei muscoli della gola e della laringe, come il tipico laringospasmo idrofobico. Ciò può essere attribuito al fatto che il virus si moltiplica e si assimila nelle ghiandole salivari dell'animale infetto, ai fini di un'ulteriore trasmissione attraverso morsi, e la capacità dell'animale infetto di trasmettere il virus potrebbe essere ridotta significativamente se ingoia la saliva, con o senza una fonte esterna di acqua.[65]
Esami di laboratorio
[modifica | modifica wikitesto]Il gold standard per la formulazione della diagnosi della rabbia è il test di immunofluorescenza (una procedura di immunoistochimica), che viene raccomandato dall'Organizzazione mondiale della sanità (OMS).[66] L'immunofluorescenza si basa sulla capacità di una molecola (solitamente l'isotiocianato di fluoresceina) accoppiata ad un anticorpo specifico per la rabbia, a formare un complesso coniugato, che lega e di conseguenza consente la visualizzazione dell'antigene della rabbia usando le tecniche di microscopia a fluorescenza. L'analisi microscopica di campioni è l'unico metodo diretto che consenta l'identificazione dell'antigene specifico del virus della rabbia in breve tempo e ad un costo ridotto, indipendentemente dall'origine geografica e dallo stato dell'ospite. Ciò deve essere considerato come il primo passo nelle procedure diagnostiche adottate in tutti i laboratori. I campioni in autolisi possono, tuttavia, ridurre la sensibilità e la specificità del FAT.[67]
La RT-PCR (una variante della reazione a catena della polimerasi) ha dimostrato di essere uno strumento sensibile e specifico per la diagnosi di routine,[68] in particolare nei campioni di decomposizione[69] o campioni d'archivio.[70]
Una diagnosi affidabile può essere formulata attraverso l'analisi di campioni di tessuto cerebrale prelevato post mortem. Possono essere analizzate anche la saliva, l'urina e campioni di liquido cerebrospinale, ma questi non sono così sensibili ed affidabili come i campioni cerebrali.[67] Una diagnosi accurata da rabbia può essere fatta, con un decimo del costo rispetto ai test tradizionali, utilizzando le tecniche di microscopia classica.[71]
Diagnosi differenziale
[modifica | modifica wikitesto]La rabbia può essere difficile da diagnosticare poiché, nelle fasi iniziali, è facilmente confondibile con altre malattie o condizioni cliniche.[72]
La diagnosi differenziale in un caso di sospetta rabbia umana può inizialmente includere qualsiasi causa di encefalite, in particolare l'infezione da virus come l'herpes virus, l'enterovirus e l'arbovirus come il virus del Nilo occidentale.
I virus più importanti da escludere sono il virus dell'herpes simplex di tipo 1, l'Herpesvirus umano 3 e (meno frequentemente) gli enterovirus, compresi i coxsackie virus, gli echovirus, i poliovirus e gli enterovirus umani da 68 a 71.[73] Sono possibili anche cause di encefalite virale nuove, come hanno dimostrato i 300 casi di encefalite avvenuti nel 1999 in Malaysia con un tasso di mortalità del 40% causata dal Nipahvirus, un paramyxoviridae appena riconosciuto.[74] Allo stesso modo, molti virus già conosciuti possono scatenare dei forti attacchi, come dimostra la recente epidemia di encefalite a causa del virus del Nilo occidentale avvenuta nella parte orientale degli Stati Uniti.[75]
Fattori epidemiologici, come la stagione, la posizione geografica, l'età del paziente, i suoi viaggi passati e l'esposizione a morsi, roditori e zecche, possono contribuire ad orientare la diagnosi.
Se possibile andrebbe analizzato anche l'animale da cui si è stati morsicati.[76]
Trattamento
[modifica | modifica wikitesto]Il trattamento a seguito dell'esposizione, se somministrato tempestivamente, può prevenire l'insorgenza della malattia; generalmente è necessario procedere entro 10 giorni dall'infezione.[51]
Entro pochi minuti è utile lavare accuratamente la ferita con acqua e sapone per circa cinque minuti in modo da ridurre il numero di particelle virali.[77] L'utilizzo di alcool o iodopovidone è raccomandato per ridurre ulteriormente i virus.[78]
Negli Stati Uniti, il Centers for Disease Control and Prevention raccomanda che le persone contagiate ricevano una sieroprofilassi con una dose di immunoglobuline della rabbia umana (HRIG) e quattro dosi di vaccino entro 14 giorni.[79] La dose di immunoglobuline non deve superare le 20 unità per kg di peso corporeo. L'HRIG è costoso e costituisce la maggior parte del costo della profilassi post-esposizione (PEP). La dose deve essere iniettata quanto più possibile intorno alle infezioni, mentre il resto deve essere somministrato per iniezione intramuscolare profonda in un sito distante dal sito di vaccinazione.[56] La prima dose di vaccino contro la rabbia deve essere somministrata appena possibile dopo l'esposizione, con ulteriori dosi a 3, a 7 e a 14 giorni dopo la prima. Ai pazienti che hanno precedentemente ricevuto la vaccinazione pre-esposizione non devono essere somministrate le immunoglobuline, solo le vaccinazioni post-esposizione nei giorni 0 e 3.[80]
Trovare un pipistrello nella stanza al risveglio, o trovarne uno nella stanza di un bambino non controllato o di un disabile mentale o di un tossicodipendente, sono situazioni in cui è indicata la profilassi post-esposizione. È oggetto di valutazione nella letteratura medica, sulla base di un'analisi costi-benefici, la raccomandazione alla profilassi post-esposizione per gli incontri con pipistrelli senza che sia avvenuto un contatto.[81] Tuttavia, uno studio del 2002 ha invitato al protocollo di somministrazione precauzionale della PEP nel caso in cui bambini o individui mentalmente compromessi siano stati da soli con un pipistrello, soprattutto durante il sonno, quando un morso o l'esposizione al virus può avvenire senza che la vittima ne sia a conoscenza.[82]
Se iniziata con poco o nessun ritardo, la PEP è efficace al 100% contro la rabbia.[83] Nel caso in cui vi sia stato un significativo ritardo nella somministrazione della profilassi, il trattamento deve essere comunque somministrato a prescindere, in quanto può essere ancora efficace.[56]
Coma indotto
[modifica | modifica wikitesto]Nel 2004, l'adolescente statunitense Jeanna Giese sopravvisse ad un'infezione di rabbia nonostante non fosse vaccinata.[83] Fu messa in coma indotto non appena si presentarono i sintomi e le furono somministrate ketamina, midazolam, ribavirina e amantadina.
I medici tentarono questo trattamento sull'ipotesi che gli effetti negativi della rabbia fossero causati da disfunzioni temporanee nel cervello, e che potessero essere evitati inducendo un'interruzione momentanea e parziale delle sue funzioni al fine di proteggerlo dai danni, dando il tempo al sistema immunitario di sconfiggere il virus. Il regime di trattamento a cui Giese venne sottoposta divenne noto come "protocollo di Milwaukee", che da allora è stato sottoposto a revisioni, con una seconda versione che omette l'uso della ribavirina.
L'anestetico ketamina ha dimostrato la potenziale inibizione del virus della rabbia nei ratti.[84] L'analisi intention to treat ha dimostrato che questo protocollo ha un tasso di sopravvivenza di circa l'8%.[85]
Dopo 31 giorni di isolamento e 76 giorni di ricovero, Giese fu dimessa dall'ospedale.[86] In lei furono preservate tutte le funzioni cerebrali di livello superiore, ma fu riscontrata l'incapacità di camminare e di mantenere l'equilibrio.[87] In un'intervista, Giese raccontò: «Ho dovuto imparare a stare di nuovo in piedi, a girare, a muovere le dita dei piedi. Ero davvero, dopo la rabbia, una neonata che non è in grado di fare nulla. Ho dovuto imparare di nuovo tutto [...] mentalmente sapevo compiere quelle azioni, ma il mio corpo non collaborava con quello che volevo fare. È stata sicuramente una prova psicologicamente dura per me. Mi sto ancora riprendendo.»[88]
Due dei 25 pazienti trattati con il primo protocollo sono sopravvissuti, mentre ulteriori 10 pazienti sono stati trattati con il protocollo revisionato ottenendo 2 guarigioni.[85]
Il 12 giugno 2011, Precious Reynolds, una bambina di otto anni della Contea di Humboldt, è diventata la terza persona segnalata negli Stati Uniti per essere sopravvissuta alla rabbia senza ricevere la profilassi post-esposizione.[89]
Prognosi
[modifica | modifica wikitesto]Negli esseri umani non vaccinati, dopo che i sintomi neurologici si sono sviluppati, la rabbia ha un tasso di letalità prossimo al 100%: i casi di remissione sono rarissimi.[12] La morte avviene per lo più da 2 a 10 giorni dopo i primi sintomi.
La sopravvivenza è rara, dal momento in cui si manifestano i sintomi, anche con la somministrazione di una corretta e intensiva terapia.[90]
La vaccinazione dopo l'esposizione, solitamente è di grande efficacia nel prevenire la malattia se somministrata tempestivamente, in generale entro 6 giorni dall'infezione. Iniziata con poco o nessun ritardo, la vaccinazione è efficace al 100% contro la rabbia.[83] Nel caso di un ritardo significativo, il trattamento può tuttavia avere ancora possibilità di successo.[56]
5 dei primi 43 pazienti (12%) trattati con il protocollo di Milwaukee sono sopravvissuti e quelli che lo hanno ricevuto sono comunque sopravvissuti più a lungo rispetto a quelli che non lo hanno ricevuto.[91]
Prevenzione
[modifica | modifica wikitesto]Quasi tutti i casi di rabbia che hanno colpito gli esseri umani si sono rivelati fatali, fino a quando nel 1885 fu sviluppato un vaccino grazie a Louis Pasteur e Émile Roux. Il loro vaccino originale fu realizzato grazie a conigli infetti, da cui il virus prelevato dal loro tessuto nervoso veniva indebolito lasciandolo essiccare per cinque-dieci giorni.[92] Vaccini derivati dal tessuto nervoso vengono ancora utilizzati in alcuni paesi, in quanto sono molto più semplici rispetto ai moderni realizzati tramite coltura cellulare.[93]
Il vaccino antirabbico prodotto da cellule umane diploidi è stato creato nel 1967. Oggi sono disponibili vaccini meno costosi provenienti da cellule embrionali di pollo e da cellule Vero purificate.[76]
Un vaccino ricombinante, chiamato V-RG, è stato utilizzato in Belgio, Francia, Germania e negli Stati Uniti al fine di prevenire focolai di rabbia negli animali selvaggi.[94]
La vaccinazione pre-esposizione è praticata sia nelle popolazioni umane che animali, e in molti paesi gli animali domestici sono obbligati ad essere vaccinati.[95]
Nella relazione annuale del 2007 del Dipartimento del Missouri dell'Health and Senior Services Communicable Disease Surveillance si afferma quanto segue al fine di aiutare a ridurre il rischio di contrarre la rabbia:[96]
- vaccinare contro la rabbia cani, gatti e furetti;
- mantenere gli animali domestici sotto supervisione;
- non avere contatti con animali selvatici o randagi;
- contattare un ufficio di controllo degli animali quando si incontra un animale selvatico o randagio, soprattutto se si comporta in modo strano;
- se morso da un animale, lavare la ferita con acqua e sapone per 10-15 minuti e rivolgersi a un medico per verificare se è necessaria la profilassi post-esposizione.
I vecchi vaccini ottenuti da tessuto nervoso, che richiedono iniezioni dolorose nell'addome mediante un ago di grosso calibro, sono poco costose ma sono in via di abbandono per essere sostituite dalle iniezioni intradermiche secondo i consigli dell'Organizzazione Mondiale della Sanità.[76] La vaccinazione deve essere somministrata per via intramuscolare nel deltoide.[97]
Prevenzione negli animali vettori
[modifica | modifica wikitesto]
La vaccinazione obbligatoria degli animali è meno efficace nelle zone rurali. Soprattutto nei paesi in via di sviluppo, gli animali domestici non possono essere controllati e la loro uccisione può essere inaccettabile.
Vaccini orali possono essere distribuiti in modo sicuro come esche, una pratica che ha ridotto con successo la rabbia nelle aree rurali del Canada, della Francia e degli Stati Uniti. A Montréal, Canada, le esche vengono utilizzate con successo sui procioni nella zona del Mont-Royal Park. Le campagne di vaccinazione possono essere costose e l'analisi costi-benefici suggerisce che le esche possano essere un metodo conveniente di controllo.[98] In Ontario, un drastico calo della rabbia è stato registrato quando è stata lanciata una campagna di vaccinazione-esca aerea.[99] In Svizzera, la malattia è stata praticamente debellata dopo che le autorità hanno distribuito nel territorio delle Alpi svizzere teste di pollo con vaccino vivo attenuato.[99] Le volpi, che avevano dimostrato di essere la fonte principale della rabbia nel paese, mangiando queste teste di pollo si sono immunizzate.[99] Attualmente nella Confederazione è prevista la pronta soppressione di eventuali animali selvatici o domestici con la rabbia[100].
L’obbligo del vaccino antirabbico per i cani italiani è decaduto nel 2013 quando il Ministero della Salute ha inoltrato una nota all’ANMVI, dopo il conseguimento per lo Stato italiano dello status di Paese indenne da rabbia, visto che l’ultimo caso accertato risale al 14 febbraio del 2011 individuato in una volpe in Provincia di Belluno.[101]
La rabbia negli animali
[modifica | modifica wikitesto]La rabbia è contagiosa per i mammiferi, dove sono riconosciuti tre stadi clinici.
- La prima fase varia da un periodo da uno a tre giorni ed è caratterizzata da cambiamenti comportamentali ed è conosciuta come la "fase prodromica".
- La seconda è la "fase eccitativa", che dura tre o quattro giorni ed è spesso conosciuto come "rabbia furiosa" per la tendenza dell'animale colpito ad essere iper-reattivo agli stimoli esterni e a mordere le cose vicine.
- La terza è la "fase paralitica" ed è causato da un danno ai motoneuroni. In questo caso si osserva difficoltà nella coordinazione degli arti posteriori, bava alla bocca e difficoltà di deglutizione dovuta a paralisi dei muscoli facciali e della gola.
La morte è solitamente causata da un arresto respiratorio.[102]
Note
[modifica | modifica wikitesto]- ^ https://www.fondazioneveronesi.it/magazine/articoli/da-non-perdere/rabbia-la-malattia-dimenticata-che-si-vince-con-linformazione
- ^ a b c d e f g h i j k l m n o p q (EN, FR, ES, RU, AR, ZH) Rabies Fact Sheet N°99, su World Health Organization, 19 febbraio 2018. URL consultato il 12 agosto 2018.
- ^ a b c Cotran RS, Kumar V e Fausto N, Robbins and Cotran Pathologic Basis of Disease, 7th, Elsevier/Saunders, 2005, p. 1375, ISBN 0-7216-0187-1.
- ^ a b Rabies, Australian bat lyssavirus and other lyssaviruses, su The Department of Health, Dec 2013. URL consultato il 1º marzo 2014.
- ^ a b c Tintinalli, Judith E., Emergency Medicine: A Comprehensive Study Guide (Emergency Medicine (Tintinalli)), McGraw-Hill, 2010, pp. Chapter 152, ISBN 0-07-148480-9.
- ^ William H. Wunner, Rabies: Scientific Basis of the Disease and Its Management, Academic Press, 2010, p. 556, ISBN 978-0-08-055009-1.
- ^ Hemachudha T, Ugolini G, Wacharapluesadee S, Sungkarat W, Shuangshoti S, Laothamatas J, Human rabies: neuropathogenesis, diagnosis, and management., in Lancet neurology, vol. 12, n. 5, maggio 2013, pp. 498-513, DOI:10.1016/s1474-4422(13)70038-3, PMID 23602163.
- ^ a b Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, Abraham J, Adair T, Aggarwal R, etal, Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010., in Lancet, vol. 380, n. 9859, 15 dicembre 2012, pp. 2095-128, DOI:10.1016/S0140-6736(12)61728-0, PMID 23245604.
- ^ WHO Expert Consultation on Rabies : second report. (PDF), 2ª ed., Geneva, WHO, 2013, p. 3, ISBN 978-92-4-120982-3.
- ^ Penang on rabies alert, The Star, 17 settembre 2015. URL consultato il 19 settembre 2015.
- ^ Rabies-Free Countries and Political Units, su CDC. URL consultato il 1º marzo 2014 (archiviato dall'url originale il 5 marzo 2014).
- ^ a b Rabies, su who.int, World Health Organization (WHO), settembre 2011. URL consultato il 31 dicembre 2011.
- ^ "Essential rabies maps".. World Health Organization (WHO).
- ^ a b Harris, Gardiner, Where Streets Are Thronged With Strays Baring Fangs, in New York Times, 6 agosto 2012. URL consultato il 6 agosto 2012.
- ^ Emily Dugan, Dead as a dodo? Why scientists fear for the future of the Asian vulture, in The Independent, London, 30 aprile 2008. URL consultato l'11 ottobre 2008.«India now has the highest rate of human rabies in the world.»
- ^ Medicine challenges Indian superstition.
- ^ Denduangboripant J, Wacharapluesadee S, Lumlertdacha B, Ruankaew N, Hoonsuwan W, Puanghat A, Hemachudha T, Transmission dynamics of rabies virus in Thailand: Implications for disease control (PDF), in BMC Infect Dis, vol. 5, giugno 2005, p. 52, DOI:10.1186/1471-2334-5-52, PMC 1184074, PMID 15985183, 52.
- ^ Bill Schiller, China cracks down on rabid dog menace, in The Toronto Star, 23 luglio 2007.
- ^ Rabies Surveillance Data in the United States, su cdc.gov, Centers for Disease Control and Prevention.
- ^ Rabies in the U.S., su cdc.gov, Centers for Disease Control and Prevention (CDC), 22 aprile 2011. URL consultato il 31 dicembre 2011.
- ^ Simpson DP, Cassell's Latin Dictionary, 5ª ed., London, Cassell, 1979, p. 883, ISBN 0-304-52257-0.
- ^ a b Yolande Rotivel, Introduction, su fas.org, Federation of American Scientists. URL consultato il 25 aprile 2009 (archiviato dall'url originale il 26 aprile 2009).
- ^ Adamson PB, The spread of rabies into Europe and the probable origin of this disease in antiquity, in The Journal of the Royal Asiatic Society of Great Britain and Ireland, vol. 2, n. 2, 1977, pp. 140-4, DOI:10.1017/S0035869X00133829, JSTOR 25210880, PMID 11632333.
- ^ Dunlop 1996.
- ^ Wasik & Murphy, pp. 16-17.
- ^ Wasik & Murphy, pp. 20-21.
- ^ Wasik & Murphy, p. 22.
- ^ Wasik & Murphy, pp. 25-26.
- ^ Baer.
- ^ Wasik & Murphy, pp. 51-52.
- ^ Wasik & Murphy, pp. 58-59.
- ^ Baer, p. 5(EN)
«The first major epizootic in North America was reported in 1768, continuing until 1771 when foxes and dogs carried the disease to swine and domestic animals. The malady was so unusual that it was reported as a new disease»
(IT)«La prima grande epidemia in Nord America fu registrata nel 1768 e continuò fino al 1771 quando volpi e cani portarono il morbo ai maiali e agli animali domestici. I sintomi erano così insoliti che fu segnalata come una nuova malattia»
- ^ https://grandicarnivori.provincia.tn.it/Il-lupo/Il-lupo-e-pericoloso
- ^ https://www.sacromontedivarallo.org/wp/2021/01/08/lassalto-del-lupo/
- ^ The Life and Times of Louis Pasteur, su pyramid.spd.louisville.edu. URL consultato il 30 gennaio 2012 (archiviato dall'url originale il 17 aprile 2013).
- ^ Ker Than, "Zombie Virus" Possible via Rabies-Flu Hybrid?, su National Geographic, National Geographic. URL consultato il 13 settembre 2015.
- ^ World Rabies Day, su who.int, World Health Organization (WHO).
- ^ Wasik & Murphy, pp. 33-36.
- ^ Srinivasan A, Burton EC, Kuehnert MJ, Rupprecht C, Sutker WL, Ksiazek TG, Paddock CD, Guarner J, Shieh WJ, Goldsmith C, Hanlon CA, Zoretic J, Fischbach B, Niezgoda M, El-Feky WH, Orciari L, Sanchez EQ, Likos A, Klintmalm GB, Cardo D, LeDuc J, Chamberland ME, Jernigan DB, Zaki SR, Transmission of rabies virus from an organ donor to four transplant recipients (PDF), in N Engl J Med, vol. 352, n. 11, marzo 2005, pp. 1103-11, DOI:10.1056/NEJMoa043018, PMID 15784663.
- ^ Pawan JL, The transmission of paralytic rabies in Trinidad by the vampire bat (Desmodus rotundus murinus Wagner, in Caribbean Medical Journal, vol. 21, 1959, pp. 110-36, PMID 13858519.
- ^ Pawan JL, Rabies in the vampire bat of Trinidad, with special reference to the clinical course and the latency of infection, in Caribbean Medical Journal, vol. 21, 1959, pp. 137-56, PMID 14431118.
- ^ Taylor PJ, A systematic and population genetic approach to the rabies problem in the yellow mongoose (Cynictis penicillata), in The Onderstepoort Journal of Veterinary Research, vol. 60, n. 4, dicembre 1993, pp. 379-87, PMID 7777324.
- ^ Rabies. Other Wild Animals: Terrestrial carnivores: raccoons, skunks and foxes., su cdc.gov, Centers for Disease Control and Prevention(CDC). URL consultato il 23 dicembre 2010.
- ^ Anderson, Janet; Frey, Rebecca. "Rabies." Gale Encyclopedia of Medicine, 3rd ed. 2006. Encyclopedia.com. 26 Aug. 2015
- ^ McRuer DL, Jones KD, Behavioral and nutritional aspects of the Virginian opossum (Didelphis virginiana), in The veterinary clinics of North America. Exotic animal practice, vol. 12, n. 2, maggio 2009, pp. 217–36, viii, DOI:10.1016/j.cvex.2009.01.007, PMID 19341950.
- ^ Shannon LM, Poulton JL, Emmons RW, Woodie JD, Fowler ME, Serological survey for rabies antibodies in raptors from California, in J. Wildl. Dis., vol. 24, n. 2, aprile 1988, pp. 264-7, DOI:10.7589/0090-3558-24.2.264, PMID 3286906.
- ^ Gough PM, Jorgenson RD, Rabies antibodies in sera of wild birds, in Journal of Wildlife Diseases, vol. 12, n. 3, 1976, pp. 392-5, DOI:10.7589/0090-3558-12.3.392, PMID 16498885.
- ^ Jorgenson RD, Gough PM, Experimental rabies in a great horned owl, in J. Wildl. Dis., vol. 12, n. 3, luglio 1976, pp. 444-7, DOI:10.7589/0090-3558-12.3.444.
- ^ Derek Wong, Rabies, su virology-online.com, Wong's Virology. URL consultato il 19 marzo 2009.
- ^ James B. Campbell e K.M. Charlton, Developments in Veterinary Virology: Rabies, Springer, 1988, p. 48, ISBN 0-89838-390-0.
- ^ a b c Drew WL, Chapter 41: Rabies, in Ryan KJ, Ray CG (editors) (a cura di), Sherris Medical Microbiology, 4th, McGraw Hill, 2004, pp. 597.–600, ISBN 0-8385-8529-9.
- ^ Finke S, Conzelmann KK, Replication strategies of rabies virus, in Virus Res., vol. 111, n. 2, agosto 2005, pp. 120-31, DOI:10.1016/j.virusres.2005.04.004, PMID 15885837.
- ^ The Merck Manual, 11th Edition (1983), p. 183
- ^ The Merck manual of Medical Information. Second Home Edition, (2003), p. 484.
- ^ Jenny Turton, Rabies: a killer disease, su nda.agric.za, National Department of Agriculture, 2000. URL consultato l'11 ottobre 2015 (archiviato dall'url originale il 23 settembre 2006).
- ^ a b c d e f Rabies Post-Exposure Prophylaxis, su cdc.gov, Centers for Disease Control and Prevention (CDC), 23 dicembre 2009. URL consultato il 30 gennaio 2010 (archiviato dall'url originale il 1º febbraio 2010).
- ^ Jackson, Alan C., Wunner, William H., Rabies, Academic Press, 2002, p. 290, ISBN 978-0-12-379077-4.
- ^ http://www.plospathogens.org/article/info%3Adoi%2F10.1371%2Fjournal.ppat.1004348
- ^ Joanne Lynn, M.D. (October 1997) Transverse Myelitis: Symptoms, Causes and Diagnosis (archiviato dall'url originale il 15 settembre 2012). The Transverse Myelitis Association
- ^ Larry Ernest Davis, Molly K. King e Jessica L. Schultz, Fundamentals of neurologic disease, Demos Medical Publishing, 15 giugno 2005, p. 73, ISBN 978-1-888799-84-2.
- ^ Schoenstadt A, Rabies Symptoms, su rabies.emedtv.com, eMedTV, 21 luglio 2008. URL consultato il 30 gennaio 2010.
- ^ www.treccani.it.
- ^ a b Symptoms of rabies, su NHS.uk, 12 giugno 2012. URL consultato il 3 settembre 2014.
- ^ Andrew Cliff, Peter Haggett, Matthew Smallman-Raynor, World atlas of epidemic diseases, London, Arnold, 2004, p. 51, ISBN 978-0-340-76171-7.
- ^ Copia archiviata, su animalswecare.com. URL consultato il 3 settembre 2014 (archiviato dall'url originale il 3 settembre 2014).
- ^ D.J. Dean e M.K. Abelseth, Ch. 6: The fluorescent antibody test, in M.M. Kaplan e H. Koprowski (a cura di), Laboratory techniques in rabies, Monograph series, vol. 23, 3rd, World Health Organization, 1973, p. 73.
- ^ a b Fooks AR, Johnson N, Freuling CM, Wakeley PR, Banyard AC, McElhinney LM, Marston DA, Dastjerdi A, Wright E, Weiss RA, Müller T, Emerging technologies for the detection of rabies virus: challenges and hopes in the 21st century, in PLoS Neglected Tropical Diseases, vol. 3, n. 9, 2009, pp. e530, DOI:10.1371/journal.pntd.0000530, PMC 2745658, PMID 19787037.
- ^ N Tordo, H Bourhy e D Sacramento, Ch. 10: PCR technology for lyssavirus diagnosis, in J.P. Clewley (a cura di), The Polymerase Chain Reaction (PCR) for Human Viral Diagnosis, CRC Press, 1994, pp. 125-145, ISBN 978-0-8493-4833-4.
- ^ David D, Yakobson B, Rotenberg D, Dveres N, Davidson I, Stram Y, Rabies virus detection by RT-PCR in decomposed naturally infected brains, in Veterinary Microbiology, vol. 87, n. 2, 2002, pp. 111-8, DOI:10.1016/s0378-1135(02)00041-x, PMID 12034539.
- ^ Biswal M, Ratho R, Mishra B, Usefulness of reverse transcriptase-polymerase chain reaction for detection of rabies RNA in archival samples, in Japanese Journal of Infectious Diseases, vol. 60, n. 5, settembre 2007, pp. 298-9, PMID 17881871.
- ^ Dürr S, Naïssengar S, Mindekem R, Diguimbye C, Niezgoda M, Kuzmin I, Rupprecht CE, Zinsstag J, Rabies diagnosis for developing countries, in Sarah Cleaveland (a cura di), PLoS Neglected Tropical Diseases, vol. 2, n. 3, 2008, pp. e206, DOI:10.1371/journal.pntd.0000206, PMC 2268742, PMID 18365035, e206. URL consultato il 23 settembre 2023 (archiviato dall'url originale il 19 febbraio 2020).
- ^ Cynthia M. Kahn, BA, MA (a cura di), The Merck Veterinary Manual, 10th, Kendallville, Indiana, Courier Kendallville, Inc, 2010, p. 1193, ISBN 0-911910-93-X.
- ^ Rabies: Differential Diagnoses & Workup, su eMedicine Infectious Diseases, 3 ottobre 2008. URL consultato il 30 gennaio 2010.
- ^ Taylor DH, Straw BE, Zimmerman JL, D'Allaire S, Diseases of swine, Oxford, Blackwell, 2006, pp. 463-5, ISBN 0-8138-1703-X. URL consultato il 30 gennaio 2010.
- ^ Alireza Minagar e J. Steven Alexander, Inflammatory Disorders Of The Nervous System: Pathogenesis, Immunology, and Clinical Management, Humana Press, 2005, ISBN 1-58829-424-2.
- ^ a b c Ly S, Buchy P, Heng NY, Ong S, Chhor N, Bourhy H, Vong S, Rabies situation in Cambodia, in Hélène Carabin (a cura di), PLoS Neglected Tropical Diseases, vol. 3, n. 9, 2009, pp. e511, DOI:10.1371/journal.pntd.0000511, PMC 2731168, PMID 19907631, e511 (archiviato dall'url originale il 5 luglio 2020).
- ^ Rabies & Australian bat lyssavirus information sheet, su health.vic.gov.au. URL consultato il 30 gennaio 2012 (archiviato dall'url originale il 18 agosto 2011).
- ^ National Centre for Disease Control, National Guidelines on Rabies Prophylaxis (PDF), su nicd.nic.in, 2014. URL consultato il 5 settembre 2014 (archiviato dall'url originale il 5 settembre 2014).
- ^ "Use of a Reduced (4-Dose) Vaccine Schedule for Postexposure Prophylaxis to Prevent Human Rabies" (PDF).. Centers for Disease Control and Prevention (CDC).
- ^ Park's textbook of Community medicine,22nd edition, 2013,p 254
- ^ De Serres G, Skowronski DM, Mimault P, Ouakki M, Maranda-Aubut R, Duval B, Bats in the bedroom, bats in the belfry: Reanalysis of the rationale for rabies post-exposure prophylaxis, in Clin Infect Dis, vol. 48, n. 11, 2009, pp. 1493-9, DOI:10.1086/598998, PMID 19400689.
- ^ Despond O, Tucci M, Decaluwe H, Grégoire MC, S Teitelbaum J, Turgeon N, Rabies in a nine-year-old child: The myth of the bite, in Can J Infect Dis, vol. 13, n. 2, marzo 2002, pp. 121-5, PMC 2094861, PMID 18159381.
- ^ a b c Jordan Lite, Medical Mystery: Only One Person Has Survived Rabies without Vaccine—But How?, in Scientific American, 8 ottobre 2008. URL consultato il 30 gennaio 2010.
- ^ Lockhart BP, Tordo N, Tsiang H, Inhibition of rabies virus transcription in rat cortical neurons with the dissociative anesthetic ketamine, in Antimicrob Agents Chemother, vol. 36, n. 8, 1992, pp. 1750-5, DOI:10.1128/AAC.36.8.1750, PMC 192041, PMID 1416859.
- ^ a b Willoughby RE, Are we getting closer to the treatment of rabies?: medical benchmarks, in Future Virology, vol. 4, n. 6, MedScape, 2009, pp. 563-70, DOI:10.2217/fvl.09.52.
- ^ Willoughby RE, Tieves KS, Hoffman GM, Ghanayem NS, Amlie-Lefond CM, Schwabe MJ, Chusid MJ, Rupprecht CE, Survival after treatment of rabies with induction of coma (PDF), in New England Journal of Medicine, vol. 352, n. 24, giugno 2005, pp. 2508-14, DOI:10.1056/NEJMoa050382, PMID 15958806.
- ^ Hu WT, Willoughby RE, Dhonau H, Mack KJ, Long-term follow-up after treatment of rabies by induction of coma (PDF), in New England Journal of Medicine, vol. 357, n. 9, agosto 2007, pp. 945-6, DOI:10.1056/NEJMc062479, PMID 17761604.
- ^ Rodney Versus Death, su radiolab.org, Radiolab, 13 agosto 2013.
- ^ UC Davis Children's Hospital patient becomes third person in US to survive rabies, in Health News, 12 giugno 2011. URL consultato il 12 giugno 2011.
- ^ Rupprecht CE, Willoughby R, Slate D, Current and future trends in the prevention, treatment and control of rabies, in Expert Review of Anti-infective Therapy, vol. 4, n. 6, 2006, pp. 1021-38, DOI:10.1586/14787210.4.6.1021, PMID 17181418.
- ^ Rabies Registry, su mcw.edu, Medical College of Wisconsin, 2005. URL consultato il 29 dicembre 2009.
- ^ Geison GL, Pasteur's work on rabies: Reexamining the ethical issues, in Hastings Center Report, vol. 8, n. 2, aprile 1978, pp. 26-33, DOI:10.2307/3560403, JSTOR 3560403, PMID 348641.
- ^ Srivastava AK, Sardana V, Prasad K, Behari M, Diagnostic dilemma in flaccid paralysis following anti-rabies vaccine, in Neurol India, vol. 52, n. 1, marzo 2004, pp. 132-3, PMID 15069272.
- ^ Reece JF, Chawla SK, Control of rabies in Jaipur, India, by the sterilisation and vaccination of neighbourhood dogs, in Vet Rec, vol. 159, n. 12, 2006, pp. 379-83, DOI:10.1136/vr.159.12.379, PMID 16980523.
- ^ Compendium of Animal Rabies Prevention and Control (PDF), su nasphv.org, National Association of State Public Health Veterinarians, 31 dicembre 2007. URL consultato il 3 gennaio 2010 (archiviato dall'url originale il 12 luglio 2010).
- ^ (EN) 2007 Annual Report (PDF), su dhss.mo.gov, Bureau of Communicable Disease Control and Prevention, 2007. URL consultato l'11 ottobre 2015 (archiviato dall'url originale l'11 maggio 2020).
- ^ Rabies, su who.int, World Health Organization. URL consultato il 1º febbraio 2015.
- ^ Meltzer MI, Assessing the costs and benefits of an oral vaccine for raccoon rabies: a possible model, in Emerg Infect Dis, vol. 2, n. 4, ottobre–December 1996, pp. 343-9, DOI:10.3201/eid0204.960411, PMC 2639934, PMID 8969251.
- ^ a b c Rebecca L Grambo, The World of the Fox, Vancouver, Greystone Books, 1995, pp. 94.–5, ISBN 0-87156-377-0.
- ^ https://www.blv.admin.ch/blv/it/home/tiere/tierseuchen/uebersicht-seuchen/alle-tierseuchen/tollwut.html
- ^ anmvi.it, https://www.anmvi.it/2013/139-decaduto-l-obbligo-di-antirabbica-in-italia-la-profilassi-resta-consigliata.html.
- ^ Ettinger, Stephen J. e Feldman, Edward C., Textbook of Veterinary Internal Medicine, 4th, W.B. Saunders Company, 1995, ISBN 0-7216-6795-3.
Bibliografia
[modifica | modifica wikitesto]- (EN) Bill Wasik e Monica Murphy, Rabid: a Cultural History of the World's Most Diabolical Virus, New York, Viking Press, 2012.
- (EN) Cotran RS, Kumar V e Fausto N, Robbins and Cotran Pathologic Basis of Disease, 7th, Elsevier/Saunders, 2005, ISBN 0-7216-0187-1.
- (EN) Tintinalli, Judith E., Emergency Medicine: A Comprehensive Study Guide (Emergency Medicine (Tintinalli)), McGraw-Hill, 2010, ISBN 0-07-148480-9.
- (EN) William H. Wunner, Rabies: Scientific Basis of the Disease and Its Management, Academic Press, 2010, ISBN 978-0-08-055009-1.
- (EN) WHO Expert Consultation on Rabies : second report., 2ª ed., Geneva, WHO, 2013, ISBN 978-92-4-120982-3.
- (EN) Rebecca L Grambo, The World of the Fox, Vancouver, Greystone Books, 1995, pp. 94.–5, ISBN 0-87156-377-0.
- (EN) Simpson DP, Cassell's Latin Dictionary, 5ª ed., London, Cassell, 1979, ISBN 0-304-52257-0.
- (EN) Robert H. Dunlop e Williams, David J., Veterinary Medicine: An Illustrated History, Mosby, 1996, ISBN 0-8016-3209-9.
- (EN) George Baer, The Natural History of Rabies, CRC Press, 1991, ISBN 978-0-8493-6760-1.
- (EN) Andrew Cliff, Peter Haggett, Matthew Smallman-Raynor, World atlas of epidemic diseases, London, Arnold, 2004, ISBN 978-0-340-76171-7.
- (EN) Drew WL, Chapter 41: Rabies, in Ryan KJ, Ray CG (editors) (a cura di), Sherris Medical Microbiology, 4th, McGraw Hill, 2004, pp. 597.–600, ISBN 0-8385-8529-9.
- (EN) James B. Campbell e K.M. Charlton, Developments in Veterinary Virology: Rabies, Springer, 1988, ISBN 0-89838-390-0.
- (EN) Jackson, Alan C., Wunner, William H., Rabies, Academic Press, 2002, ISBN 978-0-12-379077-4.
- (EN) Larry Ernest Davis, Molly K. King e Jessica L. Schultz, Fundamentals of neurologic disease, Demos Medical Publishing, 15 giugno 2005, ISBN 978-1-888799-84-2.
- (EN) Cynthia M. Kahn, BA, MA (a cura di), The Merck Veterinary Manual, 10th, Kendallville, Indiana, Courier Kendallville, Inc, 2010, p. 1193, ISBN 0-911910-93-X.
- (EN) D.J. Dean e M.K. Abelseth, Ch. 6: The fluorescent antibody test, in M.M. Kaplan e H. Koprowski (a cura di), Laboratory techniques in rabies, Monograph series, vol. 23, 3rd, World Health Organization, 1973.
- (EN) N Tordo, H Bourhy e D Sacramento, Ch. 10: PCR technology for lyssavirus diagnosis, in J.P. Clewley (a cura di), The Polymerase Chain Reaction (PCR) for Human Viral Diagnosis, CRC Press, 1994, ISBN 978-0-8493-4833-4.
- (EN) Taylor DH, Straw BE, Zimmerman JL, D'Allaire S, Diseases of swine, Oxford, Blackwell, 2006, ISBN 0-8138-1703-X.
- (EN) Alireza Minagar e J. Steven Alexander, Inflammatory Disorders Of The Nervous System: Pathogenesis, Immunology, and Clinical Management, Humana Press, 2005, ISBN 1-58829-424-2.
- (EN) Ettinger, Stephen J. e Feldman, Edward C., Textbook of Veterinary Internal Medicine, 4th, W.B. Saunders Company, 1995, ISBN 0-7216-6795-3.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikizionario contiene il lemma di dizionario «rabbia»
Wikizionario contiene il lemma di dizionario «rabbia» Wikimedia Commons contiene immagini o altri file sulla rabbia
Wikimedia Commons contiene immagini o altri file sulla rabbia
Collegamenti esterni
[modifica | modifica wikitesto]- rabbia, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- (EN) rabies, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Rabbia. su epicentro.iss.it.
- Scheda tecnica della malattia e materiale divulgativo. sul sito dell' Istituto Zooprofilattico Sperimentale delle Venezie.
- Scheda sulla rabbia. URL consultato il 4 aprile 2018 (archiviato dall'url originale il 15 gennaio 2008).su
- msd-italia.it. URL consultato il 28 luglio 2019 (archiviato dall'url originale il 20 febbraio 2009).su msd-italia.it.
- (EN) sito ufficiale. URL consultato il 23 ottobre 2017 (archiviato dall'url originale il 21 aprile 2013).sul sito ufficiale. dei Centers for Disease Control and Prevention
- https://www.who-rabies-bulletin.org/. del WHO Europe
| Controllo di autorità | Thesaurus BNCF 38723 · LCCN (EN) sh85110217 · GND (DE) 4185630-2 · BNF (FR) cb11972175z (data) · J9U (EN, HE) 987007555691105171 · NDL (EN, JA) 00567222 |
|---|