Dissecazione aortica
| Dissezione aortica | |
|---|---|
 | |
| Specialità | chirurgia vascolare |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 441.0 |
| ICD-10 | I71.0 |
| OMIM | 607086 |
| MeSH | D000784 |
| MedlinePlus | 000181 |
| eMedicine | 756835 |
| GeneReviews | Panoramica |
| Sinonimi | |
| Dissezione aortica Dissezione dell'aorta Dissecazione dell'aorta | |
La dissezione o dissecazione aortica è una malattia vascolare relativamente rara, gravata da un'alta mortalità se non trattata con chirurgia d'urgenza.[1] Si verifica quando una lesione dello strato più interno della aorta consente al sangue di fluire tra gli strati della parete aortica, costringendoli a separarsi. Si viene così a verificare uno slaminamento della tonaca intima del vaso con formazione di un secondo lume detto "falso lume".[2]
Nella maggior parte dei casi la dissecazione si associa alla comparsa di un improvviso e grave dolore toracico anteriore (ma talvolta anche al dorso), spesso descritto dai pazienti come un dolore dalle caratteristiche laceranti.[3][4] Molti pazienti riferiscono altri sintomi come vomito, sudorazione profusa e vertigini. Altri sintomi possono derivare dal diminuito afflusso di sangue ad altri organi: si verificano con relativa frequenza sintomi neurologici, fra cui l'ictus,[5][6][7] oppure l'ischemia mesenterica.[8][9] La dissezione aortica può portare rapidamente alla morte del paziente a causa di un insufficiente flusso sanguigno al cuore o per una rottura dell'aorta stessa.
La dissezione aortica è più comune nei soggetti con una storia di ipertensione, in pazienti con alcune particolari malattie del tessuto connettivo che interessano la parete dei vasi sanguigni e ne causano un indebolimento strutturale (come la sindrome di Marfan),[10][11] in chi ha una valvola aortica bicuspide e nei soggetti in precedenza sottoposti ad un intervento chirurgico al cuore.[2]
Un trauma maggiore, l’abitudine al fumo di tabacco, l’assunzione di cocaina,[12][13] lo stato di gravidanza,[14] una diagnosi di aneurisma dell'aorta toracica, una vasculite con interessamento delle arterie e livelli lipidici anormali sono tutti fattori associati a un aumento del rischio.[3]
La diagnosi è sospettata in base ai sintomi accusati dal paziente e confermata dall'esecuzione di imaging radiologico (ecografia addominale oppure TAC addome o RMN); questi esami, oltre che per conferma diagnostica, sono utilizzati anche per una migliore definizione di sede ed estensione della dissezione. I due tipi principali di dissecazione sono il tipo A di Stanford (coinvolgimento della prima parte dell'aorta) e il tipo B (assenza di coinvolgimento).[3]
La prevenzione della patologia si basa su un buon controllo della pressione sanguigna e sulla cessazione del fumo di sigaretta. Il trattamento della dissezione aortica dipende da quale parte dell'aorta è stata coinvolta. La chirurgia è solitamente necessaria per le dissecazioni che coinvolgono la prima parte dell'aorta; al contrario le dissecazioni che non coinvolgono l'aorta ascendente possono anche essere trattate con farmaci che riducono la pressione arteriosa e la frequenza cardiaca, a meno che non si verifichino complicanze.
Il trattamento chirurgico può essere eseguito a cielo aperto (con un'incisura che comporta l'apertura del torace) o ricorrendo a un intervento riparativo di aneurisma per via endovascolare (si infila protesi vascolare nella sacca aneurismatica passando per l'arteria femorale).
La dissecazione aortica è un evento relativamente raro e si verifica a un tasso stimato di 3 per 100.000 persone all'anno.[2][3] È più comune nei soggetti di sesso maschile che nelle femmine.[3] Tipicamente l'età al momento della diagnosi è di 63 anni, con circa il 10% dei casi che si verificano prima del compimento dei 40 anni.[2] Senza trattamento, circa la metà delle persone con morfologia di tipo A muore entro tre giorni e circa il 10% delle persone con morfologia di tipo B muore entro un mese.
Classificazione[modifica | modifica wikitesto]

|
|

| |
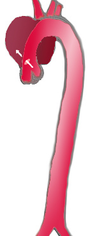
| Percentuale | 60% | 10–15% | 25–30% |
| Tipologia | DeBakey I | DeBakey II | DeBakey III |
| Stanford A (Prossimale) | Stanford B (Distale) | ||
Sono stati utilizzati diversi sistemi di classificazione per descrivere la dissecazione aortica.
Una classificazione di uso frequente si basa sul criterio temporale, e cioè sulla durata dell'esordio dei sintomi prima della presentazione: le dissecazioni aortiche sono etichette come iperacute (durata minore di 24 ore), acute (2-7 giorni), subacute (8-30 giorni) e croniche (maggiore di 30 giorni).[15]
Altri sistemi di classificazione comunemente in uso si basano sulla localizzazione anatomica dove si manifesta tale patologia (in particolare aorta ascendente o quella discendente). Il sistema Stanford è probabilmente quello oggi più comunemente utilizzato, poiché è più in sintonia con la gestione del paziente.
- DeBakey
Il sistema DeBakey (dal nome del cardiochirurgo toracico Michael E. DeBakey) fornisce una descrizione anatomica della dissecazione aortica. Classifica la dissecazione in base a dove si trova la lacerazione intimale originale e in base all'estensione della dissezione (localizzazione nell'aorta ascendente o nell'aorta discendente oppure coinvolgimento sia dell'aorta ascendente che discendente.[16]
- Tipo I – nasce nell'aorta ascendente e si estende (coinvolge l’aorta ascendente, l’arco aortico e l’aorta toracica). Si osserva più spesso in pazienti con meno di 65 anni di età ed è la forma più letale della malattia.
- Tipo II – origina ed è confinata nell'aorta ascendente
- Tipo III – coinvolge l’aorta discendente distalmente all’origine dell’arteria succlavia. Osservabile più spesso in pazienti anziani affetti da aterosclerosi e ipertensione arteriosa.
- Tipo IIIa – limitato all'aorta discendente toracica
- Tipo IIIb – coinvolge l'aorta toracica e addominale
- Stanford
La classificazione di Stanford è divisa in due gruppi, A e B, a seconda dell'interessamento o meno dell'aorta ascendente.[17]
- Tipo A – (prossimale o ascendente) è coinvolta l'aorta ascendente e/o l'arco aortico, potendosi estendersi verso l'aorta discendente. Comprende i tipi DeBakey I e II.
- Tipo B – (distale o discendente) è coinvolta l'aorta discendente distalmente all'arteria succlavia sinistra con o senza estensione distale. Include il tipo DeBakey III.
- Descrittivo
- Prossimale – Tipo I e II di DeBakey e Tipo A di Stanford
- Distale – Tipo III DeBakey e Tipo B di Stanford
La classificazione di Stanford è utile in quanto segue la pratica clinica: infatti le dissezioni ascendenti dell'aorta di tipo A generalmente richiedono un trattamento chirurgico primario; al contrario alle dissezioni di tipo B generalmente viene riservato un trattamento farmacologico (morfina, betabloccanti e vasodilatatori arteriosi), almeno inizialmente, mentre l'intervento chirurgico è riservato a eventuali complicanze. La ragione per cui si interviene chirurgicamente nella riparazione delle dissecazioni di tipo A, è che le dissecazioni aortiche ascendenti spesso coinvolgono la valvola aortica, la quale, avendo perso il supporto sospensivo, si spinge verso la radice aortica, causando così insufficienza aortica. La valvola deve così essere risospesa e adeguatamente riposizionata, così come spesso è necessario riparare eventuali lesioni a carico dell'arteria coronaria.
Inoltre, l'area coinvolta nella dissecazione viene rimossa e sostituita con un innesto di Dacron, al fine di impedire che si verifichi un'ulteriore dissezione. Infine, si tenga presente che le dissezioni di tipo B raramente hanno un'evoluzione migliore, dal punto di vista della mortalità, se sono sottoposte ad intervento chirurgico, a meno che non si verifichino rotture o compromissioni di altri organi, ad esempio i reni.
Circa il 70% delle dissecazioni avviene nel tratto ascendente, che è anche il punto più pericoloso per la sopravvivenza del paziente.
Sintomatologia[modifica | modifica wikitesto]
Circa il 96% dei soggetti con dissecazione aortica si presenta al medico accusando un dolore severo con esordio improvviso, spesso in pieno benessere (cosiddetto dolore "a colpo di pugnale").[18][19] Il dolore può essere descritto come una sensazione lacerante, lancinante o acuta. Il 17% degli individui ha la sensazione che il dolore si stia spostando mentre la dissecazione si estende lungo l'aorta (si parla di dolore toracico "migrante"). La localizzazione del dolore è associata alla localizzazione della dissecazione. Il dolore toracico anteriore o in sede precordiale è associato a dissecazioni che coinvolgono l'aorta ascendente, mentre il dolore interscapolare (dorsale) è associato a dissecazioni aortiche che colpiscono l'aorta discendente. Se il dolore è di natura pleuritica, può suggerire una pericardite acuta causata dall'emorragia nel sacco pericardico. Questa è un'eventualità particolarmente pericolosa, e deve essere temuto l'imminente instaurarsi di un tamponamento cardiaco acuto.
Il tamponamento pericardico è la causa più comune di morte per la dissecazione aortica.[20] Mentre il dolore può essere confuso con quello che in genere si associa a una sindrome coronarica acuta (attacco cardiaco), la dissecazione aortica di solito non è associata con gli altri segni che suggeriscono un infarto del miocardio (ad esempio cambiamenti dell'ECG. Tuttavia nell'evoluzione della patologia è possibile che insorgano sintomi suggestivi di insufficienza cardiaca congestizia.
Più raramente, ma è possibile che alcuni individui non presentino dolore, o più spesso siano paucisintomatici: questi soggetti hanno in genere una dissecazione aortica cronica.
Sintomi meno comuni che possono essere osservati nel contesto della dissecazione aortica comprendono la già citata insufficienza cardiaca congestizia (7%), la sincope (9%), l'ictus (6%), la neuropatia periferica da ischemia, la paraplegia e l'arresto cardiaco.[21] Se un soggetto con dissecazione aortica si è presentato riferendo un episodio di sincope, in circa il 50% dei casi ciò è dovuto a un sanguinamento nel sacco pericardio, che ha causato un tamponamento pericardico.
Le complicanze neurologiche della dissecazione aortica (ad esempio l'ictus o la plegia) sono in genere dovute al coinvolgimento di una o più arterie che irrorano una particolare zona del sistema nervoso centrale.
Se la dissecazione si estende sino al seno coronario si potrà instaurare una condizione di ischemia miocardica che, se non trattata immediatamente, potrebbe portare a infarto del miocardio. Altro segno utile ai fini diagnostici, benché piuttosto incostante, è un soffio da insufficienza aortica (riconducibile alla modificazione emodinamica instauratasi in aorta).
Se la dissezione aortica coinvolge l'aorta addominale, è possibile che siano compromessi anche alcuni dei rami di questo vaso. Nelle dissecazioni aortiche addominali, la compromissione di una o entrambe le arterie renali si verifica nel 5-8% dei casi, mentre l'ischemia mesenterica (ischemia dell'intestino) si verifica in circa il 3% dei soggetti.[8][9]
Pressione arteriosa[modifica | modifica wikitesto]
I pazienti affetti da dissecazione aortica hanno spesso una storia di ipertensione arteriosa. La pressione arteriosa dei soggetti che si presentano con dissecazione aortica acuta è abbastanza variabile e tende ad essere più elevata negli individui che hanno una dissecazione distale. Nei soggetti con una dissecazione aortica prossimale, il 36% circa si presenta con ipertensione, mentre il 25% si presenta invece con ipotensione. La dissecazione aortica prossimale tende a essere maggiormente associate all'indebolimento della parete vascolare a causa della degenerazione cistica mediale. In coloro che presentano una dissezione aortica distali (tipo B), il 60-70% si presenta con ipertensione, mentre il 2-3% si presenta con una bassa pressione arteriosa.[22]
Una grave ipotensione al momento della presentazione del paziente in una struttura sanitaria è un grave indicatore prognostico. Di solito è associata a una situazione di tamponamento pericardico, una grave insufficienza aortica o una rottura dell'aorta. La misurazione accurata della pressione arteriosa è importante. La pseudoipotensione (una misurazione della pressione sanguigna falsamente bassa) può verificarsi a causa del coinvolgimento dell'arteria brachiocefalica (che irrora il braccio destro) o dell'arteria succlavia sinistra (che fornisce il braccio sinistro).
Insufficienza aortica[modifica | modifica wikitesto]
L'insufficienza aortica (AI) si verifica nel 50% e fino al 66% delle dissecazioni aortiche ascendenti: a livello auscultatorio il soffio diastolico dovuto all'insufficienza aortica è udibile in circa il 32% delle dissecazioni prossimali. L'intensità (loudness) del soffio dipende dalla pressione del sangue, pertanto potrebbe non essere udibile in caso di bassa pressione arteriosa. Esistono molteplici cause possibili per il verificarsi di insufficienza aortica (AI) in caso di dissecazione aortica ascendente. La dissecazione può dilatare l'annulus della valvola aortica, in modo tale che i lembi della valvola non possono più giustapporsi. Un altro meccanismo possibile è che la dissecazione può estendersi nella radice aortica e provocare il distacco dei lembi della valvola stessa. Un ulteriore possibile meccanismo è associato ad una vasta lacerazione intimale: in questo caso il lembo intimale potrebbe prolassare nel tratto di efflusso del ventricolo sinistro, causando un'invaginazione dell'intima nella valvola aortica e impedendo così la corretta chiusura della valvola.
Infarto del miocardio[modifica | modifica wikitesto]
L'infarto del miocardio si verifica nell'1-2% delle dissecazioni aortiche. La causa dell'infarto è generalmente il coinvolgimento delle arterie coronarie, che riforniscono il cuore con sangue ossigenato, nella dissecazione. L'arteria coronaria destra è coinvolta più spesso rispetto all'arteria coronaria sinistra. Se l'infarto miocardico viene trattato con terapia trombolitica, la mortalità aumenta oltre il 70%, principalmente a causa del sanguinamento che si viene a verificare nel sacco pericardico e che causa tamponamento cardiaco. Poiché i soggetti con dissecazione aortica si presentano spesso al pronto soccorso con una sintomatologia simile a quella di un infarto miocardico, il medico d'emergenza-urgenza deve fare attenzione a fare la diagnosi corretta prima di iniziare il trattamento specifico per l'infarto, poiché il regime di trattamento per questa patologia può essere letale per un individuo che presenta invece una dissecazione aortica.
Versamento pleurico[modifica | modifica wikitesto]
Un versamento pleurico (ovvero una raccolta di liquido nello spazio pleurico, compreso tra i polmoni e la parete toracica o il diaframma) può essere presente nei soggetti con dissecazione aortica ed è dovuto sia al sangue che può derivare da una lacerazione transitoria dell'aorta, sia per la raccolta di fluido secondaria ad una reazione infiammatoria intorno all'aorta. Se un versamento pleurico dovesse svilupparsi a causa di una dissecazione aortica, ciò avviene più comunemente nell'emitorace sinistro piuttosto che nell'emitorace destro.
Eziologia[modifica | modifica wikitesto]

La dissecazione aortica è associata a ipertensione arteriosa (circa il 72-80% delle persone che presentano una dissecazione aortica hanno una precedente storia di ipertensione arteriosa) e molti disturbi del tessuto connettivo. Una forma di vasculite (un processo infiammatorio a carico di un'arteria) può talvolta, sia pure raramente, associarsi a una dissecazione aortica. Questa malattia in una minoranza di casi può anche essere il risultato di un trauma toracico. L'uso di droghe illecite con stimolanti (ad esempio cocaina[12][13] e metanfetamina) rappresenta un ulteriore fattore di rischio modificabile per la dissecazione aortica. Questa in alcuni individui sembra possa essere anche associata al fumo di tabacco.
Una valvola aortica bicuspide (una rara forma di anomalie congenita cardiovascolare che coinvolge la valvola aortica) si trova nel 7-14% delle persone che hanno una dissecazione aortica. Questi individui sono particolarmente portati a sviluppare una dissecazione a carico dell'aorta ascendente. Il rischio di dissecazione in soggetti con valvola aortica bicuspide non è invece associato al grado di stenosi della valvola.
Alcuni disturbi del tessuto connettivo come la Sindrome di Marfan,[10][11] la Sindrome di Ehlers-Danlos,[23] e la sindrome di Loeys-Dietz aumentano il rischio di dissecazione aortica.[22] Similmente alcune vasculiti come l'arterite di Takayasu, l'arterite a cellule giganti, la poliarterite nodosa e la malattia di Behçet sono state associate alla possibilità di sviluppo di una successiva dissecazione aortica.[15][22] La sindrome di Marfan si trova nel 5-9% delle persone che hanno avuto una dissecazione aortica. In questo sottogruppo, l'incidenza nei giovani individui è aumentata. Gli individui con sindrome di Marfan tendono ad avere aneurismi dell'aorta e sono più inclini a dissecazioni prossimali dell'aorta.[10]
Anche altre sindromi congenite come la Turner,[24][25] e la Noonan,[26] si associano ad un aumentato rischio di dissecazione aortica, in genere a seguito di una dilatazione della radice aortica.
Il trauma toracico che può comportare una dissecazione aortica può essere diviso in due gruppi, distinti in base alla causa: trauma toracico chiuso (di osservazione comune dopo un incidente automobilistico) e il trauma toracico iatrogeno (associato a procedure chirurgiche o di cardiologia interventistica). Le cause iatrogene comprendono i traumi che si verificano durante le procedure di cateterismo cardiaco o correlate al gonfiaggio di un palloncino intra-aortico.
La dissecazione aortica può essere una conseguenza tardiva della chirurgia cardiaca. Circa il 18% delle persone che presentano una dissecazione acuta aortica ha una storia personale di intervento chirurgico a cuore aperto. Gli individui sottoposti a sostituzione della valvola aortica per insufficienza aortica sono particolarmente a rischio perché l'insufficienza aortica comporta un aumento del flusso sanguigno nell'aorta ascendente. Ciò può causare dilatazione e indebolimento delle pareti dell'aorta ascendente.
La sifilide nella sua fase terziaria può potenzialmente causare una dissecazione aortica.
Fisiopatologia[modifica | modifica wikitesto]

Come tutte le altre arterie, l'aorta è composta da tre strati, l'intima, la media e l'avventizia. L'intima è in contatto diretto con il sangue all'interno del vaso e consiste principalmente in uno strato di cellule endoteliali che poggiano su una membrana basale; la tonaca media è costituita principalmente da tessuto connettivo e muscolare e il vaso è protetto all'esterno dalla tonaca avventizia, comprendente anch'essa del tessuto connettivo.[27] Nella dissecazione aortica, il sangue penetra nell'intima ed entra nello strato medio. L'alta pressione viene a lacerare il tessuto di supporto della tonaca media slaminando i due terzi interni e dividendoli dalla avventizia, cioè dal terzo di supporto esterno.[28] Questo evento può propagarsi lungo la lunghezza dell'aorta per una distanza variabile, in avanti o all'indietro. Le dissecazioni che si propagano verso la biforcazione iliaca (seguendo cioè con il flusso di sangue) sono dette dissecazioni anterograde e quelle che si propagano verso la radice aortica (opposte al flusso del sangue) sono dette dissecazioni retrograde.
La lacerazione iniziale di solito si verifica entro 100 mm dalla valvola aortica: ne consegue che una dissecazione retrograda può facilmente compromettere il pericardio e portare a un emopericardio. Le dissezioni anterograde possono propagarsi fino alla biforcazione iliaca dell'aorta, rompere la parete aortica, o ricanalizzare nel lume intravascolare portando a un'aorta "a doppia canna". L'aorta a doppia canna abbassa la pressione del flusso sanguigno e pertanto riduce il rischio di rottura. Se la dissecazione aortica si rompe, si verifica un'emorragia in una cavità corporea e la prognosi dipende dalla sede interessata dalla rottura. Sono possibili sia rotture retroperitoneali sia pericardiche.
L'evento iniziale in una dissecazione aortica è una lacerazione nel rivestimento intimale dell'aorta. A causa delle alte pressioni vigenti nel vaso, il sangue riesce a penetrare nella tonaca media in corrispondenza del punto di lacerazione. La forza del sangue che riesce a penetrare nella tonaca media fa sì che la lacerazione si estenda. Il sangue viaggia attraverso la tonica media creando un falso lume: la lacerazione in genere si estende distalmente (lontano dal cuore) ma può estendersi sia prossimalmente sia in entrambe le direzioni (il vero lume è il normale condotto del sangue nell'aorta). La separazione del falso lume dal vero lume è rappresentata da uno strato di tessuto di intima noto come lembo intimale.
La stragrande maggioranza delle dissecazione aortiche origina con una lacerazione intimale sia nel aorta ascendente (65%), sia nell'arco aortico (10%), o appena distalmente al legamento arterioso in aorta toracica discendente (20%). Non appena il sangue inizia a scorrere nel falso lume, possono verificarsi lacerazioni secondarie nell'intima. Attraverso queste lacerazioni secondarie, il sangue può rientrare nel vero lume. Mentre non è sempre chiaro il motivo per cui si viene a verificare una lacerazione intimale, molto spesso essa coinvolge la degenerazione del collagene e dell'elastina che sono costituenti fondamentali della tonaca media. Questa situazione è nota con il termine di necrosi cistica mediale ed è più comunemente associata alla sindrome di Marfan così come alla sindrome di Ehlers-Danlos.
In circa il 13% delle dissecazioni aortiche, non si trova evidenza di una rottura intimale. In questi casi, si ritiene che l'evento scatenante sia un ematoma intramurale (causato verosimilmente da sanguinamento nei media). Poiché in questi casi non esiste alcuna connessione diretta tra il lume vero e il falso lume, diagnosticare una dissezione aortica mediante arteriografia (aortografia) è difficile se la causa è un ematoma intramurale.
Epidemiologia[modifica | modifica wikitesto]
Stabilire l'incidenza della dissecazione aortica in una determinata popolazione è spesso difficile poiché molti casi vengono diagnosticati solo dopo la morte (che può spesso essere stata attribuita a un'altra causa). In caso di dissecazione aortica, infatti, errate diagnosi non sono affatto infrequenti. La dissecazione aortica colpisce circa 2,0-3,5 persone ogni 100.000 ogni anno. Studi epidemiologici eseguiti in Svezia suggeriscono che l'incidenza della dissecazione aortica potrebbe essere in aumento.[29] I soggetti di sesso maschile sono più comunemente colpiti rispetto alle donne con il 65% dei casi. L'età media alla diagnosi è di circa 63 anni.[27] Se si considerano le donne con meno di 40 anni di età, la metà di tutte le dissecazioni aortiche si verificano durante il periodo di gravidanza (in genere nel terzo trimestre o all'inizio del periodo postpartum).[30][31] Complessivamente una dissecazione aortica si verifica in circa lo 0,6% delle gravidanze.
Fattori di rischio[modifica | modifica wikitesto]
Tra i fattori non modificabili rientrano l'età e le patologie congenite quali la valvola aortica bicuspide, la sindrome di Turner e le connettivopatie come la sindrome di Marfan.[10][11] Fattori di rischio modificabili (ovvero trattabili) sono l'aneurisma dell'aorta toracica ascendente (per aterosclerosi, sifilide, traumi ed altre cause), l'aterosclerosi e le dislipidemie, il fumo e l'ipertensione arteriosa.
Cause di morte[modifica | modifica wikitesto]
La morte sopraggiunge per shock in seguito a rottura dell'aorta e grave emorragia interna.
Il rischio di rottura fulminante parte dal 40% al presentarsi della sintomatologia e cresce dell'1% ogni ora; nell'arco delle 24 ore, il rischio è superiore al 60%.
Diagnosi[modifica | modifica wikitesto]

La dissecazione aortica è una delle emergenze più impegnative in ambito cardiologico. La diagnostica è spesso impegnativa perché richiede l'uso di procedure lunghe e dispendiose in termini di tempo, non sono sempre disponibili in ogni ospedale.[32] Anche se la raccolta di una buona anamnesi dal soggetto può essere fortemente indicativa di una dissecazione aortica, la diagnosi non può sempre essere fatta sulla base della sola storia clinica e sui reperti dell'esame obiettivo. Spesso la diagnosi di conferma si ha solo in seguito alla visualizzazione del lembo intimale dopo un esame di imaging radiologico. D'altro canto l'alta mortalità della malattia (in particolare nella fase acuta) richiede un rapido chiarimento della diagnosi (in genere mediante ecocardiografia transesofagea, una TAC torace con mezzo di contrasto iodato o una RMN. L'ecocardiografia transesofagea (con uso di ultrasuoni ad alta frequenza) ha una elevata capacità di risoluzione grazie alla vicinanza anatomica dell'aorta all'esofago che consente di ottenere delle buone immagini. Altri test che possono essere utilizzati includono un aortogramma o un'angiografia a risonanza magnetica dell'aorta. Ognuno di questi test ha pro e contro, e non hanno sensibilità e specificità uguali nella diagnosi della dissezione aortica.
In generale la scelta della tecnica di imaging si basa sulla disponibilità della modalità di test nell'ospedale, sulla stabilità del paziente e sulla sensibilità e specificità dell'esame.
Sospetto iniziale[modifica | modifica wikitesto]
Ogni improvviso forte dolore alla schiena, al torace o all'addome, per i quali non può essere trovata un'altra spiegazione plausibile, deve indurre al sospetto di una dissecazione aortica o di un aneurisma aortico. In particolare se esistono ulteriori reperti, ad esempio il riscontro di ipertensione arteriosa (49% dei pazienti con dissecazione aortica), una marcata pressione differenziale (31%), un soffio diastolico (28%) o deficit neurologici focali (17%) il sospetto di dissecazione aortica diviene più consistente e corre l'obbligo di eseguire ulteriori accertamenti per chiarire l'origine del problema.
D-dimero[modifica | modifica wikitesto]
Alcuni medici nel processo di valutazione diagnostica ritengono utile misurare il livello del D-dimero nel sangue. Tale determinazione ha valore solo come predizione negativa, ovvero per escludere una possibile dissecazione; un livello inferiore a 500 ng/ml può infatti essere considerato una prova contro una diagnosi di dissecazione aortica.[33] Tuttavia questo approccio si ritiene sia applicabile solo nei casi ritenuti a "basso rischio" e se eseguito entro 24 ore dall'insorgenza dei sintomi.[34][35] In ogni caso l'American Heart Association non consiglia di usare questo test nel processo diagnostico, poiché le prove di evidenza sono ancora carenti.[36]
Radiografia del torace[modifica | modifica wikitesto]

La radiografia del torace può dimostrare un cambiamento nella morfologia dell'aorta toracica, che può essere sospetta per dissecazione aortica. Classicamente, il riscontro di un allargamento del mediastino di nuova insorgenza sulla radiografia è un reperto di moderata sensibilità per la rilevazione di una dissecazione aortica ascendente. Sfortunatamente questo reperto è di bassa specificità, in quanto molte altre condizioni possono causare un apparente allargamento del mediastino.
Altri risultati radiografici associati alla dissecazione sono:
- Il "segno del calcio": il radiologo descrive una separazione della intima calcifica dal margine aortico esterno di oltre 10 mm.
- Versamento pleurico: è più comune nelle dissecazioni aortiche discendenti, e in genere si localizza sul lato sinistro.
- Altri reperti: obliterazione del bottone aortico, depressione del bronco principale sinistro, perdita della striscia paratracheale e deviazione tracheale.
È importante sottolineare che circa il 12-20% delle dissezioni aortiche non sono rilevabili con la radiografia del torace; pertanto, una radiografia del torace "normale" non esclude la dissecazione aortica. Se vi è un alto sospetto clinico, può essere giustificato un test di imaging più sensibile (angio-TAC, angio-RMN oppure un'ecografia transesofagea).
Angio Tomografia computerizzata[modifica | modifica wikitesto]
L'angiografia con tomografia computerizzata è un test rapido e non invasivo che fornisce un'accurata valutazione tridimensionale dell'aorta e più in generale dell'albero arterioso. Queste immagini sono prodotte acquisendo molto rapidamente strati molto sottili del torace e dell'addome, affidando quindi a un sistema computerizzato la loro ricombinazione volta alla creazione di sezioni trasversali. Per delineare l'aorta con la precisione necessaria per effettuare una diagnosi corretta, è necessario iniettare un materiale di contrasto iodato in una vena periferica. Un'apposita apparecchiatura a pompa (iniettore automatico) inietta la quantità di mezzo di contrasto prestabilita e nei tempi opportuni. In sostanza si ha una gestione in tempo reale della modulazione del flusso di contrasto, in sincronia con le scansioni tomografiche del macchinario TAC. Questo tipo di scansione è programmata per acquisire le immagini quando il contrasto penetra nell'aorta. Le scansionei quindi proseguono man mano che il contrasto fluisce attraverso il vaso. La tecnica ha una sensibilità variabile dal 96 al 100% e una specificità dal 96 al 100%. Sfortunatamente l'angio-TAC spesso non è in grado di identificare il sito preciso ove è avvenuta la rottura intimale. Un'ulteriore svantaggio è dato dalla necessità di ricorrere a materiale di contrasto iodato.
-
TAC con mezzo di contrasto che dimostra una dilatazione aneurismatica e una dissecazione dell'aorta ascendente (tipo A di Stanford)
-
TAC torace che evidenzia una dissecazione (tipo B di Stanford) discendente (il cerchio in rosso)
Risonanza magnetica[modifica | modifica wikitesto]
La risonanza magnetica (RMN) può essere utilizzata dia per fare diagnosi che per una migliore valutazione della dissecazione aortica, con una sensibilità del 98% e una specificità del 98%. Un esame RMN dell'aorta comporta una ricostruzione tridimensionale dell'aorta, che consente al medico di determinare la posizione della lesione intimale, il coinvolgimento di eventuali altri vasi e ramificazioni, e di individuare eventuali lacerazioni secondarie. È un test non invasivo, non richiede l'uso di materiale di contrasto iodato e può rilevare e quantificare il grado di insufficienza aortica.
Lo svantaggio di questa modalità di imaging è soprattutto legato al fatto che la disponibilità dell'esame è ancora riservata ad un numero limitato di centri ospedalieri (spesso è disponibile solo in pochi ospedali di grandi dimensioni); inoltre le scansioni in risonanza magnetica richiedono tempi di esecuzione relativamente lunghi. L'esame presenta anche alcune controindicazioni specifiche. A causa dei campi magnetici ad alta intensità che vengono utilizzati durante l'esecuzione della risonanza magnetica, l'esame è controindicato nei soggetti con protesi metalliche. Un ulteriore problema è dato dal fatto che il paziente deve essere posizionato all'interno di un tubo di scansione di diametro di 60 cm, che può provocare un senso di oppressione e di claustrofobia.
Ecocardiografia[modifica | modifica wikitesto]
Dobbiamo distinguere tra ecocardiografia transtoracica - TTE (che identifica in modo affidabile una dissecazione dell'aorta ascendente) e l'ecocardiogramma transesofageo - TEE. Quest'ultimo è un tipo di esame relativamente affidabile nella diagnosi di dissecazione aortica, con una sensibilità fino al 98% e una specificità fino al 97%. L'esame permette di visualizzare un flap intimale flottante nel lume aortico: ovviamente è necessario verificare l'immagine in più proiezioni per essere certi che quella visualizzata non sia una falsa immagine (ad esempio un riverbero). È diventata una delle modalità di imaging più utilizzate per eseguire diagnosi in caso di sospetta dissecazione aortica. Si tratta infatti di un esame relativamente non invasivo (anche se nella modalità transesofagea richiede comunque che la sonda di ecocardiografia sia inserita nell'esofago del paziente, il quale si trova così ad ingoiarla).
L'esame è particolarmente utile nella valutazione dell'insufficienza aortica, in caso di dissecazione aortica ascendente, per determinare se e quanto siano coinvolti gli osti (le origini) delle arterie coronarie. L'ecocardiogramma transesofageo può essere eseguito, in soggetti che cooperano, senza ricorrere alla sedazione; tuttavia la maggior parte dei centri, per un maggiore comfort del paziente, preferisce ricorrere ad una sedazione blanda (ad esempio 1-2 mg di midazolam).
Tra gi svantaggi dell'ecocardiografia TEE deve essere considerata l'incapacità di visualizzare l'aorta ascendente distale (il tratto iniziale dell'arco aortico) e l'aorta addominale discendente, la parte di vaso che decorre al di sotto dello stomaco. Un TEE può essere tecnicamente difficile da eseguire in soggetti con stenosi o varici esofagee.
Aortogramma[modifica | modifica wikitesto]
Un aortogramma prevede il posizionamento di un catetere nell'aorta e l'iniezione di materiale di contrasto durante l'esecuzione di radiografie dell'aorta. La procedura rientra più in generale fra le procedure arteriogarfiche ed è anche nota come aortografia. In un passato recente era considerata il gold standard diagnostico, ma oggigiorno è stata soppiantata da altre modalità di imaging meno invasive.
Trattamento[modifica | modifica wikitesto]
In una dissecazione acuta, la scelta del trattamento dipende dalla sede in cui si verifica lo scollamento delle tonache. Nel caso di dissecazione di Stanford di tipo A (coinvolgimento dell'aorta ascendente), il trattamento chirurgico è superiore al trattamento medico. Nel caso di dissecazione di Stanford di tipo B (coinvolgimento dell'aorta distale, incluse le dissezioni aortiche addominali), il trattamento medico è preferibile rispetto a quello chirurgico. Il rischio di morte dovuto a dissecazione aortica è più alto nelle prime ore dopo l'inizio della dissecazione e diminuisce in seguito. Per questo motivo, le strategie terapeutiche differiscono a seconda che ci si trovi di fronte a una dissecazione acuta rispetto a una dissezione cronica. Si ricorda che una dissecazione acuta è, per definizione, un evento per il quale il paziente si presenta all’attenzione del medico entro le prime due settimane. Se un soggetto riesce a sopravvivere a questo periodo finestra, la sua prognosi è migliore. Circa il 66% di tutte le dissezioni si presenta in fase acuta.
Le persone che si presentano due settimane dopo l'inizio della dissecazione sono considerate affette da dissecazione aortica cronica. Questi individui in un certo qual modo si sono auto-selezionati, in quanto sopravvissuti all'episodio acuto e possono quindi essere trattati con terapia farmacologica, purché clinicamente ed emodinamicamente stabili.
Trattamento medico (farmacologico)[modifica | modifica wikitesto]
La dissecazione aortica si presenta generalmente come un'emergenza ipertensiva: ne consegue che l’obiettivo principale del trattamento medico è il rigoroso controllo della pressione arteriosa. Il trattamento iniziale deve infatti tendere ad arrestare la progressione dell'ematoma dissecante. La pressione sanguigna target dovrebbe essere una pressione arteriosa media (MAP) compresa tra i 60 e i 75 mmHg o una pressione arteriosa anche più bassa, se tollerata dal paziente. La riduzione della pressione arteriosa con la quale il paziente si presenta alla valutazione medica deve avvenire gradualmente, e le diminuzioni iniziali non dovrebbero essere superiori al 20% circa della pressione basale. Un altro obiettivo fondamentale del trattamento iniziale è la riduzione della cosiddetta forza di taglio dP/dt (cioè della forza di espulsione del sangue dal ventricolo sinistro). La gestione a lungo termine di ogni tipo di stress (fisico, emotivo e psicologico) è importante per ottenere un buon controllo della pressione arteriosa.
I farmaci betabloccanti sono il trattamento di prima linea per i pazienti con dissecazione aortica acuta e cronica. Nella dissecazione acuta, sono generalmente preferiti gli agenti ad azione rapida, in quanto possono essere somministrati per via endovenosa e presentano dosaggi più facili da regolare (ad esempio si ricorre all’esmololo, propranololo o labetalolo). I farmaci vasodilatatori, ad esempio il nitroprussiato di sodio possono essere presi in considerazione per alcuni pazienti con pressione arteriosa estremamente alta, ma non dovrebbero mai essere utilizzati da soli, poiché spesso stimolano un aumento riflesso (e non desiderabile) della frequenza cardiaca. I farmaci calcio-antagonisti possono essere utilizzati nel trattamento della dissecazione aortica, in particolare se esiste una controindicazione all'uso dei betabloccanti. I bloccanti dei canali del calcio che vengono generalmente utilizzati sono il verapamil e il diltiazem, a causa dei loro effetti combinati vasodilatatori e inotropi negativi.
Se un paziente con dissecazione aortica si presenta con un'ipertensione arteriosa refrattaria (cioè un'ipertensione persistente nonostante il ricorso alle dosi massime previste di ben tre diverse classi di agenti antipertensivi), è necessario sospettare che la dissecazione aortica abbia coinvolto anche le arterie renali.
Trattamento chirurgico[modifica | modifica wikitesto]
Le indicazioni per il trattamento chirurgico della dissecazione aortica comprendono una dissecazione aortica prossimale acuta e una dissecazione aortica distale acuta ma gravata da una o più complicanze. Le complicanze che devono essere prese in considerazione includono la compromissione di un organo vitale, una rottura o l’imminente rottura dell'aorta, la dissecazione retrograda con coinvolgimento dell'aorta ascendente e una storia personale di sindrome di Marfan o sindrome di Ehlers-Danlos.
L'obiettivo nella gestione chirurgica della dissecazione aortica è quello di asportare i segmenti dell'aorta più gravemente danneggiati e di impedire l'ulteriore ingresso di sangue nel falso lume (sia nella zona di lacerazione intimale originaria, che in qualsiasi zona di lacerazione secondaria lungo il decorso del vaso). È tecnicamente possibile eseguire l'escissione della lesione intimale, tuttavia questo tipo di intervento non cambia in modo significativo la mortalità. Ricorrere a un particolare tipo di trattamento piuttosto che ad un altro dipende dal segmento o tratto di aorta coinvolto. Alcuni trattamenti possibili comprendono:
- Chirurgia aortica “a cielo aperto” con sostituzione della sezione danneggiata di aorta e sua sostituzione con un innesto a tubo (spesso in materiale di dacron) purché si possa escludere qualsiasi tipo di danno a carico della valvola aortica.
- Procedura di Bentall-De Bono: sostituzione della sezione d’aorta danneggiata e sostituzione della valvola aortica.[37]
- Procedura di David - sostituzione della sezione danneggiata dell'aorta e reimpianto della valvola aortica[38]
- Riparazione aortica endovascolare toracica: una procedura chirurgica minimamente invasiva, solitamente associata a un trattamento medico continuo.
- Sostituzione della sezione d'aorta danneggiata con un connettore vascolare ad anello senza suture-rinforzo con innesto di Dacron: il connettore vascolare ad anello è un anello di titanio usato come stent nell'innesto vascolare per ottenere una rapida anastomosi senza ricorrere a suture. Due solchi sulla superficie dell'anello servono per il fissaggio dell'innesto vascolare e dell'aorta. I nastri utilizzati per ancorarsi all'anello forniscono una superficie di contatto più ampia rispetto ai punti tradizionali, quindi comportano la realizzazione di anastomosi più forti e risultati chirurgici migliori.
Poiché il falso lume potrebbe aver ostruito altri tronchi arteriosi emergenti, spesso si rende necessario, contestualmente all'intervento chirurgico per la dissecazione vera e propria, anche un intervento di rivascolarizzazione per eliminare l'ostruzione in questi vasi attigui, e ciò al fine di risolvere la cattiva perfusione di molti organi vicini.
Un certo numero di condizioni e di comorbilità aumentano il rischio chirurgico di intervento di riparazione nei pazienti colpiti da una dissecazione aortica. Queste condizioni includono quanto segue:
- Valutazione preoperatoria prolungata (ampio periodo temporale prima della scelta dell'intervento chirurgico)
- Età avanzata
- Presenza di comorbilità (ad esempio una malattia coronaria)
- Rottura di aneurisma
- Tamponamento cardiaco
- Shock
- Storia pregressa di infarto del miocardio
- Storia di insufficienza renale (sia acuta che cronica)
Follow up[modifica | modifica wikitesto]
Il follow-up a lungo termine nelle persone che sopravvivono alla dissecazione aortica comporta un rigoroso controllo della pressione arteriosa. Il rischio di una rottura tardiva di un aneurisma aortico è 10 volte più alto nei soggetti con ipertensione arteriosa non controllata, rispetto ai soggetti con una pressione sistolica inferiore a 130 mmHg. Pertanto l'ipertensione non controllata rimane il fattore di rischio trattabile più significativo nella dissecazione aortica.[39] Il rischio di morte è più alto nei primi due anni dopo l'evento acuto, ed i pazienti dovrebbero essere seguiti strettamente durante questo periodo di tempo. Circa il 29% delle morti tardive dopo l'intervento chirurgico è dovuto alla rottura di un aneurisma dissecante. Inoltre, esiste una rilevante incidenza (calcolata tra il 17% e il 25%) di formazione di un nuovo aneurisma, tipicamente dovuta alla dilatazione del falso lume residuo. Questi nuovi aneurismi hanno maggiori probabilità di rottura, per il fatto che sono costituiti da pareti più sottili. Molti medici suggeriscono imaging seriale dell'aorta, e la risonanza magnetica (RMN) è la tecnica di imaging preferita.
Prevenzione[modifica | modifica wikitesto]
Tra i fattori di rischio riconosciuti per la dissecazione aortica, l'ipertensione, i livelli anormalmente alti di lipidi (ad esempio il colesterolo) nel sangue e il fumo di tabacco, sono tutti considerati fattori di rischio prevenibili. Si raccomanda di intervenire chirurgicamente a riparare un ingrossamento dell'aorta ascendente dovuto a un aneurisma con una dimensione superiore a 6 cm per ridurre il rischio di dissecazione. L'intervento chirurgico può essere raccomandato quando la dimensione è superiore a 4,5 cm se la persona è affetta da una delle diverse patologie del tessuto connettivo oppure ha una storia familiare di rottura dell'aorta.
Note[modifica | modifica wikitesto]
- ^ Sono a rischio di dissezione aortica ?, in la Repubblica, 2 ottobre 2018, p. 55.
- ^ a b c d Criado FJ, Aortic dissection: a 250-year perspective, in Tex Heart Inst J, vol. 38, n. 6, 2011, pp. 694–700, PMC 3233335, PMID 22199439.
- ^ a b c d e Nienaber CA, Clough RE, Management of acute aortic dissection, in Lancet, vol. 385, n. 9970, febbraio 2015, pp. 800–11, DOI:10.1016/S0140-6736(14)61005-9, PMID 25662791. URL consultato il 22 marzo 2018.
- ^ White A, Broder J, Mando-Vandrick J, Wendell J, Crowe J, Acute aortic emergencies--part 2: aortic dissections, in Adv Emerg Nurs J, vol. 35, n. 1, 2013, pp. 28–52, DOI:10.1097/TME.0b013e31827145d0, PMID 23364404. URL consultato il 22 marzo 2018.
- ^ Gaul C, Dietrich W, Erbguth FJ, Neurological symptoms in aortic dissection: a challenge for neurologists, in Cerebrovasc. Dis., vol. 26, n. 1, 2008, pp. 1–8, DOI:10.1159/000135646, PMID 18511865. URL consultato il 22 marzo 2018.
- ^ Gaul C, Dietrich W, Friedrich I, Sirch J, Erbguth FJ, Neurological symptoms in type A aortic dissections, in Stroke, vol. 38, n. 2, febbraio 2007, pp. 292–7, DOI:10.1161/01.STR.0000254594.33408.b1, PMID 17194878. URL consultato il 22 marzo 2018.
- ^ Walma RA, Vermeij FH, Bakker S, [Neurological signs in aortic dissection], in Ned Tijdschr Geneeskd, vol. 157, n. 38, 2013, pp. A6259, PMID 24330794. URL consultato il 22 marzo 2018.
- ^ a b Orihashi K, Mesenteric ischemia in acute aortic dissection, in Surg. Today, vol. 46, n. 5, maggio 2016, pp. 509–16, DOI:10.1007/s00595-015-1193-4, PMID 26024781. URL consultato il 22 marzo 2018.
- ^ a b Kamman AV, Yang B, Kim KM, Williams DM, Michael Deeb G, Patel HJ, Visceral Malperfusion in Aortic Dissection: The Michigan Experience, in Semin. Thorac. Cardiovasc. Surg., vol. 29, n. 2, 2017, pp. 173–178, DOI:10.1053/j.semtcvs.2016.10.002, PMID 28823323. URL consultato il 22 marzo 2018.
- ^ a b c d Cook JR, Ramirez F, Clinical, diagnostic, and therapeutic aspects of the Marfan syndrome, in Adv. Exp. Med. Biol., vol. 802, 2014, pp. 77–94, DOI:10.1007/978-94-007-7893-1_6, PMID 24443022. URL consultato il 23 marzo 2018.
- ^ a b c Murdoch JL, Walker BA, Halpern BL, Kuzma JW, McKusick VA, Life expectancy and causes of death in the Marfan syndrome, in N. Engl. J. Med., vol. 286, n. 15, aprile 1972, pp. 804–8, DOI:10.1056/NEJM197204132861502, PMID 5011789. URL consultato il 23 marzo 2018.
- ^ a b Stankowski RV, Kloner RA, Rezkalla SH, Cardiovascular consequences of cocaine use, in Trends Cardiovasc. Med., vol. 25, n. 6, agosto 2015, pp. 517–26, DOI:10.1016/j.tcm.2014.12.013, PMID 25657055. URL consultato il 23 marzo 2018.
- ^ a b Singh A, Khaja A, Alpert MA, Cocaine and aortic dissection, in Vasc Med, vol. 15, n. 2, aprile 2010, pp. 127–33, DOI:10.1177/1358863X09358749, PMID 20233907. URL consultato il 23 marzo 2018.
- ^ Wanga S, Silversides C, Dore A, de Waard V, Mulder B, Pregnancy and Thoracic Aortic Disease: Managing the Risks, in Can J Cardiol, vol. 32, n. 1, gennaio 2016, pp. 78–85, DOI:10.1016/j.cjca.2015.09.003, PMID 26604124. URL consultato il 23 marzo 2018.
- ^ a b Lech C, Swaminathan A, Abdominal Aortic Emergencies, in Emerg. Med. Clin. North Am., vol. 35, n. 4, novembre 2017, pp. 847–867, DOI:10.1016/j.emc.2017.07.003, PMID 28987432. URL consultato il 23 marzo 2018.
- ^ Debakey ME, Henly WS, Cooley DA, Morris GC, Crawford ES, Beall AC, Surgical management of dissecting aneurysms of the aorta, in J. Thorac. Cardiovasc. Surg., vol. 49, gennaio 1965, pp. 130–49, PMID 14261867.
- ^ Daily PO, Trueblood HW, Stinson EB, Wuerflein RD, Shumway NE, Management of acute aortic dissections, in Ann. Thorac. Surg., vol. 10, n. 3, settembre 1970, pp. 237–47, PMID 5458238.
- ^ Slater EE, DeSanctis RW, The clinical recognition of dissecting aortic aneurysm, in Am. J. Med., vol. 60, n. 5, maggio 1976, pp. 625–33, DOI:10.1016/0002-9343(76)90496-4, PMID 1020750. URL consultato il 25 marzo 2018.
- ^ Spittell PC, Spittell JA, Joyce JW, Tajik AJ, Edwards WD, Schaff HV, Stanson AW, Clinical features and differential diagnosis of aortic dissection: experience with 236 cases (1980 through 1990), in Mayo Clin. Proc., vol. 68, n. 7, luglio 1993, pp. 642–51, DOI:10.1016/s0025-6196(12)60599-0, PMID 8350637. URL consultato il 25 marzo 2018.
- ^ (EN) Isselbacher EM, Cigarroa JE, Eagle KA, Cardiac tamponade complicating proximal aortic dissection. Is pericardiocentesis harmful?, in Circulation, vol. 90, n. 5, novembre 1994, pp. 2375–8, PMID 7955196. URL consultato il 2 agosto 2021 (archiviato dall'url originale il 27 marzo 2018).
- ^ Sheikh AS, Ali K, Mazhar S, Acute aortic syndrome, in Circulation, vol. 128, n. 10, settembre 2013, pp. 1122–7, DOI:10.1161/CIRCULATIONAHA.112.000170, PMID 24002714. URL consultato il 25 marzo 2018.
- ^ a b c Alfson DB, Ham SW, Type B Aortic Dissections: Current Guidelines for Treatment, in Cardiol Clin, vol. 35, n. 3, agosto 2017, pp. 387–410, DOI:10.1016/j.ccl.2017.03.007, PMID 28683909. URL consultato il 25 marzo 2018.
- ^ Meester JAN, Verstraeten A, Schepers D, Alaerts M, Van Laer L, Loeys BL, Differences in manifestations of Marfan syndrome, Ehlers-Danlos syndrome, and Loeys-Dietz syndrome, in Ann Cardiothorac Surg, vol. 6, n. 6, novembre 2017, pp. 582–594, DOI:10.21037/acs.2017.11.03, PMC 5721110, PMID 29270370. URL consultato il 23 marzo 2018.
- ^ Turtle EJ, Sule AA, Webb DJ, Bath LE, Aortic dissection in children and adolescents with Turner syndrome: risk factors and management recommendations, in Arch. Dis. Child., vol. 100, n. 7, luglio 2015, pp. 662–6, DOI:10.1136/archdischild-2014-307080, PMID 25573747. URL consultato il 23 marzo 2018.
- ^ Bondy CA, Aortic dissection in Turner syndrome, in Curr. Opin. Cardiol., vol. 23, n. 6, novembre 2008, pp. 519–26, PMC 2692924, PMID 18839441. URL consultato il 23 marzo 2018.
- ^ Shachter N, Perloff JK, Mulder DG, Aortic dissection in Noonan's syndrome (46 XY turner), in Am. J. Cardiol., vol. 54, n. 3, agosto 1984, pp. 464–5, PMID 6465040.
- ^ a b Hiratzka LF, Bakris GL, Beckman JA, Bersin RM, Carr VF, Casey DE, Eagle KA, Hermann LK, Isselbacher EM, Kazerooni EA, Kouchoukos NT, Lytle BW, Milewicz DM, Reich DL, Sen S, Shinn JA, Svensson LG, Williams DM, 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM guidelines for the diagnosis and management of patients with Thoracic Aortic Disease: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine, in Circulation, vol. 121, n. 13, aprile 2010, pp. e266–369, DOI:10.1161/CIR.0b013e3181d4739e, PMID 20233780. URL consultato il 26 marzo 2018.
- ^ Das M., Mahnken A.H. and Wildberger J.E., “Dual Energy: CTA Aorta” in Seidensticker P.R. and Hofmann L.K. (eds.), Dual Source CT Imaging, Springer Medizin Verlag, Heidelberg, 2008. ISBN 978-3-540-77602-4.
- ^ Olsson C, Thelin S, Ståhle E, Ekbom A, Granath F, Thoracic aortic aneurysm and dissection: increasing prevalence and improved outcomes reported in a nationwide population-based study of more than 14,000 cases from 1987 to 2002, in Circulation, vol. 114, n. 24, dicembre 2006, pp. 2611–8, DOI:10.1161/CIRCULATIONAHA.106.630400, PMID 17145990. URL consultato il 26 marzo 2018.
- ^ Yuan SM, Postpartum aortic dissection, in Taiwan J Obstet Gynecol, vol. 52, n. 3, settembre 2013, pp. 318–22, DOI:10.1016/j.tjog.2013.06.003, PMID 24075366. URL consultato il 26 marzo 2018.
- ^ Immer FF, Bansi AG, Immer-Bansi AS, McDougall J, Zehr KJ, Schaff HV, Carrel TP, Aortic dissection in pregnancy: analysis of risk factors and outcome, in Ann. Thorac. Surg., vol. 76, n. 1, luglio 2003, pp. 309–14, PMID 12842575. URL consultato il 26 marzo 2018.
- ^ Ohle R, Kareemi HK, Wells G, Perry JJ, Clinical Examination for Acute Aortic Dissection: A Systematic Review and Meta-analysis, in Acad Emerg Med, dicembre 2017, DOI:10.1111/acem.13360, PMID 29265487. URL consultato il 27 marzo 2018.
- ^ Shimony A, Filion KB, Mottillo S, Dourian T, Eisenberg MJ, Meta-analysis of usefulness of d-dimer to diagnose acute aortic dissection, in Am. J. Cardiol., vol. 107, n. 8, aprile 2011, pp. 1227–34, DOI:10.1016/j.amjcard.2010.12.027, PMID 21296332. URL consultato il 27 marzo 2018.
- ^ Asha SE, Miers JW, A Systematic Review and Meta-analysis of D-dimer as a Rule-out Test for Suspected Acute Aortic Dissection, in Ann Emerg Med, vol. 66, n. 4, ottobre 2015, pp. 368–78, DOI:10.1016/j.annemergmed.2015.02.013, PMID 25805111. URL consultato il 27 marzo 2018.
- ^ Bossone E, Suzuki T, Eagle KA, Weinsaft JW, Diagnosis of acute aortic syndromes : imaging and beyond, in Herz, vol. 38, n. 3, maggio 2013, pp. 269–76, DOI:10.1007/s00059-012-3710-1, PMID 23263244. URL consultato il 27 marzo 2018.
- ^ Lo BM, An evidence-based approach to acute aortic syndromes, in Emerg Med Pract, vol. 15, n. 12, dicembre 2013, pp. 1–23; quiz 23–4, PMID 24804329. URL consultato il 27 marzo 2018.
- ^ Bentall H, De Bono A, A technique for complete replacement of the ascending aorta, in Thorax, vol. 23, n. 4, luglio 1968, pp. 338–9, PMID 5664694. URL consultato il 24 marzo 2018.
- ^ David TE, Armstrong S, Ivanov J, Feindel CM, Omran A, Webb G, Results of aortic valve-sparing operations, in J. Thorac. Cardiovasc. Surg., vol. 122, n. 1, luglio 2001, pp. 39–46, DOI:10.1067/mtc.2001.112935, PMID 11436035. URL consultato il 24 marzo 2018.
- ^ Howard DP, Banerjee A, Fairhead JF, Perkins J, Silver LE, Rothwell PM, Population-based study of incidence and outcome of acute aortic dissection and premorbid risk factor control: 10-year results from the Oxford Vascular Study, in Circulation, vol. 127, n. 20, maggio 2013, pp. 2031–7, DOI:10.1161/CIRCULATIONAHA.112.000483, PMID 23599348. URL consultato il 24 marzo 2018.
Bibliografia[modifica | modifica wikitesto]
- Joseph C. Sengen, Concise Dictionary of Modern Medicine, New York, McGraw-Hill, ISBN 978-88-386-3917-3.
- Harrison, Principi di Medicina Interna (il manuale - 16ª edizione), New York - Milano, McGraw-Hill, 2006, ISBN 88-386-2459-3.
- Hurst, Il Cuore (il manuale - 11ª edizione), Milano, McGraw-Hill, 2006, ISBN 978-88-386-2388-2.
- Eugene Braunwald, Malattie del cuore (7ª edizione), Milano, Elsevier Masson, 2007, ISBN 978-88-214-2987-3.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su dissecazione aortica
Wikimedia Commons contiene immagini o altri file su dissecazione aortica
