Ioduro di alluminio
| Ioduro di alluminio | |
|---|---|
 | |
 | |
| Nomi alternativi | |
| ioduro di alluminio(III) | |
| Caratteristiche generali | |
| Formula bruta o molecolare | AlI3 |
| Massa molecolare (u) | 407,695 |
| Aspetto | solido incolore |
| Numero CAS | |
| Numero EINECS | 232-054-8 |
| PubChem | 82222 |
| SMILES | [Al](I)(I)I |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 3,98 |
| Solubilità in acqua | reazione violenta |
| Temperatura di fusione | 191 °C (464 K) |
| Temperatura di ebollizione | 360 °C (633 K) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | 310 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| Frasi H | 314 |
| Consigli P | 260, 301+330+331, 303+361+353, 305+351+338, 405, 501 |
Lo ioduro di alluminio (o anche triioduro di alluminio secondo le norme IUPAC) è il composto inorganico di formula AlI3. In condizioni normali è un solido incolore costituito da dimeri Al2I6. Si idrolizza rapidamente in acqua rilasciando acido iodidrico. In questo composto l'alluminio è nello stato di ossidazione +3. È di uso meno comune del corrispondente cloruro (AlCl3), e viene usato come catalizzatore in alcune reazioni di sintesi organica.
Struttura e proprietà[modifica | modifica wikitesto]
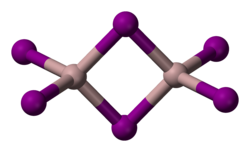
AlI3 è un composto molecolare che esiste solo come dimero Al2I6 sia allo stato solido che allo stato liquido e gassoso. In Al2I6 gli atomi di alluminio hanno coordinazione tetraedrica.[1] Le distanze Al–I sono 258 pm per gli ioduri a ponte e 253 pm per quelli terminali.[2]
Sintesi[modifica | modifica wikitesto]
AlI3 si prepara per sintesi diretta tra alluminio e iodio in atmosfera inerte:[3]
- 2Al + 3I2 → Al2I6
Reattività[modifica | modifica wikitesto]
Al pari degli altri alogenuri di alluminio, AlI3 è sensibile all'umidità e si decompone per riscaldamento all'aria formando iodio e ossido di alluminio.[3] Reagisce violentemente con l'acqua formando acido iodidrico. È un acido di Lewis forte.
Uso[modifica | modifica wikitesto]
Lo ioduro di alluminio è di uso molto meno comune del corrispondente cloruro d'alluminio. AlI3 si usa in sintesi organica come catalizzatore per attivare alcuni tipi di legami S–O e N–O. Rompe gli eteri arilici e deossigena gli epossidi.[4] Può essere usato per preparare altri composti organici iodurati.[5]
Indicazioni di sicurezza[modifica | modifica wikitesto]
AlI3 è disponibile in commercio. È un composto corrosivo che per contatto provoca gravi ustioni cutanee e gravi lesioni agli occhi. Risulta irritante per le vie respiratorie. Non ci sono dati che indichino proprietà cancerogene. Viene considerato poco pericoloso per le acque e l'ambiente.[6]
Note[modifica | modifica wikitesto]
- ^ Greenwood e Earnshaw (1997)
- ^ Apblett 2006
- ^ a b Brauer 1963, p. 814.
- ^ Gugelchuk 2001
- ^ Lee et al. 2007
- ^ Alfa Aesar, scheda di dati di sicurezza di AlI3.
Bibliografia[modifica | modifica wikitesto]
- (EN) A. W. Apblett, Aluminum: Inorganic Chemistry, in Encyclopedia of Inorganic Chemistry, 2ª ed., John Wiley & Sons, 2006, DOI:10.1002/0470862106.ia007, ISBN 978-0-470-86210-0.
- (EN) G. Brauer, Handbook of preparative inorganic chemistry, Vol. 1, 2ª ed., New York, Academic Press, 1963.
- (EN) N. N. Greenwood e A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
- (EN) M. Gugelchuk, Aluminum Iodide, in L. Paquette (a cura di), Encyclopedia of Reagents for Organic Synthesis, New York, J. Wiley & Sons, 2001, DOI:10.1002/047084289X.ra083.
- S. I. Lee, G.-S. Hwang e D. H. Ryu, Aluminum Iodide Promoted Highly Z-Stereoselective Synthesis of β-Iodo Morita-Baylis-Hillman Esters with Ketones as Aldol Acceptors, in Synlett., n. 1, 2007, pp. 59–62, DOI:10.1055/s-2006-958421. URL consultato il 24 maggio 2012.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su ioduro di alluminio
Wikimedia Commons contiene immagini o altri file su ioduro di alluminio