CCR5
| Recettore C-C per le chemochine di tipo 5 | |
|---|---|
 | |
| Gene | |
| HUGO | CCR5 CC-CKR-5; CCCKR5; CCR-5; CD195; CKR-5; CKR5; CMKBR5; IDDM22 |
| Locus | Chr. 3 p21.31 |
| Proteina | |
| UniProt | P51681 |
CCR5, acronimo per C-C chemokine receptor type 5 (recettore C-C per le chemochine di tipo 5) e nota anche come CD195, è una proteina presente sulla membrana dei leucociti e coinvolta nel sistema immunitario come recettore per le chemochine, con il ruolo di attirare in specifici tessuti e organi i linfociti T. Molte forme di HIV, il virus responsabile dell'AIDS, utilizzano nelle fasi iniziali questo recettore per entrare nelle cellule da infettare. Esistono soggetti portatori di una particolare mutazione del gene, CCR5-Δ32, che li protegge dall'infezione da parte di queste forme virali.
In tali soggetti il gene CCR5, localizzato sul cromosoma 3, risulta mutato per delezione di una particolare porzione del materiale genetico; le forme omozigotiche, ovvero i soggetti che presentano entrambi gli alleli mutati, risultano resistenti ai ceppi virali di HIV-1 R5 tropici[1].
Funzione[modifica | modifica wikitesto]
CCR5 appartiene alla famiglia dei recettori ß per le chemochine ed è una proteina integrale di membrana[2][3]. Si tratta di un recettore accoppiato a proteine G e lega specificatamente la famiglia CC delle chemochine[2].
I ligandi naturali del recettore sono RANTES, un fattore chemotattico conosciuto anche come CCL5[4][5][6] e MIP (macrophage inflammatory protein) 1α e 1β, note anche rispettivamente come CCL3 e CCL4. Interagisce inoltre con CCL3L1[5][7].
Il gene è espresso soprattutto nei linfociti T, nei macrofagi, nelle cellule dendritiche e nella microglia e, sebbene il suo esatto ruolo nella funzione immunitaria normale non sia stato chiarito, si ritiene che abbia un ruolo nella risposta infiammatoria alle infezioni.
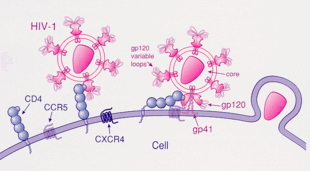
1) La proteina virale gp120 lega CD4
2) La regione variabile di gp120 lega il corecettore, solitamente CCR5 o CXCR4
3) HIV entra nella cellula
Ruolo nell'infezione da HIV[modifica | modifica wikitesto]
I corecettori che HIV utilizza per il suo ingresso nelle cellule sono CCR5 e/o CXCR4; sebbene numerosi recettori che le chemochine possano agire da corecettori virali, è CCR5 quello più importante nella storia naturale dell'infezione. I suoi ligandi fisiologici sono RANTES, MIP-1β e MIP-1α, i quali sono in grado di eliminare l'infezione da HIV-1 in vitro. Nei soggetti infettati da HIV, i ceppi che utilizzano CCR5 per l'ingresso nella cellula sono quelli maggiormente isolati nelle fasi iniziali dell'infezione[8]; ciò suggerisce che tali virus abbiano un vantaggio selettivo durante la trasmissione o la fase acuta della malattia. Inoltre, almeno metà dei pazienti infettati ospita solo virus R5-tropici durante l'intero corso dell'infezione.
Un nuovo gruppo di farmaci, gli antagonisti del recettore CCR5, è stato realizzato con lo scopo di interferire nell'interazione tra HIV e tale recettori; tra questi vi sono PRO 140, Vicriviroc, Aplaviroc e Maraviroc. Uno dei problemi limitanti in questo approccio terapeutico è che, nonostante CCR5 sia il corecettore maggiormente coinvolto nell'infezione, questo non è l'unico. Tuttavia, valutando la resistenza virale a AD101, un antagonista molecolare di CCR5, si è osservato che i virus resistenti non cambiano corecettore bersaglio, bensì continuano a utilizzare CCR5, anche utilizzando domini alternativi di legame o legando il recettore con maggiore affinità.
La variante Δ32[modifica | modifica wikitesto]
CCR5-Δ32, denominato anche CCR5-D32 o CCR5 delta 32, è una variante allelica di CCR5[9][10].
CCR5-Δ32 è una mutazione deletiva che ha un impatto specifico sulle funzioni dei linfociti T[11]. La presenza di almeno una copia di tale gene mutato (eterozigosi) è stata rilevata in circa il 4-16% degli individui di discendenza europea, la presenza di entrambe le copie del gene mutato (omozigosi), in circa il 0,16-2,5% degli individui di discendenza europea[12]. Si era speculato che tale allele potesse aver favorito la selezione naturale durante la Peste nera nei paesi dell'Europa settentrionale, ma studi più recenti hanno escluso questa possibilità, rivelando l'assenza di un ruolo protettivo in tale contesto[13]. Si ritiene che questa mutazione possa aver premesso una protezione dal vaiolo durante le epidemie in Europa[13], soprattutto nelle maggiori città commerciali e in luoghi isolati come Islanda e Azzorre[14], e che tale situazione abbia favorito un aumento della prevalenza della mutazione[9].
Si pensa che in Antica Grecia, in aree come quella di Corinto, lo sviluppo della prostituzione abbia portato alla diffusione di un'infezione simile a quella da HIV, con un quadro clinico simil-influenzale e una successiva immunodepressione. Allora nulla si sapeva sulla diffusione di questa malattia, ma si ritiene che anche la Peste di Atene e successive epidemie avutesi nei Balcani possano essere state favorite da mutazioni genetiche[15]. La mutazione CCR5-Δ32, tuttavia, è stata rilevata anche in campioni di sangue dell'età del bronzo, a tassi comparabili con quelli della popolazione europea moderna[16].
Questa mutazione ha un effetto negativo sulla funzione dei linfociti T, ma sembra svolgere un ruolo protettivo nei confronti del Variola virus e di HIV. La Yersinia pestis, agente eziologico della peste bubbonica, è stata dimostrata in laboratorio non associabile a CCR5. I soggetti con la mutazione Δ32 sono sani, e ciò suggerisce che il gene CCR5 sia piuttosto superfluo; tuttavia CCR5 pare svolgere un ruolo protettivo nei confronti del virus del Nilo occidentale e gli studi clinici hanno dimostrato che i soggetti Δ32 hanno un rischio sproporzionatamente più alto di contrarre questa infezione[17], dimostrando che non tutte le funzioni di CCR5 possono essere compensate da altri recettori.
Nonostante la grande variabilità genetica di CCR5 nelle sue regioni codificanti, la delezione di 32 pb porta a un recettore non funzionante, che previene l'ingresso nella cellula dei ceppi virali HIV R5-tropici; la presenza di tale mutazione in omozigosi fornisce una forte protezione nei confronti dell'infezione da HIV[18]. Tale allele è stato trovato nel 5-14% degli europei, ma è raro presso gli africani e gli asiatici[19]; la sua presenza fa diminuire il numero di proteine CCR5 presenti nella membrana cellulare del linfocita T CD4+, con effetti sui tassi di progressione dell'infezione da HIV. Numerosi studi condotti su persone infettate da HIV hanno dimostrato che la presenza di una copia di CCR5-Δ32 ritarda l'insorgenza di AIDS per almeno due anni. È inoltre possibile che una persona con questa mutazione possa non venir infettata dai ceppi HIV R5-tropici[20].
Dal punto di vista terapeutico si è pensato di sfruttare questa condizione per la realizzazione di anticorpi monoclonali che blocchino l'espressione genica di CCR5, da utilizzare in soggetti infettati da HIV-1[21]. In vitro è stato dimostrato che i linfociti T, modificati per non presentare CCR5 e mescolati con linfociti T normali, sono portati a prendere il sopravvento nella coltura cellulare quando HIV attacca e uccide le cellule normali[21].
Tale ipotesi fu valutata in vivo in un paziente con AIDS, Timothy Ray Brown, che sviluppò contestualmente una leucemia mieloide acuta e che fu trattato con chemioterapia; ricevette quindi un trapianto di cellule staminali ematopoietiche da un donatore con omozigosi per CCR5-Δ32. Dopo due anni dal trattamento il paziente risultò in salute, con un livello indosabile di virioni nel sangue, nel cervello e nell'epitelio rettale[22][23]. Prima del trapianto il paziente presentava anche bassi livelli di HIV XR4-tropici, che non usano CCR5 per l'ingresso nella cellula; tuttavia, successivamente al trapianto, anche questi ceppi virali divennero indosabili[23]. Tale evento è spiegabile con l'osservazione che le cellule che esprimono la variante Δ32 risultano carenti, nella membrana cellulare, sia di CCR5, sia di CXCR4, conferendo una resistenza a un ampio numero di varianti di HIV[24]. Nel 2010, dopo tre anni dal trattamento, il paziente risultò ancora resistente al virus e fu dichiarato guarito[25].
Nel 2009 è iniziato uno studio clinico su pazienti sieropositivi per valutare l'utilizzo di una terapia genica che consiste nel trasporto della variante CCR5-Δ32 tramite una nucleasi zinc finger nelle cellule prelevate dal paziente; la reinfusione di queste cellule potrebbe rivelarsi una potenziale opzione nel trattamento dell'HIV[26][27].
Note[modifica | modifica wikitesto]
- ^ Samson M, Libert F, Doranz BJ, Rucker J, Liesnard C, Farber CM, Saragosti S, Lapoumeroulie C, Cognaux J, Forceille C, Muyldermans G, Verhofstede C, Burtonboy G, Georges M, Imai T, Rana S, Yi Y, Smyth RJ, Collman RG, Doms RW, Vassart G, Parmentier M, Resistance to HIV-1 infection in caucasian individuals bearing mutant alleles of the CCR-5 chemokine receptor gene, in Nature, vol. 382, n. 6593, agosto 1996, pp. 722–5, DOI:10.1038/382722a0, PMID 8751444.
- ^ a b Genetics Home Reference (archiviato dall'url originale il 24 settembre 2009).
- ^ Samson M, Labbe O, Mollereau C, Vassart G, Parmentier M, Molecular cloning and functional expression of a new human CC-chemokine receptor gene, in Biochemistry, vol. 35, n. 11, marzo 1996, pp. 3362–7, DOI:10.1021/bi952950g, PMID 8639485.
- ^ Slimani H, Charnaux N, Mbemba E, Saffar L, Vassy R, Vita C, Gattegno L, Interaction of RANTES with syndecan-1 and syndecan-4 expressed by human primary macrophages, in Biochim. Biophys. Acta, vol. 1617, 1–2, ottobre 2003, pp. 80–8, DOI:10.1016/j.bbamem.2003.09.006, PMID 14637022.
- ^ a b Struyf S, Menten P, Lenaerts JP, Put W, D'Haese A, De Clercq E, Schols D, Proost P, Van Damme J, <2170::AID-IMMU2170>3.0.CO;2-D Diverging binding capacities of natural LD78beta isoforms of macrophage inflammatory protein-1alpha to the CC chemokine receptors 1, 3 and 5 affect their anti-HIV-1 activity and chemotactic potencies for neutrophils and eosinophils, in Eur. J. Immunol., vol. 31, n. 7, luglio 2001, pp. 2170–8, DOI:10.1002/1521-4141(200107)31:7<2170::AID-IMMU2170>3.0.CO;2-D, PMID 11449371.
- ^ Proudfoot AE, Fritchley S, Borlat F, Shaw JP, Vilbois F, Zwahlen C, Trkola A, Marchant D, Clapham PR, Wells TN, The BBXB motif of RANTES is the principal site for heparin binding and controls receptor selectivity, in J. Biol. Chem., vol. 276, n. 14, aprile 2001, pp. 10620–6, DOI:10.1074/jbc.M010867200, PMID 11116158.
- ^ Miyakawa T, Obaru K, Maeda K, Harada S, Mitsuya H, Identification of amino acid residues critical for LD78beta, a variant of human macrophage inflammatory protein-1alpha, binding to CCR5 and inhibition of R5 human immunodeficiency virus type 1 replication, in J. Biol. Chem., vol. 277, n. 7, febbraio 2002, pp. 4649–55, DOI:10.1074/jbc.M109198200, PMID 11734558.
- ^ Anderson J, Akkina R, Complete Knockdown of CCR5 by lentiviral vector-expressed siRNAs and protection of transgenic macrophages against HIV-1 infection, in Gene Therapy, vol. 14, n. 14, 2007, pp. 1287–1297, DOI:10.1038/sj.gt.3302958, PMID 17597795.
- ^ a b Galvani AP, Slatkin M, Evaluating plague and smallpox as historical selective pressures for the CCR5-Delta 32 HIV-resistance allele, in Proc. Natl. Acad. Sci. U.S.A., vol. 100, n. 25, dicembre 2003, pp. 15276–9, DOI:10.1073/pnas.2435085100, PMC 299980, PMID 14645720.
- ^ Stephens JC, Reich DE, Goldstein DB, Shin HD, Smith MW, Carrington M, Winkler C, Huttley GA, Allikmets R, Schriml L, Gerrard B, Malasky M, Ramos MD, Morlot S, Tzetis M, Oddoux C, di Giovine FS, Nasioulas G, Chandler D, Aseev M, Hanson M, Kalaydjieva L, Glavac D, Gasparini P, Kanavakis E, Claustres M, Kambouris M, Ostrer H, Duff G, Baranov V, Sibul H, Metspalu A, Goldman D, Martin N, Duffy D, Schmidtke J, Estivill X, O'Brien SJ, Dean M, Dating the origin of the CCR5-Delta32 AIDS-resistance allele by the coalescence of haplotypes, in Am. J. Hum. Genet., vol. 62, n. 6, giugno 1998, pp. 1507–15, DOI:10.1086/301867, PMC 1377146, PMID 9585595.
- ^ Buseyne F, Janvier G, Teglas JP, Ivanoff S, Burgard M, Bui E, Mayaux MJ, Blanche S, Rouzioux C, Rivière Y, Impact of heterozygosity for the chemokine receptor CCR5 32-bp-deleted allele on plasma virus load and CD4 T lymphocytes in perinatally human immunodeficiency virus-infected children at 8 years of age, in J. Infect. Dis., vol. 178, n. 4, ottobre 1998, pp. 1019–23, DOI:10.1086/515660, PMID 9806029.
- ^ John Novembre, Alison P Galvani e Montgomery Slatkin, The Geographic Spread of the CCR5 Δ32 HIV-Resistance Allele, in PLOS Biology, 18 ottobre 2005.
- ^ a b Faure E, Royer-Carenzi M, Is the European spatial distribution of the HIV-1-resistant CCR5-Delta32 allele formed by a breakdown of the pathocenosis due to the historical Roman expansion?, in Infect. Genet. Evol., vol. 8, n. 6, dicembre 2008, pp. 864–74, DOI:10.1016/j.meegid.2008.08.007, PMID 18790087.
- ^ Freitas T, Brehm A, Fernandes AT, Frequency of the CCR5-delta32 mutation in the Atlantic island populations of Madeira, the Azores, Cabo Verde, and São Tomé e Príncipe, in Hum. Biol., vol. 78, n. 6, dicembre 2006, pp. 697–703, DOI:10.1353/hub.2007.0011, PMID 17564248.
- ^ Mirko D. Grmek, Diseases in the Ancient Greek World, marzo 1991.
- ^ Hedrick PW, Verrelli BC, "Ground truth" for selection on CCR5-Delta32, in Trends Genet., vol. 22, n. 6, giugno 2006, pp. 293–6, DOI:10.1016/j.tig.2006.04.007, PMID 16678299.
- ^ Glass WG, McDermott DH, Lim JK, Lekhong S, Yu SF, Frank WA, Pape J, Cheshier RC, Murphy PM, CCR5 deficiency increases risk of symptomatic West Nile virus infection, in J. Exp. Med., vol. 203, n. 1, gennaio 2006, pp. 35–40, DOI:10.1084/jem.20051970, PMC 2118086, PMID 16418398.
- ^ Duncan SR, Scott S, Duncan CJ, Reappraisal of the historical selective pressures for the CCR5-Delta32 mutation, in J. Med. Genet., vol. 42, n. 3, marzo 2005, pp. 205–8, DOI:10.1136/jmg.2004.025346, PMC 1736018, PMID 15744032.
- ^ Sabeti PC, Walsh E, Schaffner SF, Varilly P, Fry B, Hutcheson HB, Cullen M, Mikkelsen TS, Roy J, Patterson N, Cooper R, Reich D, Altshuler D, O'Brien S, Lander ES, The case for selection at CCR5-Delta32, in PLoS Biol., vol. 3, n. 11, novembre 2005, pp. e378, DOI:10.1371/journal.pbio.0030378, PMC 1275522, PMID 16248677.
- ^ Delta32 Genetic Testing (PDF), su Briefing paper for AFAO members, Australian Federation of AIDS Organisations, 1º giugno 2007. URL consultato il 22 gennaio 2011 (archiviato dall'url originale il 19 marzo 2012).
- ^ a b Steinberger P, Andris-Widhopf J, Bühler B, Torbett BE, Barbas CF, Functional deletion of the CCR5 receptor by intracellular immunization produces cells that are refractory to CCR5-dependent HIV-1 infection and cell fusion, in Proc. Natl. Acad. Sci. U.S.A., vol. 97, n. 2, gennaio 2000, pp. 805–10, DOI:10.1073/pnas.97.2.805, PMC 15412, PMID 10639161.
- ^ Schoofs M, A Doctor, a Mutation and a Potential Cure for AIDS, in The Wall Street Journal, 7 novembre 2008. URL consultato il 15 dicembre 2010.
- ^ a b Hütter G, Nowak D, Mossner M, Ganepola S, Müssig A, Allers K, Schneider T, Hofmann J, Kücherer C, Blau O, Blau IW, Hofmann WK, Thiel E, Long-term control of HIV by CCR5 Delta32/Delta32 stem-cell transplantation, in N. Engl. J. Med., vol. 360, n. 7, febbraio 2009, pp. 692–8, DOI:10.1056/NEJMoa0802905, PMID 19213682.
- ^ Agrawal L, Lu X, Qingwen J, VanHorn-Ali Z, Nicolescu IV, McDermott DH, Murphy PM, Alkhatib G, Role for CCR5Delta32 protein in resistance to R5, R5X4, and X4 human immunodeficiency virus type 1 in primary CD4+ cells, in J. Virol., vol. 78, n. 5, marzo 2004, pp. 2277–87, DOI:10.1128/JVI.78.5.2277-2287.2004, PMC 369216, PMID 14963124.
- ^ Allers K, Hütter G, Hofmann J, Loddenkemper C, Rieger K, Thiel E, Schneider T, Evidence for the cure of HIV infection by CCR5Δ32/Δ32 stem cell transplantation, in Blood, vol. 117, n. 10, dicembre 2010, pp. 2791–2799, DOI:10.1182/blood-2010-09-309591, PMID 21148083.
- ^ Autologous T-Cells Genetically Modified at the CCR5 Gene by Zinc Finger Nucleases SB-728 for HIV (Zinc-Finger), su clinicaltrials.gov, U.S. National Institutes of Health, 9 dicembre 2009. URL consultato il 30 dicembre 2009.
- ^ Nicholas Wade, Zinc Fingers Could Be Key to Reviving Gene Therapy, in The New York Times, 28 dicembre 2009. URL consultato il 30 dicembre 2009.
Bibliografia[modifica | modifica wikitesto]
- Wilkinson D, Cofactors provide the entry keys. HIV-1, in Curr. Biol., vol. 6, n. 9, 1997, pp. 1051–3, DOI:10.1016/S0960-9822(02)70661-1, PMID 8805353.
- Broder CC, Dimitrov DS, HIV and the 7-transmembrane domain receptors, in Pathobiology, vol. 64, n. 4, 1997, pp. 171–9, DOI:10.1159/000164032, PMID 9031325.
- Choe H, Martin KA, Farzan M, Sodroski J, Gerard NP, Gerard C, Structural interactions between chemokine receptors, gp120 Env and CD4, in Semin. Immunol., vol. 10, n. 3, 1998, pp. 249–57, DOI:10.1006/smim.1998.0127, PMID 9653051.
- Sheppard HW, Celum C, Michael NL, O'Brien S, Dean M, Carrington M, Dondero D, Buchbinder SP, HIV-1 infection in individuals with the CCR5-Delta32/Delta32 genotype: acquisition of syncytium-inducing virus at seroconversion, in J. Acquir. Immune Defic. Syndr., vol. 29, n. 3, 2002, pp. 307–13, PMID 11873082.
- Freedman BD, Liu QH, Del Corno M, Collman RG, HIV-1 gp120 chemokine receptor-mediated signaling in human macrophages, in Immunol. Res., vol. 27, 2–3, 2004, pp. 261–76, DOI:10.1385/IR:27:2-3:261, PMID 12857973.
- Esté JA, Virus entry as a target for anti-HIV intervention, in Curr. Med. Chem., vol. 10, n. 17, 2004, pp. 1617–32, DOI:10.2174/0929867033457098, PMID 12871111.
- Gallo SA, Finnegan CM, Viard M, Raviv Y, Dimitrov A, Rawat SS, Puri A, Durell S, Blumenthal R, The HIV Env-mediated fusion reaction, in Biochim. Biophys. Acta, vol. 1614, n. 1, 2003, pp. 36–50, DOI:10.1016/S0005-2736(03)00161-5, PMID 12873764.
- Zaitseva M, Peden K, Golding H, HIV coreceptors: role of structure, posttranslational modifications, and internalization in viral-cell fusion and as targets for entry inhibitors, in Biochim. Biophys. Acta, vol. 1614, n. 1, 2003, pp. 51–61, DOI:10.1016/S0005-2736(03)00162-7, PMID 12873765.
- Lee C, Liu QH, Tomkowicz B, Yi Y, Freedman BD, Collman RG, Macrophage activation through CCR5- and CXCR4-mediated gp120-elicited signaling pathways, in J. Leukoc. Biol., vol. 74, n. 5, 2004, pp. 676–82, DOI:10.1189/jlb.0503206, PMID 12960231.
- Yi Y, Lee C, Liu QH, Freedman BD, Collman RG, Chemokine receptor utilization and macrophage signaling by human immunodeficiency virus type 1 gp120: Implications for neuropathogenesis, in J. Neurovirol., 10 Suppl 1, 2004, pp. 91–6, PMID 14982745.
- Seibert C, Sakmar TP, Small-molecule antagonists of CCR5 and CXCR4: a promising new class of anti-HIV-1 drugs, in Curr. Pharm. Des., vol. 10, n. 17, 2004, pp. 2041–62, DOI:10.2174/1381612043384312, PMID 15279544.
- Cutler CW, Jotwani R, Oral mucosal expression of HIV-1 receptors, co-receptors, and alpha-defensins: tableau of resistance or susceptibility to HIV infection?, in Adv. Dent. Res., vol. 19, n. 1, 2006, pp. 49–51, DOI:10.1177/154407370601900110, PMID 16672549.
- Ajuebor MN, Carey JA, Swain MG, CCR5 in T cell-mediated liver diseases: what's going on?, in J. Immunol., vol. 177, n. 4, 2006, pp. 2039–45, PMID 16887960.
- Lipp M, Müller G, Shaping up adaptive immunity: the impact of CCR7 and CXCR5 on lymphocyte trafficking, in Verhandlungen der Deutschen Gesellschaft für Pathologie, vol. 87, 2006, pp. 90–101, PMID 16888899.
- Balistreri CR, Caruso C, Grimaldi MP, Listì F, Vasto S, Orlando V, Campagna AM, Lio D, Candore G, CCR5 receptor: biologic and genetic implications in age-related diseases, in Ann. N. Y. Acad. Sci., vol. 1100, 2007, pp. 162–72, DOI:10.1196/annals.1395.014, PMID 17460174.
- Madsen HO, Poulsen K, Dahl O, Clark BF, Hjorth JP, Retropseudogenes constitute the major part of the human elongation factor 1 alpha gene family, in Nucleic Acids Res., vol. 18, n. 6, 1990, pp. 1513–6, DOI:10.1093/nar/18.6.1513, PMC 330519, PMID 2183196.
- Uetsuki T, Naito A, Nagata S, Kaziro Y, Isolation and characterization of the human chromosomal gene for polypeptide chain elongation factor-1 alpha, in J. Biol. Chem., vol. 264, n. 10, 1989, pp. 5791–8, PMID 2564392.
- Whiteheart SW, Shenbagamurthi P, Chen L, Cotter RJ, Hart GW, Murine elongation factor 1 alpha (EF-1 alpha) is posttranslationally modified by novel amide-linked ethanolamine-phosphoglycerol moieties. Addition of ethanolamine-phosphoglycerol to specific glutamic acid residues on EF-1 alpha, in J. Biol. Chem., vol. 264, n. 24, 1989, pp. 14334–41, PMID 2569467.
- Ann DK, Wu MM, Huang T, Carlson DM, Wu R, Retinol-regulated gene expression in human tracheobronchial epithelial cells. Enhanced expression of elongation factor EF-1 alpha, in J. Biol. Chem., vol. 263, n. 8, 1988, pp. 3546–9, PMID 3346208.
- Brands JH, Maassen JA, van Hemert FJ, Amons R, Möller W, The primary structure of the alpha subunit of human elongation factor 1. Structural aspects of guanine-nucleotide-binding sites, in Eur. J. Biochem., vol. 155, n. 1, 1986, pp. 167–71, DOI:10.1111/j.1432-1033.1986.tb09472.x, PMID 3512269.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
Collegamenti esterni[modifica | modifica wikitesto]
- UniProt, su UniProt. URL consultato il 20 agosto 2023.
