Condensazione: differenze tra le versioni
| Riga 22: | Riga 22: | ||
* '''Condensazione a gocce:''' il vapore condensa sotto forma di piccole gocce, che si possono staccare dalla superficie lasciandola libera per la formazione di nuove gocce. |
* '''Condensazione a gocce:''' il vapore condensa sotto forma di piccole gocce, che si possono staccare dalla superficie lasciandola libera per la formazione di nuove gocce. |
||
È evidente che la condensazione a gocce può sviluppare [[Coefficiente di scambio termico|coefficienti di scambio termico]] molto più elevati rispetto quella a film.{{vedi anche|Condensatore (tecnologie chimiche)}} |
È evidente che la condensazione a gocce può sviluppare [[Coefficiente di scambio termico|coefficienti di scambio termico]] molto più elevati rispetto quella a film. |
||
== Applicazioni == |
|||
{{vedi anche|Condensatore (tecnologie chimiche)}} |
|||
Nell'ambito della [[chimica industriale]] e della chimica sperimentale, la condensazione è un'"[[operazione unitaria]].", cioè una tappa di un insieme di processi chimico-fisici che hanno come scopo la trasformazione di una sostanza. Ad esempio viene svolta la condensazione di una [[Corrente materiale|corrente]] fluida nella parte alta di una [[colonna di distillazione]] o all'interno di un [[ciclo frigorifero]]. |
Nell'ambito della [[chimica industriale]] e della chimica sperimentale, la condensazione è un'"[[operazione unitaria]].", cioè una tappa di un insieme di processi chimico-fisici che hanno come scopo la trasformazione di una sostanza. Ad esempio viene svolta la condensazione di una [[Corrente materiale|corrente]] fluida nella parte alta di una [[colonna di distillazione]] o all'interno di un [[ciclo frigorifero]]. |
||
Versione delle 16:50, 6 dic 2018


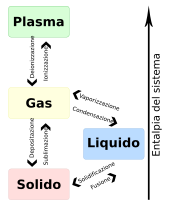
La condensazione (anche detta liquefazione) è la transizione di fase dalla fase aeriforme alla fase liquida di una sostanza.[1] Tale trasformazione si può eseguire:
- a temperatura costante per compressione, se la temperatura dell'aeriforme è inferiore a quella critica;[2]
- per raffreddamento con una fonte esterna;
- per espansione adiabatica.
La condensazione può avvenire generalmente in due modi:
- condensazione volumetrica: avviene normalmente nei fenomeni naturali, come per esempio nelle nuvole;
- condensazione su superfici: usata soprattutto per aspetti tecnici e ingegneristici, per esempio negli scambi di calore.
In ogni caso l'operazione di condensazione è esotermica, cioè avviene sottraendo calore alla sostanza che si vuole condensare.[3]
Condensazione su superfici
La condensazione su superfici può avvenire in due modi:
- Condensazione a film: il vapore condensa sulla superficie creando un film di liquido, che percola verso il basso per gravità; la presenza del film liquido ostacola la formazione di nuovo condensato.
- Condensazione a gocce: il vapore condensa sotto forma di piccole gocce, che si possono staccare dalla superficie lasciandola libera per la formazione di nuove gocce.
È evidente che la condensazione a gocce può sviluppare coefficienti di scambio termico molto più elevati rispetto quella a film.
Applicazioni
Nell'ambito della chimica industriale e della chimica sperimentale, la condensazione è un'"operazione unitaria.", cioè una tappa di un insieme di processi chimico-fisici che hanno come scopo la trasformazione di una sostanza. Ad esempio viene svolta la condensazione di una corrente fluida nella parte alta di una colonna di distillazione o all'interno di un ciclo frigorifero.
L'operazione di condensazione viene largamente usata in tecnologia chimica per condensare sostanze ottenute allo stato di vapore, onde commerciarle o trattarle sotto forma liquida: ciò vale, per esempio per la benzina, che nei processi di distillazione è ottenuta sotto forma di vapore. Mentre un vapore puro condensa a temperatura costante, i vapori misti condensano in un intervallo di temperatura, separando prima i componenti meno volatili, quindi i più volatili, il che permette la separazione di composti o di frazioni (condensazione frazionata).
-
Un esempio di condensatore utilizzato nell'industria chimica
-
Un esempio di condensatore da laboratorio
-
Schema di un ciclo frigorifero (il condensatore è posto a destra)
Inoltre il fenomeno della condensazione del vapore acqueo può essere sfruttato per recuperare l'acqua contenuta nell'atmosfera sotto forma di vapore acqueo. Su tale principio si basa il dissalatore ad energia solare ("solar still"), il "condensatore Zibold" e altre apparecchiature più complesse, quali i "condensatori a energia solare".
-
Schema di funzionamento di un distillatore ad energia solare
-
Schema di funzionamento di un condensatore Zibold
-
Un impianto a terra di condensatori a energia solare
Note
- ^ Rolla, p. 100
- ^ In tal caso l'aeriforme sarà detto vapore.
- ^ (EN) DOE Fundamentals Handbook - "Thermodynamics, Heat transfer, and fluid flow", p. 38. Archiviato il 20 dicembre 2016 in Internet Archive.
Bibliografia
- Luigi Rolla, Chimica e mineralogia. Per le Scuole superiori, 29ª ed., Dante Alighieri, 1987.
Voci correlate
- Equazione di Kelvin
- Breath figures
- Fase (chimica)
- Apparecchiature chimiche
- Operazione unitaria
- Caldaia (riscaldamento)
- Condensatore barometrico
- Diagramma di Glaser
Altri progetti
 Wikizionario contiene il lemma di dizionario «condensazione»
Wikizionario contiene il lemma di dizionario «condensazione» Wikimedia Commons contiene immagini o altri file su condensazione
Wikimedia Commons contiene immagini o altri file su condensazione
Collegamenti esterni
- (EN) condensation, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Condensazione industriale (PDF), su studenti.dicamp.units.it.