Fase (chimica)

Si definisce fase una porzione di un sistema termodinamico che presenta stato fisico e composizione chimica essenzialmente uniformi,[1] mentre altre grandezze (ad esempio temperatura e pressione) possono essere non uniformi.
Un sistema omogeneo è sempre monofasico (cioè costituito da una singola fase), mentre un sistema eterogeneo è in genere polifasico o multifase (cioè costituito da più fasi). Un sistema composto da sostanze aeriformi presenta sempre una singola fase.
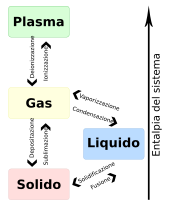
Il concetto di fase non corrisponde al concetto di stato di aggregazione, dunque quando si parla di fase solida, fase liquida o fase gassosa si sta specificando lo stato di aggregazione che caratterizza una particolare fase del sistema, ma all'interno dello stesso sistema possono essere presenti ad esempio più fasi liquide o più fasi solide.
Diagramma di fase[modifica | modifica wikitesto]

I diversi stati termodinamici di un sistema possono essere rappresentati mediante il diagramma di fase. Sugli assi di tale diagramma vengono riportate le variabili termodinamiche rilevanti, solitamente pressione e temperatura; si parla in questo caso di "diagramma p-T".
In un diagramma di fase sono rappresentate delle linee; tali linee delimitano delle aree bidimensionali e l'intersezione di due o più linee avviene in punti del diagramma. Ognuno di tali luoghi geometrici presenti nel diagramma ha un significato preciso; in particolare, nel caso di un diagramma p-T:
- i punti che stanno all'interno delle aree bidimensionali corrispondono a condizioni di temperatura e pressione per le quali il sistema è costituito da una sola fase;
- i punti che stanno su una singola linea corrispondono a condizioni di temperatura e pressione per le quali il sistema è costituito da due fasi;
- i punti individuati dall'intersezione di due linee corrispondono a condizioni di temperatura e pressione per le quali il sistema è costituito da tre fasi.
Il diagramma di fase viene detto anche "diagramma di stato" in quanto ciascuno punto del diagramma corrisponde ad un particolare stato termodinamico.
Separazione di fase[modifica | modifica wikitesto]
In un sistema possono coesistere diverse fasi, separate tra loro da superfici di separazione.
La regola delle fasi di Gibbs descrive il numero di fasi che possono essere presenti in un sistema in equilibrio al variare delle condizioni. La regola delle fasi indica che per un singolo componente di un sistema possono coesistere in equilibrio al massimo tre fasi (solitamente liquida, solida e gassosa). Le tre fasi possono coesistere esclusivamente ad un solo valore di temperatura e pressione, caratteristico del materiale, detto punto triplo. La regola delle fasi indica anche che due fasi possono coesistere in equilibrio per specifiche combinazioni di temperatura e pressione; dato un sistema liquido/gas ad una data temperatura, all'equilibrio la pressione avrà un valore definito, se il sistema si trovasse a valori di pressione inferiore una parte della fase liquida evaporerà fino a raggiungere il valore di pressione appropriato o fino a consumarsi completamente. Allo stesso modo, se la pressione della fase gassosa fosse troppo elevata, avremmo la condensazione del gas fino al raggiungimento del valore di equilibrio.
Note[modifica | modifica wikitesto]
Voci correlate[modifica | modifica wikitesto]
- Sistema bifase (termodinamica)
- Stato della materia
- Transizione di fase
- Energia libera di Gibbs
- Regola delle fasi di Gibbs
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su fase
Wikimedia Commons contiene immagini o altri file su fase
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) Simeon Potter e Ernest G. Ehlers, phase, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.