Tumore della tiroide
| Tumore della tiroide | |
|---|---|
 | |
| Specialità | Endocrinologia, chirurgia generale |
| Eziologia | mutazioni nella via delle MAPKinasi |
| Sede colpita | ghiandola tiroide |
| Incidenza mondiale | 1-5/100.000 |
| Classificazione e risorse esterne (EN) | |
| MedlinePlus | 001213 |
| eMedicine | 851968 |
| Sinonimi | |
| Cancro della tiroide | |
I tumori della tiroide possono essere benigni e maligni. Il tumore della tiroide[1] è una patologia relativamente rara (1-2% delle neoplasie), ma in grande crescita negli ultimi anni: nel periodo 1973-2002 l'incidenza è aumentata del 48% negli uomini e del 67% nelle donne.[2]
Il trattamento più efficace per i tumori tiroidei aggressivi è la rimozione chirurgica della ghiandola tiroidea (tiroidectomia), seguita dalla ablazione con iodio-131 radioattivo e dalla terapia di soppressione del TSH.[3][4] Oggigiorno, nei casi di malattia avanzata, metastatica, in progressione e non operabile si ricorre alle target therapies con gli inibitori kinasici (TKIs), prevalentemente Lenvatinib, Cabozantinib o Sorafenib[5], tali trattamenti sono peraltro gravati da vari effetti collaterali, quali ipertensione arteriosa, disturbi gastrointestinali, tossicità cutanea, biliare (colelitiasi, colecistiti) e renale (presenza di proteine[6], di solito albumina, nelle urine)[7][8]. Resta valido il ruolo della radioterapia, specie su alcune metastasi, quali ossa o encefalo. Negli Stati Uniti, i tassi di sopravvivenza a cinque anni sono del 97,8%[9], recenti studi dimostrano però che nonostante la buona sopravvivenza, chi ha avuto esperienza di cancro alla tiroide vede una diminuzione della qualità della vita e manifesta sintomi di disagio psicologico, quali ansia o depressione[10].
Anatomia chirurgica e descrittiva della tiroide[modifica | modifica wikitesto]


La tiroide è un organo impari e mediano, situato nella regione antero mediana del collo. È costituita da due lobi laterali, riuniti attraverso un istmo impari e mediano.
I due lobi hanno forma conica a base inferiore, si estendono, nell'adulto, per circa 3 cm da metà altezza della cartilagine tiroide sino a circa il 5° anello tracheale. Lo spessore dei lobi può variare tra 0,5 cm verso l'apice a 2 cm verso la base. L'istmo collega i due lobi in prossimità della loro base, e risulta applicato ai primi due anelli tracheali. Nella metà dei casi, dal margine superiore dell'istmo si diparte un prolungamento ghiandolare, di forma e dimensioni molto variabili, che si dirige in alto verso sinistra, raggiungendo l'osso ioide e talvolta superandolo verso la radice della lingua. Prende il nome di lobo piramidale o piramide di Morgagni, e rappresenta una testimonianza del percorso compiuto dalla ghiandola durante la sua organogenesi. Talvolta è presente una struttura fibromuscolare che collega l'osso ioide all'istmo o al lobo piramidale, chiamata in letteratura muscolo elevatore della tiroide.[11][12]
La tiroide risulta avvolta da una guaina fibrosa (guaina peritiroidea), considerata dipendenza della fascia cervicale media. Da questa si dipanano tralci fibrosi, con funzione di legamenti, che assicurano l'organo alla cartilagine tiroide della laringe (legamento sospensore o mediano), alla cartilagine cricoide della laringe e ai primi anelli tracheali (legamenti laterali interni), e alla guaina fibrosa che contorna il fascio vascolonervoso del collo (legamenti laterali esterni). All'interno di questa guaina è ospitata la ghiandola, a sua volta protetta da una capsula fibrosa intimamente adesa all'organo stesso. Nello spessore che separa la capsula dalla guaina, decorre un fitto intreccio vascolare, tributario delle vene e delle arterie locali, fatto che ha assegnato il nome di “spazio pericoloso peritiroideo” all'area. Inoltre, in questo spazio, sul versante posteriore della ghiandola, sono presenti le paratiroidi. Delle tre facce (mediale, antero-laterale e posteriore) la mediale è concava e abbraccia la faccia laterale della trachea e delle cartilagini cricoide e tiroide e, in maniera variabile, l'esofago. La faccia posteriore, meno estesa delle altre, contrae rapporto con la carotide comune e quindi con la vena giugulare interna, avvolte dalla propria guaina.[11][12]
L'organo risulta adeso, posteriormente, alla superficie ventrale della cartilagine tiroidea (“lo scudo tiroideo”) della laringe, e ai primi due anelli tracheali. Ventralmente, risulta coperta dai muscoli sottoioidei: in senso anteroposteriore, dall'omoioideo, dal tiroioideo e dallo sternotiroideo. A causa del decorso obliquo di questi muscoli lungo l'asse verticale del collo, si apre al di sopra del margine superiore dello sterno una finestra anatomica dove la ghiandola risulta scoperta da muscoli, fatta eccezione per la fascia cervicale media e superficiale che, fondendosi, separano l'organo dalla cute. Questo rappresenta il punto di repere ove, nella maggior parte dei casi, è possibile palpare e repertare possibili alterazioni della tiroide durante l'esame obiettivo di un paziente. Bilateralmente, la tiroide è coperta dai muscoli sternocleidomastoideo, e, più superficialmente, dai fasci del muscolo platisma del collo.[11][12]
Il margine esterno del lobo di sinistra della tiroide, posteriormente, si appoggia sulla faccia ventrale esofagea, formando un lieve corridoio attraverso il quale decorre il nervo ricorrente di sinistra. Grazie a tutte queste strutture, la tiroide risulta tenacemente adesa all'asse laringotracheale, risultando solidale nei movimenti di quest'ultimo.[11][12]
Vascolarizzazione e innervazione[modifica | modifica wikitesto]

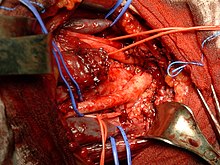
La tiroide risulta servita da un sistema di quattro arterie: le arterie tiroidee superiori e inferiori (in numero di due per lato); mentre viene drenata attraverso sei vene: le vene tiroidee superiori, medie e inferiori (in numero di tre per lato).
Sistema arterioso[modifica | modifica wikitesto]
Le arterie tiroidee superiori destra e sinistra sono rami della carotide esterna e raggiungono l'organo dall'alto. Le arterie tiroidee inferiori di destra e di sinistra, invece, nascono dal tronco tireocervicale della rispettiva succlavia, e decorrono dal basso verso l'alto. In un quarto dei casi è possibile repertare una piccola arteria tiroidea ima, ramo dell'arteria brachiocefalica oppure dell'arteria carotide comune, che raggiunge l'organo dal basso verso l'istmo, decorrendo sulla linea mediana sulla faccia ventrale della trachea.[11][12]
Di significativa importanza risulta la descrizione del punto di diramazione dei vasi terminali dell'arteria tiroidea inferiore: infatti, a questo livello, in vicinanza con i poli inferiori dei lobi laterali della tiroide, decorre il nervo ricorrente (o laringeo inferiore), ramo del nervo vago. Esso transita dal basso verso l'alto, di solito in un occhiello vascolare. Il chirurgo deve sempre prestare attenzione a questa regione durante la legatura del vaso corrispondente.
Sistema venoso[modifica | modifica wikitesto]
Il drenaggio venoso avviene attraverso una fitta rete situata nello spazio pericoloso, dalla quale prendono origine le vene tiroidee superiori e medie, che drenano nelle vene giugulari interne bilateralmente, e le vene tiroidee inferiori, tributarie del tronco brachiocefalico.[11][12]
Innervazione[modifica | modifica wikitesto]
Le strutture nervose di interesse per la regione chirurgica tiroidea sono rappresentate dal nervo laringeo superiore, più precisamente dalla sua branca esterna, e dall'inferiore. Il nervo laringeo superiore origina dal vago in prossimità del ganglio nodoso, al di sotto del forame giugulare, si porta in basso e in avanti passando dietro la carotide interna e l'esterna all'origine della linguale; giunto in corrispondenza del corno superiore dello joide si biforca nelle branche interna ed esterna. La prima decorre sul muscolo costrittore inferiore della faringe, coperta dall'arteria laringea superiore, si insinua fra muscoli tirojoideo e membrana omonima, che attraversa per fornire l'innervazione sensitiva alla mucosa laringea sovraglottica e faringea. La branca esterna scende invece verticalmente in prossimità dell'inserzione mediale del muscolo costrittore inferiore, applicata a quest'ultimo, e raggiunge il muscolo cricotiroideo che innerva mantenendo la tensione delle corde vocali; una sua lesione comporta quindi una riduzione del tono e della forza vocale, per lo più compensata dal controlaterale. Come si accennava appunto, il ramo esterno nel suo decorso contrae rapporti con l'arteria tiroidea superiore, che incrocia anteriormente, ponendosi in posizione mediale e anteriore al ramo di divisione arterioso anteriore. Il nervo laringeo inferiore o ricorrente destro emerge al limite inferiore del collo dal vago, poco al di sopra dell'incrocio di questo con l'arteria succlavia, circonda questa sulla faccia anteriore, inferiore e posteriore, e si porta in alto e medialmente.
A sinistra nasce al livello toracico, dove il vago incrocia la faccia anteriore dell'arco aortico; si riflette attorno all'arco dall'avanti all'indietro e assume un decorso verso l'alto e medialmente, passando nell'angolo fra arco stesso e il legamento arterioso sulla faccia anteriore dell'esofago. Al livello cervicale il nervo presenta un decorso ascendente convergente verso la trachea; l'angolo fra il decorso del nervo e il margine tracheale è più ampio a destra essendo qui più laterale la riflessione del nervo. Da entrambi i lati il nervo incrocia posteriormente la carotide comune all'origine e compare nella regione cervicale nello spazio compreso fra la trachea e l'arteria. Interseca quindi l'arteria tiroidea inferiore in maniera estremamente variabile: sul tronco (14%); alla divisione dell'arteria nei suoi rami (11%); in corrispondenza delle branche arteriose (75%). Le modalità di incrocio sono rese più complesse dalla possibilità che ciò avvenga in posizione retroarteriosa (47%), prearteriosa (28%) o interarteriosa (25%). Dopo un brevissimo tratto libero il nervo si porta sotto la zona di aderenza fra ghiandola e trachea (legamento di Gruber). Mantenendo questo stretto rapporto con il margine e la faccia posteriore del lobo il ricorrente raggiunge la sede di ingresso in laringe, situata in corrispondenza della articolazione crico-tiroidea, posteriormente alla faccetta articolare, coperto da muscolo costrittore inferiore della faringe (cricofaringeo).
Come già detto, a questo livello il nervo è incrociato da arteriole provenienti dalla tiroidea inferiore, che ne rendono più difficile la preparazione chirurgica e, talora, ne confondono il decorso. Qualche volta il nervo ricorrente si divide in due branche, molto raramente in un numero maggiore, generalmente in prossimità o subito sopra l'incrocio con l'arteria tiroidea inferiore; in questo caso i rami hanno un decorso parallelo rimanendo piuttosto vicini fino al loro ingresso laringeo. Quasi costantemente il laringeo inferiore fornisce un ramo cervicale, a decorso ascendente e posteriore, destinato all'innervazione sensitiva e motoria dell'ipofaringe, che si anastomizza con un corrispondente ramo, proveniente dalla branca esterna del laringeo superiore. Seppure impropriamente, nell'uso comune a questa anastomosi nervosa viene attribuito il nome di nervo di Galeno, che più propriamente spetta a un'anastomosi intralaringea fra i due nervi laringei. Decorrendo profondamente alla cartilagine tiroide il laringeo inferiore genera 5 rami. Nel loro decorso, i rami del nervo ricorrente sono situati profondamente allo scheletro cartilagineo della laringe, alquanto esposti a possibili traumatismi che provengono dall'interno del lume della via aerea (es. intubazione orotracheale) per il fatto di essere contenuti in tale struttura rigida.[11][12]
Rapporti con le ghiandole paratiroidi[modifica | modifica wikitesto]
Indispensabile nell'approccio alla chirurgia tiroidea risulta la conoscenza delle paratiroidi, dei loro rapporti anatomo-topografici. Generalmente in numero di 4, le paratiroidi vengono distinte in superiori e inferiori. Le superiori sono situate approssimativamente in un cerchio di 2,5 cm di diametro subito al di sopra del punto di ingresso nella tiroide dei rami dell'arteria tiroidea superiore; le inferiori in un cerchio analogo che comprende l'arteria e la zona sottostante. Più precisamente le superiori, la cui sede è maggiormente costante, si trovano nella porzione superiore della faccia posteriore del lobo, all'altezza della cartilagine cricoidea e in prossimità del punto di ingresso del nervo laringeo inferiore nella cricoide.[11][12]
Le inferiori, con sede più incostante, sono poste più lateralmente, tra la faccia posteriore e il margine laterale della tiroide, all'unione del terzo medio con l'inferiore della ghiandola, in stretta connessione con l'arteria tiroidea inferiore e il nervo ricorrente[13]. Con notevole frequenza sono presenti ghiandole paratiroidi ectopiche e in sovrannumero; spesso le inferiori infatti possono essere reperite nello spazio cervicomediastinico[14].
Vasi linfatici e stazioni linfonodali[modifica | modifica wikitesto]
Il drenaggio linfatico del collo è dato da numerosi gruppi linfonodali connessi tra loro. I linfonodi cervicali, immersi nel tessuto cellulare lasso interposto tra le fasce cervicali, sono distinti in una rete superficiale e una profonda, ampiamente anastomizzate tra loro e con una comunicazione tra i due lati.
- Stazioni linfonodali superficiali: comprese tra fascia cervicale superficiale e media, includono: linfonodi della loggia interdigastrica, linfonodi della loggia sottomandibolare, linfonodi della loggia parotidea, linfonodi della loggia occipitale, linfonodi della loggia mastoidea o retro auricolare, linfonodi del gruppo giugulare anteriore, linfonodi del gruppo della vena giugulare esterna.
- Stazioni linfonodali profonde: in numero di 15-30, si trovano al di sotto della fascia cervicale media e comprendono i linfonodi:
- della catena linfonodale del triangolo linfatico profondo della regione laterale del collo: linfonodi della catena giugulare interna. Si classificano in linfonodi superiori, medi e inferiori. A destra danno il dotto giugulare che comunemente si immette direttamente nella vena giugulare interna alla confluenza fra questa e la succlavia. A sinistra danno il tronco giugulare che confluisce nel dotto toracico. Ricevono la linfa della faccia, della nuca e degli organi dello spazio viscerale impari mediano.
- linfonodi dell'accessorio spinale. Sono da cinque a dieci linfonodi satelliti del ramo laterale del nervo omonimo. Ricevono la linfa dai linfonodi occipitali, retroauricolari e soprascapolari, della parte posteriore e laterale del cuoio capelluto, della nuca, della regione laterale del collo e della spalla.
- linfonodi cervicali traversi. Decorrono lungo l'arteria e la vena traversa del collo. Il linfonodo posto più medialmente di questa catena prende il nome di linfonodo di Troisier. Ricevono i linfatici provenienti dalla catena del nervo accessorio spinale, dalle regioni mammarie e antero-laterali del collo, dall'arto superiore.
- del comparto centrale o iuxtaviscerali. Quelle che sono considerate stazioni primarie degli organi contenuti nello spazio viscerale impari mediano, sono rappresentati dai linfonodi posti davanti alla laringe (prelaringei), della trachea (pretracheali) e della ghiandola tiroide (pretiroidei), dietro la faringe (retrofaringei), sulle facce laterali della trachea (latero-tracheali o catena ricorrenziali), del mediastino antero-superiore.
Il sistema linfatico della ghiandola tiroide. Intorno ai follicoli origina una fitta rete linfatica che confluisce, mediante vie linfatiche perilobulari, in un sistema capsulare e pericapsulare a sua volta tributario di stazioni diverse. Collettori linfatici dal bordo superiore dal bordo superiore dell'istmo raggiungono il linfonodo delfico davanti alla membrana cricotiroidea. Da qui si dipartono collettori per il gruppo linfonodale superiore e medio della catena giugulare interna connesso, a sua volta, con la catena linfonodale dell'accessorio spinale. Altri collettori linfatici si dipartono dal margine inferiore dell'istmo per raggiungere le catene pretracheali, ricorrenziali e cervicali traverse. Queste, a loro volta, contraggono rapporti con i collettori provenienti dalla porzione postero-mediale dei lobi tiroidei.
La classificazione più spesso usata suddivide le stazioni linfonodali del collo in “compartimenti”, utili da un punto di vista diagnostico ma soprattutto terapeutico, particolarmente nell'approccio alle linfectomie[15]
- I linfonodi sottomentonieri (Ia) e sottomandibolari (Ib). I linfonodi sottomentonieri sono inclusi nel tessuto fibroadiposo posto superficialmente al muscolo milo-joideo, tra il margine inferiore della mandibola, i margini anteriori dei muscoli sternocleidomastoidei e un piano passante per il corpo dell'osso joide. I linfonodi sottomandibolari invece circondano la ghiandola salivare omonima.
- II linfonodi giugulari superiori, giugulo-digastrici e spinali anteriori. Sono localizzati attorno al terzo superiore della vena giugulare interna, dal basi cranio fino a un piano passante per l'osso joide. Il margine anteriore è definito dal muscolo stiloiodeo, mentre quello posteriore dal muscolo sternocleidomastoideo. Vengono suddivisi a loro volta in due gruppi, IIa e IIb, i primi situati antero-medialmente a un piano verticale definito dal nervo accessorio spinale, i secondi situati postero-lateralmente allo stesso piano.
- III linfonodi giugulari medi. Sono compresi tra l'osso ioide superiormente e la cartilagine cricoide inferiormente. Il confine antero-mediale di tale livello è rappresentato dal margine laterale del muscolo sterno ioideo, quello postero-laterale dal margine posteriore del muscolo sternocleidomastoideo.
- IV linfonodi giugulari inferiori. Sono localizzati al terzo inferiore della vena giugulare interna, tra la cartilagine cricoide superiormente e la clavicola inferiormente, tra il muscolo sternotiroideo anteriormente e il muscolo sternocleidomastoideo posteriormente.
- V linfonodi dell'accessorio spinale medi e inferiori. Sono inclusi nel triangolo posteriore del collo, delimitato dal margine posteriore del muscolo sternocleidomastoideo dalla clavicola e dal margine anteriore del trapezio. Il sottolivello Va include i linfonodi dell'accessorio spinale, mentre il sottolivello Vb include i linfonodi cervicali trasversi e i linfonodi sopraclaveari, con l'eccezione del linfonodo di Virchow, localizzato nel IV livello.
- VI linfonodi del comparto centrale o anteriore. Sono compresi nello spazio delimitato dalla guaina carotidea lateralmente, dall'osso ioide superiormente e dall'incisura sternale inferiormente. Includono i linfonodi prelaringei, pretracheali, peritiroidei, paratracheali.
- VII linfonodi della regione mediastinica. Comprende i periricorrenziali inferiori e i mediastinici superiori.
Pur non rientrando a pieno titolo nei linfonodi della regione cervicale da un punto di vista strettamente anatomico, il VII livello merita importante menzione poiché, assieme al VI livello rappresentano i linfonodi più a rischio di diffusione metastatica di tumore della tiroide.
Tumori benigni[modifica | modifica wikitesto]

Si tratta di noduli solitari della tiroide e possono arrecare due tipi di problemi: ipertiroidismo e disturbi da compressione meccanica alla trachea o all'esofago. Si associano a prognosi benigna in quanto, diversamente da quelli maligni, non si diffondono nel corpo.
La presentazione clinica del tumore benigno è quella del nodulo tiroideo, che in genere viene studiato ecograficamente riconoscendo alcuni caratteri di benignità o di sospetta malignità. Caratteri ecografici di benignità sono l'aspetto cistico (i noduli cistici sono pressoché sempre benigni), l'assenza di microcalcificazioni, la regolarità dei margini periferici, l'assenza di vascolarizzazione intranodulare al power doppler, la mancanza di crescita nel tempo. Alla scintigrafia tiroidea si può distinguere il nodulo ipercaptante, cosiddetto nodulo caldo da quello ipocaptante, cosiddetto nodulo freddo. I noduli caldi sono pressoché sempre benigni però possono dare una sintomatologia di ipertiroidismo con tachicardia, cardiopatia fino all'insufficienza cardiaca, disturbi psichici e dimagrimento. Va distinto il nodulo caldo autonomo sfuggito al controllo ipofisario, non sopprimibile con terapia con ormone tiroideo, ma che non comporta segni clinici di ipertiroidismo se non l'abbassamento del TSH, dal nodulo francamente "tossico" con sintomatologia di ipertiroidismo e cardiotossicosi (adenoma tossico di Plummer).
La terapia dell'adenoma tossico è chirurgica (lobectomia) mentre la terapia radiometabolica viene riservata ai casi con controindicazioni o rifiuto all'intervento. I noduli freddi corrispondono in genere al reperto citologico di lesione follicolare (TIR3), che purtroppo non consente una distinzione certa fra lesione benigna (adenoma follicolare) e lesione maligna (carcinoma follicolare). Per tale motivo in questi casi si consiglia la terapia chirurgica che consente anche, con l'esame istologico definitivo, una diagnosi di certezza.
Normalmente il nodulo solido di dimensioni inferiori a 1 cm e senza caratteri ecografici di sospetto viene sottoposto a follow-up clinico, laboratoristico ed ecografico.
Il nodulo di dimensioni superiori al centimetro viene sottoposto ad agoaspirato e il risultato sarà determinante per le scelte terapiche successive. I noduli di grosse dimensioni che, pur di comportamento benigno, determinano fenomeni compressivi sugli organi vicini determinando dispnea e/o disfagia, vengono sottoposti a trattamento chirurgico.
Tumori maligni[modifica | modifica wikitesto]
Sono tumori che, nati nella tiroide, possono diffondersi nel corpo. La diffusione tumorale può avvenire in tre modi:
- per contiguità, infiltrando strutture vicine alla tiroide (trachea, esofago, muscoli del collo, nervo ricorrente);
- attraverso il sistema linfatico (metastasi ai linfonodi del collo);
- attraverso i vasi sanguigni (metastasi a organi distanti come il polmone).
Questa capacità di diffusione si associa a una prognosi meno favorevole o "maligna". Fortunatamente, a parte qualche rara forma a prognosi infausta, la maggior parte di loro, con cure adeguate, guarisce. Le forme più frequenti sono poco aggressive in quanto formate da cellule molto simili alle cellule sane (o differenziate).
Epidemiologia[modifica | modifica wikitesto]
Incidenza[modifica | modifica wikitesto]
Sono attesi nel 2017, in Italia 15.300 nuovi casi di tumore della tiroide di cui:
- 11.000 tra le donne;
- 4.300 tra gli uomini.[16]
Prevalenza[modifica | modifica wikitesto]
L'AIRTUM (Associazione italiana dei registri tumori) ha registrato dal 2008 al 2013 i seguenti dati di tumore della tiroide nella popolazione italiana:
- 82% tumori papillari;
- 7% tumori follicolari;
- 3% tumori midollari;
- 1% tumori anaplastici.
Mortalità[modifica | modifica wikitesto]
I decessi per tumore alla tiroide sono estremamente bassi e la sopravvivenza è strettamente correlata con l'età alla diagnosi.
Al 2014 in Italia sono stati registrati in totale 533 decessi, di cui:[senza fonte]
- 317 donne;
- 216 uomini.
Fattori di rischio[modifica | modifica wikitesto]
Gli oncologi italiani Giovanni Bernardo e Laura Locati hanno proposto una categorizzazione dei fattori dei rischio in base all'eziologia e alla popolazione target:[16]
| Tumore maligno | Natura e sottotipi del
fattore di rischio |
Eziologia | Patogenesi | Popolazione target
maggiormente suscettibile |
|---|---|---|---|---|
| Carcinoma differenziato |
|
|
Nei casi di comorbidità: associazione con obesità, tiroiditi autoimmuni, patologia tiroidea nodulare (gozzo) |
|
| Carcinoma midollare |
|
Entrambi sono:
|
|
|
| Carcinoma Anaplastico | Non disponibile | Non disponibile | Non disponibile | Non disponibile |
Epidemiologia in altre nazioni[modifica | modifica wikitesto]
Il tumore della tiroide è il più comune tumore endocrinologico, approssimativamente l'1-1,5% di tutti i nuovi casi diagnosticati ogni anno in USA[17]. La sua incidenza è in continua crescita nelle ultime tre decadi in tutto il mondo. Basandosi sui dati, il cancro della tiroide è il quinto cancro più comune nella donna[18], e, in Italia, è il secondo cancro più frequente nelle donne sotto i 45 anni[19]. Soltanto in pochissimi paesi (Norvegia e Svezia) l'incidenza è diminuita.
Fattori genetici, influenze ambientali e accesso alle cure mediche possono spiegare esaustivamente le differenze geografiche ed etniche. Report recenti hanno dimostrato che, nonostante il tasso più basso di incidenza di tumore della tiroide sia osservabile nella popolazione nera, la parte più grande dei PTC insorge nelle donne nere[20]. L'aumento dell'incidenza è quasi esclusivo della forma PTC, con nessun significativo aumento per le forme follicolare, midollare o anaplastica. L'incremento, infine, riguarda principalmente i piccoli tumori, sebbene pure i grandi tumori siano in leggero aumento[21].
Quadro clinico[modifica | modifica wikitesto]
La neoplasia tiroidea, soprattutto nelle sue fasi iniziali, può dimostrare scarsa o assente sintomatologia. Il nodulo carcinomatoso, infatti, cresce senza necessariamente sviluppare caratteristiche di iper o ipo – tiroidismo, facendo venire a mancare i tipici cortei sintomatologici che, nelle patologie infiammatorie della tiroide, pongono l'indicazione allo studio della ghiandola. Il nodulo tiroideo dà segno della propria presenza attraverso l'occupazione di spazio, in un periodo che può variare dai pochi mesi (nel caso dei tumori più aggressivi) ai dieci anni. I pazienti giungono in visita per via del cosiddetto “gozzo”, un ingrandimento localizzato della regione del collo, dovuto usualmente alla crescita del nodulo, o, nei casi di multifocalità, a un ingrandimento generalizzato del tessuto ghiandolare.
L'apprezzamento di un gozzo non può essere considerato indicatore specifico e sensibile di patologia neoplastica, essendo l'ipertrofia e l'iperplasia della ghiandola il normale meccanismo cellulare di risposta a una qualsiasi patologia tiroidea. In dipendenza dalla localizzazione di questa tumefazione del collo, che potrà essere superficiale o profonda, anteriore o posteriore, sarà possibile, per il clinico esperto, identificare la massa attraverso le normali procedure di palpazione in sede di esame obiettivo. La palpazione, sempre bimanuale, avviene con l'operatore posto alle spalle del paziente, con il collo in modesta estensione, onde favorire la superficializzazione delle strutture ghiandolari. Ci si potrà, inoltre, avvalere dell'aiuto della manovra della deglutizione (invitando il paziente a bere un sorso di acqua da un bicchiere), che permetterà di differenziare una struttura di pertinenza della tiroide da una proveniente dai tessuti viciniori: infatti, nel caso di un nodulo, per via dell'intima connessione con l'asse laringo-tracheale della ghiandola, esso seguirà l'innalzamento del laringe durante la deglutizione, muovendosi da sotto le mani dell'operatore. Sarà così possibile descrivere una tumefazione nodulare circoscritta, mobile con gli atti della deglutizione, o piuttosto un ingrandimento generalizzato del parenchima. Altrettanto, sarà possibile descrivere la consistenza della tumefazione palpata, che usualmente, nei casi di neoplasia, si presenta come dura-lignea o fibro-elastica. La repertazione di una massa non è che il primo step nel processo diagnostico necessario per inquadrare la malattia: infatti, l'esame obiettivo non è sufficiente per potere porre diagnosi, ma soltanto per indirizzare nell'iter diagnostico il medico.
L'occupazione di spazio, prodotta dal nodulo, può portare, quando ingravescente, al coinvolgimento delle strutture viciniori della tiroide, provocando alcuni sintomi tipici che permettono di sospettare una patologia tiroidea. Come precedentemente descritto in questo lavoro, l'iperplasia della ghiandola può coinvolgere le strutture nervose ricorrenti (nn. Laringei inferiori), provocando un abbassamento significativo del tono della voce, che può arrivare, nei casi più avanzati, alla paralisi di una o entrambe le corde vocali, con lo sviluppo, nel paziente, di una disfonia permanente. La crescita in senso posteriore, invece, può arrivare a coinvolgere l'asse respiratorio, ovvero la trachea, comprimendo meccanicamente il canale cartilagineo, e causando dispnea e sensazione di ostruzione (il cosiddetto “gnocco in gola”, per come viene riferito dai pazienti) nelle alte vie aeree. Nei casi più avanzati, può esserci compressione dell'esofago, che fa seguito al coinvolgimento tracheale, producendo disfagia e alterazioni nella deglutizione.
Noduli palpabili sono rinvenuti in circa il 5% della popolazione adulta, ma la frequenza varia considerevolmente tra paese e paese. Lo sviluppo dei noduli è più frequente nelle aree gozzigene, a carenza di iodio nell'alimentazione. L'iter diagnostico deve essere in grado di distinguere, da questa percentuale, le lesioni che possono avere carattere di malignità. La maggior parte dei noduli palpabili dal clinico, risulta essere più grande di 1 cm.
Tipicamente, la presenza di tessuto neoplastico nel distretto della ghiandola tiroidea, può accompagnarsi al coinvolgimento latero-cervicale delle stazioni linfonodali peri-giugulari: in questi casi, alla palpazione, sarà possibile evidenziare delle tumefazioni – mobili o ipomobili, di consistenza fibro-elastica o duro-lignea - repertabili nel II-III-IV livello del collo. L'individuazione del coinvolgimento linfonodale depone, già all'esame obiettivo, per un processo neoplastico in corso, da porre in differenziale con altre patologie a carattere linfomatoso o infettivo.
Sulla base delle caratteristiche istologiche della neoplasia (variante papillifera o follicolare), sarà possibile evidenziare o meno un interessamento, nelle forme più avanzate, di organi e tessuti extra-tiroidei: difatti, se l'istotipo papillifero metastatizza per via linfatica e soltanto eccezionalmente per via vascolare, la variante follicolare mostra una maggiore propensione per la metastatizzazione a distanza in altri organi, coinvolgendo meno frequentemente i linfonodi.
Varianti istologiche[modifica | modifica wikitesto]


Carcinomi differenziati:
- Carcinoma papillifero della tiroide (papillary thyroid carcinoma, PTC) (75% dei tumori tiroidei);
- Carcinoma follicolare della tiroide (follicular thyroid carcinoma, FTC) (15% dei tumori tiroidei):
Altri tumori tiroidei (10%):
- Carcinoma midollare della tiroide
- Carcinoma anaplastico della tiroide
- Linfoma maligno tiroideo
- Carcinoma metastatico della tiroide
Iter diagnostico[modifica | modifica wikitesto]
L'iter verso la diagnosi di carcinoma differenziato della tiroide comincia, come sopra ricordato, con l'esame obiettivo del collo del paziente. Il corretto iter diagnostico di un nodulo tiroideo è stato codificato nelle più recenti “Linee Guida per la gestione dei pazienti con nodulo tiroideo e carcinoma differenziato della tiroide”, prodotte dalla American Thyroid Association, e ratificate da molte altre società internazionali[22]. La palpazione sarà accompagnata dalla prescrizione dei comuni esami ematologici in grado di verificare la funzionalità della ghiandola tiroidea: TSH, FT3, FT4. Il primo tra questi permetterà di scegliere la metodica di immagini più appropriata per differenziare il nodulo sospetto in senso di benignità o malignità. Difatti, il rilievo di bassi valori di TSH pone indicazione all'esecuzione di una scintigrafia con radio-iodio, in quanto evidenza di una condizione di iper-tiroidismo da approfondire maggiormente. Questa condizione può essere legata alla presenza di un nodulo solitario iper-funzionante (adenoma tossico di Plummer), generalmente benigno. Il rilievo di un nodulo “freddo” (ipocaptante alla scintigrafia del collo), o di un valore di TSH nella norma o leggermente aumentato, pone indicazione all'esecuzione di un esame ecografico e citologico del nodulo sospetto.

L'ecografia del collo è uno strumento imprescindibile nella diagnosi di CDT. Un'ecografia diagnostica dovrebbe essere eseguita in tutti i pazienti con il sospetto di nodulo tiroideo o gozzo nodulare, o alterazioni radiografiche riscontrante incidentalmente mediante tomografia computerizzata (TC), risonanza magnetica nucleare (RMN), o captazione alla FDG-PET (Tomografia a emissione di positroni con fluorodesossiglucosio). La visualizzazione ecografica permette di collegare con certezza l'evidenza palpatoria di una tumefazione del collo alla presenza di un nodulo della ghiandola, confermando il coinvolgimento linfonodale (se presente), identificando le caratteristiche del contenuto del nodulo (liquido, solido o misto), e localizzando correttamente la lesione. Diverse caratteristiche ecografiche quali l'ipoecogenicità del nodulo rispetto al parenchima circostante, la vascolarizzazione intranodulare, i margini irregolari, la presenza di microcalcificazioni, l'assenza di alone periferico e la forma più alta che larga nella scansione trasversale sono stati associati a una più elevata probabilità di malignità[23][24].
Con l'eccezione della presenza di linfoadenopatie cervicali sospette, che costituisce una caratteristica altamente specifica ma poco sensibile, le altre caratteristiche ecografiche di sospetto, isolatamente o in combinazione, non costituiscono parametri adeguatamente sensibili e specifici per identificare con certezza tutti i noduli maligni, anche se alcune caratteristiche o associazioni hanno un elevato potere predittivo di malignità[22]. Inoltre, ecograficamente è possibile identificare alcuni elementi che possono distinguere la variante papillifera da quella follicolare: la prima, difatti, si presenta più spesso ipoecogena e solida, spesso con margini irregolari e aumento della vascolarizzazione. La presenza di microcalcificazioni è altamente specifica per PTC, ma queste possono essere difficili da distinguere rispetto alle lacune di colloide. Al contrario, il carcinoma follicolare è più spesso iso-iper ecogeno, con un alone spesso e irregolare, senza microcalcificazioni[25], e, quando inferiore ai 2 cm, non è mai associato a metastasi[26]. Come ulteriore elemento di valutazione, oltre al color-doppler per identificare i pattern di vascolarizzazione del nodulo, recenti studi hanno dimostrato l'utilità dell'ultra-elasto-sonografia nella diagnosi differenziale dei noduli della tiroide: una tecnica promettente, che richiede ulteriore validazione con studi prospettici[27].
Contemporaneamente all'esecuzione dell'ecografia, le linee guida ATA prevedono l'esecuzione di un esame citologico con tecnica Fine-Needle-Aspiration. La FNAc eco-guidata è il gold standard nella diagnosi differenziale dei noduli tiroidei, permettendo una accurata identificazione, nella maggior parte dei casi, delle lesioni benigne. L'esame citologico andrebbe eseguito su tutti i noduli con diametro maggiore di 1 cm, venendo sconsigliata nei casi di lesioni sub-centimetriche[22]. Tradizionalmente, i risultati della FNAc sono divisi in 5 categorie: non diagnostico (Tir1), nodulo benigno (Tir2), nodulo dal potenziale indeterminato (Tir3), nodulo con probabile comportamento maligno (Tir4), e nodulo maligno (Tir5) (rischio di malignità alla chirurgia >95%). Per ognuno di questi risultati, oggi le linee guida ATA pongono differente indicazione chirurgica:
| Classificazione AgoAspirato | Significato | Strategia terapeutica |
|---|---|---|
| Tir1 | esame non diagnostico | ripetere agoaspirato |
| Tir2 | nodulo benigno | follow-up |
| Tir3 | nodulo indeterminato | trattamento chirurgico (lobectomia? tiroidectomia radicale?) |
| Tir4 | nodulo con probabile malignità | trattamento chirurgico (tiroidectomia radicale +/- linfectomia) |
| Tir5 | nodulo maligno | trattamento chirurgico (tiroidectomia radicale + linfectomia) |
La categoria “lesione indeterminata”, classificata secondo il Bethesda System come tir3, rappresenta, oggi, uno degli scogli più difficili da superare nella diagnosi di carcinoma tiroideo. Infatti questo riscontro, evidenziabile nel 15-30% degli FNAc[28], comporta un rischio di malignità del 20-30%[29]: l'impossibilità, alla citologia, di stabilire con certezza le caratteristiche di malignità (problema legato principalmente all'impossibilità a verificare l'invasione e il superamento della capsula), pongono l'indicazione alla chirurgia come strumento di conferma diagnostica. Risulta però evidente che, in circa l'80% di questi pazienti, la tiroidectomia totale rappresenta un intervento sproporzionato rispetto alla diagnosi istologica, necessario però di fronte all'incertezza pre-operatoria. Più recentemente, la Società Italiana di Anatomia Patologica e Citologia Diagnostica – Divisione italiana della International Academy of Pathology (SIAPEC-IAP), ha proposto l'istituzione di due sottocategorie, tir3A e tir3B: nella prima rientrerebbero i casi di iperplasia adenomatoide, e le lesioni non sufficientemente maligne da rientrare nel grado successivo, ma troppo avanzate per essere classificate come benigne. Il grado tir3b verrebbe, invece, assegnato agli adenomi, ai carcinomi follicolari micro invasivi, alle lesioni ossifile a cellule di Hurtle, e infine alle varianti follicolari dei PTC. Inoltre, la SIAPEC-IAP pone indicazione all'intervento chirurgico soltanto nei casi classificati come tir3B, consigliando il follow-up ecografico a sei mesi per le lesioni tir3A[30].
Diversi markers molecolari[31], nello specifico la galectina-3, citocheratina-19 e Hector-Batifora-Mesothelial-1 (HBME-1), sono stati proposti per migliorare l'accuratezza diagnostica dell'agoaspirato[32]. Anche l'uso di marcatori genetici è stato proposto[33], con particolare successo nel caso dei kit per l'individuazione della mutazione BRAF-V600E (vd. successivamente capitolo “Biologia”). Proprio la ricerca di questa mutazione sembra correlare con una maggiore aggressività, maggior rischio di recidiva post-operatoria, un rischio più alto di invasione vascolare, e una maggiore resistenza alla terapia con radio-iodio. L'esecuzione del test per la mutazione BRAF-V600E potrebbe non essere cost-effective in tutti i pazienti da sottoporre a FNAc, e il suo potenziale per migliorare la selezione dei noduli da portare all'intervento chirurgico potrebbe non essere così elevato. D'altro canto, quando i patologi individuano lesioni citologiche che fanno propendere il sospetto diagnostico verso un PTC, l'esecuzione del test potrebbe portare a maggiori informazioni rispetto al risk-staging del paziente e alla sua prognosi, candidandosi come fattore prognostico in grado di modificare la radicalità dell'intervento chirurgico da proporre[34]. Ancora dibattuto, seppur sempre più al centro del dibattito scientifico, il ruolo dei microRNA all'esame citologico: ai risultati incoraggianti, sarà necessario affiancare un poderoso studio prospettico in grado di identificare l'accuratezza diagnostica di queste metodiche.
Una volta eseguito l'esame citologico, in tutti i casi classificati come tir3b-4-5 vi è indicazione alla chirurgia. Il coinvolgimento linfonodale può essere individuato, con tecniche anatomo-patologiche standard, nel 20-50% dei pazienti con carcinoma differenziato della tiroide (particolarmente nell'istotipo papillifero)[35], e può essere presente anche quando il tumore è piccolo e intratiroideo[36]. Micrometastasi coinvolgenti le stazioni linfonodali sono evidenziabili in circa il 90% dei casi[37], ma il loro significato clinico è ancora discusso, risultando controverso il ruolo nel peggiorare la prognosi rispetto alle macrometastasi. L'ecografia del collo individua un coinvolgimento linfonodale nel 20-31% dei casi, influenzando in un 20%[38] dei pazienti l'approccio chirurgico e la relativa radicalità[39]. In ogni caso, a causa dell'effetto-copertura esercitato dalla tiroide, l'ecografia individua soltanto la metà dei linfonodi poi evidenziabili durante la procedura chirurgica[40].
Esistono delle caratteristiche ecografiche in grado di discriminare tra linfonodi patologici e no: la forma rotondeggiante e non più ovalare, l'aspetto cistico, la vascolarizzazione interna anziché periferica, la perdita dell'ilo, l'ipoecogenicità e le microcalcificazioni. Nessuno di questi parametri, da solo, è abbastanza sensibile da potere essere condizione certa diagnostica di metastasi da carcinoma tiroideo. L'aspetto ecografico con maggiore sensibilità (100%) è la perdita dell'ilo, che però mostra una specificità del 29%[41]. Le stazioni linfonodali coinvolte possono aiutare a porre il sospetto, risultando i livelli III-IV-VI maggiormente interessati dalla malattia rispetto al II livello. Una conferma della malignità è possibile ottenerla attraverso esame FNAc con dosaggio della tireoglobulina nel liquido di lavaggio. Quest'ultimo è affidabile anche in pazienti con anticorpi anti-Tg circolanti[42].
Uno staging accurato è conditio sine qua non per determinare la prognosi e per individualizzare il trattamento dei pazienti con tumore differenziato della tiroide. La presenza di tessuto metastatico non solleva dalla necessità di procedere alla rimozione chirurgica del tumore primitivo. Infatti, poiché le metastasi possono rispondere al trattamento con radio-iodio, la rimozione del tumore e del tessuto tumorale loco-regionale rimane una componente importante del trattamento iniziale[22].
Indicazioni alla chirurgia[modifica | modifica wikitesto]
L'obiettivo della terapia chirurgica consiste nella rimozione del tumore primitivo, il tessuto tumorale esteso oltre la capsula tiroidea e i linfonodi cervicali coinvolti. La completezza della resezione chirurgica costituisce un importante fattore capace di influenzare il risultato finale, mentre eventuali linfonodi metastatici residui rappresentano il più comune sito di persistenza/ripresa di malattia. Altri obiettivi, individuati sempre dalle linee guida internazionali stilate dall'ATA, prevedono l'accurata stadiazione post-operatoria attraverso l'esame istologico della ghiandola asportata; e la facilitazione del trattamento post-operatorio con iodio radioattivo, per il quale la rimozione di tutto il tessuto tiroideo normale costituisce requisito fondamentale.
Nei casi di citologia non diagnostica o indeterminata, ai pazienti con una neoplasia inferiore ai 4 cm, che lo vogliano, può essere proposto un intervento meno radicale, consistente nella lobectomia tiroidea. Questo intervento, che permette comunque di stadiare e inquadrare istologicamente la neoplasia, si caratterizza per una minore radicalità, giustificata dall'alto tasso di pazienti privi di lesione maligna (circa l'80%). Ma in un 20% circa dei casi, costringe il paziente a sottoporsi a un secondo intervento di totalizzazione, indicato dallo studio istologico del lobo asportato, qualora il risultato confermasse il sospetto di malignità[43].
Di fronte a una biopsia diagnostica per nodulo maligno, si pone indicazione all'esecuzione di una tiroidectomia totale, in tutti i casi in cui la massa sia maggiore di 1 cm. Ulteriori evidenze, più recenti, hanno dimostrato l'utilità di un approccio maggiormente radicale anche nei confronti delle masse minori di 1 cm (cosiddetti microcarcinomi): uno studio con oltre 50.000 pazienti con PTC ha mostrato all'analisi multivariata che la tiroidectomia totale migliora significativamente i tassi di sopravvivenza e recidiva in pazienti con tumore <1 cm[44]. Anche l'età avanzata (>45 anni) può essere un'indicazione al trattamento chirurgico totale o quasi-totale anche per tumori <1-1,5 cm a causa degli alti tassi di recidiva di malattia in questa fascia di età[45][46][47][48].
Le metastasi linfonodali, alla diagnosi, sono presenti nel 20-90% dei pazienti con PTC, e proporzionalmente in misura minore negli altri istotipi[49][50]. Anche se le metastasi linfonodali da PTC hanno dimostrato di avere, secondo alcuni, un importante effetto sull'esito di pazienti a basso rischio, uno studio del database della Surveillance, Epidemiology, and END research (SEER) ha mostrato che su 9 904 pazienti con PTC, la presenza di metastasi linfonodali, l'età >45anni, metastasi a distanza e aumentate dimensioni tumorali erano predittori significativi di prognosi poco favorevole all'analisi multivariata[51]. La sopravvivenza assoluta a 14 anni era dell'82% per PTC senza metastasi linfonodali, e del 79% con metastasi linfonodali (p < 0,05).
In definitiva, il ruolo della linfoadenectomia non trova ancora sufficiente accordo tra gli esperti. Difatti, già nelle linee guida ATA, si consiglia di eseguire una tiroidectomia totale con linfoadenectomia centrale soltanto se si repertano linfonodi patologici, nel caso in cui l'operatore che esegue la procedura non sia sufficientemente esperto. Allo stato attuale, si pone indicazione all'intervento di linfoadenectomia centrale terapeutica (VI livello), contemporaneamente all'intervento di tiroidectomia totale, quando è presente un coinvolgimento clinico dei linfonodi del compartimento centrale o laterocervicali, assicurando una completa liberazione da malattia nella regione centrale del collo. Invece, per la linfoadenectomia profilattica, si lascia libertà di giudizio all'operatore, consigliandola nei casi di malattia avanzata (T3 o T4).
Terapia radiometabolica[modifica | modifica wikitesto]
Questa terapia è spesso utilizzata nel trattamento dei tumori tiroidei differenziati (cioè in grado di accumulare il radioiodio), successivamente all'intervento chirurgico, per distruggere il tessuto tiroideo residuo, la malattia residua eventualmente presente nel letto operatorio e le metastasi a distanza (che possono anche essere rilevate mediante scintigrafia).
Si esegue somministrando al paziente, in regime di ricovero protetto all'interno di un reparto di medicina nucleare, il radioiodio stesso (per la precisione, l'isotopo 131 dello iodio). Questa sostanza, comportandosi esattamente come lo iodio stabile normalmente assunto con la dieta dal paziente, si accumula solo nel tessuto tiroideo residuo e nelle eventuali metastasi linfonodali e a distanza, permettendone la distruzione selettiva mediante il rilascio in loco di un'alta dose di radiazioni. Non è mai stato dimostrato un aumento di incidenza di secondi tumori nei pazienti trattati. Controindicazioni assolute sono la gravidanza in atto[52] e l'allattamento (se non interrotto definitivamente). La quantità di iodio somministrata al paziente col trattamento è molto bassa e quindi non sufficiente a scatenare reazioni in soggetti allergici allo iodio; l'allergia allo iodio pertanto non è una controindicazione.
Fattori prognostici e sistemi di risk staging[modifica | modifica wikitesto]
La prognosi dei tumori papilliferi della tiroide è condizionata da differenti fattori, composti da elementi clinici, patologici e molecolari. Nonostante una prognosi generalmente molto favorevole, i PTC – che ricordiamo essere la più frequente neoplasia maligna endocrinologica negli umani – possono essere suddivisi in due gruppi: una grossa maggioranza di pazienti che va incontro a remissione completa, e una percentuale più piccola che va incontro a un decorso clinico maggiormente aggressivo, se non anche all'exitus. Questa constatazione si associa all'evidenza che, nel 10-15% dei PTC[53], si assiste a una trasformazione – per lo più ancora inspiegata - di queste neoplasie, che da responsive alla terapia divengono radio-iodio-resistenti, e possono causare la morte del paziente. In generale, comunque, nei pazienti affetti da PTC ben differenziato (DTC), si è evidenziato un tasso di sopravvivenza a dieci anni superiore all'85% nella maggior parte delle casistiche[54][55][56].
Moltissimi fattori sono stati studiati per cercare di determinare la prognosi, e più nello specifico il rischio di recidiva, di questa patologia. Alcuni di questi possono essere studiati pre-operativamente, permettendo di dare un'indicazione alla tipologia di intervento a cui candidare il paziente, mentre altri sono calcolabili solamente dopo l'intervento chirurgico, e sono utili per programmare il follow-up. Un elemento di difficoltà in proposito è rappresentato dalla necessità di un periodo di osservazione lungo, dell'ordine dei 15-20 anni, per poter rilevare differenze prognostiche e per escludere definitivamente la possibilità di recidiva.
Lo staging della neoplasia è considerato essere, sicuramente, uno dei fattori prognostici più importanti, esattamente come negli altri modelli di cancro umano. La classificazione proposta dalla UICC/AJCC attualmente è quella che riscuote maggiore successo ai fini stadiativi, basandosi sul sistema internazionale TNM. Questa classificazione, inoltre, ha dimostrato di riuscire a prevedere il rischio di morte dei pazienti affetti da carcinoma differenziato, ma non il rischio di recidiva[22].
L'età alla diagnosi si conferma, negli studi più recenti[53], un importante elemento di valutazione: infatti, l'effetto avverso dell'età nella prognosi aumenta gradualmente ogni dieci anni di vita, soprattutto dopo i 40-45 anni[47]. Da un punto di vista pratico, i pazienti con diagnosi prima dei 45 anni hanno una prognosi migliore rispetto a quelli più anziani. Questo cut-off fissato a 45 anni è uno dei parametri più importanti utilizzati nella stadiazione proposta dalla UICC/AJCC staging system. Questa relazione è stata osservata grazie a studi condotti su bambini, i quali hanno mostrato un tasso di mortalità più basso, anche se nelle età più giovani è più frequente la presentazione della malattia sotto forma di neoplasia estesa e metastatica[57]. I pazienti più anziani sono affetti da una maggiore incidenza di varianti istologiche aggressive, malattia estesa e metastasi a distanza alla diagnosi. I tumori tendono a essere meno differenziati nell'anziano, con un uptake dello iodio-131 minore se comparati con soggetti giovani[58], e nel primo si assiste a una maggiore e più rapida incidenza di ricorrenza di malattia dopo il trattamento iniziale. Almeno 5 classificazioni (EORTEC, TNM, AGES, AMES e MACIS), sviluppate attorno agli anni ottanta, hanno avuto una notevole diffusione, ma almeno altrettante sono state proposte da singoli gruppi di ricerca (MSK, Ohio, ecc.). Premettiamo da subito che tutte queste classificazioni, per quanto ancora possano essere oggetto di dibattito in letteratura, trovano sempre meno applicazione nella pratica clinica, sostituite dalle classificazioni proposte dall'American Thyroid Association (ATA), dalla European Thyroid Association (ETA) e dalla Latin American Thyroid Society (LATS), ma soprattutto dalla stadiazione AJCC basata sulla classificazione TNM.
Sopravvivenza generale a 5 e 10 anni in base alla variante istologica di tumore della tiroide[59][60][61][62][63][64]
| Tipo di tumore delle tiroide |
Sopravvivenza a 5 anni | Sopravvivenza a 10 anni | ||||
|---|---|---|---|---|---|---|
| Stadio I | Stadio II | Stadio III | Stadio IV | Complessivamente | Complessivamente | |
| Papillare | 100% | 100% | 93% | 51% | 96%-97% | 93% |
| Follicolari | 100%< | 100%< | 71% | 50% | 91% | 85% |
| Midollare | 100%< | 98% | 81% | 28% | 80%, 83% o 86% | 75% |
| Anaplastico | (spesso stadio IV) | 7% | 7%-14% | (nessun dato) | ||
Recupero dopo la malattia[modifica | modifica wikitesto]
Per garantire la migliore qualità della vita possibile a chi viene trattato per un cancro alla tiroide, è necessario un approccio multidisciplinare che prenda in considerazione componenti fisiche e psicologiche. L'attività fisica, il rilascio miofasciale, una terapia manuale eseguita da fisioterapisti, la mobilizzazione articolare e degli esercizi posturali sono raccomandati per migliorare i risultati e limitare gli effetti collaterali dell'eventuale chirurgia e delle terapie; la riabilitazione personalizzata permette di gestire la disfonia e la disfagia[65].
Biologia molecolare[modifica | modifica wikitesto]
Le alterazioni genetiche, alla base delle mutazioni in senso oncogenetico, delle neoplasie maligne delle cellule follicolari della tiroide sono concentrate attorno a due vie molecolari: la via della protein chinasi mitogeno attivata (MAP) e la via della fosfatidil-inositolo-3-chinasi (PI-3K)/AKT. Nella loro normale attivazione, queste vie sono utilizzate temporaneamente attraverso il legame tra il fattore di crescita e le tirosin-chinasi recettoriali (mediato attraverso il dominio extracellulare), che comporta l'autofosforilazione del dominio citoplasmatico, consentendo la traduzione del messaggio. Nei carcinomi della tiroide, così come in altri tumori solidi, le mutazioni che comportano un'acquisizione di funzione, lungo le componenti di queste vie, portano a un'attivazione costitutiva anche in assenza di ligando, promuovendo in tal modo la cancerogenesi[66]. Nei carcinomi papillari, l'attivazione della via delle MAP-chinasi è pressoché costante, e avviene in seguito a due meccanismi di seguito descritti. Il primo comporta riarrangiamenti di RET o NTRK1 (Neurotrophic Tyrosine Kinase Receptor 1), entrambi codificanti per tirosin-chinasi transmembrana. Il secondo meccanismo implica invece mutazioni puntiformi del gene BRAF, il cui prodotto è una componente intermedia della via delle MAP-chinasi. La trasformazione neoplastica, inoltre e più in generale, può dipendere da vari meccanismi genetici ed epigenetici che includono: attivazione e inattivazione di mutazioni somatiche, alterazioni nei pattern di espressione genica, disregolazione dei microRNA e metilazione aberrante dei geni[67].
Il gene RET si trova sul cromosoma 10q11, e la proteina derivante dalla codificazione del gene non è normalmente espressa dalle cellule epiteliali della tiroide, bensì dalle cellule parafollicolari C. A causa di fenomeni non ancora completamente compresi, nell'oncogenesi dei PTC è possibile rinvenire inversioni paracentriche del cromosoma 10 o una traslocazione reciproca tra i cromosomi 10 e 17: queste alterazioni cromosomiche mettono sotto il controllo trascrizionale dei geni costitutivamente espressi dalle cellule epiteliali della tiroide le tirosin-chinasi espresse dal gene RET. I geni di fusione, chiamati RET/PTC sono presenti in circa il 20-40% dei carcinomi papilliferi della tiroide. Vi sono oltre 15 partner di fusione di RET, due in particolare – RET/PTC1 e RET/PTC2 – sono osservabili comunemente nelle forme sporadiche. La frequenza di questi riarrangiamenti è più alta nei pazienti esposti a radiazioni. La proteina RET/PTC è una classica oncoproteina che attiva le vie MAPK e PI3K-AKT[68]. Essa è in grado di attivarle entrambe, reclutando adattatori di segnale e legandoli per fosforilazione al dominio intracellulare della proteina di fusione.
Allo stesso modo, inversioni paracentriche o traslocazioni di NTRK1 sul cromosoma 1q21 sono presenti nel 5-10% dei PTC. Le proteine derivate sono espresse costitutivamente dai tireociti, e portano all'attivazione della via delle MAP-chinasi e di altre vie di regolazione.
In circa il 45% dei carcinomi papilliferi della tiroide[69] si presenta una mutazione puntiforme con acquisizione di funzione del gene BRAF, specificamente una variazione valina-glutammato sul codone 600 (BRAFV600E), che porta alla mutazione di queste serina/treonina chinasi.
Poiché le mutazioni dei geni RET, NTRK1 e BRAF hanno effettori simili sul tessuto tiroideo (tutte quante portano all'attivazione costitutiva della via delle MAP-chinasi), nei carcinomi papilliferi non è possibile individuare entrambe le mutazioni contemporaneamente: i PTC mostrano, infatti, o l'una o l'altra mutazione molecolare. Infine, queste mutazioni non sono rinvenibili nell'istotipo follicolare o nell'adenoma tiroideo.
Nella variante follicolare del PTC, l'analisi mutazionale dei geni mostra una differente storia oncologica: difatti, si notano una minore frequenza dei riarrangiamenti RET/PTC e una frequenza maggiormente aumentata di mutazioni RAS. Inoltre, spesso la mutazione BRAF è distinta rispetto a quella convenzionale, caratterizzandosi per una ridotta attivazione della proteina BRAF-K[66].
La variante a cellule alte presentano mutazioni BRAF in quasi tutti i casi (55-100%) e mostrano spesso traslocazioni di RET/PTC. La presenza, non convenzionale, di entrambe le mutazioni, può correlare con la peggiore prognosi di queste neoplasie. La variante sclerosante diffusa non presenta mai mutazioni di BRAF, ma prevalentemente (nella metà dei casi) traslocazioni di RET/PTC.
Mutazioni genetiche[modifica | modifica wikitesto]

La mutazione BRAFV600E è stata associata quasi dieci anni fa, attraverso uno studio multicentrico, a una maggiore aggressività clinico-patologica, con un maggiore tasso di recidiva, di resistenza alla terapia con radioiodio, fallimento terapeutico, e in generale una maggiore aggressività[70].
A destare l'attenzione e l'interesse per questa mutazione, è stata la recente scoperta, in alcuni PTC umani, di un'eterogeneità intra-tumorale nel genotipo di BRAF: in una minoranza di casi si è rinvenuta la mutazione BRAFV600E, e in una maggioranza il BRAF-wilde typ[71]. Questo ha dato vita a un dibattito, ancora acceso, su cosa venga prima (“chicken and eggs puzzle”): se la mutazione del BRAF dia l'avvio alla tumorigenesi, o se invece segua l'evoluzione verso la malignità. Da ciò, comunque, si possono trarre due conclusioni: che la mutazione del BRAF sia un evento genetico secondario nella tumorigenesi[72]; oppure che una volta che la mutazione del BRAF ha attivato la trasformazione neoplastica in PTC, ulteriori alterazioni oncogeniche possono subentrare, guidando la tumorigenesi e scalzando il ruolo di BRAF[73]. L'evidenza che la mutazione è presente nel 20-40% dei carcinomi scarsamente differenziati, e nel 30-40% degli anaplastici, fa ritenere che la proteina di fusione giochi un ruolo importante nella de-differenziazione dei tireociti e quindi, più in generale, per una maggiore aggressività della neoplasia[74][75][76].
Seconda per prevalenza, dopo BRAF, è la mutazione di RAS. Questa proteina è costituzionalmente espressa dai tireociti, e si attiva attraverso il legame con il GTP. La GTPasi intrinseca di questa proteina, attraverso l'idrolisi dei legami, scinde la GTP dai recettori di RAS, defosforilandoli, e portando RAS in uno stato inattivato, ponendo fine alla trasmissione del segnale. Mutazioni in questa proteina possono comportare la deattivazione della GTPasi, lasciando RAS in uno stato di perenne attivazione. Ci sono 3 isoforme di RAS: HRAS, KRAS e NRAS. Quest'ultima è quella che si associa, più frequentemente, ai tumori della tiroide. Inoltre, RAS è una proteina fondamentale per l'attivazione della via delle MAPK e PI3K-AKT. Queste mutazioni occorrono frequentemente negli adenomi follicolari della tiroide, una lesione presumibilmente pre-maligna, fatto che sta facendo supporre che RAS-attivato abbia un ruolo nella tumorigenesi dei tumori follicolari della tiroide, anche se la sua sola mutazione non è sufficiente per generare la trasformazione nell'istotipo carcinomatoso[77]. Delezioni di PTEN (un gene oncosoppressore) sono le tipiche alterazioni genetiche che portano a un'attivazione della via PI3K-AKT, e sono la base genetica per la tumorigenesi delle cellule follicolari tiroidee nella sindrome di Cowden.
Infine, altri importanti geni mutati includono la beta-catenina (CTNNB1), TP53, isocitrato-deidrogenasi-1, chinasi del linfoma anaplastico (ALK), e il recettore del fattore di crescita dell'epidermide (EGFR). La maggiore frequenza di queste mutazioni nelle forme anaplastiche di tumore della tiroide, fa supporre che esse potrebbero avere un ruolo nella progressione verso l'aggressività.
Oncogenesi e progressione: un modello biomolecolare[modifica | modifica wikitesto]
Dagli studi traslazionali e molecolari più recenti, emerge con decisione il ruolo principale delle vie metaboliche delle MAPKinasi e della via PI3K-ATK. L'analisi genetica della neoplasia nelle sue varie forme evolutive, sembra dimostrare come l'attivazione preferenziale, attraverso specifiche alterazioni, di una delle due vie, indirizza lo sviluppo neoplastico in senso papillare (MAPK), o in senso adenomatoso (FTA) e follicolare (FTC). Quando le alterazioni si accumulano, ed entrambe le vie vengono attivate, si assiste a una progressione in senso de-differenziativo, verso le forme scarsamente differenziate (PDTC) e anaplastiche (ATC). Questa evoluzione può essere accelerata o mediata anche da altri eventi genetici, includenti mutazioni in TP53, CTNNB1 e ALK.
Questo modello è supportato da studi su topi transgenici, nei quali la delezione di Pten e il knock-in di Kras G12D (atto ad attivare entrambe le vie metaboliche sopra citate), causa lo sviluppo di una forma aggressiva di cancro della tiroide[78].
Riarrangiamenti di RET/PTC sono individuati sino all'80% dei PTC in individui esposti a radiazioni ionizzanti accidentali o terapeutiche. L'esposizione alle radiazioni di Černobyl' ha particolarmente aumentato la frequenza della mutazione RET/PTC3[79]. È vero l'opposto, invece, nel caso delle mutazioni puntiformi di BRAF e di RAS, le quali sono rare nei tumori correlati all'esposizione alle radiazioni, ma comuni nella popolazione generale[80].
Note[modifica | modifica wikitesto]
- ^ Debbie W. Chen, Brian H. H. Lang e Donald S. A. McLeod, Thyroid cancer, in Lancet (London, England), vol. 401, n. 10387, 6 maggio 2023, pp. 1531–1544, DOI:10.1016/S0140-6736(23)00020-X. URL consultato il 4 agosto 2023.
- ^ Briseis A. Kilfoy et al., International Patterns and Trends in Thyroid Cancer Incidence, 1973–2002, in Cancer Causes & Control, vol. 20, n. 5, Springer, luglio 2009, pp. 525-531. Accesso condizionato via Jstor
- ^ Luca Revelli, L'importanza dello iodio nei disturbi della tiroide, in la Repubblica, 23 luglio 2013, p. 23.
- ^ Pierluigi Rossi, Tiroide, la salute viene dallo iodio, in la Repubblica, 20 febbraio 1997, p. 13.
- ^ Bryan R. Haugen, Erik K. Alexander e Keith C. Bible, 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer: The American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer, in Thyroid: Official Journal of the American Thyroid Association, vol. 26, n. 1, 2016-01, pp. 1–133, DOI:10.1089/thy.2015.0020. URL consultato il 9 agosto 2021.
- ^ Proteinuria - Disturbi genitourinari, su Manuali MSD Edizione Professionisti. URL consultato il 24 novembre 2021.
- ^ Robert I. Haddad, Martin Schlumberger e Lori J. Wirth, Incidence and timing of common adverse events in Lenvatinib-treated patients from the SELECT trial and their association with survival outcomes, in Endocrine, vol. 56, n. 1, 2017-04, pp. 121–128, DOI:10.1007/s12020-017-1233-5. URL consultato il 24 novembre 2021.
- ^ (EN) Alice Nervo, Alberto Ragni e Marco Gallo, Symptomatic Biliary Disorders During Lenvatinib Treatment for Thyroid Cancer: An Underestimated Problem, in Thyroid, vol. 30, n. 2, 1º febbraio 2020, pp. 229–236, DOI:10.1089/thy.2019.0355. URL consultato il 24 novembre 2021.
- ^ SEER Stat Fact Sheets: Thyroid Cancer, su NCI. URL consultato il 18 giugno 2014.
- ^ Margherita Dionisi-Vici, Marta Fantoni e Rossana Botto, Distress, anxiety, depression and unmet needs in thyroid cancer survivors: a longitudinal study, in Endocrine, 18 giugno 2021, DOI:10.1007/s12020-021-02786-y. URL consultato il 4 agosto 2021.
- ^ a b c d e f g h Anastasi
- ^ a b c d e f g h Testut
- ^ Paletto
- ^ DeAntoni, pp.209-216.
- ^ AJCC, American Join Committee on Cancer et al., Cancer staging manual, 7ª ed., NewYork, Springer, 2010, ISBN 978-0-387-88440-0 (archiviato dall'url originale il 30 settembre 2015).
- ^ a b AIOM, I numeri del cancro (PDF).
- ^ MP Curado et al., Cancer incidence in Five continents, IARC Scientific Publications, 2014, ISBN 978-92-832-2165-4.
- ^ A. Jemal et al., Cancer statistics, 2010, in CA: a cancer journal for clinicians, vol. 60, n. 5, settembre-ottobre 2010, pp. 277-300.
- ^ L. Dal Maso et al., Incidence of thyroid cancer in Italy, 1991-2005: time trends and age-period-cohort effects., in Ann Oncol, vol. 22, n. 4, Apr 2011, pp. 957-63, DOI:10.1093/annonc/mdq467, PMID 20952599.
- ^ B. Aschebrook-Kilfoy et al., The acceleration in papillary thyroid cancer incidence rates is similar among racial and ethnic groups in the United States., in Ann Surg Oncol, vol. 20, n. 8, agosto 2013, pp. 2746-53, DOI:10.1245/s10434-013-2892-y, PMID 23504142.
- ^ L. Enewold et al., Rising thyroid cancer incidence in the United States by demographic and tumor characteristics, 1980-2005., in Cancer Epidemiol Biomarkers Prev, vol. 18, n. 3, marzo 2009, pp. 784-91, DOI:10.1158/1055-9965.EPI-08-0960, PMID 19240234.
- ^ a b c d e Cooper DS et al., Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer, in Thyroid, vol. 19, n. 11, 2009, pp. 1167–214, DOI:10.1089/thy.2009.0110, PMID 19860577.
- ^ Baloch ZW et al., Diagnostic terminology and morphologic criteria for cytologic diagnosis of thyroid lesions: a synopsis of the National Cancer Institute Thyroid Fine-Needle Aspiration State of the Science Conference, in Diagn. Cytopathol., vol. 36, n. 6, 2008, pp. 425–37, DOI:10.1002/dc.20830, PMID 18478609.
- ^ Cappelli C et al., The predictive value of ultrasound findings in the management of thyroid nodules, in QJM, vol. 100, n. 1, 2007, pp. 29–35, DOI:10.1093/qjmed/hcl121, PMID 17178736.
- ^ Moon WJ et al., Benign and malignant thyroid nodules: US differentiation--multicenter retrospective study [collegamento interrotto], in Radiology, vol. 247, n. 3, 2008, pp. 762–70, DOI:10.1148/radiol.2473070944, PMID 18403624.
- ^ Jeh SK et al., Evaluating the degree of conformity of papillary carcinoma and follicular carcinoma to the reported ultrasonographic findings of malignant thyroid tumor, in Korean J Radiol, vol. 8, n. 3, 2007, pp. 192–7, PMC 2627417, PMID 17554185.
- ^ Rago T et al., Elastography: new developments in ultrasound for predicting malignancy in thyroid nodules [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 92, n. 8, 2007, pp. 2917–22, DOI:10.1210/jc.2007-0641, PMID 17535993.
- ^ Hegedüs L, Clinical practice. The thyroid nodule, in N. Engl. J. Med., vol. 351, n. 17, 2004, pp. 1764–71, DOI:10.1056/NEJMcp031436, PMID 15496625.
- ^ C. Carmeci et al., Ultrasound-guided fine-needle aspiration biopsy of thyroid masses., in Thyroid, vol. 8, n. 4, Apr 1998, pp. 283-9, PMID 9588492.
- ^ M. Bongiovanni et al., The Bethesda System for Reporting Thyroid Cytopathology: a meta-analysis, in Acta Cytol, vol. 56, n. 4, 2012, pp. 333-9, DOI:10.1159/000339959, PMID 22846422.
- ^ Jennifer A. Sipos e Matthew D. Ringel, Molecular testing in thyroid cancer diagnosis and management, in Best Practice & Research. Clinical Endocrinology & Metabolism, vol. 37, n. 1, 2023-01, pp. 101680, DOI:10.1016/j.beem.2022.101680. URL consultato il 4 agosto 2023.
- ^ Armando Bartolazzi et al., Galectin-3-expression analysis in the surgical selection of follicular thyroid nodules with indeterminate fine-needle aspiration cytology: a prospective multicentre study, in Lancet Oncol., vol. 9, n. 6, 2008, pp. 543–9, DOI:10.1016/S1470-2045(08)70132-3, PMID 18495537.
- ^ Sapio MR et al., Detection of RET/PTC, TRK and BRAF mutations in preoperative diagnosis of thyroid nodules with indeterminate cytological findings, in Clin. Endocrinol. (Oxf), vol. 66, n. 5, 2007, pp. 678–83, DOI:10.1111/j.1365-2265.2007.02800.x, PMID 17381488.
- ^ M. Mekel, C. Nucera, R. Hodin e S. Parangi, «Surgical implication of brafv600e mutation in fine-needle aspiration of thyroid nodules,» Am J Surg, vol. 200, n. 1, 2010.
- ^ E. Papini, R. Guglielmi, A. Bianchini, A. Crescenzi, S. Taccogna, F. Nardi, C. Panunzi, R. Rinaldi, V. Toscano e C. Pacella, «Risk of malignancy in nonpalpable thyroid nodules: predictive value of ultrasound and color-doppler features,» J Clin Endocrinol Metab, vol. 87, pp. 1941-1946, 2002.
- ^ S. Chow, S. Law, J. Chan, S. Au, S. Yau e W. Lau, «Papillary microcarcinoma of the thyroid-Prognostic significance of lymph node metastasis and multifocality.,» Cancer, vol. 98, pp. 31-40, 2003.
- ^ S. Qubain, S. Nakano, M. Baba, S. Takao e T. Aikou, «Distribution of lymph node micrometastasis in pN0 welldifferentiated thyroid carcinoma.,» Surgery, vol. 131, pp. 249-256, 2002.
- ^ J. Stulak, C. Grant, D. Farley, G. Thompson, J. van Heerden, I. Hay, C. Reading e J. CHarboneau, «Value of preoperative ultrasonography in the surgical management of initial and reoperative papillary thyroid cancer,» Arch Surg, vol. 141, pp. 489-494, 2006.
- ^ C. Solorzano, D. Carneiro, M. Ramirez, T. Lee e G. Irvin, «Surgeon-performed ultrasound in the management of thyroid malignancy,» Am Surg, vol. 70, pp. 576-580, 2004.
- ^ S. Leboulleux, E. Girad, M. Rose, J. Travagli, N. Sabbah, B. Caillou, D. Hartl, N. Lassau, E. Baudin e M. Schlumberger, «Ultrasound criteria of malignancy for cervical lymphnodes in patients followed up for differentiated thyroid cancer,» J Clin Endocrinol Metab, vol. 92, pp. 3590-3594, 2007.
- ^ S. Kuna, I. Bracic, V. Tesic, K. Kuna, G. Herceg e D. Dodig, «Ultrasonographic differentiation of benign from malignant neck lymphadenopathy in thyroid cancer,» J Ultrasound Med, vol. 25, pp. 1531-1537, 2006.
- ^ F. Boi, G. Baghino, F. Atzeni, M. Lai, G. Faa e S. Mariotti, «THe diagnostic value for differentiated thyroid carcinoma metastases of thyroglobulin measurement in washout fluid from fine needle aspiration biopsy of neck lymph nodes is maintained in the presence of circulating anti-Tg antibodies,» J Clin Endocrinol Metab, p. 91, 1364-1369.
- ^ H. Gharib, J. Goellner, A. Zinsmeister, C. Grant e J. Van Heerden, «Fine-needle aspiration biopsy of the thyroid. The problem of suspicious cytologic findings,» Ann Intern Med, vol. 101, pp. 25-28, 1984
- ^ K. Bilimora, D. Bentrem, C. Ko, A. Stewart, D. Winchester, M. Talamonti e C. Sturgeon, «Extent of surgery affects survival for papillary thyroid cancer,» Ann Surg, vol. 246, pp. 375-381, 2007.
- ^ J. van Heerden, I. Hay, J. Goellner, D. Salomao, J. Ebersold, E. Bergstralh e C. Grant, «Follicular thyroid carcinoma with capsular invasion alone: a nonthreatening malignancy,» Surgery, vol. 112, pp. 1130-1136, 1992.
- ^ I. Hay et al., Predicting outcome in papillary thyroid carcinoma: development of a realiable progonostic scoring system in a cohort of 1779 patients surgically treat at our institution during 1940 throught 1989, in Surgery, vol. 114, n. 6, dicembre 1993, PMID 8256208.
- ^ a b ID. Hay et al., Papillary thyroid carcinoma managed at the Mayo Clinic during six decades (1940-1999): temporal trends in initial therapy and long-term outcome in 2444 consecutively treated patients., in World J Surg, vol. 26, n. 8, Aug 2002, pp. 879-85, DOI:10.1007/s00268-002-6612-1, PMID 12016468.
- ^ J. Lin, T. Chao, M. Huang, H. Weng e K. Tzen, «Use of radioactive iodine for thyroid remnant ablation in welldifferentiated thyroid carcinoma to replace thyroid reoperation,» Am J Clin Oncol, vol. 21, pp. 77-81, 1998.
- ^ S. Grebe e I. Hay, «Thyroid cancer nodal metastases: biologic significance and therapeutic considerations,» Surg Oncol Clin N AM, vol. 5, pp. 43-63, 1996.
- ^ M. Kouvaraki, S. Shapiro, B. Fornage, B. Edeiken-Monro, S. Sherman, R. Vassilopoulou-Sellin, J. Lee e D. Evans, «Role of preoperative ultrasonography in the surgical management of patients with thyroid cancer,» Surgery, vol. 134, pp. 946-954, 2003
- ^ Y. Podnos, D. Smith, L. Wagman e J. Ellenhorn, «The implication of lymph node metastasis on survival in patients with well-differentiated thyroid cancer,» Am Surg, vol. 71, pp. 731-734, 2005.
- ^ Jonathan Langdon, Akshya Gupta e Kedar Sharbidre, Thyroid cancer in pregnancy: diagnosis, management, and treatment, in Abdominal Radiology (New York), vol. 48, n. 5, 2023-05, pp. 1724–1739, DOI:10.1007/s00261-023-03808-1. URL consultato il 4 agosto 2023.
- ^ a b P. Soares, R. Celestino, M. Melo, E. Fonseca e M. Sobrinho-Simoes, «Prognostic biomarkers in thyroid cancer,» Virchows Archive, 2013.
- ^ S. Hundahl, I. Fleming, A. Fremgen e H. Menck, «A national cancer data base report on 53,856 cases of thyroid carcinoma treated in the US, 1985-1995,» Cancer, vol. 12, n. 83, pp. 2638-2648, 1998.
- ^ F. Gilliland, W. Hunt, D. Morris e C. Key, «Prognostic factors for thyroid carcinoma. A population-based study of 15,698 cases from the Surveillance, Epidemiology and End Results (SEER) program 1973-1991,» Cancer, vol. 3, n. 79, pp. 564-573, 1997.
- ^ R. Elisei, E. Molinaro, L. Agate, V. Bottici, L. Masserini, C. Ceccarelli, F. Lippi, L. Grasso, F. Basolo, G. Bevilacqua, P. Miccoli, G. Di Coscio, P. Vitti, F. Pacini e A. Pinchera, «Are the clinical and pathological features of differentiated thyroid carcinoma really changed over the last 35 years? Study on 4187 patients from a single italian institution to answer this question,» J Clin Endocrinol Metab, vol. 4, n. 95, pp. 1516-1527, 2010.
- ^ S. Leboullex, D. Hartl, F. Baudin e M. Schlumberger, «Differentiated thyroid cancer in childhood,» Bull du Cancer, pp. 1093-1099, 2012.
- ^ M. Schlumberger, C. Challeton, F. De Vathaire, J. Travagli, P. Gardet, J. Lumbroso, C. Francese, F. Fontaine, M. Ricard e C. Parmentier, «Radioactive iodine treatment and external radiotherapy for lung and bone metastases from thyroid carcinoma,» J Nuclear Medicine, vol. 4, n. 37, pp. 598-605, 1996
- ^ Thyroid Cancer Survival Rates, in AJCC Cancer Staging Manual, 7ª ed., The American Cancer Society.. URL consultato il 26 ottobre 2015 (archiviato dall'url originale il 18 ottobre 2013).
- ^ Thyroid cancer, su books.google.se, p. 10.
- ^ F. Grünwald et al., Thyroid cancer, Berlin, Springer, 2005, ISBN 3-540-22309-6.
- ^ Luigi Santacroce, Silvia Gagliardi e Andrew Scott Kennedy, Papillary Carcinoma, su emedicine.medscape.com, settembre 2010.
- ^ Barbet J et al., Prognostic Impact of Serum Calcitonin and Carcinoembryonic Antigen Doubling-Times in Patients with Medullary Thyroid Carcinoma, in Journal of Clinical Endocrinology & Metabolism, vol. 90, n. 11, 2005, pp. 6077–6084, DOI:10.1210/jc.2005-0044, PMID 16091497.
- ^ Medullary Thyroid Cancer, su cancer.gov, National Cancer Institute, dicembre 2010.
- ^ (EN) Lorenzo Lippi, Alessio Turco e Stefano Moalli, Role of Prehabilitation and Rehabilitation on Functional Recovery and Quality of Life in Thyroid Cancer Patients: A Comprehensive Review, in Cancers, vol. 15, n. 18, 2023-01, pp. 4502, DOI:10.3390/cancers15184502. URL consultato l'11 settembre 2023.
- ^ a b Robbins.
- ^ (EN) Y. E. Nifikorov e M. N. Nifikorova, Molecular genetics and diagnosis of thyroid cancer, in Nature Rev. Endocrinol., n. 7, 2011, pp. 569-580.
- ^ (EN) M. Castellone et al., The beta-catenin axis integrates multiple signals downstream from RET/papillary thyroid carcinoma leading to cell proliferation, in Cancer Res., n. 69, 2009, pp. 1867-1876.
- ^ (EN) M. Xing, BRAF mutation in Thyroid cancer, in Endocr Relat Cancer, n. 12, 2005, pp. 245-262.
- ^ Xing M et al., BRAF mutation predicts a poorer clinical prognosis for papillary thyroid cancer [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 90, n. 12, 2005, pp. 6373–9, DOI:10.1210/jc.2005-0987, PMID 16174717.
- ^ Guerra A et al., The primary occurrence of BRAF(V600E) is a rare clonal event in papillary thyroid carcinoma [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 97, n. 2, 2012, pp. 517–24, DOI:10.1210/jc.2011-0618, PMID 22170714.
- ^ Vasko V et al., High prevalence and possible de novo formation of BRAF mutation in metastasized papillary thyroid cancer in lymph nodes [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 90, n. 9, 2005, pp. 5265–9, DOI:10.1210/jc.2004-2353, PMID 15998781.
- ^ Xing M, BRAFV600E mutation and papillary thyroid cancer: chicken or egg? [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 97, n. 7, 2012, pp. 2295–8, DOI:10.1210/jc.2012-2201, PMC 3387401, PMID 22774213.
- ^ Namba H et al., Clinical implication of hot spot BRAF mutation, V599E, in papillary thyroid cancers [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 88, n. 9, 2003, pp. 4393–7, DOI:10.1210/jc.2003-030305, PMID 12970315.
- ^ Nikiforova MN et al., BRAF mutations in thyroid tumors are restricted to papillary carcinomas and anaplastic or poorly differentiated carcinomas arising from papillary carcinomas [collegamento interrotto], in J. Clin. Endocrinol. Metab., vol. 88, n. 11, 2003, pp. 5399–404, DOI:10.1210/jc.2003-030838, PMID 14602780.
- ^ Ricarte-Filho JC et al., Mutational profile of advanced primary and metastatic radioactive iodine-refractory thyroid cancers reveals distinct pathogenetic roles for BRAF, PIK3CA, and AKT1 [collegamento interrotto], in Cancer Res., vol. 69, n. 11, 2009, pp. 4885–93, DOI:10.1158/0008-5472.CAN-09-0727, PMC 2690720, PMID 19487299.
- ^ Xing M, Molecular pathogenesis and mechanisms of thyroid cancer, in Nat. Rev. Cancer, vol. 13, n. 3, 2013, pp. 184–99, DOI:10.1038/nrc3431, PMC 3791171, PMID 23429735.
- ^ Miller KA et al., Oncogenic Kras requires simultaneous PI3K signaling to induce ERK activation and transform thyroid epithelial cells in vivo, in Cancer Res., vol. 69, n. 8, 2009, pp. 3689–94, DOI:10.1158/0008-5472.CAN-09-0024, PMC 2669852, PMID 19351816.
- ^ Rabes HM et al., Pattern of radiation-induced RET and NTRK1 rearrangements in 191 post-chernobyl papillary thyroid carcinomas: biological, phenotypic, and clinical implications, in Clin. Cancer Res., vol. 6, n. 3, 2000, pp. 1093–103, PMID 10741739.
- ^ Nikiforova MN et al., Low prevalence of BRAF mutations in radiation-induced thyroid tumors in contrast to sporadic papillary carcinomas, in Cancer Lett., vol. 209, n. 1, 2004, pp. 1–6, DOI:10.1016/j.canlet.2003.12.004, PMID 15145515.
Bibliografia[modifica | modifica wikitesto]
- Léo Testut e O. Jacob, Trattato di anatomia topografica : con applicazioni medico-chirurgiche, 1: Testa, rachide, 2ª ed., Torino, Utet, 1977, ISBN 978-88-7051-287-8.
- A.E. Paletto et al., Nuovo trattato di tecnica chirurgica, 1 Generalità, collo, mammella, Torino, Utet, 1996, ISBN 978-88-02-05118-5.
- G. Anastasi et al., Trattato di anatomia umana, 4ª ed., Edi.Ermes, agosto 2007, ISBN 978-88-7051-287-8.
- E. DeAntoni, Il carcinoma differenziato della tiroide. Collana Monografica della Società Italiana di Chirurgia, Torino, Utet, 2006.
- Robbins e Cotran, Le basi patologiche delle malattie. Patologia generale, 8ª ed., Elsevier, 2010, ISBN 978-88-214-3175-3.
Voci correlate[modifica | modifica wikitesto]
- Classificazione TNM
- Metastasi
- Stadio tumorale
- Recettori accoppiati a chinasi
- Ecografia
- Tiroide
- Tiroidectomia
- Linfonodo
- Ormoni tiroidei
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su tumore della tiroide
Wikimedia Commons contiene immagini o altri file su tumore della tiroide
Collegamenti esterni[modifica | modifica wikitesto]
- American Thyroid Association (ATA), su thyroid.org.
- European Thyroid Association (ETA), su eurothyroid.com.
- Ambulatorio carcinoma tiroideo - policlinico Umberto I di Roma [collegamento interrotto], su medicinasapienza.it.
- Endocrinochirurgia Forlì, su ausl.fo.it. URL consultato il 7 febbraio 2008 (archiviato dall'url originale il 31 maggio 2009).
- Linee Guida dell’Associazione Italiana di Medicina Nucleare ed imaging molecolare (AIMN) per la terapia radiometabolica.
| Controllo di autorità | LCCN (EN) sh85135165 · GND (DE) 4140890-1 · J9U (EN, HE) 987007536576505171 · NSK (HR) 005700149 · NDL (EN, JA) 00566929 |
|---|