Radiochimica
La radiochimica è la branca della chimica nucleare che si occupa dello studio e impiego pratico delle sostanze radioattive. Sfrutta le reazioni chimiche di isotopi radioattivi per fini analitici e per l'effettuazione di altre indagini come ad esempio quelle relative alla cinetica chimica.
Decadimento radioattivo[modifica | modifica wikitesto]
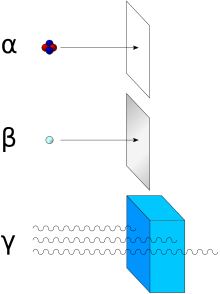
I radioisotopi sono isotopi instabili degli elementi chimici, ciascuno caratterizzato da un proprio tempo di emivita, che subiscono decadimento radioattivo emettendo una qualche forma di radiazione. Le radiazioni emesse sono principalmente di tre tipi: alfa, beta, e gamma.
- Le radiazioni alfa consistono in una emissione di particelle alfa (formate da due protoni e due neutroni, indicate spesso 42He2+) da parte di un nucleo atomico. Quando avviene questo tipo di decadimento la massa atomica originaria scalerà quindi di quattro unità, mentre il numero atomico diminuirà di due unità.
- Le radiazioni beta sono generate dalla trasmutazione di un neutrone in un elettrone e un protone. L'elettrone ad alta energia emesso costituisce la particella β (β−). Un altro decadimento di tipo beta implica la trasmutazione in una coppia neutrone-positrone più un neutrino (β+).
- Le radiazioni gamma consistono in una emissione di energia elettromagnetica, come i raggi X, dal nucleo atomico. Questa emissione solitamente accompagna un decadimento alfa o beta.
I tre tipi di radiazione possono essere distinti in base al loro potere penetrante. Le più penetranti sono le radiazioni gamma, costituite da fotoni che richiedono per il loro schermaggio un grosso spessore di metallo pesante (come il piombo o il bario). Di contro, le radiazioni alfa si bloccano dopo aver percorso alcuni centimetri in aria o a causa di un foglio di carta da legno. Le radiazioni beta richiedono invece un foglio di alluminio con spessore di pochi millimetri.
Radiotraccianti[modifica | modifica wikitesto]
Un radiotracciante è una sostanza contenente un radionuclide utilizzata in modo da poter studiare i processi chimici, fisici, biologici e ambientali sfruttandone la radioattività. Le tecniche basate sui radiotraccianti godono di elevata sensibilità e si basano sulle proprietà chimiche simili possedute dagli isotopi di uno stesso elemento. Una causa di differente comportamento chimico è rappresentato dall'effetto isotopico cinetico, particolarmente rilevante per gli elementi a più basso peso atomico. Inoltre la radioattività non deve modificare le caratteristiche del sistema oggetto di studio. Il radionuclide e il nuclide stabile devono essere soggetti a scambio isotopico, e affinché ciò si verifichi è necessario che il tracciante e l'atomo stabile possiedano lo stesso stato di ossidazione.
Esempi di radionuclidi utilizzati comunemente sono rappresentati dal trizio (3H, frequentemente utilizzato in studi biochimici), carbonio-11 (tracciante nella tomografia a emissione di positroni) e carbonio-12 (svariati utilizzi in campi diversi), fosforo-32 (studio di amminoacidi, fosfoproteine e fosforilazione da parte delle chinasi), zolfo-35 (studio di amminoacidi e acidi nucleici solforati), iodio-123 (in medicina nucleare nello studio della tiroide) e iodio-125 (nel dosaggio radioimmunologico).
Esempi dell'utilizzo dei radiotraccianti in chimica riguardando la determinazione della costante di solubilità dei composti poco solubili e lo studio dei meccanismi di reazione, con la possibilità di determinare lo specifico legame coinvolto in una reazione chimica analizzando la radioattività dei prodotti. L'utilizzo dei radiotraccianti in ambito analitico viene descritto successivamente.
Metodiche radioanalitiche[modifica | modifica wikitesto]
I metodi radiochimici d'analisi sono basati sulla misura della radioattività prodotta dall'analita o per aggiunta di piccole quantità di reattivi marcati o a seguito di radioattività indotta. In questo modo è possibile rilevare quantità di analita molto basse, spesso non rilevabili con metodiche analitiche più comuni.
Rivelatori radioanalitici[modifica | modifica wikitesto]
I rivelatori radioanalitici permettono di ricavare informazioni analitiche sfruttando la quantità di radiazione che viene loro convogliata. Secondo la loro costituzione e il principio fisico sfruttato, si dividono in:
- Rivelatori a ionizzazione: sfruttano la ionizzazione di un gas a bassa pressione, gas contenuto in una camera cilindrica e posto sotto l'azione di un campo elettrico, che genera una corrente elettrica proporzionale alla radiazione ricevuta. I comuni contatore Geiger e contatore Müller sfruttano tale principio.
- Rivelatori a scintillazione: sono i rivelatori prediletti per i raggi γ, per i quali il Geiger è poco sensibile. Il fascio radioattivo viene convogliato su un cristallo tipicamente di ioduro di sodio drogato con tallio, NaI(Tl): in questo modo si ha emissione di radiazione elettromagnetica nel visibile che, catturata da un fotomoltiplicatore, genera una corrente elettrica.
- Rivelatori a semiconduttori: sfruttano un cristallo di germanio drogato con litio e interposto tra altri due cristalli di germanio, uno di tipo p e l'altro di tipo n. Sono indicati per analisi in presenza di matrici complesse e necessitano di essere portati alla temperatura dell'azoto liquido.
Analisi radiochimica[modifica | modifica wikitesto]
Tra le principali modalità analitiche figurano l'attivazione neutronica, la diluizione isotopica e la titolazione radiochimica.[1]
- Metodo per attivazione neutronica (NAA): la specie in esame viene sottoposta a bombardamento di neutroni e diviene radioattiva. La misura di tale radioattività ci permette di risalire alla quantità di sostanza.
- Metodo della diluizione isotopica: alla sostanza in esame di peso X si aggiunge una quantità A della medesima sostanza però radioattiva, il miscuglio avrà quindi una radioattività RX+A. Se P è la quantità di sostanza ottenuta a seguito di aggiunta di poco reattivo precipitante, alla quale è associata la radioattività RP, essendo le attività misurate funzione dell'aggiunta iniziale, è verificata l'eguaglianza K= (X+A)/P = RX+A/RP dalla quale si ricava X. Questa metodica è utilizzata in presenza di matrice con proprietà chimiche simili all'analita.
- Titolazione radiochimica: viene eseguita una normale titolazione che consenta una rapida separazione di fasi, come avviene nel caso delle reazioni di precipitazione. Viene misurata la radioattività R della soluzione in funzione del volume V di titolante marcato aggiunto e costruito un grafico R/V. All'inizio la radioattività della soluzione e pressoché nulla e costante, oltre il punto di equivalenza si ha un brusco aumento di R in funzione di V in quanto il titolante radioattivo, non più precipitato, aumenta man mano la sua concentrazione in soluzione.
Campi di applicazione della radioanalisi[modifica | modifica wikitesto]
- Analisi di tracce di elementi in acque naturali
- Analisi di tracce di elementi nel suolo e terreni
- Analisi petrografiche e mineralogiche
- Analisi di liquidi biologici e varie determinazioni biochimiche
Altre applicazioni della radiochimica[modifica | modifica wikitesto]

Il decadimento radioattivo segue la cinetica di ordine uno.
- Datazione delle rocce: Uno dei metodi principali sfrutta la radioattività naturale generata dall'isotopo dell'uranio 23892U. L'equazione totale del decadimento, con emivita 4,5 miliardi di anni, è 23892U → 20682Pb + 8 42He + 6 0-1β.
- Età dei reperti organici: si misura la radioattività dell'isotopo 146C, prodotto per reazione dei neutroni provenienti dalla radiazione cosmica con azoto atmosferico, inglobato per scambio isotopico nel biossido di carbonio presente nell'atmosfera. 146C decade emettendo particelle β con t1/2= 5 730 anni. Gli organismi viventi vegetali assorbono biossido di carbonio (anidride carbonica) radioattivo tramite la fotosintesi, gli animali e quindi l'uomo attraverso la catena alimentare e marginalmente mediante la respirazione, mentre i giacimenti petroliferi e carboniferi non contengono più quantità significative di 146C, dato il lungo tempo trascorso dalla loro formazione.
- Studio del metabolismo di organismi vegetali e animali, mediante la tecnica dei radiotraccianti.
- In medicina nucleare, per la radioterapia radiante (es. cobalto-60 per vari tumori solidi), la radioterapia metabolica di tumori ed altre patologie (ioduro di sodio marcato con 131I per i tumori tiroidei) e radiodiagnostica (mezzi di contrasto o radiofarmaci diagnostici sistemici o per recettori specifici, es: marcati con 123I per la SPECT o 18F per la PET).
- Studio delle reazioni e dell'equilibrio chimico, cinetica chimica e meccanismi di reazione.
- Studio di disinfettanti, insetticidi, anticrittogamici e loro meccanismo d'azione.
Note[modifica | modifica wikitesto]
- ^ G. Amandola, V. Terreni, "Analisi chimica strumentale e tecnica", Masson Scuola, 1995, ISBN 9788808095077
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) IUPAC Gold Book, "radiochemistry", su goldbook.iupac.org.
- Gruppo Interdivisionale di Radiochimica della Società Chimica Italiana, su wwwlasa.mi.infn.it. URL consultato il 28 gennaio 2010 (archiviato dall'url originale il 6 febbraio 2010).
- (EN) Division of Nuclear and Radiochemistry of EuCheMS, su euchems.org. URL consultato il 28 gennaio 2010 (archiviato dall'url originale il 19 novembre 2006).
- (EN) Radiochemistry Society, su radiochemistry.org.
- (EN) Journal of Radioanalytical and Nuclear Chemistry, su springerlink.metapress.com.
- (EN) Radiochemistry (Radiokhimiya), su maik.rssi.ru. URL consultato il 21 aprile 2022 (archiviato dall'url originale il 21 dicembre 2012).
| Controllo di autorità | Thesaurus BNCF 21668 · LCCN (EN) sh85110675 · GND (DE) 4138529-9 · BNF (FR) cb119783331 (data) · J9U (EN, HE) 987007558198905171 · NDL (EN, JA) 00563510 |
|---|