Diborano
| Diborano | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| diborano(6) | |
| Nomi alternativi | |
| boretano | |
| Caratteristiche generali | |
| Formula bruta o molecolare | B2H6 |
| Massa molecolare (u) | 27,7 |
| Aspetto | gas incolore |
| Numero CAS | |
| Numero EINECS | 242-940-6 |
| SMILES | [H][B]1([H])[H][B]([H])([H])[H]1 |
| Proprietà chimico-fisiche | |
| Densità (kg·m−3, in c.s.) | 1,18 |
| Temperatura di fusione | −165 °C (108 K) |
| Temperatura di ebollizione | −92,5 °C (180,7 K) |
| ΔebH0 (kJ·mol−1) | 515,39 |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | 36,4 |
| ΔfG0 (kJ·mol−1) | 87,6 |
| S0m(J·K−1mol−1) | 232,1 |
| C0p,m(J·K−1mol−1) | 56,7 |
| Indicazioni di sicurezza | |
| Limiti di esplosione | 0,9 - 98% vol. |
| Temperatura di autoignizione | 38 °C (311 K) |
| Simboli di rischio chimico | |
  
| |
| Frasi H | 330 - 220 - 280 |
| Consigli P | 260 - 210 - 304+340 - 315 - 377 - 381 - 405 - 403 [1] |
Il diborano è un composto inorganico del boro e dell'idrogeno, con formula chimica B2H6. È il più semplice dei borani. In condizioni normali è un gas incolore. Si infiamma spontaneamente in aria a temperatura ambiente, e reagisce violentemente con l'acqua. È uno dei composti più importanti del boro e viene generalmente commercializzato in bombole, diluito con altri gas inerti.
Storia[modifica | modifica wikitesto]
Il diborano fu sintetizzato per la prima volta nel XIX secolo per idrolisi di boruri metallici, senza poter essere isolato. Fu Alfred Stock a creare la chimica degli idruri di boro. Dal 1912 al 1936 con le sue ricerche sviluppò metodi per la sintesi e la manipolazione degli idruri di boro, che sono sostanze volatili, molto reattive, e spesso tossiche. Stock propose una prima struttura tipo etano per il diborano.[2] Misure di diffrazione elettronica effettuate da Bauer inizialmente sembrarono confermare questa struttura.[3][4]
In seguito ad una comunicazione personale con Linus Pauling, che era a favore alla struttura tipo etano, H. I. Schlesinger non discusse in particolare il legame a tre centri e due elettroni nella sua classica rassegna del 1942.[5] In questa pubblicazione, tuttavia, discusse una struttura con simmetria C2v: "Va riconosciuto che questa formulazione rende conto facilmente per molte delle proprietà chimiche dei diborano..."
Nel 1943 Christopher Longuet-Higgins, allora studente del Balliol College di Oxford, pubblicò insieme a Ronnie Bell la struttura ora accettata.[6] Curiosamente, questa struttura era già stata proposta nel 1921,[7] ed era nota a scienziati sovietici nel 1940.[8][9] Negli anni successivi la proposta di Longuet-Higgins e Bell fu al centro di colorite discussioni. La disputa terminò nel 1951 con la misura di diffrazione elettronica di K. Hedberg e V. Schomaker, che confermarono la struttura illustrata in questa pagina.[10]
Negli anni cinquanta William Lipscomb confermò ulteriormente la struttura dei borani tramite misure di diffrazione a raggi X, e sviluppò le teorie per interpretarne i legami. In seguito applicò gli stessi metodi alle strutture dei carborani. Per i suoi studi sulla struttura dei borani Lipscomb ricevette nel 1976 il premio Nobel per la chimica.
Struttura molecolare e configurazione elettronica[modifica | modifica wikitesto]
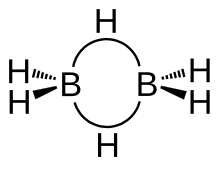

La molecola del diborano ha simmetria D2h. La struttura comprende quattro idrogeni terminali e due a ponte. La struttura elettronica di legame nel diborano è razionalizzata nel modo seguente.[11] La molecola possiede un totale di 12 elettroni a disposizione per formare i suoi legami. La geometria attorno a ciascun atomo di boro è approssimativamente tetraedrica. Ogni atomo di boro è ibridato sp3, e utilizza due di questi orbitali ibridi per fare un normale legame σ a due elettroni con gli idrogeni terminali. Di conseguenza, i legami con gli idrogeni terminali utilizzano in totale di otto elettroni. Gli altri due orbitali ibridi di ogni atomo di boro puntano nella direzione degli idrogeni a ponte. Per spiegare i due legami B–H–B è necessario ricorrere al formalismo degli orbitali molecolari. Semplificando, per ciascuno dei due legami B–H–B si considera un orbitale ibrido sp3 per ogni atomo di boro e l'orbitale 1s dell'idrogeno. Questi sono tre orbitali atomici che si combinano formando tre orbitali molecolari (vedi figura). Dalle diverse combinazioni algebriche si ottiene un orbitale legante ψb, un orbitale antilegante ψa e uno non legante ψn. Nell'orbitale legante vanno a disporsi due elettroni, formando un legame a tre centri e due elettroni. Lo stesso avviene anche per l'altro idrogeno a ponte, utilizzando un totale di quattro elettroni per i due legami B–H–B.
Le distanze dei legami B-Ha ponte e B-Hterminale sono rispettivamente 131 e 119 pm; queste differenze riflettono diverse energie di legame, e i legami B-Ha ponte sono più deboli. La struttura del diborano è isoelettronica con quella di C2H62+, che si otterrebbe aggiungendo due protoni alla molecola planare dell'etene.[12] Tra gli elementi del gruppo 13 il gallio forma un composto analogo, il digallano, Ga2H6. L'alluminio forma un idruro polimerico (AlH3)n. Un composto instabile Al2H6 isostrutturale con il diborano è stato osservato solo in idrogeno solido.[13] Non si conoscono ancora idruri di indio e tallio.[14]
Sintesi[modifica | modifica wikitesto]
Il diborano è un composto molto importante e studiato, e può essere sintetizzato in vari modi.[15] La maggior parte delle sintesi utilizza reazioni tra donatori di idruro e alogenuri o alcossidi di boro. La sintesi industriale prevede la riduzione di BF3 con idruro di sodio:
- 2 BF3 + 6 NaH → B2H6 + 6 NaF
Due metodi di laboratorio partono da tricloruro di boro e litio alluminio idruro o da trifluoruro di boro e sodio boroidruro. In entrambi i casi la resa di diborano può arrivare al 30%:
- 4 BCl3 + LiAlH4 → 2 B2H6 + 3 LiAlCl4
- 4 BF3 + 3 NaBH4 → 2 B2H6 + 3 NaBF4
Metodi precedenti usavano la reazione diretta tra sali di bororidruro e acidi non ossidanti come l'acido fosforico o l'acido solforico diluito:
- 2 BH4− + 2 H+ → B2H6 + 2 H2
Una sintesi di laboratorio adatta a ottenere piccole quantità di diborano è l'ossidazione di sali di boroidruro con iodio:
- 2 NaBH4 + I2 → B2H6 + 2 NaI + H2
Reattività[modifica | modifica wikitesto]
Il diborano è termodinamicamente instabile, dato che ha una entalpia standard di formazione positiva (36 kJ/mol), ma puro è abbastanza inerte dal punto di vista cinetico. Il composto è molto sensibile all'ossidazione e va evitato ogni contatto con l'ossigeno atmosferico e l'acqua. All'aria si infiamma spontaneamente, perché la reazione con l'ossigeno è molto esotermica:
- B2H6 + 3 O2 → B2O3 + 3 H2O ΔH = –2138 kJ
Con acqua si formano acido borico e idrogeno:
- B2H6 + 6 H2O → 2 B(OH)3 + 6 H2
Per pirolisi oltre 100 °C si decompone formando idrogeno e borani superiori (come pentaborano, esaborano, decaborano e altri).
Anche in atmosfera inerte il diborano rimane una specie molto reattiva.[16] Il tipo di reattività principale consiste nella formazione di addotti con basi di Lewis, che attaccano il ponte B–H–B, deficiente di elettroni. Ad esempio, ammine piccole provocano rotture asimmetriche, e ammine più grandi rotture simmetriche:
- B2H6 + 2 NH3 → [H2B(NH3)2]+[BH4]–
- B2H6 + 2 NMe3 → 2 Me3N+–-BH3
Un modo pratico per utilizzare il diborano è tramite i complessi con THF e dimetil solfuro. In entrambi i casi si forma un complesso 1:1, con il boro coordinato tetraedricamente a tre ioni idruro e alla base di Lewis (THF o Me2S). Questi due addotti sono reagenti comuni in chimica organica. L'addotto con THF, (THF)BH3, si prepara come soluzione 1:5 in THF, ed è stabile indefinitamente a temperatura ambiente se conservato sotto atmosfera inerte.
La reazione del diborano con alcheni e alchini è detta idroborazione e permette di accedere agli organoborani, reagenti molto utili:
- (THF)BH3 + 3 RCH=CH2 → B(CH2CH2R)3 + THF
Questa reazione è regioselettiva, e i trialchilborani prodotti possono essere convertiti in utili derivati organici. Con alcheni ingombrati si possono preparare specie tipo [HBR2]2, che sono utili in applicazioni più specialistiche.
Riducendo il diborano con sodio o idruri metallici si ottiene il più semplice anione boroidruro, l'anione tetraidroborato, BH4–, molto usato in chimica organica e inorganica come riducente e fonte di ioni idruro, nonché come ione non coordinante:
- B2H6 + 2 NaH → 2NaBH4
Per produrre industrialmente i tetraidroborati non si usa però questa procedura, ma si riduce borace e quarzo con sodio e idrogeno:
- Na2B4O7 + 7 SiO2 + 16 Na + 8 H2→ 4 NaBH4 + 7 Na2SiO3
Usi[modifica | modifica wikitesto]
Il diborano è un reagente molto reattivo e versatile, con un gran numero di applicazioni.[17] Viene usato principalmente come propellente per razzi, nella sintesi di boroidruri e organoborani, come riducente e come catalizzatore per la polimerizzazione di olefine. Utilizzi minori comprendono la vulcanizzazione della gomma, il drogaggio di semiconduttori di tipo p e la produzione di boro ultrapuro.
Tossicità / Indicazioni di sicurezza[modifica | modifica wikitesto]
Il diborano è un composto estremamente infiammabile, tossico per inalazione, per contatto con la pelle e per ingestione. È inoltre irritante per gli occhi, le vie respiratorie e la pelle.[18] L'esposizione al diborano a breve termine può causare una sensazione di oppressione toracica, respiro affannoso, tosse e dispnea. Questi sintomi possono presentarsi immediatamente o anche fino a 24 ore di distanza. L'esposizione a lungo termine a basse quantità di diborano ha provocato irritazione delle vie respiratorie, convulsioni, stanchezza, eccessiva sonnolenza diurna, confusione e tremori occasionali. Danneggia inoltre nervi e reni.
Note[modifica | modifica wikitesto]
- ^ scheda della sostanza su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ Stock 1933
- ^ Bauer 1937
- ^ Bauer 1942
- ^ Schlesinger e Burg 1942
- ^ Longuet-Higgins e Bell 1943
- ^ Dilthey 1921
- ^ Nekrassov 1940a
- ^ Nekrassov 1940b
- ^ Hedberg e Schomaker 1951
- ^ Huheey et al. 1999
- ^ Rasul et al. 2005
- ^ Andrews e Wang 2003
- ^ Downs e Pulham 1994
- ^ Hosmane e Maguire 2002
- ^ Greenwood e Earnshaw 1997
- ^ Patnaik 2003
- ^ Sigma-Aldrich, scheda di sicurezza del diborano.
Bibliografia[modifica | modifica wikitesto]
- L. Andrews, X. Wang, The Infrared Spectrum of Al2H6 in Solid Hydrogen, in Science, vol. 299, n. 5615, 2003, pp. 2049–2052, DOI:10.1126/science.1082456. URL consultato il 20 ottobre 2011.
- S. H. Bauer, The Structure of Diborane, in J. Am. Chem. Soc., vol. 59, n. 6, 1937, pp. 1096–1103, DOI:10.1021/ja01285a041. URL consultato il 20 ottobre 2011.
- S. H. Bauer, Structures and Physical Properties of the Hydrides of Boron and of their Derivatives, in Chem. Rev., vol. 31, n. 1, 1942, pp. 43-75, DOI:10.1021/cr60098a002. URL consultato il 20 ottobre 2011.
- W. Dilthey, Über die Konstitution des Wassers, in Angew. Chem., vol. 34, n. 95, 1921, p. 596, DOI:10.1002/ange.19210349509. URL consultato il 20 ottobre 2011.
- A. J. Downs, C. R. Pulham, The hydrides of aluminium, gallium, indium and thallium: A re-evaluation, in Chem. Soc. Rev., vol. 23, n. 3, 1994, pp. 175–184, DOI:10.1039/cs9942300175. URL consultato il 20 ottobre 2011.
- (EN) N. N. Greenwood, A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
- K. Hedberg, V. Schomaker, A Reinvestigation of the Structures of Diborane and Ethane by Electron Diffraction, in J. Am. Chem. Soc., vol. 73, n. 4, 1951, pp. 1482–1487, DOI:10.1021/ja01148a022. URL consultato il 20 ottobre 2011.
- N. S. Hosmane, J. A. Maguire, Boron Hydrides, in Encyclopedia of Inorganic Chemistry, John Wiley & Sons, 2002, DOI:10.1002/0470862106.ia024.
- J. E. Huheey, E. A. Keiter, R. L. Keiter, Chimica inorganica - principi, strutture, reattività, 2ª ed., Padova, Piccin, 1999, ISBN 88-299-1470-3.
- H. C. Longuet-Higgins, R. P. Bell, 64. The structure of the boron hydrides, in J. Chem. Soc., 1943, pp. 250-255, DOI:10.1039/JR9430000250. URL consultato il 20 ottobre 2011.
- B. M. Mikhailov, Russ. Chem. Rev., vol. 31, n. 4, 1962, pp. 207-224, DOI:10.1070/RC1962v031n04ABEH001281, https://oadoi.org/10.1070/RC1962v031n04ABEH001281. URL consultato il 20 ottobre 2011.
- B. V. Nekrassov, J. Gen. Chem. USSR, vol. 10, 1940, pp. 1021-1030.
- B. V. Nekrassov, J. Gen. Chem. USSR, vol. 10, 1940, pp. 1056-1066.
- P. Patnaik, Handbook of Inorganic Chemicals, McGraw-Hill, 2003, ISBN 0-07-049439-8.
- G. Rasul, G. K. S. Prakash, G. A. Olah, Comparative ab Initio Study of the Structures and Stabilities of the Ethane Dication C2H62+ and Its Silicon Analogues Si2H62+ and CSiH62+, in J. Phys. Chem. A, vol. 109, n. 5, 2005, pp. 798–801, DOI:10.1021/jp0404652. URL consultato il 20 ottobre 2011.
- H. I. Schlesinger, A. B. Burg, Recent Developments in the Chemistry of the Boron Hydrides, in Chem. Rev., vol. 31, n. 1, 1942, pp. 1–41, DOI:10.1021/cr60098a001. URL consultato il 20 ottobre 2011.
- A. Stock, The Hydrides of Boron and Silicon, New York, Cornell University Press, 1933.
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «diborano»
Wikizionario contiene il lemma di dizionario «diborano» Wikimedia Commons contiene immagini o altri file su diborano
Wikimedia Commons contiene immagini o altri file su diborano
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) diborane, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh2006002731 · J9U (EN, HE) 987007551793305171 |
|---|