Acido clorico
Vai alla navigazione
Vai alla ricerca
| Acido clorico | |
|---|---|
 | |
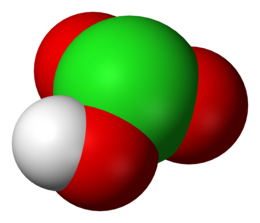 | |
| Nome IUPAC | |
| acido triossoclorico (V) | |
| Nomi alternativi | |
| acido triossoclorico (V) | |
| Caratteristiche generali | |
| Formula bruta o molecolare | HClO3 |
| Peso formula (u) | 84.45914 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 232-233-0 |
| PubChem | 19654 |
| DrugBank | DB14150 |
| SMILES | OCl(=O)=O |
| Proprietà chimico-fisiche | |
| Densità (g/l, in c.s.) | ca. 1000 g/L |
| Costante di dissociazione acida a 293,15 K | 10 |
| Solubilità in acqua | 400 g/L |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi R | 9-20/22-35 |
| Frasi S | 2-13-16-27 |
L'acido clorico è un ossiacido del cloro pentavalente, Cl(V), avente formula HClO3. Non è noto allo stato puro, ma solo nelle sue soluzioni acquose, dove si comporta da acido forte. Ha spiccate proprietà ossidanti, che condivide con i suoi sali, i clorati.
Sintesi[modifica | modifica wikitesto]
Viene prodotto trattando clorati con un acido forte come l'acido solforico.
Il solfato di bario, insolubile, viene eliminato dai prodotti. Un altro metodo consiste nel riscaldamento dell'acido ipocloroso, con produzione di acido cloridrico e acido clorico:
Caratteristiche[modifica | modifica wikitesto]
È stabile in soluzioni acquose fino al 30%. A pressione ridotta, si può concentrare sopra il 40% per evaporazione dell'acqua. Sopra queste concentrazioni, e per riscaldamento, l'acido clorico si decompone producendo diversi prodotti:
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su acido clorico
Wikimedia Commons contiene immagini o altri file su acido clorico



