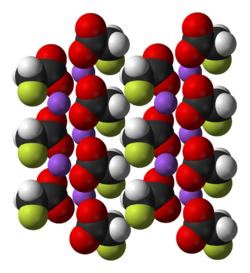
Fluoroacetato di sodio
| Fluoroacetato di sodio | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| 2-fluoroacetato di sodio | |
| Nomi alternativi | |
| Composto 1080 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H2FNaO2 |
| Massa molecolare (u) | 100,02 |
| Aspetto | polvere incolore e inodore |
| Numero CAS | |
| Numero EINECS | 200-548-2 |
| PubChem | 16212360 |
| SMILES | C(C(=O)[O-])F.[Na+] |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | solubile |
| Temperatura di fusione | 200 °C (473 K) dec. |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 0,1 ratto orale[1] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| Frasi H | 300, 310, 330, 400 |
| Consigli P | 260, 264, 273, 280, 284, 301+310 |
Il fluoroacetato di sodio è il composto chimico di formula FCH2CO2Na. In condizioni normali è una polvere incolore e inodore, facilmente solubile in acqua. Si trova in natura in varie piante come metabolita anti-erbivori, ma viene prodotto anche artificialmente. Il composto è fortemente tossico ed è stato ampiamente usato in passato come rodenticida (veleno per topi). Data l'estrema pericolosità l'uso è stato proibito in molti stati.
Storia[modifica | modifica wikitesto]
Il fluoroacetato fu scoperto in Germania da chimici militari durante la seconda guerra mondiale. Le sue proprietà rodenticide furono scoperte poco dopo negli Stati Uniti.[2] Il nome "1080" era inizialmente un numero di catalogo, che diventò poi una denominazione di prodotto.[3]
Sintesi[modifica | modifica wikitesto]
Il fluoroacetato di sodio è preparato trattando con fluoruro di potassio l'estere etilico dell'acido monocloroacetico per trasformarlo in estere etilico dell'acido monofluoroacetico; segue quindi idrolisi con NaOH.[4][5]
Presenza in natura[modifica | modifica wikitesto]

L'anione fluoroacetato è presente in natura in almeno 40 piante in Australia, Brasile e Africa. Fu identificato per la prima volta da Marais nel 1944 nelle foglie velenose del gifblaar (Dichapetalum cymosum), un arbusto dell'Africa meridionale.[6][7] Già dal 1904 i coloni in Sierra Leone per avvelenare i topi utilizzavano estratti di Chailletia toxicaria, che pure contiene acido fluoroacetico o suoi sali.[8][9] Quantità molto piccole di fluoroacetato sono state trovate in molte piante, compreso il tè.[10] Questo veleno è presente in molte piante native dell'Australia, tra le quali specie dei generi Gastrolobium, Gompholobium, Oxylobium, Nemcia e Acacia.
Tossicologia[modifica | modifica wikitesto]
Il fluoroacetato è fortemente tossico per mammiferi e insetti.[11] La tossicità varia a seconda della specie.
La dose orale letale per l'uomo è 2–10 mg/kg.[12] La dose letale LD50 per i gatti è 0,3–0,5 mg/kg.[13] Per varie specie di uccelli come il passero e lo storno i valori di LD50 sono 2–3 mg/kg. Per le cavie si ha un LD50 di 0,3 mg/kg.[3][14] Uccelli e carnivori si avvelenano spesso cibandosi da carcasse avvelenate.
Per gli organismi acquatici invece il fluoroacetato è sostanzialmente non tossico (per i pesci LC50 a 96 ore è 54 mg/L; per i crostacei EC50 a 48 ore è 350 mg/L).[1]
Il fluoroacetato di sodio è molto tossico, può essere fabbricato facilmente ed è semplice da utilizzare; è stato notato che queste caratteristiche lo rendono un'arma potenzialmente utile nelle mani di terroristi.[15]
Meccanismo d'azione[modifica | modifica wikitesto]
L'anione fluoroacetato è simile all'acetato, che ha un ruolo fondamentale nel metabolismo cellulare. Il fluoroacetato interrompe il ciclo dell'acido citrico (conosciuto anche come ciclo di Krebs). Si combina con il coenzima A per formare fluoroacetil CoA, che reagisce con la citrato sintasi formando fluorocitrato. Un metabolita del fluorocitrato si lega molto fortemente all'aconitasi, arrestando il ciclo dell'acido citrico. Ne risulta un accumulo di citrato nel sangue che priva le cellule di energia.[11]
Sintomi[modifica | modifica wikitesto]
Nell'uomo i sintomi di avvelenamento appaiono di solito da 30 minuti a tre ore dopo l'esposizione. Inizialmente i sintomi tipici sono nausea, vomito e dolori addominali; seguono poi sudorazione, confusione e agitazione. Se l'avvelenamento è importante si sviluppano anomalie come tachicardia o bradicardia, ipotensione e modifiche dell'elettrocardiogramma. Dal punto di vista neurologico si hanno spasmi muscolari e convulsioni; la coscienza viene progressivamente compromessa e dopo alcune ore si arriva al coma. La morte è di solito causata da aritmie ventricolari, ipotensione progressiva che non risponde a trattamenti, e infezioni polmonari secondarie.[11]
Negli animali domestici i sintomi variano: i cani tendono a mostrare disfunzioni del sistema nervoso come convulsioni epilettiche e movimenti incontrollabili di corsa, mentre i grandi erbivori come i bovini e le pecore mostrano più spesso disturbi cardiaci.[3]
Dosi non letali di fluoroacetato di sodio possono causare danni ai tessuti con alto fabbisogno energetico, in particolare cervello, gonadi, cuore, polmoni e feto. Dosi non letali sono in genere completamente metabolizzate ed escrete nel giro di quattro giorni.[16]
Trattamento[modifica | modifica wikitesto]
Non sono noti antidoti efficaci. Ricerche su scimmie hanno mostrato che l'uso di monoacetato di glicerina può prevenire problemi se somministrato dopo l'ingestione del veleno; questa terapia è stata sperimentata su animali domestici con qualche risultato positivo. In teoria il monoacetato di glicerina dovrebbe fornire gli ioni acetato per permettere la respirazione cellulare interrotta dal fluoroacetato di sodio.[17]
In casi clinici sono stati necessari anche miorilassanti, anticonvulsanti, ventilazione artificiale e altri metodi di supporto. Pochi animali o persone sono stati trattati con successo dopo l'ingestione di quantità significative di fluoroacetato di sodio.[18]
Uso[modifica | modifica wikitesto]

Il composto è stato ampiamente usato in passato per il controllo di roditori ed altri mammiferi.[19] Data l'estrema pericolosità l'uso è stato tuttavia proibito in molti stati. Viene ancora usato in Australia contro le volpi. In Giappone, Israele e Messico come rodenticida. Negli Stati Uniti contro i coyote per difendere le pecore. In Nuova Zelanda è usato contro mammiferi come ermellino, topi, gatti, opossum e altri predatori introdotti.[20] Viene inoltre utilizzato in Canada, India e Olanda.[21]
Note[modifica | modifica wikitesto]
- ^ a b Pagina sul fluoroacetato di sodio nel Database GESTIS
- ^ Kalmbach 1945
- ^ a b c Gupta 2007
- ^ Villavecchia e Eigenman 1982, p. 55.
- ^ Elliott 1998
- ^ Marais 1943
- ^ Marais 1944
- ^ Renner 1904
- ^ Power e Tutin 1906
- ^ Vartiainen e Kauranen 1984
- ^ a b c Proudfoot et al. 2006
- ^ M. Beasley, Guidelines for the safe use of sodium fluoroacetate (1080) (PDF), su osh.govt.nz, New Zealand Occupational Safety & Health Service. URL consultato il 29 gennaio 2012 (archiviato dall'url originale il 10 settembre 2008).
- ^ Kraft et al. 2003, p. 121.
- ^ Ward 1946
- ^ Holstege et al. 2007
- ^ Eason et al. 1993
- ^ Bent 2005
- ^ Irwin e Rippe 2008, pp. 1666-1667.
- ^ Olson 1999, p. 189.
- ^ Department of Conservation (New Zealand), 1080 questions and answers, su doc.govt.nz. URL consultato il 30 gennaio 2012 (archiviato dall'url originale il 20 gennaio 2012).
- ^ (EN) Fluoride Action Network - Pesticide Project, Sodium fluoroacetate, su 208.109.172.241. URL consultato il 6 novembre 2021 (archiviato dall'url originale l'8 luglio 2012).
Bibliografia[modifica | modifica wikitesto]
- J. Bent, Critical care toxicology: diagnosis and management of the critically poisoned patient, St. Louis, Mosby, 2005, p. 970, ISBN 0-8151-4387-7.
- C. T. Eason, C. M. Frampton, R. Henderson, M. D. Thomas e D. R. Morgan, Sodium monofluoroacetate and alternative toxins for possum control, in New Zealand Journal of Zoology, vol. 20, n. 3, 1993, pp. 329-334. URL consultato il 29 gennaio 2012.
- A. J. Elliott, Fluorinated acetic acids, in Kirk-Othmer Encyclopedia of Chemical Technology, 4ª ed., Wiley, 1998.
- R. C. Gupta, Veterinary Toxicology: Basic and Clinical Principles, Academic Press, 2007, ISBN 978-0-12-370467-2.
- C. P. Holstege, L. K. Bechtel, T. H. Reilly, B. P. Wispelwey e S. G. Dobmeier, Unusual but potential agents of terrorists, in Emerg. Med. Clin. North Am., vol. 25, n. 2, 2007, pp. 549-66. URL consultato il 29 gennaio 2012.
- R. S. Irwin e J. M. Rippe, Irwin and Rippe's intensive care medicine, Philadelphia, Wolters Kluwer Health / Lippincott Williams & Wilkins, 2008, ISBN 0-7817-9153-7.
- E. R. Kalmbach, "Ten-Eighty," a War-Produced Rodenticide, in Science, vol. 102, n. 2644, 1945, pp. 232–233, DOI:10.1126/science.102.2644.232.
- W. R. Kraft, U. M. Dürr e K. Hartmann, Katzenkrankheiten, Schaper, 2003, ISBN 978-3-7944-0199-4.
- J. C. S. Marais, The isolation of the toxic principle "K cymonate" from "Gifblaar", "Dichapetalum cymosum", in Onderstepoort Jour. Vet. Sci., vol. 18, 1943, pp. 203-206.
- J. C. S. Marais, Monofluoroacetic acid, the toxic principle of "Gifblaar", "Dichapetalum cymosum", in Onderstepoort Jour. Vet. Sci., vol. 20, 1944, pp. 67-73.
- K. R. Olson (a cura di), Intossicazioni Acute: Veleni, Farmaci e Droghe, 2ª ed., Springer, 1999, ISBN 88-470-0030-0.
- F. B. Power e F. Tutin, Chemical and Physiological Examination of the Fruit of "Chailletia toxicaria", in J. Am. Chem. Soc., vol. 28, n. 9, 1906, pp. 1170-1183, DOI:10.1021/ja01975a007.
- A. T. Proudfoot, S. M. Bradberry e J. A. Vale, Sodium Fluoroacetate Poisoning, in Toxicological Reviews, vol. 25, n. 4, 2006, pp. 213-219, DOI:10.2165/00139709-200625040-00002.
- W. Renner, Native Poison, West Africa, in Jour African Soc., 1904, pp. 109-111.
- T. Vartiainen e P. Kauranen, The determination of traces of fluoroacetic acid by extractive alkylation, pentafluorobenzylation and capillary gas chromatography-mass spectrometry, in Anal. Chim. Acta, vol. 157, n. 1, 1984, pp. 91-97, DOI:10.1016/S0003-2670(00)83609-0.
- V. Villavecchia e G. Eigenman, Nuovo dizionario di merceologia e chimica applicata, vol. 1, Hoepli, 1982, ISBN 978-88-203-0528-4.
- J. C. Ward, Rodent control with 1080, ANTU, and other war-developed toxic agents, in Am. J. Public Health Nations Health, vol. 36, 1946, pp. 1427-1431.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Fluoroacetato di sodio
Wikimedia Commons contiene immagini o altri file su Fluoroacetato di sodio
Collegamenti esterni[modifica | modifica wikitesto]
- Gruppo SGD, Tecniche di derattizzazione, su grupposgd.it. URL consultato il 30 gennaio 2012.
- Azienda Sanitaria di Firenze, La lotta contro i roditori nelle strutture della filiera alimentare (PDF), su comune.fi.it. URL consultato il 30 gennaio 2012 (archiviato dall'url originale il 2 dicembre 2008).